INTRODUCCIÓN
El cáncer de mama, sigue siendo una de las principales prioridades en salud global y salud pública y permanece como la neoplasia maligna más frecuente y mortal en mujeres en todo el mundo1,2. Para el año 2020, se reportaron más de 2 millones de casos nuevos y aproximadamente 700 mil muertes; se estima que este número aumente en un 50% para el año 2040: más de tres millones de casos nuevos y un millón de muertes1. La implementación de programas de tamizaje, diagnóstico precoz, tratamiento oportuno y asequible, así como seguimiento estricto para evaluación de riesgo de recurrencia son líneas sobre las que se trabaja intensamente en la actualidad3-5. No obstante, se ha observado en los últimos años un tipo de cáncer de mama cada más frecuente, de comportamiento incierto y agresivo, asociado a una intervención cotidiana, la mamoplastia6.
El linfoma anaplásico de células grandes asociado a implante mamario (LACG-AIM), consiste en un linfoma No-Hodgkin de tipo raro, y pertenece a trastornos linfoproliferativos cd30 positivos, del cual se desconoce mucho sobre su patogenia y fisiopatología6,7. Se cree que el contenido y superficie de los implantes se asocia a una respuesta inflamatoria, crónica y aberrante, que desencadena los cambios adaptativos celulares y podría progresar hasta la malignidad7. A la fecha, existen limitaciones en cuanto al conocimiento sobre el comportamiento clínico, se manifiesta de muchas formas, con un tiempo de evolución variable y desenlaces quirúrgicos inciertos a mediano y largo plazo8. Dentro de los vacíos existentes, se encuentra que casi la totalidad de casos y estudios de prevalencia publicados poseen datos exclusivamente de países de altos ingresos; cabe resaltar que se desconoce casi la totalidad del comportamiento de esta entidad en Latinoamérica8-11. Además, no existe mucha evidencia en habla hispana.
Teniendo en cuenta que las cirugías estéticas son cada vez más frecuentes, se espera que la incidencia de estos casos sea cada vez mayor, por lo que se deben sospechar, conocer sobre aspectos clínicos para su identificación desde la atención primaria y evaluar las consideraciones y desenlaces quirúrgicos, para determinar el pronóstico y adaptar el seguimiento de acuerdo al riesgo y contexto de cada paciente. Con base en lo anterior, el objetivo de esta revisión consiste en resumir evidencia sobre las consideraciones clínicas y desenlaces quirúrgicos del cáncer asociado a implante mamario, que faciliten la identificación y abordaje de esta condición, por parte de médicos y especialistas.
METODOLOGÍA
Se realizó una búsqueda bibliográfica utilizando términos como "Breast Implant-Associated Cancer ", y “Outcomes”, así como sinónimos, que se combinaron con los operadores booleanos "AND" y "OR", en los motores de búsqueda y bases de datos bases de datos PubMed, ScienceDirect, Embase, EBSCO y MEDLINE. Como criterio de inclusión, se definió que cualquier artículo relacionado con la evaluación de características clínicas y desenlaces quirúrgicos del LACG-AIM o de cualquier cáncer asociado a implante mamario, sería incluido y se daría prioridad a los estudios originales y a las revisiones sistemáticas y metanálisis. También, se incluyeron artículos relacionados a descripciones fisiopatológicas de esta condición, así como de otros conceptos básicos sobre cáncer de mama.
Además, debían estar disponibles en texto completo. Como criterios de no inclusión, se estableció que no se incluirían los artículos publicados en un idioma distinto al español y al inglés. Teniendo en cuenta la amplitud del tema y la gran variedad de publicaciones, se incluyeron los artículos publicados entre 2000 y 2022. Se identificaron un total de 76 artículos potencialmente relevantes, con una revisión del título y el resumen de todos , de los que, finalmente, se incluyeron 43 artículos, tras su discriminación según los criterios de inclusión y no inclusión. Se tomaron en cuenta otras referencias de utilidad para la discusión de conceptos generales. Las estimaciones y cálculos encontrados se expresaron en sus medidas originales, ya sean frecuencias, porcentajes, intervalos de confianza (IC), diferencia de medias (DM), riesgo relativo (RR), odds ratio (OR), tasa de incidencia (IRR) o hazard ratio (HR).
RESULTADOS
Aspectos fisiopatológicos sobre el cáncer asociado a implante mamario
Aunque se conoce muy poco en la actualidad sobre la patogenia y fisiopatología de esta condición, los reportes de caso y estudios de prevalencia, han permitido ampliar significativamente el panorama sobre posibles asociaciones causales y factores de riesgo a considerar. El primer caso fue publicado alrededor del año 2000, y desde entonces, se ha encontrado una incidencia de 1 caso por cada 3000 implantes mamarios texturizados colocados12. A inicios de los 2010, la FDA (food and drug administration) advirtió sobre la posible asociación entre esta exposición y el evento de cáncer, para lo cual solicitó la realización de estudios colaborativos a nivel internacional, para conocer el comportamiento clínico y posibles factores de riesgo adicionales13. Por tal motivo, fue creado el registro PROFILE (patient registry and outcomes for breast implants and anaplastic large cell lymphoma etiology and epidemiology), con el objetivo de recopilar datos epidemiológicos detallados, que permitirán comprender mejor la historia natural de la enfermedad14.
A partir de este tipo de datos, se fueron direccionando estudios basándose en la tendencia de enfermedad encontrada con ciertos factores de riesgo; el primero, la texturización del implante15-17). Se ha planteado que este tipo de implantes promueven la respuesta inmune e infiltración de células T, lo que genera inflamación crónica, demostrada por algunos estudios en ciencias básicas que han identificado la presencia de numerosos receptores de interleucinas de superficie, en células de LACG-AIM, así como de señalizaciones participantes en la activación de estas moléculas proinflamatorias15,17. También, se ha descrito un potencial mecanismo alérgico, debido a la expresión de células con polarización th1/th17 en tejidos capsulares y seromas, expresión de interleucina 13 e IGE, por lo que se sugiere estimulación antigénica crónica y proliferación de células t sostenida a16.
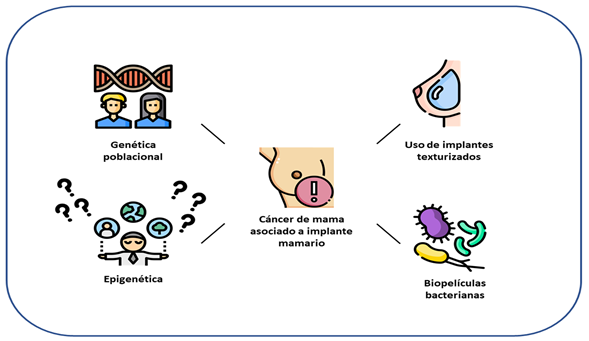
Adicionalmente, se ha hipotetizado que las biopelículas bacterianas y la genética del paciente juegan un rol fundamental en este proceso fisiopatológico18-22. Los implantes texturizados, pueden desarrollar una carga de biopelículas bacterianas mucho mayor, en comparación a implantes lisos19,21. Evidencia reciente, ha encontrado un patrón común en número representativo de casos (aproximadamente el 70% de casos), de mutaciones en la vía de señalización JAK/STAT, en el gen supresor de tumores p53, y en la enzima ADN-metiltransferasa 3a (DNMT3A)18. Otro dato interesante consiste en los polimorfismos del antígeno leucocitario humano, que se encuentra íntimamente relacionado con una línea celular germinal del linfoma, el cual, se ha descrito, difiere entre estos casos y la población general. Algunos estudios que han evaluado este fenómeno a través de proteómica y transcriptómica, y publicados en los últimos años, han reportado regulación al alza y a la baja en algunos genes, como lo son el CCR6 (receptor de quimiocinas 6), c-Met (receptor de tirosina quinasa), HGF (factor de crecimiento hepatocitario), CXCL14 (ligando 14 de quimiocina), PPARG (receptor gamma activado por proliferador de peroxisoma) y JAK2 (quinasa Janus 2). Esencialmente, se han encontrado mutaciones en más del 50% de las copias de PD-L1 (ligando 1 de muerte programada), lo cual contribuiría a la proliferación celular descontrolada en el contexto de malignidad 18-22. Todos estos hallazgos sugieren la presencia de un microambiente a expensas de reactividad inmune sustenida, que afecta considerablemente los puntos de control inmunitarios y precipitan los procesos de proliferación, diferenciación, migración e invasión, secundario a múltiples factores, como los mencionados previamente. Ahora bien, basados en el efecto de la predisposición genética sobre el desarrollo de este cáncer, es necesario considerar la genética y epigenética de poblaciones, la cual no ha sido ampliamente estudiada (figura 1)(18. La gran mayoría de la evidencia, disponible en la actualidad, consiste en casos reporte y series de caso, provenientes la gran mayoría de países de altos ingresos. En este orden de ideas, se deben llevar a cabo estudios en ciencias básicas y traslacionales, que permitan identificar las mutaciones y expresión génica y de señalizaciones en regiones como Latinoamérica, donde existe una diversidad étnica y cultural, que difiere sustancialmente de características genéticas de la población caucásica o europea. Así, se dispondría de mayor información sobre la posibilidad de extrapolar los resultados de ensayos que se realizan en la actualidad, sobre potenciales inmunoterapias para el tratamiento del LACG-AIM.
Consideraciones clínicas y epidemiológicas sobre el cáncer asociado a implante mamario
Las manifestaciones y el abordaje clínico, probablemente, sea de los puntos más críticos a discutir en este tópico. En la actualidad, se observa que las mamoplastias se realizan en diversos grupos etarios, desde edades muy tempranas hasta tardías. Esto puede ocasionar cierta confusión en el abordaje de manifestaciones locales, que, puedan suponerse, son resultado de una condición propia de la edad, de los cambios hormonales o no asociado a malignidad. También, para comprender la tendencia de la historia natural de la enfermedad, los signos y síntomas más frecuentes y los tiempos que deben considerarse en la atención directa y remisión a especialidades médicas.
Ionesco et al.23realizaron un mapeo epidemiológico para proveer de datos novedosos, y comunicaron que, hasta octubre de 2021, existían alrededor de 950 casos de LACG-AIM y 32 muertes reportadas a nivel global, provenientes principalmente de Estados Unidos (n=384), Australia (n=104), Reino Unido (n=78) y Francia (n=78); el riesgo absoluto de desarrollar este tipo de cáncer en mujeres con mutaciones en los genes BRCA 1 y 2 era de 1:1551 a los 75 años, comparado con la población general: 1:7507; del total de estudios encontrados, más de 200 no describen la texturización del implante; el tiempo promedio de la exposición hasta la presentación del cáncer es de ocho años y, aproximadamente, el 80% de los casos se diagnostican en estadio 1a-iia23. Por su parte, Tevis et al24analizaron, de forma prospectiva, una serie de casos de 52 pacientes con LACG-AIM y encontraron que el 61.5% se realizó la mamoplastia de aumento, mientras que un 36,5% fue por reconstrucción. De forma predominante, la manifestación principal fue un seroma de presentación tardía (69,2%), sin síntomas sistémicos asociados (86,5%). La recurrencia reportada fue 3.8% (n=2)24.
Cordeiro et al.25ejecutaron un estudio de cohorte con 3546 mujeres sometidas a 6023 reconstrucciones de mama, principalmente por mastectomía profiláctica bilateral o mastectomía por cáncer, en quienes se utilizó implantes texturizados. Se evidenció que 10 mujeres desarrollaron LACG-AIM después de una mediana de 11 años; ello generó un estimado de riesgo de 0,3 casos por cada 1000 personas/año. De los casos, el 70% se presentó como seroma unilateral y estadio 1a-1b: un caso con seroma y tumefacción (estadio IIA), uno con una masa que invadía el musculo pectoral y ganglios axilares inflamados (estadio III) y otro con inflamación de ganglios axilares solamente (IIB O III)25. Patzelt et al.26reportaron el caso de una mujer transgénero de 33 años, quien durante su proceso de transformación se sometió a una mamoplastia y desarrolló una masa tumoral de aproximadamente 5 cm, siete años después. Se le removió el implante, capsula, masa y musculo pectoral, se le sometió a quimioterapia y quedó libre de enfermedad dos años después26. Este último caso genera nuevas dudas sobre la influencia de terapia hormonal o de factores desconocidos que son independientes del sexo biológico, que predisponen a la presentación del cáncer, como lo puede ser la reactividad alérgica e inmune en sí.
Nelson et al.27realizaron un estudio de cohorte retrospectivo con 9373 mujeres y 16 065 implantes (59.7% [n=9589] fueron texturizados), quienes fueron seguidas por un periodo de 26 años aproximadamente, con el objetivo de determinar la incidencia y riesgo de LACG-AIM. Los autores evidenciaron que 11 pacientes fueron diagnosticadas con este cáncer, de las cuales el 100% recibieron implantes texturizados. La mediana de tiempo hasta el diagnóstico fue de aproximadamente 10 años y un análisis del tiempo hasta el evento reveló una incidencia de 4.4 casos por cada 1000 pacientes de 10 a 12 años, y de 9,4 por cada 1000 pacientes de 14 a 16 años27. Hasta este punto, la evidencia clínica dirige la tendencia hacia el uso de implantes texturizados, sin discriminar otros factores que pudieran estar asociados, como el origen o edad de la paciente. Otros estudios, enfocados en los conocimientos autopercibidos por parte de los cirujanos plásticos, determinó que de 254 cirujanos europeos encuestados, el 73% desconocía esta enfermedad, y solo el 8% había enfrentado un caso de estos28. No obstante, y de forma interesante, se han empezado a reportar casos de neoplasias malignas distintas al LACG-AIM29. Xia et al29describieron el caso de un carcinoma escamocelular asociado a implante mamario, en un paciente masculino de 52 años con antecedente de síndrome de poland, por lo que fue intervenido 18 años previos para una reconstrucción mamaria izquierda. La manifestación principal fue la presencia de una masa multinodular de 20 cm, la cual fue removida quirúrgicamente, además del implante (texturizado). Se realizó el diagnóstico de carcinoma escamocelular y, a pesar de recibir terapia neoadyuvante, el paciente tuvo un pronóstico desfavorable con metástasis a restructuras adyacentes29. Este constituye uno de los pocos casos descritos sobre un cáncer asociado a implante mamario distinto al LACG-AIM, el cual debe ser estudiado con mayor profundidad, para evaluar si el sexo o el antecedente del síndrome de Poland, pudiera haber sido el factor causal de esta malignidad.
Entonces, sobre las consideraciones clínicas y epidemiológicas del LACG-AIM y otros cánceres también asociados a implante mamario, se puede decir que gran parte de las revisiones sistemáticas se concentran en determinar el riesgo30-32, y no en describir la presentación clínica y manifestaciones postcirugía o postneoadyuvancia, que son esenciales para el conocimiento y tamizaje del médico de atención primaria y otros especialistas involucrados en el manejo integral del paciente oncológico. Aun así, se puede afirmar que la gran mayoría de los casos están asociados al uso de implantes texturizados y cuya presentación se da como seroma tardío o sensación de masa sugestiva de lesión tumoral. Sigue persistiendo el vacío de evidencia disponible, debido a la falta de datos de nuestra región, sin conocer manifestaciones, manejo, desenlaces y pronósticos, así como percepción del paciente y conocimientos del cirujano.
Desenlaces quirúrgicos y evolución del cáncer asociado a implante mamario
Aunque hay poca evidencia de interés que provee información útil sobre los desenlaces quirúrgicos obtenidos en este tipo de pacientes, podría servir de base para la toma de decisiones en la práctica clínica y cuidado posterior.
Nelson et al.33realizaron una revisión sistemática con el objetivo de evaluar el riesgo quirúrgico de acuerdo a técnicas utilizadas, en el que incluyeron 276 estudios, de los cuales ninguno cumplió con los criterios de inclusión, al ser casi la totalidad, casos reporte o series de caso. Sin embargo, los autores realizaron recomendaciones basadas en la experiencia y en consensos institucionales y manifestaron que, inicialmente: 1) no se recomienda la extracción de implantes texturizados en pacientes asintomáticos; 2) aquellos pacientes que deseen solicitar intervención, tienen tres opciones (remoción del implante, con o sin capsulectomía, y con reemplazo por implante liso o reconstrucción con tejido autólogo); 3) se debe considerar capsulectomía parcial en pacientes de alto riesgo; 4) todo líquido periprotésico debe ser enviado a análisis para descarte de LACG-AIM; y 5) la reconstrucción autóloga es la opción asociada con los mejores desenlaces reportados por pacientes y con el menor riesgo quirúrgico33. Lillemoe et al.34resumieron los escenarios clínicos del LACG-AIM descritos a la fecha: efusión local, masa infiltrante de tejidos blandos, imagen sospechosa de afectación ganglionar, afectación ganglionar extensa, masa extensa en pared torácica, o erupción cutánea, las cuales deben despertar la alarma en el contexto de una persona con antecedente de implante mamario, de posible desarrollo de cáncer asociado a implante mamario. Estos mismos autores reportaron un caso para cada escenario, los cuales, manejados quirúrgicamente de forma variada, de acuerdo al riesgo y severidad de cada paciente, recurriendo principalmente a la capsulectomía bilateral con tratamiento neoadyuvante, tuvieron una evolución favorable con promedio de seguimiento de dos años, sin signos de recurrencia34.
Lamaris et al.35desarrollaron un estudio prospectivo de casi 20 años, en el que evaluaron los desenlaces y características de pacientes con LACG-AIM que recibieron reconstrucción mamaria. Obtuvieron un total de 66 pacientes, de los cuales el 56% se encontraba en estadio 1a (t1n0m0), mientras que un 17%, en 1b. Se les realizó reconstrucción con colocación de implante liso en un 72%, seguido de pexia mamaria (11%) y colgajo autólogo (11%). Dentro de los desenlaces quirúrgicos reportados, no existieron complicaciones. Se encontró que el 94% de los pacientes reportó estar satisfechos con la reconstrucción y tratamiento recibido35. Nestler et al.36describieron el caso de una mujer con 15 años de historia de implante mamario, el cual desarrolló una masa palpable acompañada de efusión alrededor del implante en la mama derecha y se realizó el diagnóstico de LACG-AIM invasivo estadio iii. La paciente fue tratada por medio de resección incompleta, debido a la invasión a la pared torácica, recibió quimioterapia y radioterapia posteriormente y llegó a evolucionar de forma favorable hasta un año después36. Collins et al.37caracterizaron 104 casos de LACG-AIM publicados en la literatura, observaron que 39 pacientes tenían enfermedad avanzada y, de estos, 7 tenían enfermedad bilateral; 24 se encontraban entre estadios IIB y IV y 8 fallecieron por esta causa. La gran mayoría fue sometida a cirugía incompleta (65.5%) y recibieron quimioterapia: 89.7%. Se encontró que la tasa de remisión completa para aquellos casos con enfermedad bilateral y afectación ganglionar fue 57% y 67%, respectivamente. Comparado con casos de estadio temprano, aquellos con estadio tardío, tuvieron mayor retraso entre el diagnóstico y la cirugía (p = 0.03) y menor razón de cirugía completa: 59% versus 88%.37
Di Napoli et al.38reportaron el caso de una mujer de 76 años, quien fue sometida a reconstrucción bilateral de mama posterior a un cáncer de mama y acude 15 años después con un LACG-AIM. A la paciente se le realizó capsulectomía con márgenes quirúrgicos incompletos y permaneció con enfermedad local residual, la cual fue manejada con radioterapia. Durante un año de seguimiento, la mujer no presentó signos de recurrencia38. Sharma et al.11publicaron la que sería la revisión sistemática más reciente sobre los desenlaces obtenidos en el manejo de LACG-AIM a la fecha. Se analizaron 39 artículos y 51 pacientes; se reportó que la edad promedio de presentación fue de 52 años, la indicación del implante fue principalmente por razones estéticas (46%) o reconstructivas (38%); en el 94%, se utilizó implante texturizado, las manifestación principal fue el edema o inflamación (82%), el promedio de tiempo entre la colocación de implante y diagnóstico fue de 11 años y se realizó remoción del implante afectado en el 100% de los casos. También, se evidenció que se realizó capsulectomía en el 94% de los casos y mastectomía en la población restante; no hubo afectación de ganglios axilares en un 75%; solo el 37%, 39% y 4%, recibieron radioterapia, quimioterapia e inmunoterapia, respectivamente11. El 76% se ubicó entre estadio 1a - 1c, tuvieron un promedio de seguimiento de 19 meses y el 69% reportó estar libre de enfermedad a los 18 meses. Dentro de los estudios analizados, se encontró un rango de recurrencia entre un 4.3% - 26% a 26 meses y de supervivencia a cinco años entre un 72 - 100%. En un análisis por supervivencia, se encontró mayor probabilidad de supervivencia general en aquellos sometidos a cirugía completa y radioterapia: alrededor del 70% y mayor supervivencia libre de enfermedad en aquellos en estadio I: 40%, aproximadamente11.
En este orden de ideas, aunque la evidencia disponible, casi en su totalidad, consiste en reporte de casos y serie de casos, se ha encontrado un patrón útil en la identificación y seguimiento de casos, como lo es el antecedente de colocación de implante texturizado, tiempo promedio entre la colocación del implante y el inicio de manifestaciones: entre 8 a 12 años aproximadamente. Las principales manifestaciones: edema o inflamación en piel sugestiva de seroma tardío, masa en mama, masa extensa en pared torácica o afectación de ganglios, los estadios más frecuentes al momento del diagnóstico (de I a III), la intervención más frecuente fue la capsulectomía completa con vaciamiento ganglionar y utilización de radioterapia y quimioterapia. La tasa de recurrencia es relativamente baja, y la supervivencia general es favorable, comparable con otro tipo de canceres. Sin embargo, se debe tener en cuenta que el LACG-AIM no es el único tipo de neoplasia asociado a implante, sino que también se han descrito otros como el carcinoma escamocelular.
Perspectivas futuras
Actualmente, existen estudios en ciencias básicas e investigación traslacional que estudian las modificaciones en las superficies de implantes, para intentar mejorar la biointegración y biocompatibilidad, que evite la respuesta alérgica e inflamatoria, que induzcan los cambios celulares adaptativos que promuevan la neoplasia, especialmente a nivel de la contractura capsular y biocapas39,40. Aunque la características y actividad inmune son variables de acuerdo a la biocapa formada, también se debe considerar que el microbioma varía entre zonas y regiones, por lo que la patogénesis de este cáncer también es dependiente de este ambiente, y debe estudiarse con mayor profundidad la interacción de microorganismos en esta biocapa40.
Aún se desconoce mucho sobre el cáncer asociado a implante mamario, ya sea LACG-AIM, carcinoma escamocelular u otro tipo de canceres, sobre factores de riesgo, fisiopatología, factores pronósticos, entre otros. Considerando que el cuidado del cáncer de mama y la investigación sobre estrategias para el control de la carga de enfermedad por este tipo de neoplasia maligna es un tópico de interés en nuestra región41,42, se debe impulsar el diseño de estudios que permitan caracterizar y determinar los factores asociados al desarrollo y pronóstico de esta entidad en población latina43, para diseñar algoritmos de toma de decisiones adaptados al contexto sociodemográfico y de salud de Latinoamérica y el caribe e impactar de forma eficaz sobre la población a riesgo en este continente.
CONCLUSIONES
El cáncer asociado a implante mamario es una enfermedad cada vez más frecuente, debido al aumento de intervenciones estéticas, la cual debe ser vigilada a largo plazo, de acuerdo al tiempo del curso de la historia natural de la enfermedad. Dentro de las consideraciones clínicas y quirúrgicas, se debe tener en cuenta el tipo del implante utilizado (texturizado), así como el del tiempo del antecedente del implante, la severidad de las manifestaciones y la estadificación para poder determinar la oportunidad de intervención quirúrgica y terapia neoadyuvante e intentar garantizar la supervivencia y evitar recurrencia. Aquellos pacientes sometidos a capsulectomía completa, acompañado de radioterapia, tienen mejores desenlaces, por lo que se debe considerar este tipo de protocolos para el manejo del LACG-AIM u otro cáncer asociado a implante mamario.











 texto en
texto en