INTRODUCCIÓN
La pandemia causada por el coronavirus tipo 2 induce el síndrome respiratorio agudo severo (SARS-CoV-2) y causa la COVID-19 1. Al momento de este estudio, el Perú atravesaba por una segunda ola, con mayor índice de letalidad e ingreso a las unidades de cuidados intensivos (UCI) debido a las nuevas variantes del virus 2-4). Al mismo tiempo, la población comenzó a vacunarse, lo que disminuyó no solo las muertes sino también las estancias hospitalarias y, por el lado de la ciencia, se generó el interés por conocer lo que sucede con los mecanismos básicos del sistema inmune ante este estímulo vacunal. Un evento importante es la tormenta de citocinas IFN-α, IFN-γ (interferones tipo alfa y gamma), IL-1β, IL-6 (interleucinas tipo 1 beta y 6), TNF-α (factor de necrosis tumoral tipo alfa) entre otras) inducida por el virus, pero promovida por distintas células inmunes, lo que lleva a reacciones hiperinflamatorias y procoagulantes. 5-8
El incremento de TNF-α en adultos mayores puede inducir apoptosis en los linfocitos T (LT) 9. La linfopenia observada en COVID-19 podría predecirse con los niveles de TNF- α. 10
La inmunidad adaptativa es un poco más lenta, ya que requiere reconocimiento, procesamiento, presentación y activación del sistema de linfocitos 11. La inmunidad adaptativa celular no solo es importante porque los LT CD4+ estimulan la respuesta por LT CD8+ antivirales, sino también porque colaboran con la producción de anticuerpos a través de un mecanismo T-dependiente 12,13. Diao et al. 14, demostraron que en pacientes con COVID-19 se presenta una disminución de LT totales y subpoblaciones CD4+ y CD8+, además esta disminución tuvo correlación negativa con las concentraciones en suero de TNF- α, IL-6 e IL-10. Tal disminución podría promoverse por una sobre expresión de TNF-α. 15,16
Por otro lado, el agotamiento celular de LT aparece ante la persistencia de antígenos en infecciones virales o cáncer y produce falla en el desarrollo de LTCD8+ de memoria y un deterioro en las funciones de LTCD8+ efectores 17. En la fase aguda y convaleciente de la COVID-19 el agotamiento celular se caracteriza por la pérdida gradual y progresiva de las funciones celulares; expresión sostenida de receptores inhibidores o ¨checkpoints¨ PD-1(Receptor de muerte celular programada tipo 1), CTLA-4 (Antígeno 4 de linfocito T citotóxico), NKG2A (Subfamilia K de receptores similares a lectina de células NK) entre otros; cambios en el panorama epigenético-transcripcional y reprogramación metabólica 17-22. En la COVID-19 se presentan altos porcentajes de LT, CD8+PD-1+ y CD4+PD-1+ con altos niveles de PD-1, lo que demuestra que el SARS-CoV-2 induce el agotamiento celular. 21,23,24
En la COVID-19 existe linfopenia y pérdida de la funcionalidad de los linfocitos totales 21,23,25,26. Diao B et al. 23, reportaron que el 82,1% de pacientes con la COVID-19 tenían linfopenia, además, 522 casos tenían alta producción de PD-1 y Tim-3 (inmunoglobulina de células T que contiene dominio de mucina-3) en LT CD4+ y CD8+ . Por tanto, es importante investigar el grado de agotamiento celular en personas vacunadas. Además, debido al rol cooperador de los LT sobre la producción de anticuerpos, la disminución de los niveles de LT afectaría indirectamente los niveles de anticuerpos IgG. Bajo este contexto, el objetivo del estudio fue evaluar el comportamiento de los niveles de TNF-α, anticuerpos IgG y poblaciones de LT, incluyendo su agotamiento celular, antes y después de la tercera dosis de la vacunación contra el SARS-CoV-2.
MATERIAL Y MÉTODOS
Estudio exploratorio; los participantes fueron enrolados por el equipo de investigación del Laboratorio de Inmunología # 108 - LID - FACI - UPCH. Los criterios de inclusión fueron: 1. Varones o mujeres mayores de 18 años; 2. Con o sin comorbilidades; 3. Grupo G1 (n=07), contó con un esquema de vacunación de primera y segunda dosis con la vacuna de BNT162b2, tuvo infección entre 0 y 4 meses postvacunación y además recibió una tercera dosis de la misma vacuna; 4. Grupo G2 (n= 08), similar al G1 pero sin infección y 5. Grupo G3 (n=10), similar al grupo G2, pero con tercera dosis de la vacuna ChAdOx1-S. Aunque los G2 y G3 no tuvieron infección, se les catalogó como asintomáticos debido a que no fue posible comprobar la no infección con pruebas antigénicas.
Obtención de muestras
Se obtuvieron muestras de sangre periférica de 25 personas, las cuales se colectaron antes y después de la tercera dosis de vacunación. A partir de estas muestras se obtuvo el suero y se aislaron las células mononucleares de sangre periférica (PBMC). Los sueros fueron almacenados a -20 ºC hasta el momento de las mediciones y las PBMC se procesaron inmediatamente.
Ensayo inmunoabsorbente ligado a enzima (ELISA) en suero humano
Se usaron dos tipos de ELISA cuantitativos, uno indirecto, para medir la concentración de los anticuerpos IgG anti-SARS-CoV-2 (EDITM Novel Coronavirus COVID-19 IgG ELISA kit, USA), micropozos revestidos con la proteína recombinante de la nucleocápside (N) y otro tipo sándwich, para medir la concentración de la citocina TNF-α (BD OptEIATM Human TNF ELISA kit II, USA). En ambos casos, se siguieron estrictamente las indicaciones del fabricante.
Citometría de flujo
Las muestras de sangre periférica fueron obtenidas en tubos con EDTA, las PBMC fueron obtenidas por gradiente de centrifugación y sembradas por 24h a 37°C y 5% CO2 sin otro estímulo adicional. Los porcentajes linfocitarios y el agotamiento celular de LT fueron detectados usando 100µl de PBMC, los que fueron coloreados con anticuerpos CD3-PerCp (Cat347344/SK7); CD4-FITC (Cat561842/RPA-T4); CD8-APC (Cat561953/RPA-T8) y PD-1-PE (Cat557946/MIH4), todos de BD Biosciences, USA. Después de la tinción, las PBMC fueron medidas por citometría de flujo en un analizador celular FACSCalibur (BD Biosciences) y los datos fueron analizados con el paquete de prueba gratis FlowJo ™ v10 del Laboratorio de Inmunología.
La estrategia del análisis de citometría de flujo consistió en determinar la población de linfocitos totales por tamaño y granularidad (FSC/SSC) (gráfico 1A); determinación de LT (SSC/CD3+) (gráfico 1B); a partir de la región o ¨gate¨ de los LT CD3+ se determinaron las subpoblaciones de LT citotóxicos (CD8+CD4-) y helper (CD8-CD4+) (gráfico 1C) y a partir de cada subpoblación se determinó porcentualmente el nivel de agotamiento celular a través de PD-1, es decir, CD8+PD-1+ y CD4+PD-1+ (gráfico 1D y 1E).
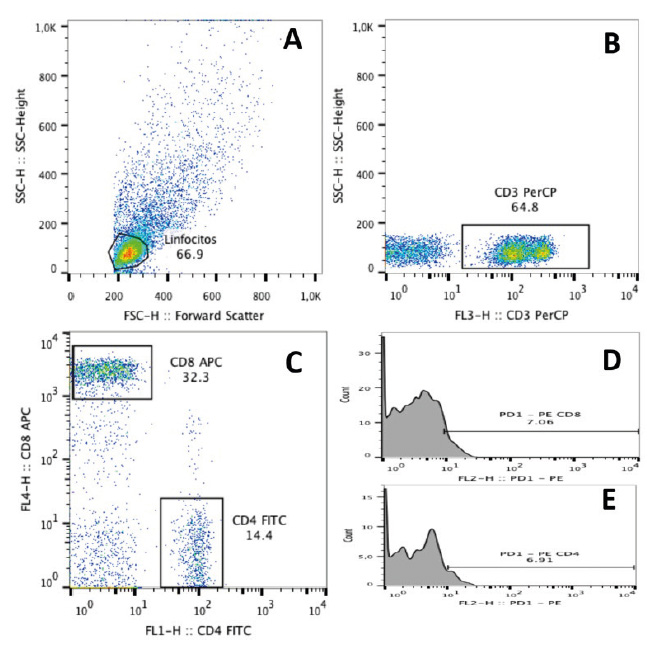
Gráfico 1 Estrategia de análisis de citometría de flujo. A. Determinación de la población de linfocitos totales (T, B y NK) de acuerdo con su tamaño y granularidad (FSC/SSC). B. A partir del gating o región de linfocitos totales, se determinó la población de LT (SSC/CD3+) de acuerdo con su granularidad (SSC) y la señal de fluorescencia del fluorocromo CD3-PerCP. C. Mediante gatings o regiones de cuadrados, se seleccionaron las subpoblaciones de LT, CD8+CD4- y CD8-CD4+. D y E. A partir de cada subpoblación de LT se realizó una gráfica de histograma que representa el porcentaje de LT, CD8+PD-1+ y CD4+PD-1+, respectivamente. El análisis fue realizado con FlowJo X 10.0.7.
Análisis estadístico
Se usó el paquete de prueba gratis GraphPad versión 9 del Laboratorio de Inmunología. Se realizó la prueba de normalidad de Shapiro-Wilk para estimar la distribución de los datos. Cuando los datos de las variables a evaluar pasaban la prueba de normalidad (p>0,05) se eligieron pruebas paramétricas como la prueba t pareada (igual cantidad de datos por grupos a comparar) o no pareado (diferente cantidad de datos por grupos a comparar) y el ANOVA de una vía o ¨one way ̈ seguido de la prueba de Tukey para comparaciones múltiples y cuando no pasaban la prueba de normalidad (p<0,05) se eligieron pruebas no paramétricas como la prueba de Wilcoxon. Adicionalmente, cuando fue necesario, se aplicó la prueba de ¨outliers¨ para descartar los valores que no seguían el comportamiento de los grupos evaluados. Para graficar los resultados se realizaron gráficas de de violín y gráficas de símbolos y líneas. En todos los casos se determinaron valores de mediana con intervalos de confianza al 95%. La correlación estadística fue evaluada con la prueba de Pearson cuando los datos de las variables seguían una distribución normal y con la prueba de Spearman cuando los datos de las variables no seguían una distribución normal. En ambos tipos de correlaciones se tomó en cuenta el valor de r (Rho) para un intervalo de confianza del 95% y la significancia estadística (p<0,05).
RESULTADOS
Niveles de anticuerpos IgG (anti-N) antes y después de la tercera dosis de vacunación
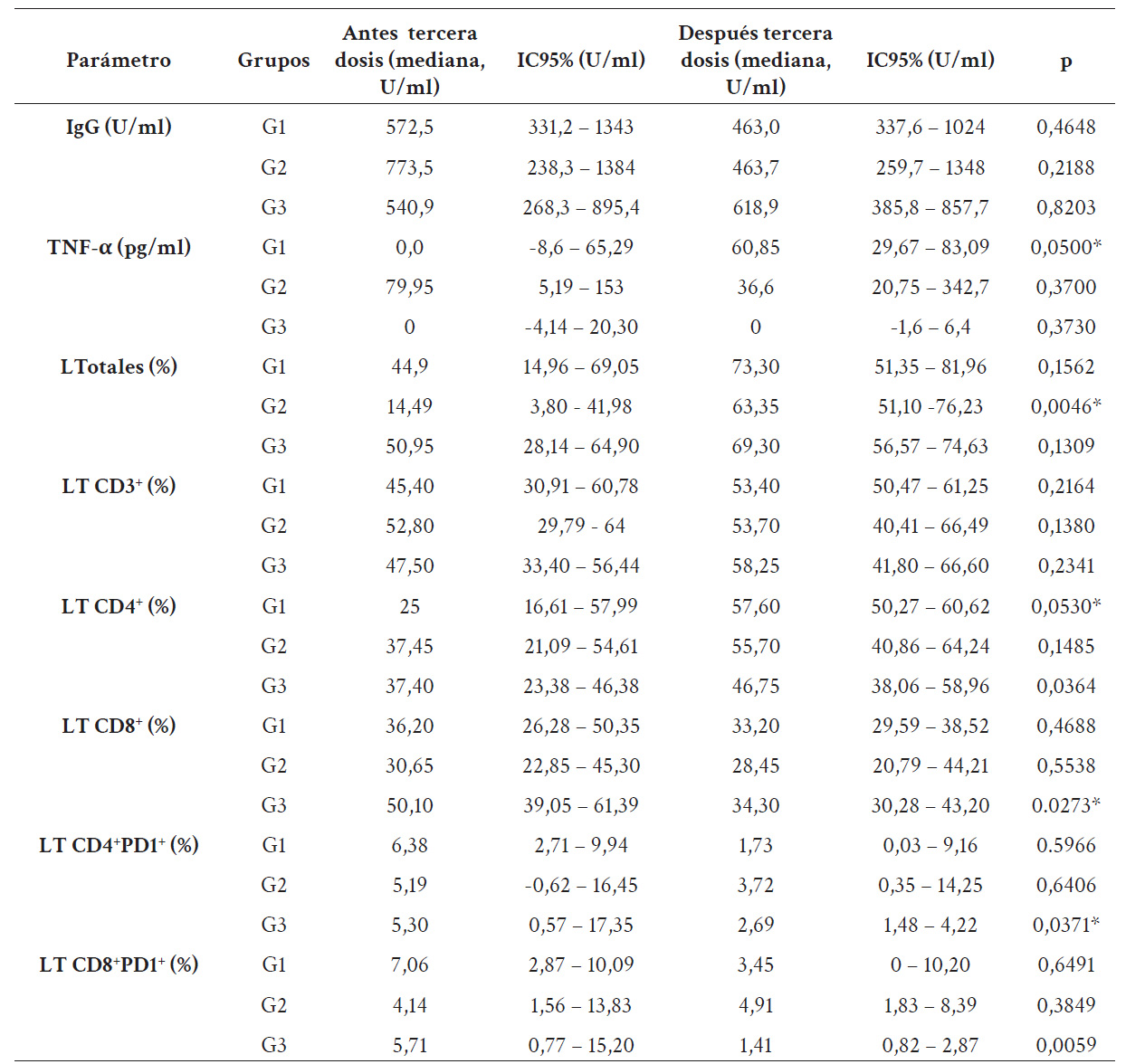
En G1 fue 572,5 U/ml; IC95% 331,2-1343 y 463,0 U/ml; IC95% 337,6-1024,0 antes y después, respectivamente; en G2 fue 773,5 U/ml; IC95% 238,3-1384,0 y 463,7 U/ml; IC95% 259,7-1348,0 y en G3 (540,9 U/ml; IC95% 268,3-895,4 y 618,9 U/ml; IC95% 385,8-857,7 no se encontró diferencia estadísticamente significativa en la mediana de concentración de anticuerpos IgG anti-nucleocápside antes y después de la tercera dosis de vacunación. La mediana del tiempo transcurrido entre antes y después de la vacunación fue G1= 42 días (IC95% 30 - 122 días); G2= 89 días (IC95% 26 - 136 días) y G3= 47,5 días (IC95% 27-135 días) (gráfico 2, tabla 1).
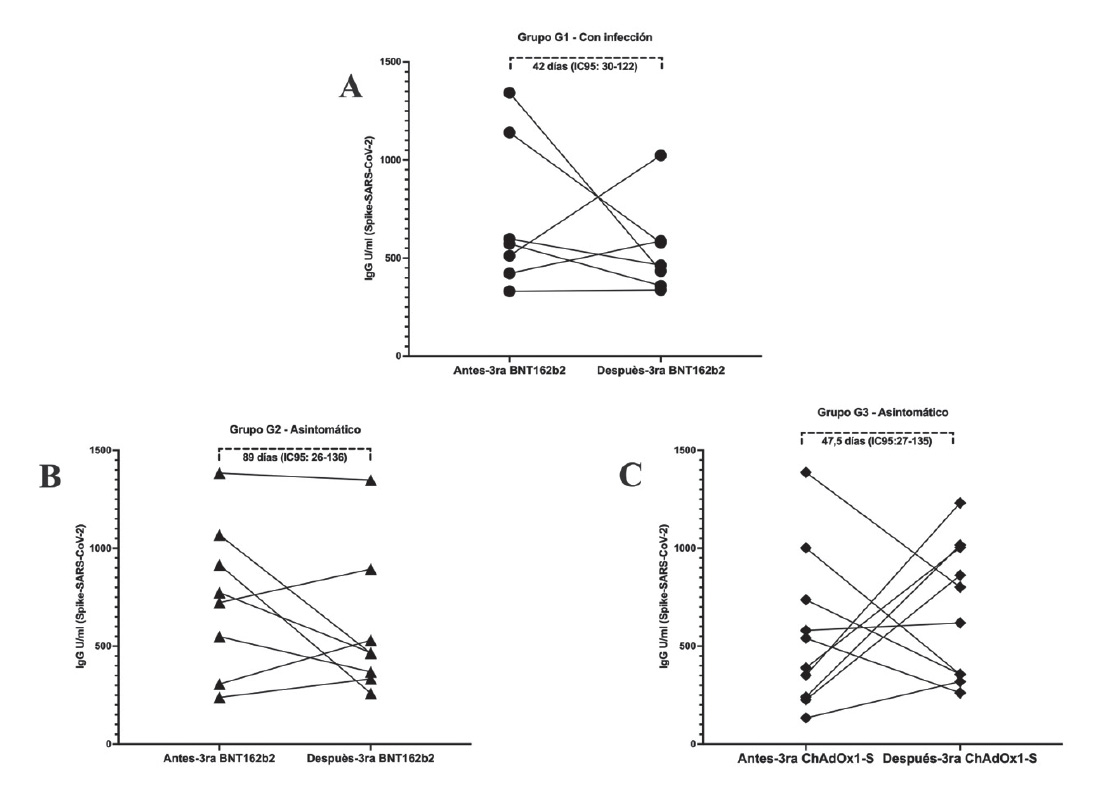
Gráfico 2 Anticuerpos IgG (anti-N-SARS-CoV-2) antes y después de la tercera dosis de vacunación. Concentración de IgG (U/ml) mediante ELISA en suero antes y después de la tercera dosis de vacunación A. G1, n=07. Luego de 0 a 4 meses de haber tenido infección, recibieron la tercera dosis de la vacuna BNT162b2. B. G2, n=08. Al momento de la tercera dosis de la vacuna BNT162b2 no tenían infección (asintomáticos). C. G3, n=10 al momento de la tercera dosis de la vacuna ChAdOx1-S no tenían infección (asintomáticos). Se indica la mediana y el IC95% de los días transcurridos entre las tomas de muestra.
Niveles de TNF-α antes y después de la tercera dosis de vacunación
Únicamente el grupo G1 presentó una diferencia estadísticamente significativa (p=0,05) con una mediana de la concentración de TNF-a mayor después de la tercera dosis (0 pg/ml; IC95%: -8,6-65,29 vs 60,85 pg/ml; IC95% 29,67-83,09); mientras que en los grupos G2 (79,95 pg/ml; IC95% 5,19-153 vs 36,36 pg/ml; IC95% -20,75-342,7) y G3 (0 pg/ml; IC95% -4,14-20,30 vs 0 pg/ml; IC95% -1,6-6,4) no hubo diferencia entre las medianas antes y después de la tercera dosis (gráfico 3, tabla 1).
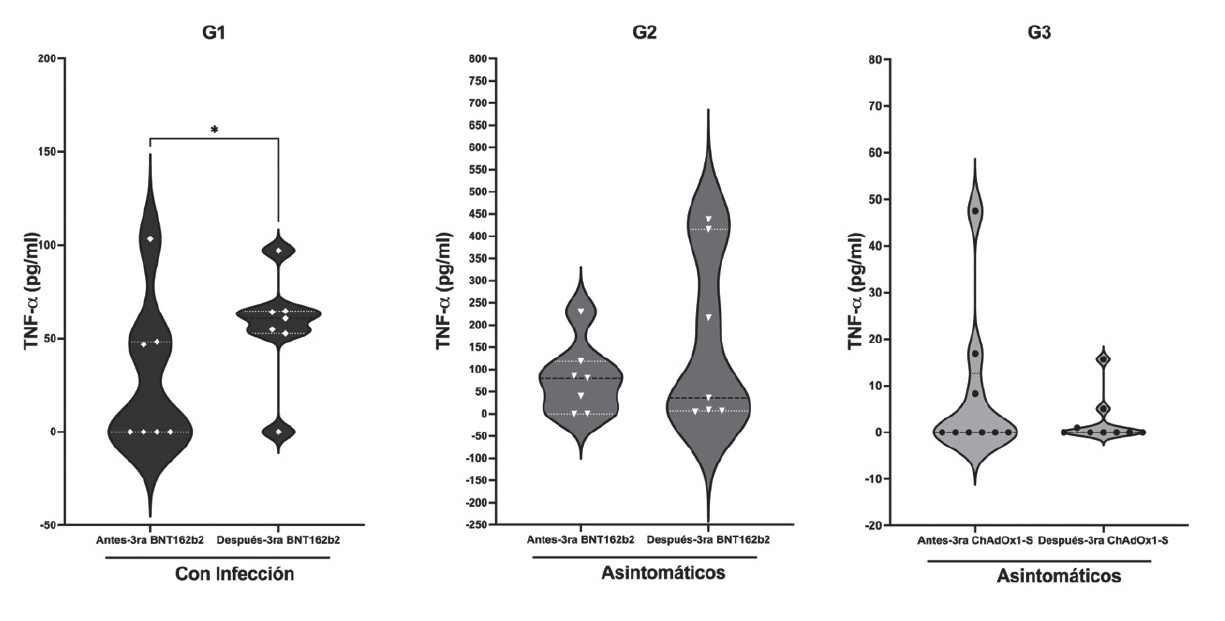
Gráfico 3 TNF-α antes y después de la tercera dosis de vacunación. Concentración de TNF-α (pg/ml) mediante ELISA en suero obtenido antes y después de la tercera dosis de vacunación. Donde G1, n=07 luego de 0 a 4 meses de haber tenido infección recibieron tercera dosis de la vacuna BNT162b2; G2, n=08 al momento de la tercera dosis de la vacuna BNT162b2 no tenían infección (asintomáticos) y G3, n=10 al momento de la tercera dosis de la vacuna ChAdOx1-S no tenían infección (asintomáticos). Significancia estadística si * p<0,05, Prueba t pareada. Se representa la línea mediana de concentración de TNF-α y los límites superior e inferior representan el intervalo de confianza al 95% en gráficos de violín.
Niveles porcentuales de linfocitos totales (T, B y NK), LTCD3+, subpoblaciones CD4+ y CD8+ y su agotamiento celular PD-1+
El porcentaje de linfocitos totales aumentó significativamente después de la tercera dosis en el grupo G2 (gráfico 4A); no se encontró diferencia en los LT en los grupos de vacunación (gráfico 4B); los porcentajes de LT helper aumentaron y los citotóxicos disminuyeron significativamente (gráfico 4C y D); mientras que el nivel porcentual de agotamiento celular (PD-1+) de ambas subpoblaciones disminuyó significativamente después de la vacunación en el grupo G3 (gráfico 4E y F, tabla 1).
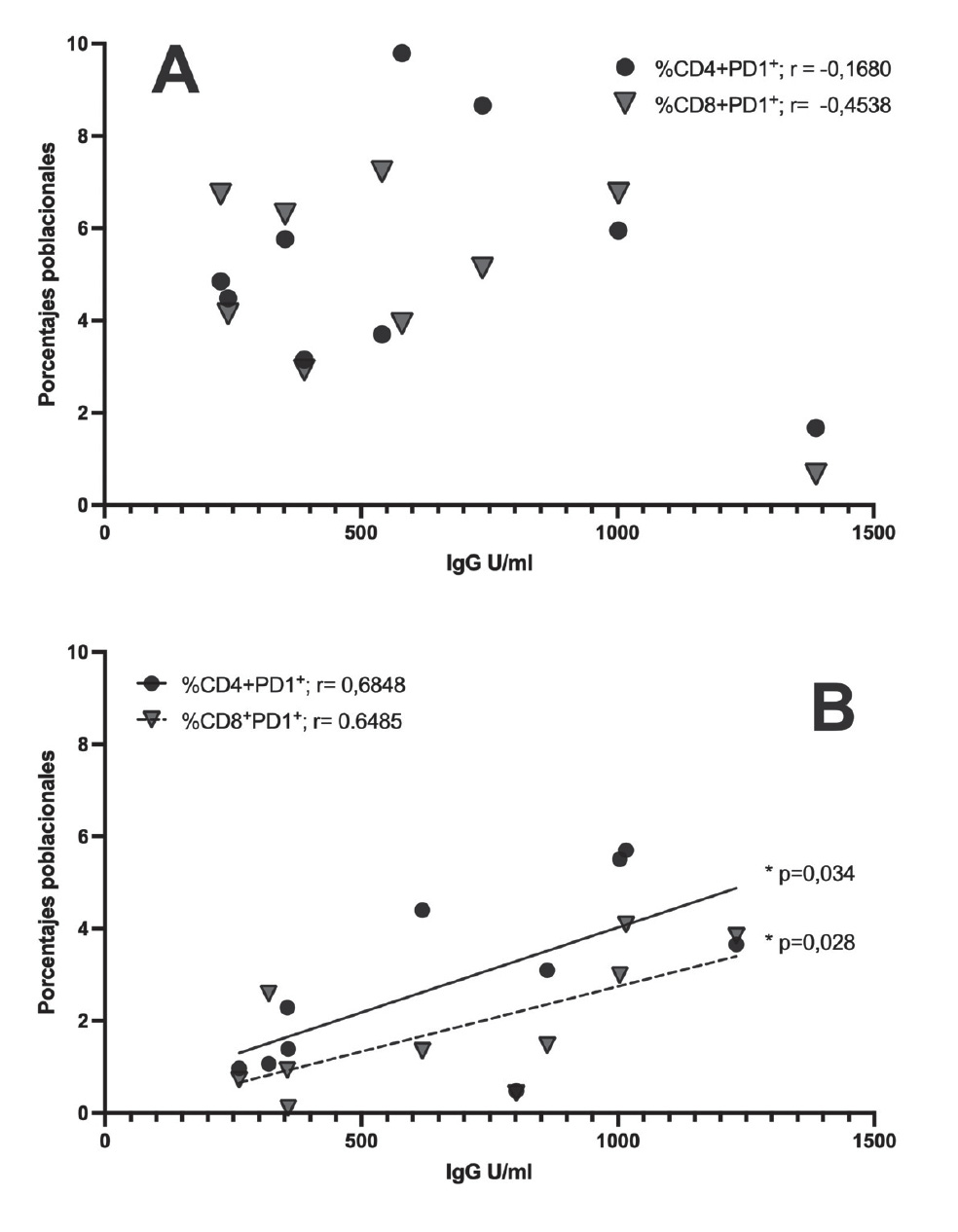
Gráfico 4 Porcentajes de linfocitos totales, LT, subpoblaciones y su nivel de agotamiento celular antes y después de la tercera dosis de vacunación. Porcentajes poblacionales de linfocitos según los parámetros de tamaño y granularidad (FSC/SSC) para linfocitos totales (A) y fluorescencia para LT, CD3+ (B), subpoblaciones CD4+ (C) y CD8+ (D) y agotamiento celular PD-1+ (E y F) antes y después de la tercera dosis de vacuna. Donde G1, n=07 luego de 0 a 4 meses de haber tenido infección, recibieron tercera dosis de vacuna BNT162b2; G2, n=08 al momento de la tercera dosis de vacuna BNT162b2 no tenían infección (asintomáticos) y G3, n=10 al momento de la tercera dosis de vacuna ChAdOx1-S no tenían infección (asintomáticos). Significancia estadística si * p<0,05 o ** p<0,01. Prueba T pareada (A), G2; (C y D), G3 y Prueba de Wilcoxon pareada (E y F), G3. Se representa la línea mediana de concentración del porcentaje poblacional y los límites superior e inferior representan el intervalo de confianza al 95% en gráficos de violín.
Correlación entre IgG (anti-N), TNF-α y poblaciones linfocitarias antes y después de la tercera dosis de vacunación
Se realizó la correlación estadística entre las variables IgG vs. TNF-a; IgG vs. LTCD3+/CD4+/CD8+ e IgG vs. LTCD4+PD-1+/LTCD8+PD-1+ (datos no publicados). Únicamente se encontró una correlación positiva estadísticamente significativa después de la tercera dosis de vacunación en el grupo G3 entre la concentración de anticuerpos IgG y las subpoblaciones de CD4+PD-1+ (p=0,034; r=0,6848) y CD8+PD-1+ (p=0,028; r=0,6485), respectivamente (gráfico 5).
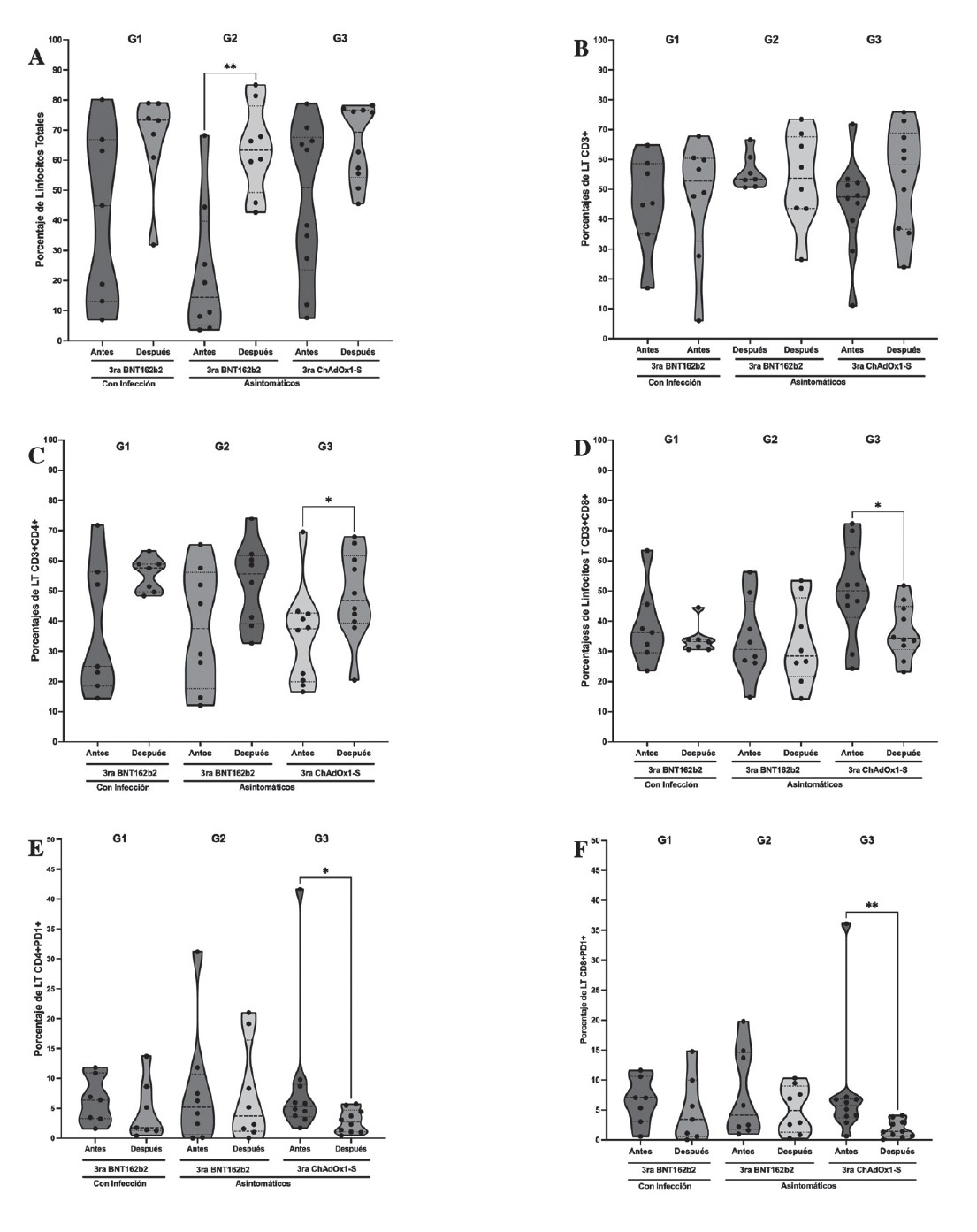
Gráfico 5 Correlación entre la concentración de anticuerpos IgG (anti-N-SARS-CoV-2) y los porcentajes poblaciones de LT, CD4+PD-1+ y CD8+PD-1+ después de la tercera dosis de vacunación. Correlación estadística de Pearson entre la concentración de IgG (U/ml) y los porcentajes de CD4+PD-1+ y CD8+PD-1+, respectivamente antes (A) y después (B) de la tercera dosis de vacuna. G3, n=10 al momento de la tercera dosis de vacuna ChAdOx1-S no tenían infección (asintomáticos). Significancia estadística si p<0,05; Rho (r) para un intervalo de confianza de 95%.
DISCUSIÓN
El estudio es de tipo exploratorio y pretende contar con evidencia que permita ahondar en el estudio de los mecanismos inmunes afectados antes y después de la tercera dosis de vacunación homóloga o heteróloga contra el SARS-CoV-2.
En el análisis individual de las variables medidas se encontró un aumento estadísticamente significativo de TNF-α después de la tercera dosis de la vacuna de BNT162b2 en G1; sin embargo, analizando el valor estadístico de p=0,05 y el tamaño muestral bajo llegamos a la conclusión que no se puede aseverar certeramente el resultado de que la vacuna induce el aumento de una citocina pro inflamatoria, el que es posible que sea un rezago de la etapa de infección con SARS-CoV-2 por la que atravesó el grupo G1 (tuvo infección entre 0 a 4 meses después de las dos primeras dosis de la vacuna de BNT162b2). Otro aspecto a tener en cuenta es que, los niveles encontrados son tan bajos (<100pg/ml) que no se puede atribuir a esta citocina un efecto tal como un shock tóxico e inflamación o agotamiento celular sobre células como los LTCD4+ como lo indican Aguillón JC. et al. 23 y Diao B. et al. (27, respectivamente.
La concentración de anticuerpos IgG (anti-N) en todos los grupos de vacunación no cambió después de la tercera dosis de vacuna, lo que significa que al menos en la mediana de tiempo de los tres grupos (47,5 días; IC95% 42-89 días) los niveles de anticuerpos se mantienen y pueden proteger a los vacunados independientemente del esquema de vacunación. Nuestro resultado concuerda con los estudios sobre la cinética de anticuerpos inducidos por la vacunación que indican que después de las dos primeras dosis se alcanza un pico de producción de anticuerpos que con un booster o tercera dosis se puede mantener títulos constantes de anticuerpos. 28
La evaluación de los niveles porcentuales de LT indica que el mejor esquema de vacunación es el G3 o heterólogo, en el que después de la administración de la vacuna de ChAdOx1-S se incrementan los LT helper, que son vitales para sostener la respuesta de anticuerpos y LT citotóxicos, pero además reduce el agotamiento celular de ambas subpoblaciones de LT, lo que mejoraría la respuesta celular contando con células con señales de coestimulación activen más eficientemente cuando el sistema inmune se enfrente a una infección por SARS-CoV-2.
En este estudio exploratorio se planteó la posibilidad de la existencia de una correlación entre las variables del eje IgG-TNF-α-LT, en la que la inducción de TNF-α podría causar linfopenia con lo que habría una disminución o agotamiento celular de LT, que a su vez afectaría la producción de anticuerpos antivirales. Únicamente se encontró que a mayor concentración de IgG (anti-SARS-CoV-2) mayor agotamiento celular en las subpoblaciones porcentuales de LT. Este resultado es contradictorio porque se esperaría que los LT mejoren su nivel de activación, pero el incremento de células PD-1+, una molécula inhibidora de la activación del LT, indicaría lo contrario; sin embargo, para corroborar esta hipótesis se tendría que evaluar LT-antígeno específicos contra SARS-CoV-2. Esta contradicción en el agotamiento celular de subpoblaciones de LT cuando se evalúan individualmente o comparados a una variable como la concentración de IgG anti-SARS-CoV-2 se debería dilucidar con LT antígeno-específicos a SARS-CoV-2, ya que es posible que LT que presentan mayor agotamiento celular a mayor concentración de IgG anti-SARS-CoV-2 se deba a LT con otras especificidades. De comprobarse este agotamiento celular antígeno-específico, se podría corregir la falta de funcionalidad de los LT con inmunoterapia con anticuerpos monoclonales anti-PD-1 en el tratamiento de la COVID-19, como lo experimentó Roy S. et al. 29 en un modelo animal de herpes ocular.
En personas con cáncer, los efectos de la vacunación (Sinopharm) sobre el tratamiento anti-PD-1 no son afectados y, más bien, la administración de ambos mejora las señales coestimuladoras y reduce la regulación co-nhibidora. 30
Tras los resultados obtenidos, se plantea la pregunta si es necesario, medidas profilácticas adicionales como el uso de anticuerpos monoclonales, además de las dosis de refuerzo. Existen LT que aumentan su nivel de agotamiento celular y, por lo tanto, la investigación futura es importante para determinar la respuesta inmune a largo plazo a dosis adicionales de la vacuna.
Dentro de las principales limitaciones de este estudio se encuentran, no haber podido catalogar laboratorialmente como sujetos sin infección a los grupos G2 y G3, limitándonos a describir lo indicado por el donante, por tal razón, preferimos denominarlos asintomáticos; el bajo tamaño muestral, lo que probablemente influye en las diferencias estadísticas encontradas particularmente en la medición de TNF-α (G1) donde a pesar de existir una diferencia significativa (p=0,05), el valor limítrofe impide concluir con certeza un evento pro inflamatorio postvacunación en el grupo G1. Es posible que se requieran más puntos de medición en el tiempo para las variables, concentración de anticuerpos y citocinas. Además, de TNF-α sería interesante medir otras citocinas proinflamatorias como IL-6 e IL-1. En el caso de IL-6 se conoce su influencia sobre la producción de anticuerpos; sin embargo, con este estudio se abren nuevas vías de estudio en la infección por SARS-CoV-2.
En conclusión, en este estudio exploratorio se observó que el esquema de vacunación heterólogo del grupo G3 fue el mejor, ya que incrementó los niveles de LT CD4+, una subpoblación que sostiene la inmunidad adaptativa antiviral y evitó el agotamiento celular de las subpoblaciones de LT con lo que se evidencia una mejora de la respuesta inmune celular; sin embargo, es posible que el costo de mantener el nivel de anticuerpos se correlacione positivamente con el agotamiento celular de las subpoblaciones de LT. Ninguno de los esquemas de vacunación modificó significativamente la respuesta humoral (IgG) e inflamatoria (TNF-α), manteniéndolas en un nivel de normalidad frente a la vacunación.