INTRODUCCIÓN
La pandemia de COVID-19 ha tenido un impacto significativo en América Latina y en Perú, con altas tasas de contagio y mortalidad 1. Desde el primer caso reportado en Brasil en febrero de 2020 y el primer fallecimiento en Argentina, la infección se propagó rápidamente en Latinoamérica. En Perú, el primer caso fue reportado el 6 de marzo de 2020, y desde entonces, el aumento de casos fue progresivo en las olas pandémicas 2.
La infección viral fue en sus inicios altamente transmisible y patogénica, e infectó a más de 607 millones de personas en todo el mundo, con más de 4,1 millones de casos en Perú 3. Los cuadros clínicos de la enfermedad fueron desde asintomáticos leves hasta graves. Los cuadros asintomáticos son los más inadvertidos, pero también pueden trasmitir activamente la enfermedad, lo que puede subestimar el impacto real de los casos positivos. Los fallecidos con diagnóstico de COVID-19 en el mundo superan los 6,5 millones, y en Perú, más de 216 mil fallecidos fueron reportados, lo que refleja el gran impacto en mortalidad que causó en el país 4.
Diversos países del mundo han realizado estudios de seroprevalencia para conocer el impacto de la pandemia, y se encontró que, hasta después de la primera ola pandémica, la mayoría de la población humana del mundo todavía era altamente susceptible a la infección por SARS-CoV-2. La inmunidad humoral ―determinada por la presencia de anticuerpos IgM/IgG― es un elemento importante en la evaluación de la inmunidad, y diferentes estudios de inmunidad en COVID-19 han mostrado una evolución de la inmunidad poblacional 5.
En este contexto, investigadores de la Dirección General de Donaciones, Trasplantes y Banco de Sangre (DIGDOT), así como del Instituto Nacional de Salud (INS), realizaron esta investigación que estudió el comportamiento de la inmunidad humoral contra el SARS-CoV2 en las muestras de los donantes de sangre de los bancos de sangre de 6 establecimientos de salud de hospitales públicos del departamento de Lima.
MÉTODOS
Diseño del estudio
Realizamos un estudio observacional transversal. Se analizó bases de datos que describían la presencia de anticuerpos IgM/IgG contra SARS-CoV-2 determinados mediante inmunoensayo cromatográfico de flujo lateral (prueba rápida) en muestras de sangre de donantes sanos y asintomáticos a COVID-19 obtenidas en 6 bancos de sangre de Lima. El estudio fue realizado en coordinación con la Dirección de Banco de Sangre y Hemoterapia (DIBAN) de la Dirección General de Donaciones, Trasplantes y Banco de Sangre (DIGDOT).
Evaluación serológica
La prueba rápida utilizada corresponde a la marca Cellex q Rapid Test del fabricante Cellex Biotech. La prueba denominada cassette Cellex qSARS-CoV-2 IgG/ IgM permite la detección cualitativa de anticuerpos IgM/IgG contra el SARS-CoV-2 en muestras de suero. Esta prueba rápida contiene antígenos recombinantes de SARS-CoV-2 conjugados con oro coloidal (conjugados SARS-CoV-2) y conjugados IgG-oro de conejo, además, tiene una tira de membrana de nitrocelulosa que contiene una línea IgG (línea G) recubierta con anticuerpos anti-IgG humana, una línea IgM (línea M) recubierta con un anticuerpo anti-IgM humano, y la banda C (Control) está cubierta previamente con IgG de cabra anti-conejo 6. Según su fabricante esta prueba rápida tiene una sensibilidad de 93,75% (IC95%: 88,06% a 97,26%) y una especificidad de 96,40% (IC95%: 92,26% a 97,78%) para IgG, IgM o ambas 7.
Además, el INS realizó un reporte técnico de verificación de estas pruebas rápidas, encontrando sensibilidad diagnóstica de 93,33% para IgM, y de 100% para IgG; especificidad diagnóstica de 98% para IgM y de 98% para IgG; y especificidad analítica de 96,67% para IgM y de 100% para IgG. Para obtener la sensibilidad y especificidad diagnóstica, se evaluaron 30 muestras de suero y plasma de personas clínicamente diagnosticadas con 7 días de haber iniciado la sintomatología a COVID-19 y con resultado positivo a RT-PCR en tiempo real para SARS-CoV-2 y 50 muestras de suero y plasma de personas sin sintomatología con resultado negativo a RT-PCR en tiempo real para SARS-CoV-2. Para la especificidad analítica se evaluaron 25 muestras de suero sanguíneo positivos a 7 etiologías infecciosas (Treponema pallidum, Dengue, Zika, VIH, HTLV, Citomegalovirus, Malaria) y 5 muestras de gestantes reactivas a sífilis.
Población y muestra
Se utilizaron 44 477 kits de pruebas rápidas cassette Cellex qSARS-CoV-2 IgG/ IGM, de los cuales 591 (1,3%) resultaron ser repeticiones y/o pruebas inválidas, debido al estado de conservación de la muestra. Finalmente, se obtuvo 43 886 resultados válidos de muestras de sangre de donantes entre el 01 de abril del 2020 y el 30 de junio del 2022. Los datos de estas muestras provienen de la seroteca de los bancos de sangre de los establecimientos de salud: Hospital Nacional Arzobispo Loayza, Hospital Nacional Hipólito Unanue, Hospital General de Huacho, Hospital Nacional Sergio Enrique Bernales, Hospital Emergencia Ate Vitarte y Hospital Nacional Luis N. Saénz (Hospital PNP) pertenecientes al departamento de Lima. Todas las muestras de donantes de sangre fueron evaluadas con la prueba rápida.
Criterios de inclusión y exclusión
Fueron incluidos donantes de sangre, aparentemente sanos de entre 18 y 70 años, libres de síntomas recientes posiblemente relacionados con COVID-19. Los donantes fueron sometidos a una entrevista clínica, evaluación médica, historia clínica y análisis de laboratorio descritos en la «Guía Técnica para la Selección del Donante de Sangre Humana y Hemocomponentes» aprobada por la Resolución Ministerial N°241-2018/ MINSA, y modificada por las Resoluciones Ministeriales N°440-2018/MINSA y N°129-2020-MINSA. Los criterios de exclusión fueron las muestras de sueros con volumen menores a 300 uL, muestras de donantes sanos cuya edad no podía confirmarse por errores de digitación en el sistema y otras muestras que no contaron con la información demográfica del donante de sangre.
Análisis estadístico
Los datos de los donantes de sangre con los resultados de las pruebas inmunocromatográficas fueron recogidos en una hoja de cálculo (Excel) y analizados en el programa STATA versión 17®. Se realizó la limpieza de los datos, posteriormente se analizaron de forma descriptiva las variables cualitativas con proporciones y porcentajes. Como pruebas estadísticas se usó la chi cuadrado de tendencia con un nivel de significancia de 0,05. Los gráficos y tendencias de seroprevalencia se evaluaron utilizando el software de análisis estadístico R 3.5.2 (https://www.r-project.org/).
Consideraciones éticas
El protocolo de estudio fue aprobado por el Comité Institucional de Ética en Investigación del Instituto de Medicina Tropical “Daniel Alcides Carrión” de la Universidad Nacional Mayor de San Marcos (Constancia de Aprobación N° CIEI-202311). Se trabajó con datos secundarios anonimizados. Los donantes de sangre llenaron un consentimiento informado antes de la toma de muestra en donde aceptaban donar su muestra de sangre para fines médicos terapéuticos y de investigación.
RESULTADOS
Entre las 43 886 muestras de donantes de sangre el 71,8% fueron de varones. El 39,4% de donantes tuvo 18 a 30 años, luego de 31 a 40 años con 32,1%, de 41 a 50 años con 20,5%, de 51 a 60 años con 7,8% y más de 60 años con 0,2% (Tabla 1).
Tabla 1. Características sociodemográficas y reactividad IgM/IgG de SARS-CoV-2 de los donantes de 6 bancos de sangre del departamento de Lima.
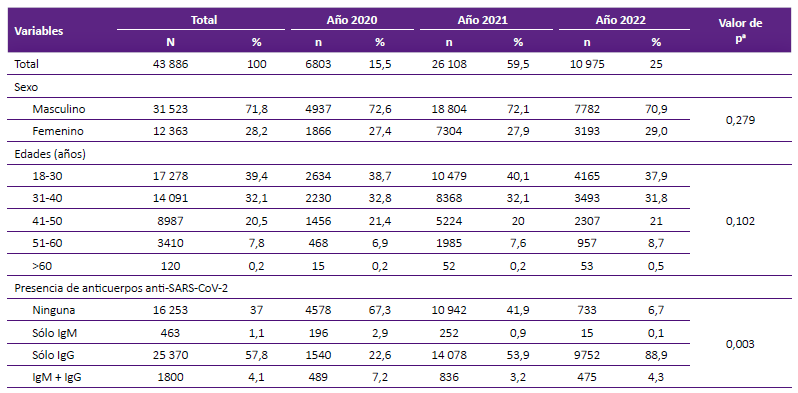
a Chi-cuadrado de tendencia.
La presencia de anticuerpos IgM de SARS-CoV-2 disminuyó con el tiempo: 2,9% en el año 2020, 0,9% en el año 2021 y 0,1% en el año 2022. Por otro lado, la presencia de anticuerpos IgG de SARSCoV-2 aumentó de 22,6% en el año 2020, 53,9% en el año 2021 y 88,9% en el año 2022 (Tabla 1). Se observó una mayor reactividad en la población de 51 a 60 años durante el 2021 con 69,4% y en mayores de 60 años CON 67,3%. En cuanto a la reactividad total, se observó un aumento progresivo de la presencia de anticuerpos IgM/IgG contra SARS-CoV-2, con 32,7% en el 2020, 58,1% en el 2021 y 93,3% en el 2022 (Tabla 2).
Tabla 2. Reactividad IgM/IgG de SARS-CoV-2 de los donantes de 6 bancos de sangre del departamento de Lima según grupos etarios
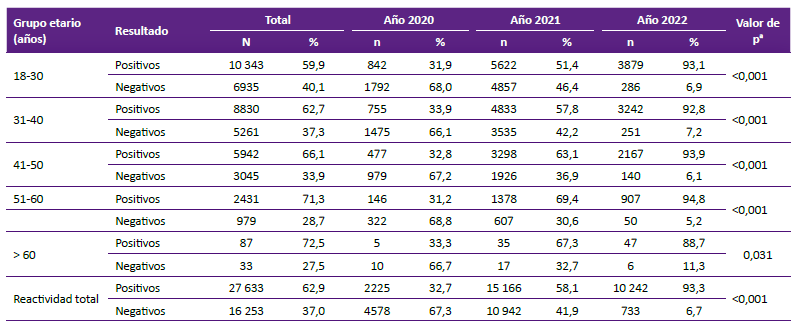
a Chi-cuadrado de tendencia.
En la figura 1 se muestra la evolución de la presencia de anticuerpos contra IgM e IgG de SARS-CoV-2, destacando un incremento progresivo en los niveles de anticuerpos IgG, a diferencia de los anticuerpos IgM, que se presentan en menor cantidad y muestran una tendencia decreciente. La figura 2 muestra la reactividad a IgG de las muestras evaluadas, evidenciándose un incremento progre-sivo de la seroprevalencia de COVID-19. La figura 3 muestra a los pacientes que resultaron reactivos únicamente a IgM de SARS-CoV-2, con un pico detectable de 2,9% durante el 2020 que disminuyó progresivamente en los años subsiguientes. Por último, la figura 4 evidencia el crecimiento total de la seroprevalencia, sobre las sucesivas olas pandémicas de COVID-19 y las etapas iniciales de la cam-paña de vacunación contra la COVID-19. La seroprevalencia indica un aumento, alcanzando un 98,4% de positividad en marzo del 2022.
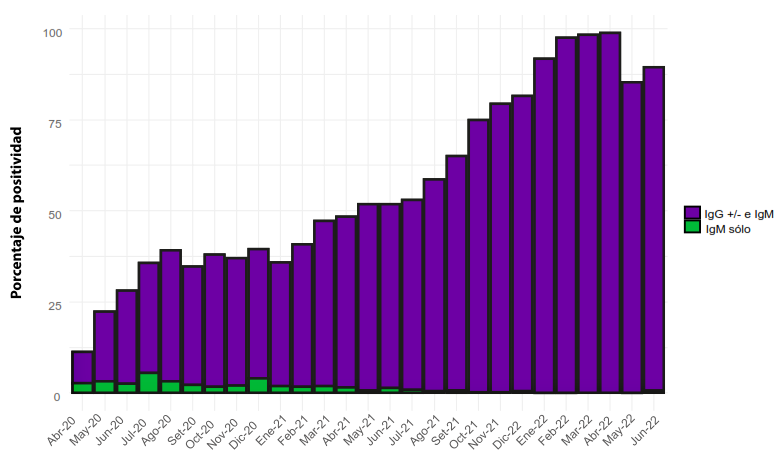
Figura 1. Presencia de anticuerpos contra IgM e IgG de SARS-CoV-2 de los donantes de 6 bancos de sangre del departamento de Lima.
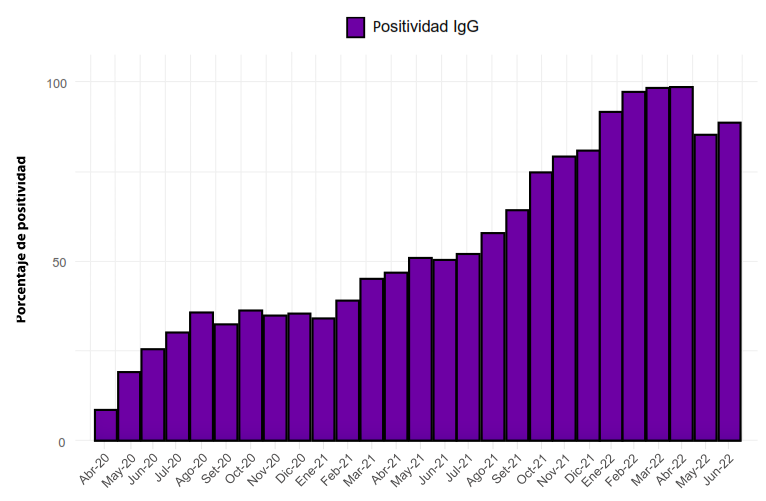
Figura 2. Seroprevalencia IgG de SARS-CoV-2 de los donantes de 6 bancos de sangre de EESS del departamento de Lima.
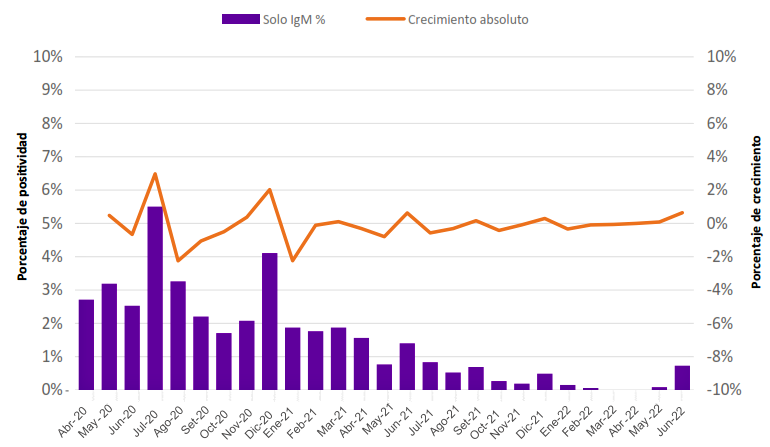
Figura 3. Presencia de anticuerpo IgM SARS-CoV-2 de los donantes de 6 bancos de sangre del departamento de Lima.
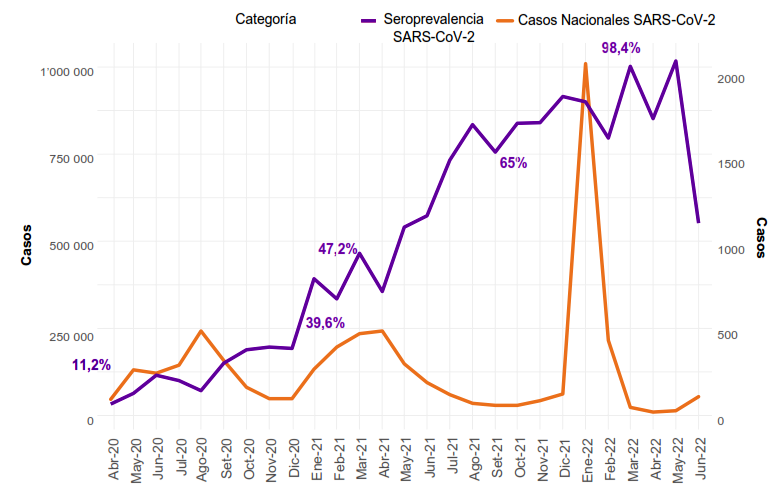
Figura 4. Seroprevalencia de SARS-CoV-2 de los donantes de 6 bancos de sangre del departamento de Lima y casos de COVID-19 en el Perú.
El conteo y porcentajes según resultado negativo, positivo sólo a IgM, positivo sólo a IgG, y positivo IgM e IgG, en cada DIRIS de Lima o provincia de Lima, se muestra en el Material Suplementario 1. Asimismo, el conteo y porcentajes según resultado negativo, positivo sólo a IgM, positivo sólo a IgG, y positivo IgM e IgG, según cada mes de los años de pandemia, se muestra en el Material Suplementario 2.
DISCUSIÓN
La decisión de seleccionar bancos de sangre para el presente estudio de seroprevalencia de SARS-CoV-2, al igual que en investigaciones internacionales realizadas en México 8, Egipto 9 e India 10 ha demostrado ser ventajoso. Los resultados de las pruebas rápidas empleadas en el estudio, no sólo mostró con precisión la respuesta inmunitaria frente al virus en la población, sino que también permitió un análisis detallado y longitudinal de la evolución de la inmunidad, aprovechando la Red Nacional de Bancos de Sangre. La selección de donantes de sangre, que comúnmente representan a individuos sanos asintomáticos, proporcionó una oportunidad para rastrear tanto la exposición no detectada como la acumulación de inmunidad a lo largo del tiempo, incluyendo casos asintomáticos. Esta estrategia, que garantiza la calidad de los datos a través de protocolos estrictos, ha facilitado comparaciones internacionales significativas destacando la importancia de adaptar las estrategias de salud pública a contextos específicos.
Nuestros resultados reflejan un aumento de la seroprevalencia desde 11,2% en abril del 2020, a 39,6% en diciembre del 2020, ilustrando el impacto acumulativo de la trasmisión del virus, llegando a 98,4% durante marzo del 2022. Este hallazgo evidencia una intensa actividad de infección y respuesta inmunitaria por infecciones y vacunas. Diversos estudios han reportado una amplia gama de seroprevalencias desde el comienzo de la pandemia, desde un 3,38% en 2020 11 hasta un 80% a 90% en 2022 12. En particular, la evolución de la seroprevalencia muestra un aumento significativo de los anticuerpos IgG a lo largo del tiempo. Este contraste enfatiza la necesidad de personalizar las estrategias de salud pública según las condiciones locales y resalta la importancia de realizar estudios longitudinales que permitan monitorear la seroprevalencia en esta y otras enfermedades.
La evaluación de diferentes pruebas serológicas para detectar la infección por SARS-CoV-2 13) proporciona un marco importante para interpretar nuestros resultados. El análisis de la eficacia de varias pruebas serológicas subraya la necesidad de seleccionar metodologías adecuadas que aseguren la fiabilidad y precisión de los datos sobre la seroprevalencia. Este aspecto es fundamental para la validez de nuestro estudio, donde la elección de la metodología de detección puede influir significativamente en la interpretación de la seroprevalencia en la población estudiada, en este caso en particular se optó por una metodología aprobado por el INS.
En Perú, estudios de seroprevalencia, mostraron una variabilidad significativa en diferentes contextos; a gran altitud en Cusco de 25,9% a 38,8% desde septiembre del 2020 al 2021 14,15; en la selva en la ciudad de Iquitos la seroprevalencia fue de 70% para julio del año 2020 16, mientras que en la costa, en Lambayeque la proporción fue 29,5% para junio del 2020 17; en Tumbes, 24,8% en marzo de 2021 18; y en Lima, 20,8% en julio del año 2020, siendo más alta en áreas con mayor hacinamiento y bajo estatus socioeconómico 19. Diversos estudios en el Perú han identificado factores ambientales, geográficos, económicos y sociales que influyen heterogéneamente en la trasmisión del virus reflejado en la seroprevalencia. Mostramos la seroprevalencia de 25,5% a 30% entre los meses de junio y julio del 2020, similar a la prevalencia de 20,8% reportado por Reyes-Vega et al19.
Las nuevas variantes impactaron la dinámica de trasmisión en Perú 20, la cual fue diferente al inicio y finales de pandemia COVID-19 21, al igual que la respuesta inmunitaria. La emergencia de las variables resalta la importancia de adaptar continuamente las estrategias de salud pública a la evolución del virus SARS-CoV-2. En ese sentido, nuestros resultados revelaron un aumento gradual de los anticuerpos IgG y una reducción de los IgM, con pequeñas detecciones de IgM hasta el final del estudio explicadas por las constantes infecciones producto de nuevas variantes.
Las limitaciones de nuestro estudio fueron que utilizamos solo las muestras disponibles de los bancos de sangre seleccionados, se excluyeron aquellas que no pudieron ser identificadas o no tenían muestra suficiente para análisis. Usamos bases de datos de pruebas inmunocromatográficas rápidas para la detección de anticuerpos contra IgM e IgG de SARSCoV-2. Utilizar anticuerpos neutralizantes o test cuantitativos hubiera mejorado nuestro análisis, pero a pesar de ello los resultados grafican bien la evolución de la seroprevalencia durante la pandemia COVID-19. Otras limitaciones fueron que no se tenían los datos de donantes infectados por COVID-19, así como de donantes vacunados por COVID-19 que participaron en este estudio, tampoco se tenía la información de la proporción de los donantes vacunados por COVID-19 que fueron infectados por COVID-19.
En conclusión, la reactividad y presencia de anticuerpos anti-SARS-CoV-2 aumentaron progresivamente durante la pandemia COVID-19 hasta el 98,4%, este incremento es explicado posiblemente con el impacto de las olas pandémicas y la campaña de vacunación contra la COVID-19 en el Perú. La selección de bancos de sangre para estudios de seroprevalencia de SARS-CoV-2 ha permitido una evaluación adecuada de la respuesta inmunitaria y una monitorización longitudinal, destacando la importancia de adaptar las estrategias de salud pública ante la evolución del virus SARS-CoV-2.















