INTRODUCCIÓN
En el quinquenio 2019 - 2023, Perú ha notificado 43 883 casos de infección por el virus de la inmunodeficiencia humana (VIH). En el 2023, se estimó una tasa de 28,05 casos por 100 000 habitantes. Estas cifras resultan alarmantes por ser una enfermedad que no tiene cura ni vacuna. A pesar de que este quinquenio se vio afectado por la pandemia de la COVID-19, hubo más notificaciones de casos de VIH que en los quinquenios anteriores 1. Dicho incremento podría ser explicado por una mejor cobertura de medios diagnósticos y a la aplicación del nuevo algoritmo para la definición de caso de VIH 2,3.
El algoritmo convencional describe que los resultados reactivos a alguna prueba de tamizaje: prueba rápida (PR), ensayo por inmunoabsorción ligado a enzimas (ELISA), quimioluminiscencia (CLIA) o electroquimioluminiscencia (ECLIA) son confirmados por las pruebas serológicas de inmunofluorescencia indirecta (IFI) e inmunoblot o western blot 2-5.
El nuevo algoritmo establece que los pacientes cuyas muestras presenten resultados reactivos en dos pruebas de tamizaje de diferentes fabricantes, se notifican como casos de VIH. Estos pacientes son derivados para el análisis de PCR-carga viral y el inicio de tratamiento antirretroviral (TAR) 3. Es fundamental que la muestra para la carga viral se obtenga antes de iniciar el tratamiento antirretroviral o la profilaxis post exposición. De lo contrario, existe el riesgo de un resultado indetectable, lo que podría impedir confirmar la infección 6,7. Por otro lado, el último algoritmo recomendado por la Organización Mundial de la Salud (OMS) indica que se utilicen tres pruebas reactivas de tamizaje secuenciales para dar un diagnóstico positivo a VIH 8,9.
En el Perú, el año 2019, el nuevo algoritmo diagnóstico de VIH generó un 1,4% (21/1522) de falsos positivos; estos pacientes recibieron TAR sin tener la infección por VIH 6. Por ello, la Organización Mundial de la Salud (OMS) orienta a que los países verifiquen sus algoritmos de las pruebas del VIH, con la finalidad de que tomen decisiones de combinaciones que den resultados fiables 10,11. En 2023, Perú notificó 9490 casos de VIH 1 y no contando con información actualizada sobre la magnitud del problema, nos propusimos como objetivo determinar la proporción de verdaderos positivos y falsos positivos a pruebas de tamizaje de VIH en tres algoritmos de diagnóstico en Perú para el 2023.
MÉTODOS
Diseño de estudio
Realizamos un estudio observacional descriptivo entre enero y junio del 2024; se estructuró un estudio secundario a partir de datos de un estudio primario 12. El estudio se realizó en el Laboratorio de Referencia Nacional de Virus de Transmisión Sexual del Instituto Nacional de Salud (INS) de Perú, el cual confirma el VIH por las pruebas de IFI e Inmunoblot y recibe muestras de todas las regiones del Perú que no cuenten con la prueba de IFI. Para el 2023, el INS atendió el 73,4% (5240/7144) de las muestras para confirmación serológica, mientras que 26,6% (1904/7144) fueron atendidas por los laboratorios referenciales regionales (LRR).
Población y muestra
La recolección de datos se realizó a partir del sistema de información y gestión de laboratorios NetLabv2 (13. Se recolectaron los resultados de los pacientes con pruebas serológicas confirmatorias a VIH, que fueron analizadas del 1 de enero al 31 de diciembre del 2023. Simultáneamente, se hizo la búsqueda de los resultados de las pruebas de tamizaje a partir de las fichas de solicitud de diagnóstico confirmatorio de VIH. 1904 pacientes fueron excluidos por no tener alcance a sus fichas de diagnóstico, debido a que su muestra fue analizada en los LRR; también se excluyó a 1210 pacientes cuyas fichas no contaban con al menos una prueba de tamizaje reactivo a VIH (Figura 1).
Variables de estudio y procedimiento
Los resultados de las pruebas serológicas confirmatorias a VIH (IFI 14) e Inmunoblot: sensibilidad 100,0% y especificidad 96.7% 15) fueron comparados frente a los resultados reactivos de las pruebas de tamizaje, separándolos en tres grupos según el tipo de algoritmo. Para el algoritmo convencional, los pacientes requirieron un resultado reactivo a una prueba de tamizaje; para el algoritmo nuevo, los pacientes requirieron dos resultados reactivos a dos pruebas de tamizaje de diferente fabricante o principio; para el último algoritmo recomendado por la OMS, los pacientes requirieron resultados reactivos a tres pruebas de tamizaje de diferente fabricante o principio. Además, se estratificaron a los casos verdaderos positivos y falsos positivos según región sexo, grupo etario y grupo poblacional.
Análisis estadístico
Los datos registrados se importaron a una hoja de cálculo Microsoft Excel® 2016. Para asegurar la calidad de los datos y evitar errores e inconsistencias, se realizó la limpieza, edición y control de calidad de la base de datos. Se estimaron las proporciones de los verdaderos positivos y falsos positivos a VIH y se diseñaron gráficas usando los softwares R4.2.1 y RStudio 2023.06.1 mediante las librerías Tidyverse y ggplot2.
Aspectos éticos
Para el análisis de datos secundarios, los datos de los pacientes fueron previamente decodificados y anonimizados, además las muestras correspondieron a pacientes de la vigilancia del VIH en el Perú. La presente investigación es un sub análisis del estudio aprobado por el Comité Institucional de Ética en Investigación del Instituto Nacional de Salud de Perú con el código OI-012-22 12.
RESULTADOS
En 2023, Perú atendió 7144 pacientes para el diagnóstico serológico confirmatorio de VIH; el total de pacientes que fueron seleccionados para el estudio luego de aplicar los criterios de exclusión, fueron 4030 (Figura 1).
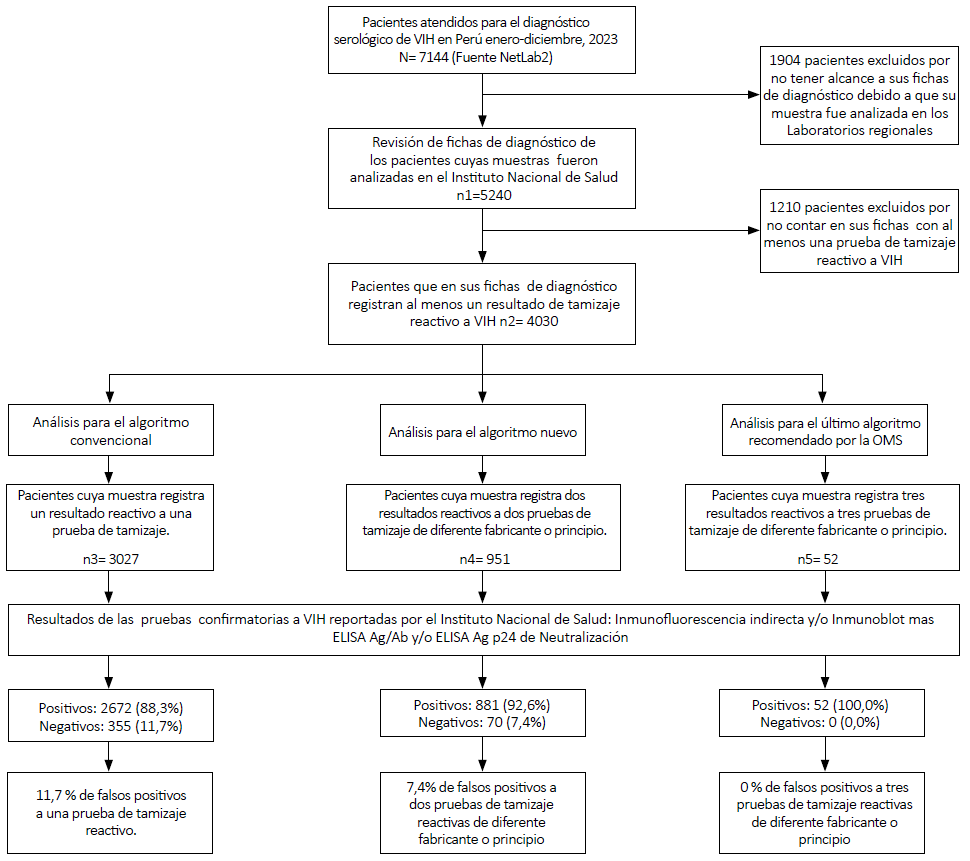
Figura 1. Resultados de los algoritmos convencional, nuevo y el último recomendado por la OMS en base a los pacientes incorporados al estudio del diagnóstico serológico de VIH. Perú, 2023.
En relación al algoritmo convencional, de 3027 personas reactivas a una prueba de tamizaje, un 88,3% (2742/3027) fueron positivas a la prueba serológica confirmatoria, es decir verdaderos positivos. Además, correspondió un 11,7% (355/3027) de falsos positivos (Figura 1 y 2A).
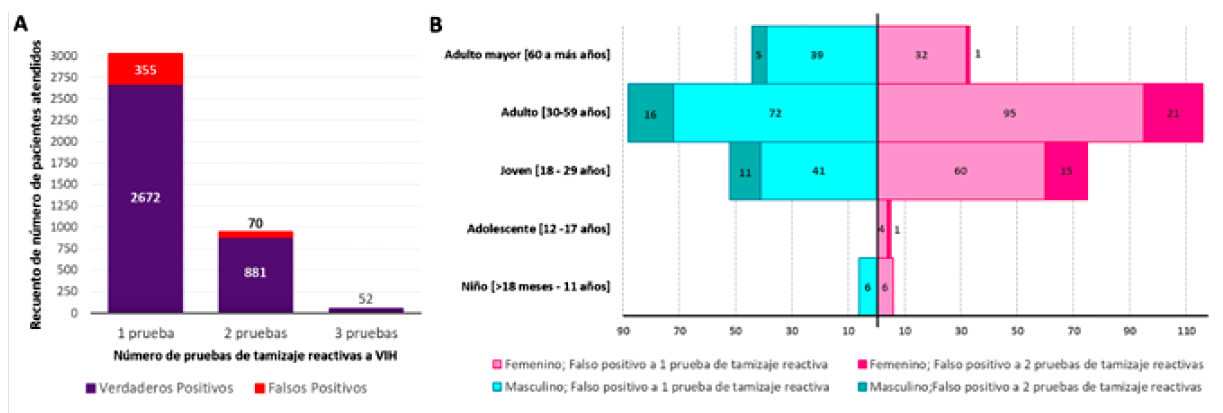
Figura 2. A. Verdaderos positivos y falsos positivos a 1, 2 y 3 pruebas de tamizaje reactivas a VIH (n=4030). B. Falsos positivos a 1 y 2 pruebas de tamizaje reactivas a VIH (n=425), distribuidos según grupo etario y según sexo. Diagnóstico serológico de VIH, Perú, 2023.
En cuanto al algoritmo nuevo, de 951 personas reactivas a dos pruebas de tamizaje, un 92,6% (881/951) fueron positivas a la prueba serológica confirmatoria, es decir verdaderos positivos. Además, correspondió un 7,4% (70/951) de falsos positivos (Figura 1 y 2A).
En cuanto al último algoritmo recomendado por la OMS destacamos que los pacientes cuya muestra registró tres resultados reactivos a las tres pruebas de tamizaje de diferente fabricante o principio, no presentaron ningún falso positivo (0/52) (Figura 1 y 2A).
El mayor número de falsos positivos a 1 y 2 pruebas de tamizaje a VIH estuvo en el grupo etario adulto (204/425), siendo mayor en el sexo femenino que en el masculino (Figura 2B).
En la figura 3A se muestra la distribución geográfica por regiones de los pacientes verdaderos positivos a VIH confirmados por serología y reactivos a 1, 2 y 3 pruebas de tamizaje a VIH (N=3605). Además, en la figura 3B mostramos la distribución geográfica por regiones de los pacientes falsos positivos a VIH descartado por prueba serológica confirmatoria y reactivos a 1 y 2 pruebas de tamizaje a VIH (n=425).

Figura 3. A. Distribución geográfica de los pacientes verdaderos positivos a VIH confirmados por serología y reactivos a 1, 2 y 3 pruebas de tamizaje a VIH (n=3605). B. Distribución geográfica de los pacientes falsos positivos a VIH descartado por prueba serológica confirmatoria y reactivos a 1 y 2 pruebas de tamizaje a VIH (n=425). Diagnóstico serológico de VIH, Perú, 2023.
Las poblaciones que tuvieron más falsos positivos a VIH fueron: población general (71,6%: 304/425), gestantes (13,2%: 56/425) y aspirantes a donar sangre (7,5%: 32/425) (Figura 4).
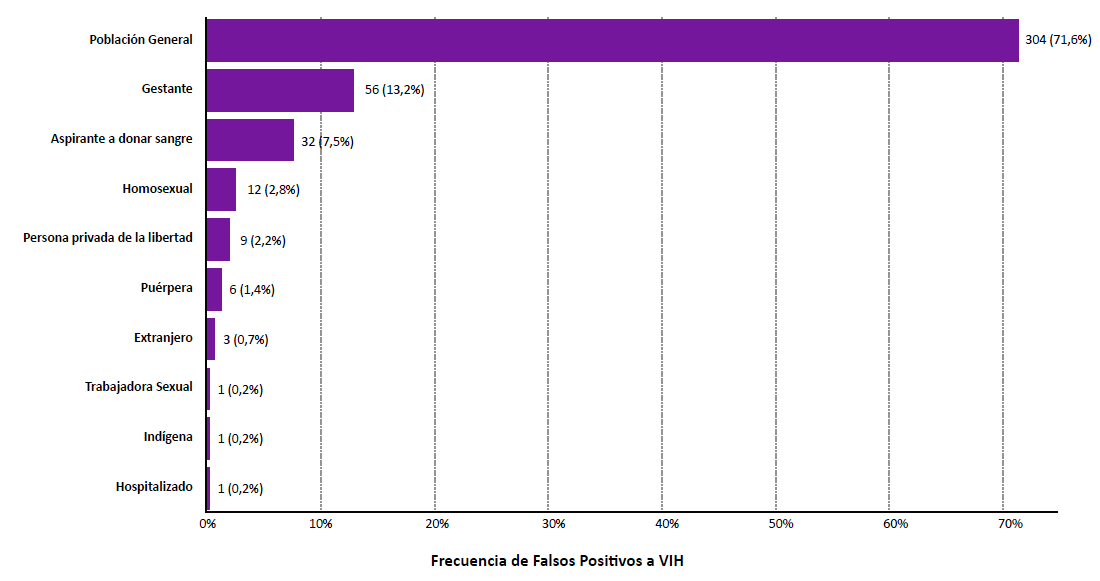
Figura 4. Falsos positivos a VIH según tipo de población (n=425). Diagnóstico serológico de VIH, Perú, 2023.
Resaltamos que Lima es la región con más verdaderos positivos (65,9%: 2374/3605) y más falsos positivos (58,1%: 247/425) (Material Suplementario).
DISCUSIÓN
Al analizar el escenario del algoritmo convencional, encontramos un 11,7% de falsos positivos, pudiendo ser esto consecuencia de diversos factores, entre ellas, posibles reacciones cruzadas a las diferentes marcas de las pruebas de tamizaje 16,17,18, mal manejo del aseguramiento de la calidad que incluye la gestión de compras, limitaciones en el control de reactividad al no usar un tamaño de muestra más robusto en la verificación de las pruebas rápidas a cargo del MINSA o a la escasa experticia de algunos analistas en la detección del VIH(11). Sin embargo, esto se esclarece con los análisis de las pruebas serológicas confirmatorias que han mostrado buena eficiencia diagnóstica 14,15.
En el escenario del algoritmo nuevo, obtuvimos un 7,4% de falsos positivos (70/951), es decir las muestras de estos setenta pacientes que registraron dos resultados reactivos a dos pruebas de tamizaje de diferente fabricante o principio, fueron realmente personas no infectadas con VIH; nuestros resultados son cinco veces mayores a los encontrados en Perú para el año 2019 donde se reportó un 1,4% (21/1522) de falsos positivos 6. Las interesantes ventajas que ofrece este algoritmo nuevo, implica iniciar un TAR temprano sin demora a realizar la prueba confirmatoria serológica, la cual no está disponible en siete de los veinticuatro departamentos del Perú; sin embargo, destacamos que los pacientes que en su primera CV salga indetectable, deben ser derivados a la confirmación serológica para su descarte final de la infección por VIH. Esto evitará que las personas que realmente no están infectadas reciban innecesariamente el TAR.
Para el último algoritmo recomendado por la OMS, hallamos que las muestras con resultados reactivos a tres pruebas de tamizaje de diferente fabricante o principio ofreció una alta eficiencia diagnóstica concordante al 100% con las pruebas serológicas confirmatorias. Nuestros resultados responden a las directrices innovadoras de la OMS, que proponen a los países a adoptar como estrategia a que utilicen tres pruebas reactivas secuenciales en vez de dos pruebas reactivas para dar un diagnóstico positivo; con este nuevo enfoque, los países alcanzarán una máxima precisión en las pruebas del VIH 8,9.
Si con los resultados que obtuvimos se hace un análisis previo de estimación costo/beneficio, resultaría que para el 2023 en Perú, el gasto de una tercera prueba diagnóstica para 9490 pacientes 1) sería 18 980 dólares (2 dólares/prueba diagnóstica), monto muy similar al comparado en el gasto sólo para el primer año del tratamiento y monitoreo de los 70 pacientes falsos positivos que asciende a 19 460 dólares (para un paciente nuevo en el primer año = 278 dólares [un TAR: 82 dólares; tres CV: 117 dólares; dos citometría: 79 dólares]); sin embargo, al comparar con una esperanza de vida del paciente para dos décadas, los gastos ascenderían a 169 400 dólares (paciente en seguimiento por 20 años = 2420 dólares [veinte TAR: 1640 dólares; veinte CV: 780 dólares]). En consecuencia, sería beneficioso asumir los gastos de la tercera prueba diagnóstica, ahorrándonos en costos de pérdidas que incluyen tratamientos innecesarios de por vida, además de los costos para las personas y la sociedad 8,9.
El VIH sigue siendo un gran problema de salud pública. Se evidencia que en el 2023 hubo un importante número de nuevos casos positivos, corresponde incorporar nuevas estrategias de prevención en las poblaciones clave para evitar seguir con el aumento de nuevos contagios (12,19; una estrategia importante sería que en las regiones más alejadas donde no está disponible la prueba confirmatoria, se les analice a los pacientes con tres metodologías o marcas diferentes de pruebas rápidas con la finalidad de llegar a un diagnóstico definitivo y a un TAR oportuno.
En nuestro estudio se muestra que la población gestante tuvo un porcentaje importante de falsos positivos (13,2%: 56/425), algunas investigaciones señalan que los factores de riesgo de ser joven y multípara eleva la causa de los falsos positivos 20. La prevalencia de VIH encontrada en donantes de sangre varía entre 0,19 a 0,33%, sin embargo, en un hospital de Lima encontraron una prevalencia de 0,81%, los autores señalan entre sus limitaciones que dicho cálculo solo se realizó con pruebas de tamizaje y no de confirmación por lo que estaría sobreestimado, lo cual concuerda con nuestro estudio, ya que nosotros hayamos que los aspirantes a donar sangre presentaron un porcentaje importante de falsos positivos (7,5%) al ser confirmado con las pruebas serológicas confirmatorias 21.
Una limitante del estudio radica que actualmente en el Perú no se puede diferenciar a los pacientes que son derivados para el análisis de la CV producto del algoritmo nuevo versus los pacientes ya infectados antiguos que siguen su monitoreo, esto porque todavía el personal de salud no usa la ficha de diagnóstico diferenciada.
En conclusión, los algoritmos convencional y nuevo en Perú son fiables, pero debe considerarse en el caso del algoritmo nuevo, la confirmación serológica cuando la primera prueba de CV sea indetectable; es por ello que recomendamos se incorpore en Perú el escenario del último algoritmo recomendado por la OMS (pacientes cuya muestra obtenga resultados reactivos a tres pruebas de tamizaje de diferente fabricante o principio).















