INTRODUCCIÓN
El sector ganadero en Perú constituye un importante pilar económico y fuente de empleo y seguridad alimentaria a nivel nacional, con énfasis en las regiones altoandinas que es donde se encuentra el 68% de las unidades agropecuarias (INEI, 2013). Dentro de los problemas sanitarios que afectan al ganado se encuentran las parasitosis. Fasciola hepatica es un parásito ampliamente difundido a nivel mundial, habiéndose detectado en más de 50 países en el mundo; produciendo la enfermedad denominada fasciolosis o distomatosis, clasificada en salud pública, como una enfermedad tropical desatendida (Mehmood et al., 2017). Los hospederos definitivos son mayormente rumiantes (bovinos y ovinos) y como hospederos intermediarios se tienen a los caracoles del género Lymnaea, en donde se desarrolla la fase infectiva del parásito (Admassu et al., 2015).
La fasciolosis produce varios efectos negativos en el animal, tales como la disminución de la producción (leche, carne y lana, entre otros), estimándose a nivel mundial una pérdida de 3.2 mil millones de dólares estadounidenses por año debido a esta parasitosis (Mehmood et al., 2017). En el Perú se puede evidenciar el impacto económico que causa esta enfermedad, principalmente por el decomiso de hígados infectados. Entre los años 2011 y 2016 en la provincia de Andahuaylas, se estimó una pérdida de US$ 238 000 (Reinoso, 2018), mientras que para Huancayo, solo con el decomiso de órganos infectados durante 16 meses se calculó una pérdida de US$ 35 000 (Arias-Pacheco et al., 2020) y en la provincia de Huaura, entre mayo y agosto del 2018, Silva-Castro et al. (2023) reportan 59.5% de hígados infectados.
El principal y más común método de control es el uso periódico de antihelmínticos con eficacia comprobada (Charlier et al., 2013). Avances en cuanto al desarrollo de nuevas drogas contra Fasciola hepatica son escasos; los fármacos que se utilizan con mayor frecuencia (triclabendazol y rafoxanida) fueron desarrollados hace más de 40 años (Campbell y Brotowidjoyo, 1975; Craig y Huey, 1984). Por tal motivo y debido a la capacidad de adaptación que tienen los parásitos, se han ido reportando diversos casos de eficacia disminuida (Fairweather et al., 2020).
Se ha reportado resistencia al triclabendazol en vacunos lecheros en el norte y centro del Perú (Chávez et al., 2012; Ortiz et al., 2013), por lo que se requiere evaluar este emergente problema con otros fasciolocidas en vacunos. Más recientemente, Zárate-Rendón et al. (2023) evaluó rafoxanida, clorsulón, nitroxinil, closantel y triclabendazol en bovinos del Valle del Mantaro, encontrando óptimos niveles de eficacia, con excpeción del triclabendazol. Ante esto, el objetivo del presente estudio fue evaluar la eficacia de una combinación de rafoxanida y albendazol contra Fasciola hepatica en vacunos de un centro de engorde intensivo con animales provenientes de la provincia de Chiclayo, región Lambayeque, Perú.
MATERIALES Y MÉTODOS
Población y Área de Estudio
Los animales del estudio estuvieron conformados por ganado bovino macho criollo y cruces, principalmente Brown Swiss, Fleckvieh, Holstein y Brahman. Las edades, a partir de la dentadura, fueron entre 1 a 3 años, con peso vivo entre 200 a 350 kg y condición corporal entre 1.5 a 3 en una escala de 0 a 5.
Para el estudio se consideró la totalidad de ganado que llegó al Centro de Engorde «Establo Doña Lola» en el distrito de Lurín, Lima. Se trabajó con 98 toros provenientes de las ferias ganaderas realizadas en la provincia de Chiclayo, región Lambayeque, zona ubicada en la costa norte del Perú, a una altitud entre 0 a 50 msnm y con temperaturas promedio de 14 a 34.1 °C; donde en la época lluviosa (enero-abril) se presenta una precipitación media de 37.5 mm/mes (SENAMHI, 2021). La crianza en el lugar de origen era de tipo extensiva y con alimentación únicamente al pastoreo, por lo que fueron naturalmente infectados.
El estudio se realizó en el periodo marzo-abril de 2022 y el análisis de las muestras se ejecutó en el Laboratorio de Parasitología de la Facultad de Zootecnia de la Universidad Nacional Agraria La Molina (UNALM).
Muestras y Técnica Coproparasitológica
La muestra de heces (50 g) se tomó directamente del recto del animal a la llegada de los bovinos al centro de engorde, utilizando guantes de exploración obstétrica, y fueron colocadas en bolsas de polietileno debidamente rotuladas. Las muestras fueron trasladadas al laboratorio en una caja térmica con gel refrigerante. El tiempo transcurrido entre la toma de muestras y su procesamiento fue alrededor de 5 horas.
Para el análisis de las muestras se utilizó el método FLUKEFINDER® a fin de determinar la presencia de huevos de Fasciola hepatica. Se utilizaron 2 g de heces en un vaso precipitado junto a 30 mL de agua destilada. La mezcla se vertió en el equipo FLUKEFINDER® para tamizarla. El contenido fue colocado en un tubo falcon de 15 mL, se dejó reposar, se retiró el sobrenadante y el sedimento se colocó en una placa petri marcada con cuadrantes. Se aplicaron tres gotas de azul de metileno para tener una mejor visualización de los huevos en un estereoscopio Leica EZ4 (Godoy, 2020). Se determinó el total de huevos que había en la placa petri y número se dividió entre dos para obtener la cantidad de huevos por gramo de heces (hpg).
Se seleccionaron 21 animales con una carga parasitaria mayor a 13 hpg para ser tratados con una combinación de rafoxanida y albendazol (Ranide Forte®, TQC, Perú) a dosis de 10 mg/kg y 9 mg/kg respectivamente (entre 20 a 35 mL de producto), siguiendo las indicaciones del fabricante y tomando como referencia las indicaciones de SENASA (2017), teniendo en cuenta que podrían haber estadios inmaduros del parásito, por lo que se aumenta ligeramente la dosis. Los días 14 y 30 posteriores al tratamiento se tomó una nueva muestra de heces para determinar la cantidad de hpg. Las muestras fueron procesadas siguiendo el método mencionado previamente.
Análisis Estadístico
El porcentaje de eficacia en términos de reducción del conteo de hpg se determinó con la fórmula de la «Prueba de reducción de conteo de huevos fecales» (FECRT, por sus siglas en inglés) (Ortiz et al., 2013): % Reducción = ([Promedio hpg Día 0 -Promedio hpg día 14 o 30] / Promedio hpg Día 0)*100. Asimismo, se tuvo en consideración la directriz pautada por la Asociación Mundial para el Avance de Parasitología Veterinaria (WAAVP) que menciona que un fasciolicida es muy efectivo cuando pasa el 98%, efectivo entre 90 y 98%, moderadamente efectivo entre 80 y 89%, e insuficientemente activo cuando es menor de 80% (Wood et al., 1995).
Adicionalmente se determinaron los intervalos de confianza al 95% utilizando la técnica estadística de Bootstrapping (Cabaret y Berrag, 2004). Todos los análisis estadísticos fueron realizados con el software R v. 4.1.2. (R Core Team, 2013).
RESULTADOS
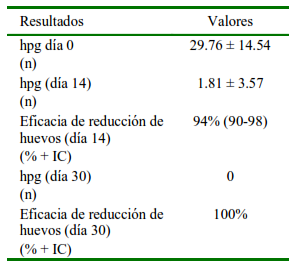
Se evidenció que utilizando una dosis única de 10 mg/kg de rafoxanida y 9 mg/kg de albendazol al día 14 del tratamiento existe eficacia del 94% (90-98 IC 95%) contra F. hepatica y al día 30 esta fue aún más efectiva (100%) (Cuadro 1)
DISCUSIÓN
Los resultados confirman la alta eficacia de una combinación de rafoxanida y albendazol en el control de fasciolosis en bovinos procedentes del norte del país. Pese a que la zona periurbana de Lima no es un área con presencia de distomatosis bovina, se ha reportado la existencia de zonas hiperendémicas y mesoendémicas en provincias aledañas (Marcos et al., 2007); por otro lado, la presencia de centros de engorde intensivo en la zona de Lima involucra el arribo de animales infectados de otras provincias, tal como se ha comprobado en este estudio.
Uno de los pocos estudios que evaluan rafoxanida en Perú es el de Zárate-Rendón et al. (2023) en bovinos del Valle del Mantaro quiénes reportan una eficacia de 92.1% (79.698.9%) y 97.4% (94.1-99.4%) a los 15 y 30 días pos-tratamiento respectivamente, considerándose una buena opción terapéutica. Sin embargo, no es fácil poder extrapolar resultados de eficacia de este fármaco hacia otras regiones por la variabilidad que hay en los genes de resistencia (gen de la glicoproteína P) (Hodgkinson et al., 2018; Fairweather et al., 2020).
Kelley et al. (2016) sustenta que la alta frecuencia de uso sin rotación de antihelmínticos es uno de los principales factores de riesgo asociados a la aparición de resistencia. El rafoxanida es un fasciolicida introducido en el mercado hace varias décadas (Fairweather y Boray, 1999), pero fue largamente superado en ventas por el éxito del triclabendazol; sin embargo, debido a los numerosos reportes de resistencia de este último fármaco, se ha empezado a usar con mayor frecuencia el rafoxanida (D. Zárate, comunicado personal, 2023).
Estudios en otros países como el de Shokier et al. (2013) quiénes evaluaron la eficacia de cinco antihelmínticos contra F. hepatica en ganado bovino de Egipto, teniendo una reducción de hpg al día 14 del 100% para triclabendazol, oxiclozanida y levamizol, mientras que fue solo de 80.6 y 75% de eficacia para rafoxanida y albendazol, respectivamente. Un reporte similar presenta Elitok et al. (2006) en Turquía donde el fármaco que obtuvo mayor eficacia fue el clorsulón (84.2%), y mucho menos que albendazol (66.7%) y rafoxanida (68.2%), lo que demuestra un claro caso de resistencia antihelmíntica hacia estos dos fármacos en estas zonas del mundo.
La técnica FLUKEFINDER® no está muy difundida en el país a pesar de tener altos valores de sensibilidad y especificidad. En Perú se realizó un comparativo contra la prueba Dennis modificada, donde Godoy (2020) concluyó que FLUKEFINDER® tiene un desempeño similar a la prueba de Dennis en cuanto a la detección de huevos, pero a su vez, dicho método detectó mayores cargas del parásito, así como una mayor practicidad al momento de ejecutarse.
Para obtener la eficacia del fármaco, se utilizó el FECRT con la fórmula que establece la WAAVP. Este método está validado y utilizado en diversos trabajos (Chávez et al., 2012; Murguia, 2023) que evalúan resistencia antihelmíntica, obteniéndose buenos resultados. Con esta fórmula se pudo evidenciar una eficacia para rafoxanida de 94% (90:98 IC 95%) a los 14 días que, según los parámetros de Wood et al. (1995), corresponde a un fármaco efectivo (entre 90 y 98%), teniendo así una buena opción terapéutica contra la distomatosis.












 uBio
uBio