INTRODUCCIÓN
La Organización Mundial de la Salud (OMS) señala que más de 500 millones de personas están en riesgo de contraer infecciones por trematodos transmitidos por peces, de los cuales 18 millones ya se encuentran infectados (Chai et al., 2005). Los agentes causales de estas trematodiasis incluyen miembros de la familia Heterophyidae, parásitos que habitan en el intestino delgado de aves, mamíferos, y también en seres humanos (Derraik, 2008; Chai y Jung, 2017; Pulido-Murillo et al., 2018; Metz et al., 2023). La infección por estos heterófidos se cataloga como una enfermedad emergente debido a varios factores, entre los cuales se destaca su alta prevalencia. Esta enfermedad se informa principalmente en Asia; sin embargo, existen registros de brotes ocasionados por Ascocotyle longa en Brasil. Además, se ha observado la introducción de parásitos como Centrocestus formosanus y Haplorchis pumilio desde Asia a las Américas (Acosta-Pérez et al., 2023). Por último, se identificó a Procerovum varium como un agente causante de una enfermedad ocular en seres humanos (Pulido-Murillo et al., 2018).
El caracol trompeta de Malasia, Melanoides tuberculata (Caenagastropoda: Thiaridae), es un molusco partenogenético y polimórfico originario de Asia y África, que se encuentra distribuido globalmente en hábitats de agua dulce tropicales y subtropicales (Preston et al., 2021). La invasión de esta especie provocó el desplazamiento de caracoles dulceacuícolas autóctonos en varios países, además de ser portador de más de 50 tipos de larvas de trematodos en su hábitat original, algunas de las cuales son patógenas para los humanos (Pinto y Melo, 2011; Krailas et al., 2014; Jihad y Makaw, 2022; Tolley-Jordan et al., 2022). En el humedal costero Los Pantanos de Villa (HCLPV) en Lima, Perú, se ha observado una disminución de los caracoles dulceacuícolas nativos durante la última década. Esto sugiere que estos organismos representan uno de los taxones afectados en este humedal debido a la presencia de M. tuberculata (Torres-Zevallos et al., 2020).
Este caracol actúa como hospedero intermediario para siete especies de trematodos heterófidos (Krailas et al., 2014), de un total de 30 especies reconocidas a nivel mundial (Chai y Jung, 2017), incluyendo a C. formosanus y H. pumilio (Pulido-Murillo et al., 2018; Schols et al., 2020). Asimismo, un análisis de 136 estudios reveló que M. tuberculata podría ser portador de trematodos, abarcando 17 taxones a nivel de familias, 25 a nivel de género y 37 en la categoría de especies (Pinto y De Melo, 2011). En Tailandia, se encontraron varios morfotipos de cercarias, siendo principalmente de H. pumilio, Haplorchis taichui, Stictodora tridactyla y C. formosanus (Krailas et al., 2014). En Texas (EE. UU.), un cuerpo de agua fue invadido por M. tuberculata produciéndose la invasión por tres de sus parásitos trematodos (Philophthalmus gralli en la década de 1960; C. formosanus en la década de 1990 y H. pumilio en la década de 2000). Además, existen registros de formas larvarias de trematodos en M. tuberculata para varios países deAmérica (Schultz-Lopes et al., 2021; Tolley-Jordan et al., 2022). En el Perú se han reportado cercarias de C. formosanus con 1.8 y 1% en 2857 caracoles M. tuberculata recolectados en los humedales de la costa peruana, como Ventanilla y Pantanos de Villa, respectivamente (Pulido-Murillo et al., 2018).
La variación estacional de las cercarias está estrechamente vinculada a múltiples factores, incluyendo la ubicación de los hospederos vertebrados finales, la disponibilidad y cantidad de caracoles hospederos intermediarios, la probabilidad de contacto entre la larva miracidio y los caracoles, el comportamiento de estos últimos y el nivel de precipitación anual. Estos elementos pueden considerarse como predictores claves de la ecología parasitaria (Ben-Ami y Heller, 2008; Lal y Vishvajeet, 2020). Un análisis de regresión logística mostró que el tamaño del caracol fue también una variable significativa para predecir la prevalencia de infección en M. tuberculata (Tolley-Jordan y Chadwick, 2018).
En el Perú no se tiene información sobre los predictores de la ecología parasitaria de C. formosanus en M. tuberculata en el humedal costero Los Pantanos de Villa (HCLPV). Por lo tanto, el objetivo del presente trabajo fue determinar los predictores de la ecología parasitaria en M. tuberculata en HCLPV, Lima, Perú.
MATERIALES Y MÉTODOS
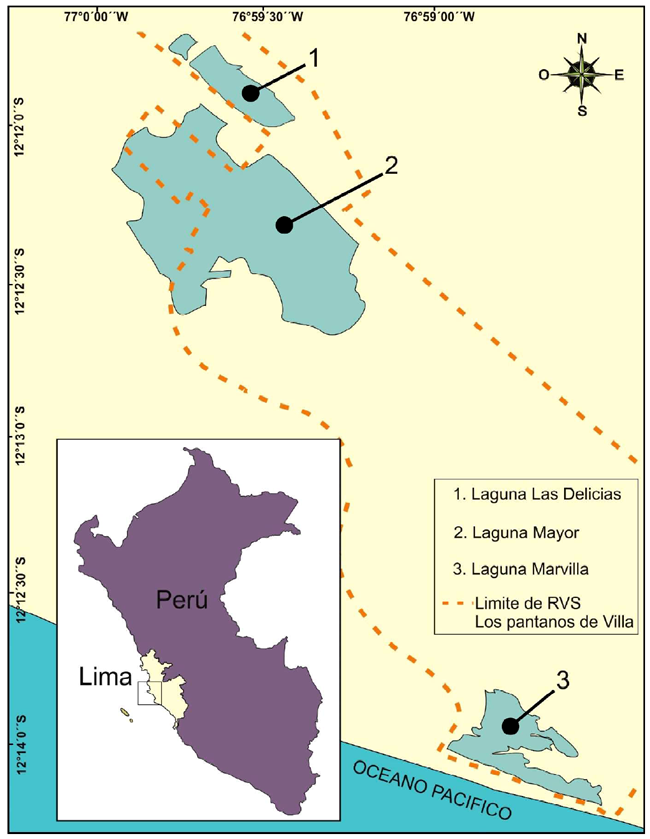
Entre abril de 2009 y junio de 2011, se recolectaron especímenes de M. tuberculata en tres lagunas ubicadas en Lima, Perú, cada una con distintos niveles de perturbación del HCLPV. Estas lagunas fueron: «Las Delicias», catalogada como de «perturbación alta» por su proximidad al área Residencial de Densidad Baja (RDB), Sector Cerro Las Delicias de Villa, donde se abarcó el otoño e invierno de 2009. «Mayor», clasificada como de nivel «medio» de perturbación debido a su ubicación intermedia respecto al área RDB, incluyó el otoño y verano de 2011. Por último, «Marvilla», considerada de «baja» perturbación por su lejanía al área RDB, abarcó la primavera y otoño de 2010 (Figura 1; Cuadro 1).
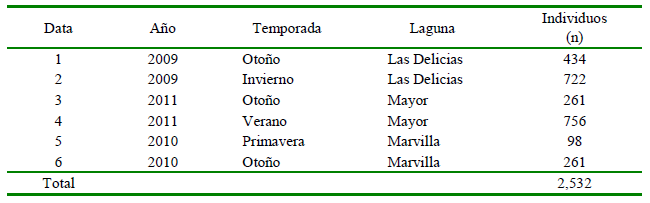
Cuadro 1. Ámbito espacial y temporal según año, temporada, laguna, y número de caracoles de Melanoides tuberculata recolectados en el humedal costero Los Pantanos de Villa (HCLPV), Lima, Perú
De acuerdo con el protocolo de recolecta de M. tuberculata se utilizó un tamiz de 1000 µm (Iannacone et al., 2003; Smith y Shackley, 2004; Paredes et al., 2007) acoplado a un mango de plástico, el cual se introdujo en la superficie del sedimento (Vizcardo y Gil-Kodaka, 2015). Se removió el sedimento para luego proceder a la selección aleatoria de ejemplares de M. tuberculata. Se midió tanto la temperatura del agua superficial (TºC) con un termómetro digital sumergible acuático OEM HT-7, con una precisión: ± 1 °C, como la profundidad en cada laguna (cm) con una varilla maciza cilíndrica de aluminio de 1 m de longitud y con un diámetro de 4 mm (Iannacone et al., 2003: Canales-Cuadros et al., 2022). En condiciones de laboratorio se midió la longitud total (LT) de la concha en mm, desde el «ápice o protoconcha» hasta el extremo posterior de la abertura o base de la «última espira» con la ayuda de un malacómetro manual tipo «L» con divisiones de 1 mm de marca Krausshenke modelo KHMalakos-200L (Elkarmi y Ismail, 2007). Para la emisión de las cercarias (método de emergencia), e inspección de las redias y los esporoquistes (método de trituración) se siguieron los criterios de Ladd y Rogowski (2012) y de Tolley-Jordan et al. (2022).
Los especímenes de M. tuberculata se individualizaron en pocillos de láminas excavadas con agua destilada, y la estimulación para la liberación de las cercarías se realizó mediante luz artificial por un periodo de 2 h (método de emergencia). Finalmente, las cercarías fueron teñidas in vivo con rojo neutro 0.5%. Para el método de trituración, todas las conchillas se diseccionaron para la separación del tejido blando. Este fue colocado entre dos portaobjetos y se realizó un squash en láminas porta y cubre objetos, con posterior observación a 10X en microscopio estereoscópico (Bdir yAdwan, 2011; Tolley-Jordan et al., 2022).
La identificación de M. tuberculata se realizó de acuerdo con las características de diagnóstico a nivel de morfoespecie (Vivar et al., 1990; Simone, 2006). Para la identificación de la especie de la redia-esporoquiste y de la cercaria para C. formosanus se siguieron claves de identificación e ilustraciones especializadas (Martin, 1972; Frandsen y Christensen, 1984; Scholz et al., 2000). Otras especies de larvas de trematodos fueron excluidas de la investigación.
El tamaño de muestra malacológica entre las tres lagunas que pudo ocasionar sesgo de captura de «hospederos activos» (Beldomenico y Begon, 2010) se descartó mediante una correlación de Spearman y por regresión lineal simple (logaritmo natural) entre la prevalencia y el tamaño de muestra (Torres et al., 2018). El análisis estadístico parasitológico correspondió a lo indicado por Reiczigel et al. (2019). Se calculó la prevalencia de las cercarias y los esporoquistes-redias de C. formosanus para las seis fechas y las tres lagunas de colecta. El test exacto de Fisher evaluó las diferencias de la prevalencia de las cercarias y los esporoquistes-redias de C. formosanus en relación a las fechas de recolecta y las lagunas, respectivamente. El análisis de las fechas requirió de las simulaciones de Monte Carlo (replicaciones = 20000), debido al número elevado de niveles de la variable. La posible desigualdad de la LT de la concha de M. tuberculata entre lagunas y fechas de colecta se evaluó mediante la prueba de «U» -Mann Whitney.
La posible asociación de los predictores de la ecología parasitaria como la temperatura del agua, profundidad, LT de la conchilla de M. tuberculata, prevalencia de las cercarias y las redias-esporoquiste de C. formosanus se evaluaron mediante la prueba no paramétrica Rho de Spearman y la regresión logística que empleó el AIC «criterio de información de Akaike», y el BIC «criterio de información de Bayes» del modelo estadístico. El análisis fue autónomo para cada laguna. En el caso de existir asociación significativa, se procedió a realizar un gráfico de densidad condicional basado en el teorema de Bayes. Todas las pruebas fueron evaluadas con un nivel de significancia de alfa igual a 0.05. Los análisis parasitológicos se realizaron utilizando el programa «Quantitative Parasitology» (Reiczigel et al., 2019). Para los gráficos se usó el paquete «ggplot2» del software R v. 3.5.1 (R Core Development Team, 2009; Wickham, 2016).
RESULTADOS
Longitud total de M. tuberculata como predictor de la ecología parasitaria de trematodos en el humedal costero Los Pantanos de Villa
Entre el 2009 y 2011 se recolectaron 2532 especímenes de M. tuberculata procedentes de las tres lagunas: Las Delicias (n = 1156), Mayor (n = 1017) y Marvilla (n = 359). La LT promedio (± EE) de la concha de M. tuberculata fue de 19.69 ± 11.00 mm, alcanzando un valor mínimo de 4 mm y máximo de 36 mm. El mayor tamaño de la LT de M. tuberculata se presentó en Marvilla con un promedio de 21.13 mm, valor significativamente mayor al que se encontró en Mayor y en Delicias (p<0.0001), y sin diferencias significativas entre estas últimas (Cuadro 2).
Cuadro 2. Estadísticos de la Longitud total (LT) de Melanoides tuberculata y prevalencia e intervalo de confianza del trematodo parásito Centrocestus formosanus por estadio larvario y por laguna evaluada en el humedal costero Los Pantanos de Villa (HCLPV), Lima, Perú

No se encontró relación entre el tamaño de muestra de caracoles por fecha con la prevalencia del trematodo C. formosanus, según la correlación de Spearman (r s = 0.14; p=0.80) y el coeficiente de determinación (R2 = 0.017; p=0.80), descartando la posible existencia de un sesgo de captura de moluscos «hospederos activos».
Prevalencia de trematodos parásitos en M. tuberculata en las tres lagunas del humedal costero Los Pantanos de Villa
La proporción global de ejemplares infectados con C. formosanus fue 26.89%, mientras que a nivel de estadio larvario la prevalencia global esporoquiste-redia y de la cercaria fue 18.25 y 24.64%, respectivamente. De acuerdo con el test exacto de Fisher, los valores de prevalencia encontrados exhibieron heterogeneidad con respecto a las tres lagunas evaluadas para esporoquistes-redia (p<0.0001) y para las cercarias (p<0.0001). Los caracoles evaluados en la Laguna Mayor presentaron las mayores prevalencias de C. formosanus, en tanto que el orden decreciente de prevalencias respondió de forma similar para esporoquiste-redia y la cercaria: Mayor > Marvilla > Las Delicias (Cuadro 2).
Años y temporadas de evaluación como predictores de la ecología parasitaria en M. tuberculata entre las tres lagunas en el humedal costero Los Pantanos de Villa
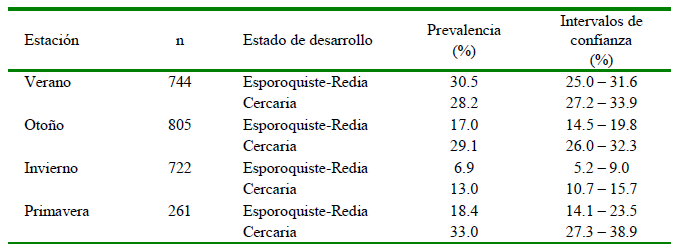
La prevalencia de esporoquiste-redia (p<0.0001) y de cercaria (p<0.0001) para C. formosanus por estación del año fueron significativamente diferentes. Para esporoquiste-redia alcanzó el mayor valor en verano (30.5%), y en la primavera se registró la mayor prevalencia de la cercaria (33%). En contraste, el invierno presentó las menores prevalencias de esporoquiste-redia (6.9%) y de la cercaria (13%) de C. formosanus (Cuadro 3).
Cuadro 3. Prevalencia e intervalo de confianza del trematodo parásito Centrocestus formosanus por estadio y estación del año en Melanoides tuberculata en el humedal costero Los Pantanos de Villa (HCLPV). Lima, Perú
El Cuadro 4 muestra el efecto predictor mediante la regresión logística usando laAIC y BIC con base a las variables: LT de M. tuberculata, temperatura del agua superficial de cada laguna (ºC), y profundidad del cuerpo de agua de cada laguna (cm) en la prevalencia de las cercarias y de los esporoquisteredia del trematodo parásito C. formosanus. La LT y la profundidad fueron predictores significativos para la prevalencia de la cercaria y de los esporoquiste-redia. En el caso de la temperatura del agua superficial de cada laguna solo fue predictor significativo para los esporoquiste-redia, pero no para las cercarías de C. formosanus.
Cuadro 4. Efecto predictor de la regresión logística de la longitud total (LT) de Melanoides tuberculata, de la temperatura del agua superficial de cada laguna, y de la profundidad del cuerpo de agua de cada laguna en la prevalencia de la cercaria y de los esporoquiste-redia del trematodo parásito Centrocestus formosanus en el humedal costero Los Pantanos de Villa (HCLPV), Lima, Perú
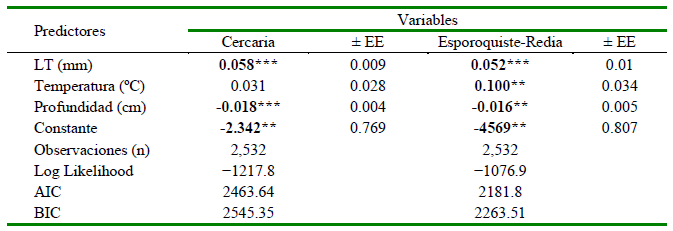
*p<0.05; **p<0.01; ***p<0.001
EE = error estándar; AIC = criterio de información de Akaike del modelo estadístico; BIC= criterio de información de Bayes
La figura 2 muestra el gráfico de probabilidad de incidencia basado en el teorema de Bayes para la temperatura superficial de la laguna (ºC), profundidad de la laguna (cm) y LT (mm) de M. tuberculata para la cercaria y esporoquiste-redia del trematodo parásito C. formosanus para cada una de las tres lagunas: A = Las Delicias, B = Mayor y C = Marvilla en el HCLPV, Lima, Perú. Todas mostraron asociaciones significativas, a excepción de la cercaria con la temperatura para la Laguna Las Delicias, la cercaria con la LT para Laguna Mayor, esporoquiste-redia con la profundidad de la Laguna Las Delicias, esporoquiste-redia con la LT para Laguna Mayor y para la Laguna Marvilla.
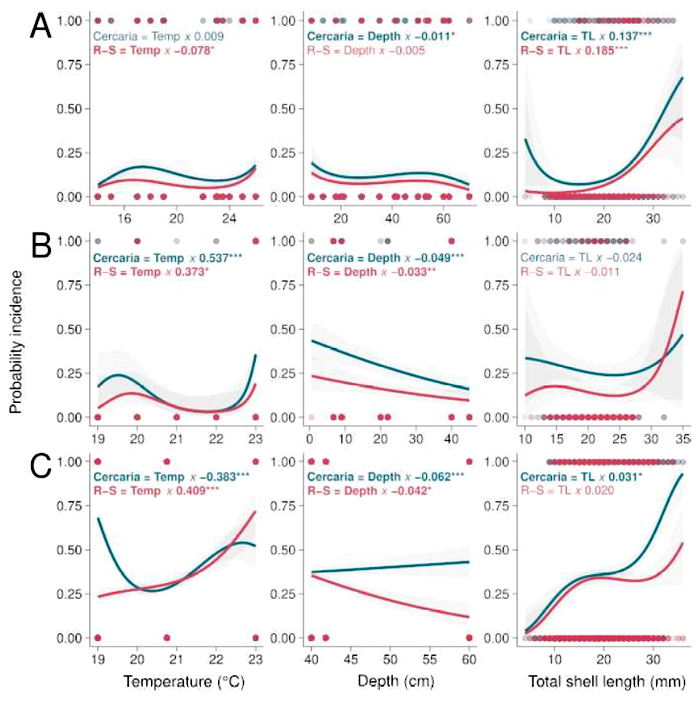
Figura 2. Probabilidad de incidencia basado en el teorema de Bayes para la temperatura superficial del agua (ºC), profundidad (cm) y longitud total (LT) (mm) de Melanoides tuberculata para la cercaria y los esporoquiste-redia (R-S) del trematodo parásito C. formosanus para las tres lagunas. A: Las Delicias. B: Mayor y C: Marvilla en el humedal costero Los Pantanos de Villa (HCLPV), Lima, Perú
DISCUSIÓN
Se encontró en estadio de esporoquisteredia y de cercaria al trematodo C. formosanus en M. tuberculata. El caracol cuerno M. tuberculata ha sido identificado como hospedero intermediario de ~40 especies de trematodos, encontrándose entre estos a agentes conocidos de enfermedades oculares e intestinales transmitidas por peces (Omondi-Outa et al., 2020; Pinto et al., 2023). En cuanto a M. tuberculata, la literatura científica registra las formas larvarias del trematodo parásito C. formosanus (Carranza et al., 2023; Pinto et al., 2023).
La prevalencia global de ejemplares infectados con C. formosanus fue de 26.89%, la prevalencia de esporoquiste-redia y de las cercarias fue del 18.25 y 24.64%, respectivamente. Autores como Pulido-Murillo et al. (2018) encontraron valores bastante bajos de prevalencia en M. tuberculata; así observaron que 112 (1.7%) estaban infectados con cercarias de heterófidos, y encontraron cercarias de C. formosanus en 71 (1.8%) de 3874 caracoles recolectados en el área de Conservación Regional los humedales de Ventanilla, Callao y en 29 (1.0%) de 2857 caracoles recolectados igualmente en dicha área. De igual forma se observó que en los hábitats nativos de M. tuberculata, la prevalencia de larvas de trematodos fue inferior al 5% y las infecciones tienden a agregarse espacialmente (Ladd y Rogowski, 2012; Tolley-Jordan y Chadwick, 2018). Sin embargo, en las áreas donde se introdujo este caracol como la del presente estudio, las tasas de infección fueron más altas, pudiendo llegar según algunos autores al 53% (Ladd y Rogowski, 2012).
El mayor tamaño de la LT de M. tuberculata se presentó en la Laguna Marvillas. La literatura señala que el tamaño de este puede estar relacionado con la prevalencia de infección por trematodos (Genner et al., 2008). Las dimensiones de las conchas de los moluscos dulceacuícolas pueden verse influenciadas por el parasitismo. La literatura científica señala que estos caracoles obtienen un mayor tamaño cuando se encuentran infectados con trematodos (Nunes-dos Santos et al., 2013). En el presente estudio los caracoles de la Laguna Marvilla, considerada como de perturbación baja, presentaron un mayor tamaño que los ambientes de perturbación media (Laguna Mayor) y alta (Laguna Las Delicias).
Los caracoles de la Laguna Mayor mostraron las mayores prevalencias de C. formosanus, donde el orden decreciente de prevalencias respondió de forma similar para las cercarias y los esporoquiste-redia (Mayor > Marvilla > Las Delicias). Se informa una baja prevalencia de trematodos en caracoles de hábitats acuáticos que enfrentan presiones antropogénicas, como la presencia de metales pesados que tienen efectos negativos y adversos en las etapas de vida libre de los trematodos (miracidios y cercarias) y, por lo tanto, afectan su transmisión (Tramboo et al., 2022). Esto puede tener efectos de amplio alcance y duraderos en la población del parásito, lo que lleva a una baja prevalencia en los caracoles a pesar de una alta abundancia de hospederos (Omondi-Outa et al., 2020).
Por otro lado, Omondi-Outa et al. (2020) sugieren una alta prevalencia de trematodos que corresponden a ambientes con poca influencia antropogénica, y una baja prevalencia de especies de trematodos lo que reflejan condiciones ambientales degradadas. El presente estudio concuerda con dichos hallazgos toda vez que se observaron valores más altos de prevalencia de esporoquistes-redia y cercaria de C. formosanus en la Laguna Mayor considerada de perturbación media y en la Laguna Marvilla considerada como de perturbación baja, pero una prevalencia más baja de esporoquistes-redia y de las cercarias de trematodos en M. tuberculata en la Laguna Las Delicias considerada de alta perturbación antropogénica.
La variación estacional de las cercarias de los trematodos parásitos depende de la ubicación de los hospederos vertebrados definitivos, de la disponibilidad y de la población de los caracoles hospederos intermediarios, de las posibilidades de contacto de la larva de miracidio que nada libremente a los caracoles hospederos, del comportamiento de los caracoles y finalmente de los factores abióticos como las precipitaciones anuales (Lal y Vishvajeet, 2020). En el presente trabajo en la primavera se registró la mayor prevalencia de cercarias de C. formosanus, mientras que el esporoquiste-redia alcanzó el mayor valor durante verano.
La regresión logística mostró que la LT y la profundidad fueron predictores significativos para la prevalencia de las cercarias y de los esporoquiste-redia de C. formosanus. En el caso de la temperatura del agua superficial de cada laguna solo fue predictor significativo para los esporoquiste-redia del trematodo parásito, pero no para las cercarias. Los gráficos de densidad condicional basados en el teorema de Bayes mostraron asociaciones significativas para la mayoría de las variables, a excepción de las cercarias con la temperatura para la Laguna Las Delicias, cercaria con la LT para laguna Mayor, esporoquiste-redia con la profundidad de la laguna Las Delicias, y esporoquisteredia con la LT para laguna Mayor y para la laguna Marvilla.
La LT del caracol, la profundidad y la temperatura del agua superficial fueron predictores significativos para la ecología parasitaria de las cercarias y del esporoquisteredia de C. formosanus en M. tuberculata en el HCLPV, Lima, Perú. Los resultados concuerdan con la literatura académica, la cual ha demostrado que el tamaño corporal y la infección por trematodos pueden asociarse en las distribuciones espaciales y las asociaciones de hábitat en los caracoles acuáticos invasores como M. tuberculata (Tolley-Jordan y Chadwick, 2018). Así, una relación positiva entre el tamaño corporal del caracol y la infección también podría deberse a modificaciones tisulares, específicamente, el desarrollo de tejidos gonadales. La alimentación de los trematodos con tejido gonadal, y la resultante castración de los caracoles ocurre con frecuencia en M. tuberculata y puede ser necesaria para que algunos trematodos completen su desarrollo larvario (Tolley-Jordan y Chadwick, 2018).
CONCLUSIONES
El mayor tamaño de la longitud total (LT) de M. tuberculata se presentó en la laguna Marvilla, en comparación con Mayor y Las Delicias.
La prevalencia de C. formosanus fue en esporoquiste-redia de 18.25% y en la cercaria de 24.64%. El orden decreciente de prevalencia para esporoquiste-redia y la cercaria para las lagunas fue Mayor > Marvilla > Las Delicias. El esporoquiste-redia presentó el mayor valor en verano, y la primavera registró la mayor prevalencia de la cercaria.
La regresión logística mostró que la LT del caracol y la profundidad de la laguna fueron predictores significativos para la prevalencia de esporoquiste-redia y cercaria de C. formosanus. En el caso de la temperatura superficial del agua de cada laguna solo fue predictor significativo para el esporoquiste-redia, pero no para la cercaría.
La densidad condicional basados en el teorema de Bayes mostraron asociaciones significativas para la todas de las variables, a excepción de la cercaria con la temperatura para la laguna Las Delicias, la cercaria con la LT para laguna Mayor, esporoquiste-redia con la profundidad de la laguna Las Delicias, y esporoquiste-redia con la LT para Lagunas Mayor y Marvilla.












 uBio
uBio