INTRODUCCIÓN
La paracoccidioidomicosis es una enfermedad infecciosa crónica causada por el hongo dimórfico Paracoccidioides spp., que incluye Paracoccidioides lutzii y el complejo Paracoccidioides brasiliensis, el cual abarca linajes como P. brasiliensis en sentido estricto (S1a y S1b), P. americana (PS2),
P. restrepiensis (PS3) y P. venezuelensis (PS4). El hongo tiene una fase micelial con conidios infecciosos a temperaturas inferiores a 28 °C y una fase levaduriforme a 37 °C, adaptándose a diferentes ambientes térmicos 1.
La paracoccidioidomicosis es endémica de América Latina, siendo más prevalente en Brasil, Argentina, Paraguay, Venezuela y Colombia 1. En Perú, la enfermedad se encuentra en áreas rurales y selváticas, especialmente en la ceja de selva y la selva baja amazónica, con casos reportados en Ucayali, Huánuco, Cerro de Pasco, Loreto, San Martín, Cusco, Ayacucho, Huancavelica y Madre de Dios 2.
La infección se adquiere por la inhalación de esporas del hongo Paracoccidioides, produciendo inicialmente una infección pulmonar que puede diseminarse a otros órganos 1. No existe correlación entre la especie y las manifestaciones clínicas de la enfermedad 3. Afecta predominantemente a hombres, especialmente agricultores rurales expuestos al hongo 4, que cumplan con ciertos factores, como el tabaquismo, el consumo excesivo de alcohol y condiciones de inmunosupresión, como infección por el virus de inmunodeficiencia humana (VIH), linfomas, receptores de trasplantes de órganos y usuarios de inmunosupresores 4,5.
Una coinfección rara pero documentada es con el virus linfotrópico de células T humano (HTLV-1). Aunque su impacto en la progresión de la enfermedad aún no está completamente claro 6, se ha sugerido que la inmunosupresión inducida por HTLV-1 podría influir en la evolución de la enfermedad.
Presentamos el caso de un hombre con paracoccidioidomicosis diseminada, con afectación de mucosas, piel y pulmones, y con coinfección por HTLV-1, ofreciendo perspectivas sobre el papel de esta asociación en el curso de la enfermedad.
PRESENTACIÓN DE CASO
Varón de 68 años, natural de Huancayo y residente de Lima, Perú, carpintero de ocupación. Tiene como antecedente tuberculosis pulmonar tratada hace 30 años y vitíligo hace cinco. Al momento de la consulta, se encontraba con tratamiento irregular con clobetasol, triamcinolona y tacrolimus.
Presentó un cuadro de seis meses de dolor abdominal tipo cólico moderado e intermitente, astenia progresiva e hiperpigmentación en las mucosas, el rostro, los brazos y las manos. Cuatro meses antes, fue hospitalizado por coledocolitiasis, con lito de 30 x 13 mm y colédoco de 16 mm, siendo sometido a laparotomía exploratoria y colecistectomía por colangitis moderada. Un mes previo al ingreso, persistía el dolor abdominal, acompañado de exacerbación de la astenia, cefalea frontoparietal pulsátil, odinofagia progresiva, pérdida de ocho kilos y disfagia a sólidos. Una semana antes de su ingreso, presentó fiebre, odinofagia intensa, diaforesis, escalofríos, náuseas y episodios de vómito bilioso. Ingresó a emergencias con presión arterial de 80/50 mmHg y glucemia de 57 mg/dl.
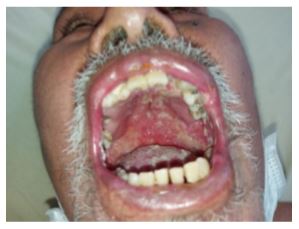
El examen físico, realizado en mayo de 2024, mostró hiperpigmentación en manos y pliegues cutáneos, así como máculas acrómicas en el cuero cabelludo y las extremidades inferiores, sin nevus ni tumoraciones. Presentaba macroqueilia, especialmente en el labio superior, y múltiples lesiones ulcerativas en la cavidad bucal. Estas úlceras eran superficiales, de bordes irregulares, con un fondo granular amarillento y puntos rojos, caracterizando el patrón de “piel de fresa”, típico de la estomatitis moriforme de Aguiar-Pupo (Figura 1). En la auscultación pulmonar, se identificaron ruidos crepitantes en el tercio inferior de ambos pulmones. A nivel abdominal, se palpó una masa de 7 x 5 cm en la fosa iliaca derecha, con leve dolor a la palpación profunda. Neurológicamente, el paciente estaba somnoliento, con reflejos osteotendinosos sin alteraciones.
Los parámetros hematológicos mostraron hemoglobina de 13,3 mg/dL, leucocitos de 16 000 células/µL y linfopenia severa de 400 células/µL. En los parámetros bioquímicos, se evidenció hiponatremia (122 mEq/l) e hiperpotasemia (5,4 mEq/l). La gasometría arterial reveló acidosis respiratoria con pH 7,31, pCO2 de 48,5 mmHg y HCO3 de 21,7 mEq/L. La serología para HTLV-1 fue positiva, mientras que la prueba para VIH resultó negativa. Las baciloscopias seriadas y la prueba Xpert MTB/RIF fueron también negativas.
La tomografía torácica mostró lesiones nodulares y micronodulares diseminadas con predominio peribroncovascular y subpleural, acompañadas de bronquiectasias en las regiones apicales (Figura 2).
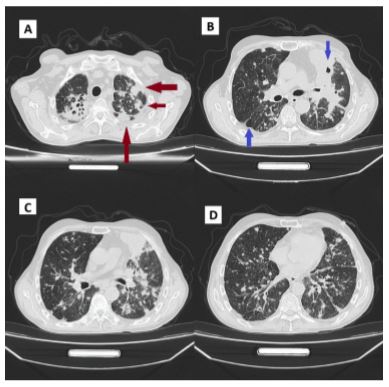
Figura 2 Tomografía de tórax. A) Patrón nodular en lóbulos superiores (flechas rojas) compatible con paracoccidioidomicosis. B) Cavitaciones en los lóbulos inferiores (flechas azules). C) Extensión de la enfermedad a la periferia pulmonar. D) Áreas de consolidación con patrón en vidrio esmerilado.
La tomografía abdominal contrastada mostró múltiples nódulos hipodensos en el parénquima hepático, sugestivos de compromiso micótico diseminado. Además, una leve dilatación del colédoco. En la fosa iliaca derecha, se identificó una lesión hipodensa quística bien delimitada (Figura 3).
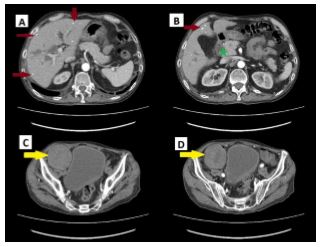
Figura 3 Tomografía de abdomen contrastada. A) Nódulos hipodensos en el parénquima hepático (flecha roja). B) Dilatación del colédoco (asterisco verde). C) y D) Lesión quística en fosa ilíaca derecha (flecha amarilla).
Se realizó una biopsia incisional de una placa papulomatosa en las mucosas de los paladares duro y blando. El análisis histológico con hematoxilina-eosina (H-E) y ácido periódico de Schiff (PAS) reveló epitelio plano paraqueratinizado con acantosis e hiperplasia pseudoepiteliomatosa. El corion mostró infiltrado linfoplasmocitario, histiocitos, algunas células gigantes multinucleadas y tejido de granulación. También se observaron estructuras redondas basofílicas (3-20 μm) compatibles con levaduras PAS positivas, rodeadas por un halo claro y vacuolas colapsadas. Algunas levaduras presentaban gemaciones con la característica morfología de “timón de barco”, confirmando el diagnóstico de paracoccidioidomicosis (Figura 4).
El cultivo de aspirado bronquial fue positivo para Staphylococcus aureus y Klebsiella pneumoniae. La prueba de Papanicolau y la técnica Block Cell del aspirado bronquial fueron negativas para la presencia de células malignas. Asimismo, la citología de la tumoración abdominal reveló células desvitalizadas con pigmento negruzco, sugiriendo melanoma metastásico.
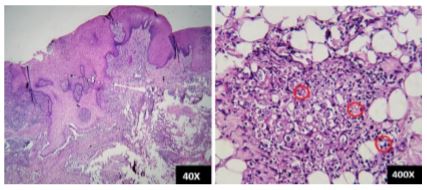
Figura 4 Hallazgos histopatológicos de la biopsia de la lesión. Corte histológico con tinción PAS a 400×, donde se evidencian levaduras redondeadas PAS positivas con gemaciones características en forma de “timón de barco” (círculos rojos).
El paciente evolucionó desfavorablemente, desarrollando hipoxemia y falla multiorgánica, y falleció tras 20 días de hospitalización, pese al tratamiento con antibióticos, anfotericin B e inotrópicos.
DISCUSIÓN
La paracoccidioidomicosis es una micosis sistémica endémica en América Latina; Brasil concentra alrededor del 80 % de los casos 1,4. En Perú, está subdiagnosticada, particularmente en zonas rurales como Oxapampa, donde el paciente trabajó como agricultor. Esta enfermedad afecta principalmente la mucosa oral y los pulmones en adultos, siendo común en la forma crónica 1,4. En nuestro caso, se observaron úlceras granulomatosas en las encías, el paladar y la lengua, características de la enfermedad 7. Estas lesiones causan odinofagia, disfagia y disfonía, afectando la calidad de vida del paciente 1,4,8.
El compromiso pulmonar en la paracoccidioidomicosis crónica, que afecta hasta al 95 % de los pacientes, puede ser asintomático o presentar síntomas respiratorios inespecíficos.
En este paciente, los estudios radiológicos mostraron lesiones bilaterales y simétricas, predominantemente en las regiones parahiliares, con nódulos dispersos y opacidades alveolares, características típicas de la forma crónica de la enfermedad 1,5,8. Estos hallazgos, que afectan más de un tercio del parénquima pulmonar, son sugestivos de una afección grave 9, especialmente cuando se observa un patrón en “alas de mariposa” en las zonas medias de ambos pulmones 5. Aunque el agrandamiento de ganglios mediastínicos o hiliares y los derrames pleurales son raros en la forma crónica, su presencia puede orientar el diagnóstico diferencial. Estos hallazgos fueron claves para diferenciar la paracoccidioidomicosis de otras enfermedades pulmonares, como la tuberculosis 10 y las metástasis pulmonares. Además, la histopatología reveló la presencia de levaduras con gemaciones en “timón de barco”, un hallazgo característico de la enfermedad 1. La negatividad de las baciloscopias, del Xpert MTB/RIF, de la técnica Block Cell y de la prueba de Papanicolau del aspirado bronquial alejan aún más la posibilidad de tuberculosis y metástasis pulmonar, confirmando así el diagnóstico, incluso en ausencia de métodos moleculares como la PCR para paracoccidioidomicosis.
Un hallazgo importante fue la insuficiencia suprarrenal, que se presenta en hasta el 50 % de los casos de paracoccidioidomicosis crónica diseminada 1. Esta afectación explicaba los síntomas gastrointestinales inespecíficos y la astenia marcada del paciente 11. La afectación suprarrenal destaca la importancia de un monitoreo estricto y un tratamiento oportuno, ya que la insuficiencia suprarrenal, si no se aborda a tiempo, puede progresar a una crisis addisoniana, una complicación potencialmente mortal 1. Desafortunadamente, el compromiso suprarrenal por paracoccidioidomicosis no pudo ser confirmado mediante biopsia debido a los riesgos del procedimiento en el estado del paciente.
El HTLV-1 es un retrovirus que infecta linfocitos T CD4+ y se asocia a enfermedades graves como leucemia/linfoma de células T del adulto y mielopatía/paraparesia espástica tropical. También se ha asociado a presentaciones severas de enfermedades infecciosas, tales como tuberculosis, sarna noruega y formas graves de estrongiloidiosis. La coinfección con paracoccidioidomicosis ha sido observada en inmunosuprimidos, pudiendo agravarse la micosis, probablemente, debido a la alteración de la inmunidad celular mediada por linfocitos T 6,12-14. En este paciente, la coinfección con el HTLV-1 podría explicar las dificultades en el manejo clínico, debido a una manifestación más severa de la micosis. Esto, junto con infecciones bacterianas secundarias como Staphylococcus aureus y Klebsiella pneumoniae, contribuyeron al deterioro progresivo del paciente y su falla multiorgánica.
El tratamiento de primera línea para la paracoccidioidomicosis es itraconazol (200 mg/día durante 6-9 meses en enfermedad leve y 12-18 meses en formas moderadas). En casos graves, se recomienda anfotericina B liposomal (3-5 mg/kg/día), seguida de azoles orales. La trimetoprima-sulfametoxazol es menos efectiva, requiere tratamientos prolongados (24 meses) y presenta mayores tasas de recaída 1,4.
En conclusión, la sospecha de melanoma metastático en este paciente resalta la necesidad de considerar posibles complicaciones derivadas de la inmunosupresión local, favorecida por la paracoccidioidomicosis y la coinfección con HTLV-1. Si bien la asociación entre paracoccidioidomicosis y neoplasias no está bien definida, se han reportado casos de neoplasias, siendo los carcinomas de células escamosas los más frecuentes, seguidos de neoplasias hematológicas 15.
Este caso presenta limitaciones, como la falta de biopsia suprarrenal y la ausencia de estudios longitudinales, lo que dificulta la evaluación del impacto de la coinfección con HTLV-1 en el pronóstico de la paracoccidioidomicosis. La detección temprana, un enfoque diagnóstico exhaustivo y un tratamiento adecuado son cruciales para mejorar el pronóstico y reducir la mortalidad, especialmente en pacientes con evolución atípica o respuesta insuficiente al tratamiento antifúngico.