INTRODUCCIÓN
El cáncer de cuello uterino es el cuarto cáncer más común en mujeres 1,2. Durante el 2006-2012, el 14.9% de todos los casos de cáncer notificados en el Perú, fueron cáncer de cuello uterino 3. Un tratamiento precoz en estadios tempranos, donde la enfermedad tiene una extensión de milímetros o unos pocos centímetros ofrece altas probabilidades de ser efectivo 4.
Por ello, la Dirección de Guías de Práctica Clínica, Farmacovigilancia y Tecnovigilancia del Instituto de Evaluación de Tecnologías en Salud e Investigación (IETSI) del Seguro Social del Perú (EsSalud) elaboró la guía de práctica clínica (GPC) basada en evidencias para el manejo de cáncer de cuello uterino estadios tempranos (IA1, IA2, IB1, IB2 o IIA1), cuyas preguntas y recomendaciones se presentan en la tabla 1. El presente artículo es un resumen de dicha GPC.
METODOLOGÍA
El procedimiento seguido para la elaboración de la presente GPC está detallado en su versión “in extenso”, la cual puede descargarse de la página web del IETSI de EsSalud (http://www.essalud.gob.pe/ietsi/guias_pract_clini.html).
En resumen, se aplicó la siguiente metodología:
Conformación del grupo elaborador de la guía local (GEG): Este incluyó metodólogos y médicos especialistas en gineco-oncología, cirugía oncológica y oncología médica.
Formulación de preguntas: Se formularon 8 preguntas clínicas (Tabla 1), cada una de las cuales pudo tener una o más preguntas PICO (Population, Intervention, Comparator, Outcome). A su vez, cada pregunta PICO pudo tener uno o más desenlaces (o outcomes) de interés.
Búsqueda y selección de la evidencia: Para cada pregunta PICO, se realizó la búsqueda y selección de la evidencia. Para ello, durante el 2017-2018 se buscaron revisiones sistemáticas (RS) publicadas como artículos científicos (mediante búsquedas sistemáticas en PubMed, Embase y CENTRAL) o realizadas como parte de una GPC previa (mediante una búsqueda sistemática de GPC sobre el tema) (Apéndice S1). Cuando se encontraron RS de calidad aceptable, se escogió una RS para la toma de decisiones, la cual fue actualizada cuando el GEG lo consideró necesario. Cuando no se encontró ninguna RS de calidad aceptable, se realizó una búsqueda de novo de estudios primarios.
Evaluación de la certeza de la evidencia: La certeza de la evidencia para cada desenlace de cada pregunta PICO pudo ser alta, moderada, baja, o muy baja (tabla 2). Para evaluar la certeza de la evidencia, se siguió la metodología de Grading of Recommendations Assessment, Development, and Evaluation (GRADE) 5 y se usaron tablas de perfiles de evidencias de GRADE (Apéndice S2). Finalmente, se le asignó a la pregunta PICO el nivel de certeza más bajo alcanzado por alguno de estos desenlaces.
Formulación de las recomendaciones: El GEG revisó la evidencia seleccionada para cada pregunta clínica en reuniones periódicas, y formuló recomendaciones fuertes o condicionales (tabla 2) usando la metodología GRADE 6. Para ello, se tuvo en consideración: 1) Beneficios y daños de las opciones, 2) Valores y preferencias de los pacientes, 3) Aceptabilidad por parte de los profesionales de salud, 4) Factibilidad de las opciones en los establecimientos de salud de EsSalud, y 5) Uso de recursos. Luego de discutir estos criterios para cada pregunta, el GEG formuló las recomendaciones por consenso o por mayoría simple. Asimismo, el GEG formuló puntos de buenas prácticas clínicas (BPC), usualmente en base a su experiencia clínica.
Revisión por expertos externos: La presente GPC fue revisada en reuniones con médicos especialistas representantes de otras instituciones y tomadores de decisiones. Asimismo, su versión “in extenso” fue enviada por vía electrónica a expertos externos para su revisión (mencionados en la sección de agradecimientos). El GEG tuvo en cuenta los resultados de estas revisiones para modificar las recomendaciones finales.
Aprobación de la GPC: La presente GPC fue aprobada para su uso en EsSalud, con Resolución N 27-IETSI-ESSALUD-2020.
Actualización de la GPC: La presente GPC tiene una validez de tres años. Al acercarse al fin de este período, se procederá a realizar una RS de la literatura para su actualización, luego de la cual se decidirá si se actualiza la presente GPC o se procede a realizar una nueva versión.
Recomendaciones
Se abordaron 8 preguntas clínicas en relación al manejo quirúrgico primario y adyuvante de cáncer de cuello uterino en estadios tempranos. En base a dichas preguntas se formularon 10 recomendaciones (2 recomendaciones fuertes y 8 recomendaciones condicionales), 7 puntos de buena práctica clínica, y 4 flujogramas (ver Tabla 1 y Figuras 1-4).
La presente GPC se enfoca en los pacientes con cáncer de cuello uterino estadio tempranos (IA1, IA2, IB1, IB2 o IIA1), en esta etapa de la enfermedad, se debe decidir el tipo de terapia a usar (pregunta 1 y 2), qué procedimientos y técnicas quirúrgicas usar (pregunta 3 y 4), sobre el abordaje de mujeres con deseo de mantener fertilidad (preguntas 5 y 6), y finalmente sobre alguna terapia adyuvante, de ser necesaria (pregunta 7 y 8).
A continuación, se expondrán las recomendaciones para cada pregunta clínica, así como un resumen del razonamiento seguido para llegar a cada recomendación.
Pregunta 1: En mujeres con cáncer de cuello uterino en estadios tempranos (IA1, IA2, IB1, IB2 o IIA1), ¿cuál debería ser el tratamiento inicial?
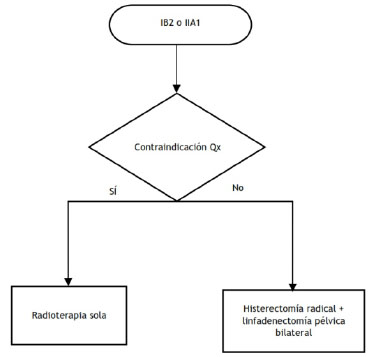
En mujeres con cáncer de cuello uterino en estadios tempranos, se suele usar la cirugía como terapia estándar, pero existen otras alternativas: la radioterapia y quimioterapia. La cirugía remueve el tejido comprometido, mientras que en la radioterapia y la quimioterapia no se remueve tejido, sino se eliminan las células cancerosas a través de radiación y medicamentos, respectivamente 7,8.
El ensayo clínico aleatorizado (ECA) de Landoni (n=337) 9 comparó cirugía vs radioterapia y no encontró diferencias entre ellas para sobrevivencia (general o libre de enfermedad) a los 5 años, ni recaída; sin embargo, la radioterapia disminuyó el riesgo morbilidad de grado 2-3 (que requiera tratamiento médico o quirúrgico) en comparación con la cirugía. Por otro lado, se hallaron estudios observacionales que describen eventos adversos a largo plazo de la radioterapia (diarrea, náuseas, sangrado rectal, cistitis, problemas urinarios, disfunciones sexuales entre otros) 10,11.
No se halló evidencia para quimioterapia.
El GEG considera que el balance de beneficios y daños es similar para cirugía y radioterapia; sin embargo, siendo, la cirugía, la práctica más extendida entre los profesionales, y no habiéndose evidenciado beneficios adicionales con la radioterapia, el GEG decide emitir una recomendación a favor de la cirugía.
A pesar que la certeza de la evidencia fue muy baja, el GEG considera que la cirugía permite evaluar directamente la magnitud del daño y asegurarse del estado ganglionar de la mujer, por lo que decide emitir una recomendación fuerte .
Puntos de BPC:
Pregunta 2: En mujeres con cáncer de cuello uterino en estadio tempranos (IA1, IA2, IB1, IB2 o IIA1), ¿qué tratamiento quirúrgico debería realizarse?
Los tratamientos quirúrgicos disponibles son la histerectomía simple o radical, traquelectomía y conización. Difieren entre sí respecto a la extensión de la remoción de tejido. La histerectomía remueve la totalidad del útero con o sin anexos, la traquelectomía, todo el cuello uterino, y la conización, una porción del cuello uterino 12,13.
La RS de Feng 14 (4 estudios observacionales -EO-, n=616), no encontró diferencias entre histerectomía radical y traquelectomía para sobrevivencia (general y libre de enfermedad a los 5 años) ni eventos adversos (transfusión sanguínea, complicaciones intraoperatorias y post operatorias). No se hallaron estudios que compararan conización con los otros procedimientos quirúrgicos.
Debido a la ausencia de ECA que comparen estas intervenciones, el GEG consideró que la evidencia hallada no es suficiente para demostrar que una es mejor que la otra. Sin embargo, considera que realizar una cirugía en la que haya remoción de mayor tejido sería lo más prudente, y se emitió una recomendación a favor de la histerectomía radical.
Debido a la baja certeza de la evidencia, se emitió una recomendación condicional .
Puntos de BPC:
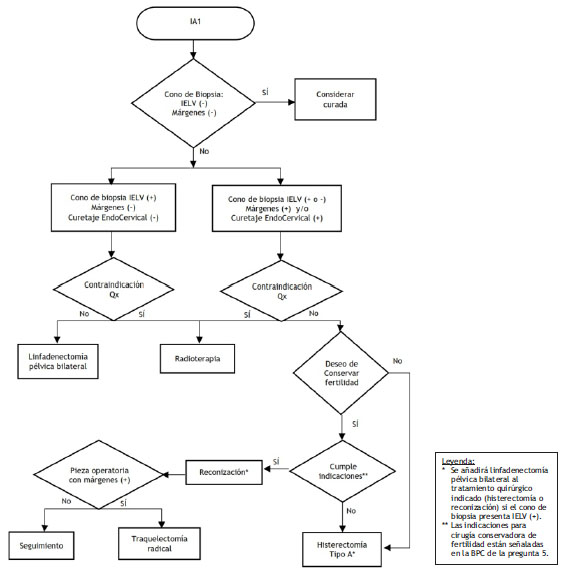
El GEG considera que en estadios donde la extensión del tejido comprometido no excede los tres milímetros (mm), se puede optar por una terapia menos invasiva, siempre que se tengan en cuenta ciertas características (compromiso de márgenes, invasión del espacio linfovascular -IELV-, y resultado del curetaje endocervical -CEC-).
En aquellas mujeres en estadio IA1 con márgenes libres de por lo menos de 3 mm 15 sin IELV y CEC negativo, el GEG considera que no se necesitaría otra intervención terapéutica más allá del seguimiento.
En aquellas mujeres en estadio IA1 con márgenes libres de por lo menos de 3 mm 15 con CEC negativo, pero con IELV, el GEG considera que se debe realizar evaluación ganglionar pélvica debido la asociación de IELV con pobre sobrevida 16-18.
En aquellas mujeres en estadio IA1 con márgenes positivos y/o CEC positivo, pero sin IELV, el GEG considera que se debe realizar solo histerectomía tipo A 16,19.
En aquellas mujeres en estadio IA1 con márgenes positivos y/o CEC positivo y con IELV, el GEG considera que se debe realizar histerectomía tipo A más evaluación ganglionar pélvica, debido a un mayor riesgo de metástasis 16,19.
En mujeres con indicación de histerectomía, se consideró realizar cirugía conservadora de inervación pélvica para evitar secuelas vesicales, rectales y sexuales que deterioran la calidad de vida de las mujeres 20,21.
En mujeres tratadas quirúrgicamente sin signos de progresión en la pieza patológica, la frecuencia del seguimiento debe ser cada 6 meses durante los 5 primeros años, y luego anualmente. En cada consulta se realizará una radiografía de tórax, examen físico, papanicolaou y ecografía pélvica dependiendo de los síntomas.
Pregunta 3: En mujeres con cáncer de cuello uterino en estadios tempranos (IA1, IA2, IB1, IB2 o IIA1) con indicación de evaluación ganglionar pélvica, ¿se debería realizar biopsia de ganglio centinela o linfadenectomía pélvica bilateral como parte del manejo quirúrgico?
La linfadenectomía pélvica bilateral extrae todo el tejido linfático pélvico para su posterior evaluación microscópica, mientras que, para la biopsia de ganglio centinela, se detecta y extrae los primeros ganglios linfáticos a los que drena el tumor en cada lado de la pelvis para su posterior evaluación. Este último es menos invasivo 22,23.
El estudio observacional de Lenox 2017 24 (n=1078) no encontró diferencias entre linfadenectomía pélvica bilateral y biopsia de ganglio centinela en términos de sobrevida libre de recurrencia, complicaciones intraoperatorias, transfusión sanguínea, morbilidad a corto plazo e infección post operatoria.
A pesar que la biopsia de ganglio centinela es menos invasiva que la linfadenectomía pélvica bilateral, el GEG considera que la evidencia es insuficiente para determinar la comparabilidad de las intervenciones. Por ende, se consideró que, por ahora, un procedimiento más invasivo ofrecería mejor información para evaluar compromiso ganglionar. Por ende, se emitió una recomendación a favor de la linfadenectomía pélvica bilateral.
Debido a la baja certeza de la evidencia, se decidió emitir una recomendación condicional .
Puntos de BPC:
Pregunta 4: En mujeres con cáncer de cuello uterino en estadios temprano (IA1, IA2, IB1, IB2 o IIA1), ¿se debería realizar cirugía laparoscópica o cirugía abierta?
Ambas son técnicas quirúrgicas ampliamente utilizadas en diferentes tipos de cirugías. La cirugía laparoscópica ofrece menores complicaciones que la laparotomía y aparentemente presenta la misma eficacia 25. Sin embargo, estudios recientes advierten de un escenario distinto 26.
La RS de Zhao 25 (23 EO n=4205) no encontró diferencias entre cirugía laparoscópica y laparotomía para recurrencia ni complicaciones intraoperatorias, pero encontró que la cirugía laparoscópica presentaba menor posibilidad de trasfusión sanguínea y menor tiempo de estancia hospitalaria comparado con la laparotomía. Por otro lado, el ECA de Ramírez (26) (n=631) encontró, en un tiempo de seguimiento menor al programado, que la cirugía laparoscópica presentaba mayor probabilidad de recurrencia de enfermedad o muerte por cáncer de cuello uterino, recurrencia loco-regional, y muerte por cualquier causa que el grupo de laparotomía.
Ambos estudios llegan a conclusiones diferentes y presentan sesgos importantes. El GEG optó por una posición conservadora y decidió emitir una recomendación a favor de la laparotomía o cirugía abierta debido a que el ECA de Ramírez 26 sugiere una mayor mortalidad en el grupo de mujeres a las que se les realizó cirugía laparoscópica.
Debido a que la certeza de la evidencia fue muy baja, se decide emitir una recomendación condicional.
Pregunta 5: En mujeres con cáncer de cuello uterino en estadios tempranos (IA1, IA2, IB1, IB2 o IIA1), ¿cuáles son las indicaciones de cirugía conservadora de fertilidad?
La cirugía conservadora de fertilidad es aquella, menos invasiva, que preserva el útero para posibles futuras gestaciones. Sin embargo, el deseo de maternidad en sí no es suficiente para realizarla, algunas características de la enfermedad de cada mujer limitarían esta posibilidad.
Se hizo una búsqueda de factores o características en las cuales se podría realizar una cirugía conservadora de fertilidad con la misma seguridad y eficacia que las técnicas quirúrgicas estándar.
No se hallaron estudios para responder a esta pregunta por lo que se decide emitir un punto de BPC.
Puntos de BPC:
El GEG tomó en consideración las recomendaciones de otras GPC y estudios observacionales que señalaban al tamaño tumoral como un factor de riesgo para recurrencia 27-29, así como los tumores de células neuroendocrinas 30, y metástasis en nódulos linfáticos 31. Por lo que, en consenso, se precisaron las siguientes indicaciones para realizar cirugía conservadora de fertilidad:
Deseo explícito de preservar la fertilidad
Posibilidad de conseguir un embarazo.
Estadios IA1-IB1 según FIGO.
Tamaño de la lesión de menos de 2 cm.
No evidencia de metástasis en los ganglios de la pelvis según evaluación radiológica (resonancia magnética).
No evidencia de tumor de células neuroendocrinas u otros tipos no frecuentes.
Pregunta 6: En mujeres con cáncer de cuello uterino en estadio IA1, IA2 o IB1 ¿qué cirugía conservadora de fertilidad se debería realizar: conización o traquelectomía?
Ambos procedimientos conservan el útero para una futura gestación; sin embargo, la traquelectomía remueve mayor tejido, mientras que la conización solo remueve una porción del cuello uterino.
Se buscaron estudios realizados en mujeres con criterios para cirugía conservadora de fertilidad; sin embargo, no se hallaron comparaciones directas entre conización y traquelectomía. La RS de Kyrgiou 32 (24 EO, n=3 793 874) encontró que las mujeres con conización tenían mayor probabilidad de prematuridad, prematuridad severa, prematuridad extrema y mortalidad perinatal que las mujeres sin tratamiento. La RS de Zhang 33 (60 EO de un solo brazo n=2854) encontró que, los estudios que incluían mujeres con conización presentaban una tasa mayor de embarazos, una tasa similar de aborto, y una tasa menor de parto pretérmino que los estudios de mujeres con traquelectomía radical.
La evidencia es insuficiente para evaluar eficacia terapéutica de ambas terapias; sin embargo, el GEG ha sugerido que la histerectomía radical, remoción de tejido más extensa que las intervenciones evaluadas, sea el tratamiento estándar (ver pregunta 2). Sin embargo, en términos obstétricos, la evidencia sugiere que conización (remoción de tejido menos extensa) tendría mejores resultados que traquelectomía.
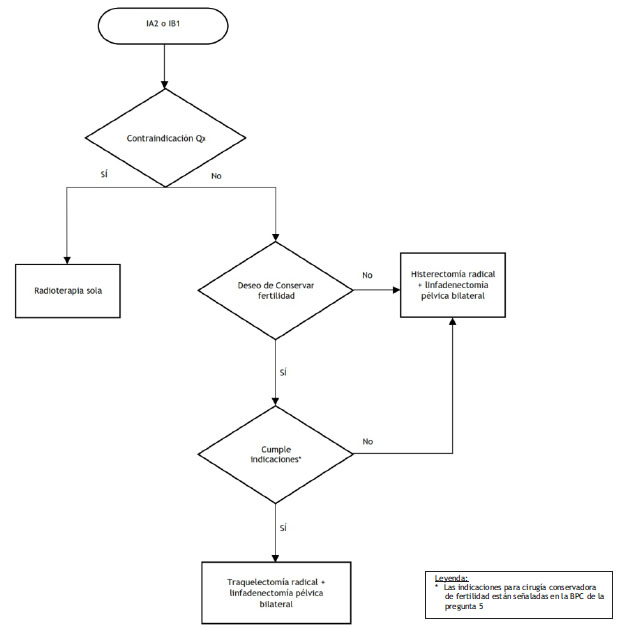
El GEG considera, además, el estadio y características de la enfermedad y, por ende, decide emitir tres recomendaciones. En mujeres con estadio IA1 con cono de biopsia con márgenes positivos y/o CEC positivo, y sin IELV, decide emitir una recomendación a favor de re-conización con diámetro más amplio. En mujeres con cáncer de cuello uterino estadio IA1 con cono de biopsia con márgenes positivos y/o CEC positivo, con IELV decide emitir una recomendación a favor de reconización con diámetro más amplio más linfadenectomía pélvica bilateral, pudiendo ésta última ser realizada por vía laparoscópica. Y en mujeres con cáncer de cuello uterino estadios IA2 o IB1 decide emitir una recomendación a favor de traquelectomía radical más linfadenectomía pélvica bilateral.
La certeza del cuerpo de la evidencia fue muy baja y las recomendaciones se emitieron en base a consenso de expertos por lo que todas las recomendaciones son condicionales .
Puntos de BPC:
El GEG consideró importante la toma de decisión compartida con la mujer sobre la posible pérdida de capacidad reproductiva, estudios señalan que la participación de la mujer en la decisión de su tratamiento generaría mejor calidad de vida, menor ansiedad y remordimiento 34,35. Por lo que la decisión terapéutica debe ser tomada de manera compartida con la paciente explicándole los riesgos y beneficios de cada intervención de manera clara, amigable y explícita.
Pregunta 7: En mujeres con cáncer de cuello uterino en estadios tempranos (IA1, IA2, IB1, IB2 o IIA1) luego de tratamiento quirúrgico y con indicaciones de terapia adyuvante ¿Qué terapia adyuvante se debería usar: quimioterapia (QT), radioterapia (RT), o quimio-radioterapia (QRT)?
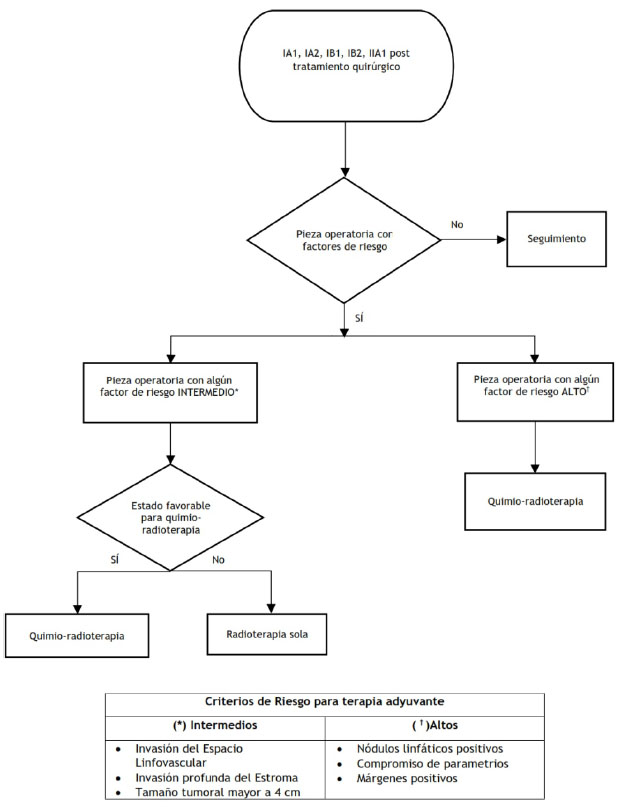
El tratamiento adyuvante se refiere al uso de medicamentos (quimioterapia) y/o radiación (radioterapia) añadido a la terapia inicial cuando existen factores de riesgo para recurrencia 36. Los factores de riesgos se dividen en altos e intermedios. Factores de riesgo alto: presencia de nódulos linfáticos positivos, compromiso de parametrios, márgenes positivos. Factores de riesgo intermedio son: invasión del espacio linfovascular, invasión profunda del estroma y tamaño tumoral mayor a 4 cm 37-41. (ver tabla 3)
La RS de Roger 36 (2 ECA, n=397) encuentra que radioterapia adyuvante (RTA), en mujeres con factores de riesgo intermedio, disminuye el riesgo de progresión de enfermedad a los 5 años comparado con no terapia adyuvante (NTA), pero no tiene efecto sobre mortalidad a los 5 años, ni eventos adversos (hematológicos, gastrointestinales, genitourinarios). La RS de Falcetta 42 (2 ECA, n=297) encuentra que la quimio-radioterapia adyuvante (QRTA), en mujeres con factores de riesgo alto, disminuye la probabilidad de muerte por todas las causas y progresión de enfermedad, pero también aumenta la probabilidad de toxicidad, en comparación con RTA.
En mujeres con factores de riesgo alto, los beneficios de QRTA superan los daños, por ende, el GEG emite una recomendación a favor de QRTA. A pesar que la certeza de la evidencia fue muy baja, el GEG valora el potencial del QRTA de salvar la vida de las mujeres, por ende, decide emitir una recomendación fuerte .
En mujeres con factores de riesgo intermedio, la evidencia es insuficiente para reconocer a RTA como superior a no tratamiento; además, el GEG considera que se debe tomar medidas más agresivas para salvaguardar la vida de las mujeres, por ende, emite una recomendación a favor de QRTA. Debido a los riesgos de la intervención y la muy baja certeza de la evidencia, el GEG emite una recomendación condicional .
Puntos de BPC:
Pregunta 8: En mujeres con cáncer de cuello uterino en estadios tempranos (IA1, IA2, IB1, IB2 o IIA1) con indicación de quimio-radioterapia ¿qué esquema de quimioterapia se debería dar: en base a cisplatino, a gemcitabina o a paclitaxel-carboplatino concomitante a radioterapia?
Estos esquemas se basan en medicamentos que actúan en diferentes momentos del ciclo celular. Todos incluyen radioterapia.
El ECA de Sehouli et al 43 (n=263) encuentra que el esquema de paclitaxel + carboplatino (PC) seguido de radioterapia; y encuentra que el grupo de PC tiene mayor probabilidad de sobrevida libre de progresión que el grupo de cisplatino (C) administrado al mismo tiempo que radioterapia, pero no encuentra diferencias para sobrevida general a los 5 años ni recurrencia en ambos grupos. No se encontró evidencia para gemcitabine.
El GEG considera que la evidencia es insuficiente para considerar al esquema con PC superior al esquema con C. Además, se toma en cuenta que el esquema con PC es mucho más costoso que el esquema con C, por ende, el GEG emite una recomendación a favor del esquema con cisplatino.
Debido a que la certeza de la evidencia fue muy baja se decide emitir una recomendación condicional .
Puntos de BPC:
El GEG consideró, en consenso, que la dosis de cisplatino debe ser ajustada según las características de los pacientes.
Así mismo, la dosis de radiación se estableció en 45 a 50 Gy en fracciones estándar (1.8 o 2.0 Gy diario) siguiendo recomendaciones de GPC internacionales y ECA 15,43-47, pudiendo ésta ser ajustada según las características del paciente.
Se consideró importante mencionar que la adición de braquiterapia a la QRTA aún es un procedimiento con escaza evidencia de su efectividad 48.
En relación a mujeres con falla renal, el GEG considera que, debido a la nefrotoxicidad de cisplatino, ellas deberían recibir un esquema basado en carboplatino, en base a los resultados del ECA de Sehouli 43.
Tabla 1 Lista completa de recomendaciones
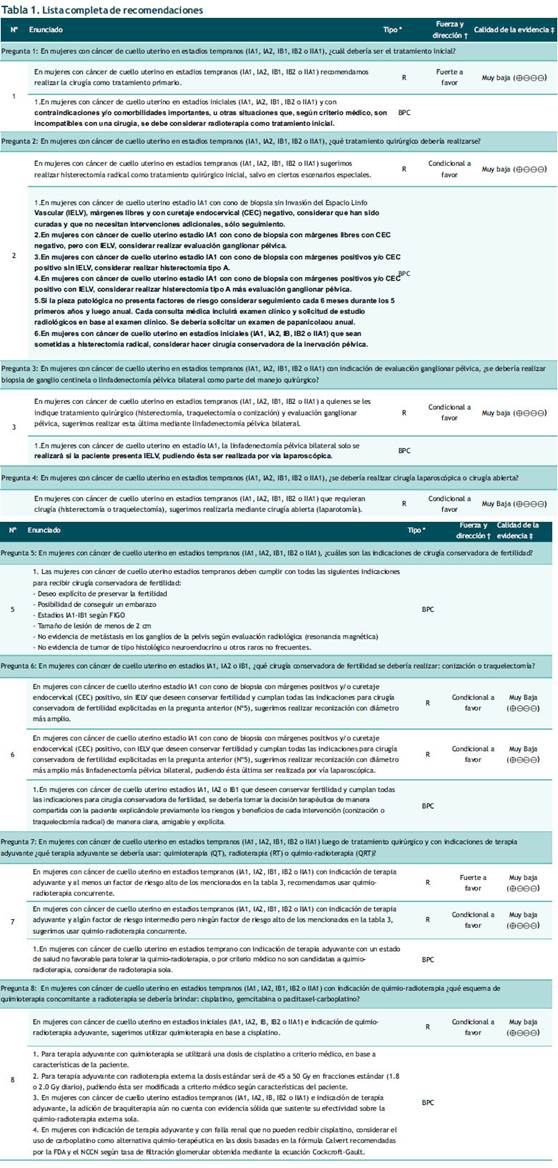
* Punto de buena práctica clínica (BPC) o recomendación
† La certeza de la evidencia solo se establece para las recomendaciones, mas no para los puntos de BPC
‡ La fuerza, dirección y certeza de la evidencia solo se establecen para las recomendaciones, mas no para los puntos de BPC
Tabla 2 Significado de los niveles de certeza de la evidencia y de la fuerza de la recomendación
| Significado | |
|---|---|
| Certeza de la evidencia | |
| (⨁⨁⨁⨁) Alta | Es muy probable que el verdadero efecto sea similar al efecto estimado. |
| (⨁⨁⨁◯) Moderada | Es moderadamente probable que el verdadero efecto sea similar al efecto estimado, pero es posible que sea sustancialmente diferente |
| (⨁⨁◯◯) Baja | Nuestra confianza en el efecto es limitada. El verdadero efecto podría ser sustancialmente diferente al efecto estimado |
| (⨁◯◯◯) Muy baja | Nuestra confianza en el efecto es pequeña. El verdadero efecto probablemente sea sustancialmente diferente al efecto estimado |
| Fuerza de la recomendación | |
| Recomendación fuerte (a favor o en contra) | El GEG considera que todos o casi todos los profesionales que revisan la evidencia disponible seguirían esta recomendación. En la formulación de la recomendación se usa el término “se recomienda” |
| Recomendación Condicional (a favor o en contra) | El GEG considera que la mayoría de los profesionales que revisan la evidencia disponible seguirían esta recomendación, pero un grupo de profesionales podría optar por no aplicarlas en alguna población particular, siempre que sea justificado. En la formulación de la recomendación se usa el término “se sugiere” |
Tabla 3 Criterios de Riesgo para terapia adyuvante
| Criterios de Riesgo para terapia adyuvante | |
|---|---|
| Intermedios | Altos |
| Invasión del Espacio Linfovascular Invasión profunda del Estroma Tamaño tumoral mayor a 4 cm | Nódulos linfáticos positivos Compromiso de parametrios Márgenes positivos |