Introducción
La enfermedad cardiovascular (ECV) es la principal causa de mortalidad e incapacidad en Colombia y a nivel mundial 1,2. Dentro de este grupo, el síndrome coronario agudo (SCA) representa un número significativo de ingresos hospitalarios, afectando aproximadamente al 50% de los adultos mayores que sufren infartos 3. La interacción entre el envejecimiento, el número de comorbilidades y la polifarmacia puede alterar la relación riesgo-beneficio de las intervenciones en pacientes con SCA. Por ejemplo, los adultos mayores presentan un mayor riesgo cardiovascular, así como un mayor riesgo de complicaciones. Además, esta población suele ser excluida o estar infrarrepresentada en los ensayos clínicos, lo que limita la generalización de los resultados. Debido a esto, algunos grupos proponen que la adherencia estricta a las guías en estos pacientes podría aumentar los efectos adversos, mientras que los beneficios clínicos serían limitados 4.
Para identificar factores que permitan reclasificar a los pacientes, se ha sugerido la evaluación de la fragilidad. La fragilidad es una condición biológica que implica una reducción de la reserva y la capacidad de resistencia frente a factores estresores, lo que conduce a una pérdida de la homeostasis y a una mayor vulnerabilidad a eventos adversos 5. Estratificar a los pacientes según su grado de fragilidad ayuda a predecir la mortalidad, las rehospitalizaciones y la discapacidad, siendo también una herramienta útil en la evaluación previa a intervenciones y procedimientos quirúrgicos 6,7. En el contexto del SCA, se ha demostrado que la fragilidad tiene un valor pronóstico, permitiendo reclasificar el riesgo y mejorar la toma de decisiones clínicas 8-11.
En América Latina, los datos sobre el impacto de la fragilidad en pacientes ancianos con SCA son escasos. El presente estudio tiene como objetivo determinar la asociación entre la fragilidad y los desenlaces adversos intrahospitalarios y a 30 días en pacientes mayores de 65 años sometidos a arteriografía coronaria por SCA.
Materiales y métodos
Diseño, población y muestra del estudio
Este estudio de cohorte prospectivo se llevó a cabo entre el 1 de marzo y el 1 de octubre de 2023. Se incluyeron pacientes mayores de 65 años ingresados a la sala de hemodinamia del Hospital Universitario San Vicente Fundación (HUSVF) en Medellín, con diagnóstico de síndrome coronario agudo (SCA) según la cuarta definición universal de infarto 12. Se excluyeron pacientes con diagnóstico alternativo confirmado, aquellos bajo anestesia, con deterioro cognitivo grave o con dificultades para la evaluación de fragilidad, así como quienes no aceptaron participar. La selección del tratamiento farmacológico y la estrategia (invasiva o conservadora) quedó a criterio del médico tratante, sin tener en cuenta el resultado de la escala FRAIL.
El muestreo fue por conveniencia. Con base en estudios previos 8-11 sobre la asociación entre fragilidad y mortalidad a corto plazo en pacientes mayores de 65 años con SCA, se estimó una incidencia del desenlace primario del 10% en el grupo frágil y del 2% en el grupo no frágil. Con un nivel de significancia del 5% y un poder del 80%, se determinó que se necesitaban al menos 274 pacientes.
Evaluación de la fragilidad
Para evaluar la fragilidad se utilizó la escala FRAIL, recomendada por varias sociedades científicas de cardiología y geriatría, validada en México y empleada en estudios locales 13-16. Esta escala consta de 5 ítems: fatiga, resistencia (capacidad de subir un piso de escaleras), deambulación (capacidad de caminar ≥100 m), pérdida de peso (>5 % en los últimos 6 meses) y comorbilidades (5 o más enfermedades confirmadas). Se asigna 1 punto por cada ítem positivo. Según el puntaje, los pacientes se clasificaron en frágiles (≥3 puntos), prefrágiles (1 o 2 puntos) y robustos (0 puntos). La fragilidad se evaluó al ingreso a la sala de hemodinamia en aquellos pacientes que cumplían los criterios de inclusión y dieron su consentimiento informado. Si el paciente no podía proporcionar el consentimiento, pero un tercero lo aceptaba y se disponía de datos suficientes, el paciente era incluido.
Recolección de datos y selección de variables
Las características clínicas y sociodemográficas se extrajeron de la historia clínica electrónica y se registraron en una base de datos en Microsoft Excel. Se incluyeron variables que pudieran actuar como factores de confusión: edad, sexo, antecedente de enfermedad cardiovascular (ECV), estrato socioeconómico (clasificación de 6 niveles, siendo el nivel 1 el más bajo y el 6 el más alto), diabetes mellitus, tabaquismo, enfermedad renal crónica, fibrilación auricular y antecedente de insuficiencia cardiaca. La ECV se definió como revascularización coronaria previa (quirúrgica o percutánea), accidente cerebrovascular (ACV), enfermedad arterial periférica o documentación de enfermedad coronaria mediante pruebas invasivas o no invasivas. Al ingreso se calculó el puntaje GRACE y se evaluó el estado cognitivo con la herramienta Mini-Cog (puntaje de 0 a 5, donde <3 puntos indica posible deterioro cognitivo). Se registraron los valores de colesterol LDL, creatinina y hemoglobina al ingreso, y se estimó la tasa de filtración glomerular (TFG) utilizando la ecuación CKD-EPI de 2009. Durante la arteriografía coronaria, se consideraron el tipo de acceso vascular, el vaso culpable y el número de vasos comprometidos. Todos los pacientes fueron sometidos a un ecocardiograma transtorácico.
Desenlaces
El desenlace primario fue la mortalidad por cualquier causa a los 30 días después del egreso. Los desenlaces secundarios incluyeron la estancia hospitalaria y un desenlace compuesto que abarcaba mortalidad a los 30 días, nefropatía inducida por contraste (NIC), complicaciones vasculares, complicaciones hemorrágicas, insuficiencia cardiaca aguda, choque cardiogénico y rehospitalización a los 30 días.
Los desenlaces exploratorios incluyeron los componentes individuales del desenlace compuesto. La NIC se definió según las guías KDIGO 17, mientras que los sangrados se clasificaron en menores y mayores según el consenso BARC 18. Las complicaciones vasculares incluyeron hematomas, pseudoaneurismas y ACV periprocedimental, según consenso 19. La insuficiencia cardiaca aguda se definió como el inicio o empeoramiento de los signos de congestión sistémica en presencia de disfunción cardiaca estructural o funcional, y el choque cardiogénico como hipotensión arterial (presión sistólica <90 mmHg) con hipoxia tisular, requiriendo vasopresores o inotrópicos. Otros desenlaces exploratorios incluyeron arritmias y bloqueos auriculoventriculares según consenso 20,21, y la necesidad de transfusión.
Se realizó seguimiento telefónico a los 30 días para evaluar el estado vital y las rehospitalizaciones.
Análisis estadístico
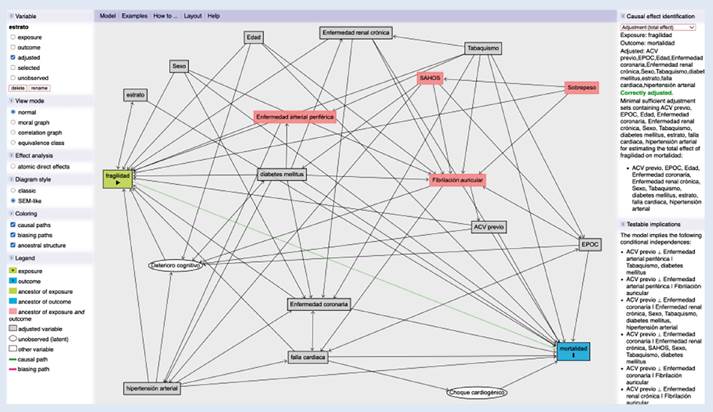
Las variables categóricas se presentan como frecuencias absolutas y porcentajes, mientras que las variables continuas se expresan como medianas y rangos intercuartílicos. Para evaluar la asociación entre fragilidad y mortalidad a 30 días, así como con los desenlaces exploratorios, se utilizó un modelo quasi-Poisson con función de enlace logarítmico para estimar la razón de riesgo (RR) y su intervalo de confianza (IC) del 95 %. El análisis se ajustó por edad, sexo, tabaquismo, antecedentes de enfermedad coronaria, estrato socioeconómico, manejo médico y diabetes. La selección de estos factores de confusión se realizó mediante discusión entre los investigadores y la construcción de un gráfico acíclico directo (Material suplementario) 22. Las diferencias en la estancia hospitalaria se evaluaron mediante la diferencia del coeficiente biserial por rangos (rbiserial rango) como medida de tamaño del efecto. Un valor superior a 0,40 se consideró una diferencia “grande”. El desenlace compuesto se analizó con un modelo quasi-Poisson utilizando estimaciones quasi-verosímiles de los parámetros, y se calculó el riesgo relativo (RR) con su IC del 95 %. Se utilizó el software R para el análisis de los datos.
Resultados
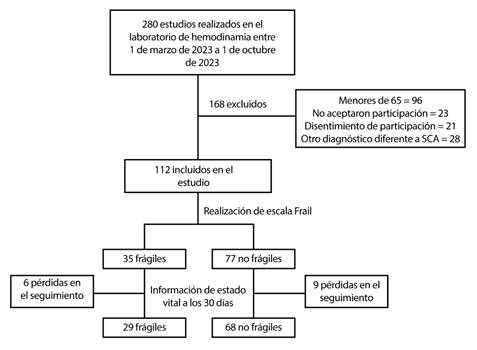
Entre el 1 de marzo y el 1 de octubre de 2023, se realizaron 280 procedimientos en el Laboratorio de Hemodinamia del Hospital Universitario San Vicente Fundación (HUSVF) en Medellín. Se incluyeron 112 pacientes en el estudio (Figura 1). Un total de 35 (31,3%) pacientes fueron clasificados como frágiles, 56 (50%) como prefrágiles y 21 (18,8%) como robustos. Los pacientes se agruparon en dos categorías: frágiles (n=35; 31,3%) y no frágiles (que incluyó a los prefrágiles y robustos) (n=77; 68,8%).
Las características clínicas y sociodemográficas se presentan en la Tabla 1. Los pacientes frágiles (PF) tenían una mediana de edad de 78 años, mientras que los no frágiles (PNF) presentaron una mediana de 73 años. Los PF tenían puntuaciones más altas en GRACE (mediana de 185 frente a 137 en los PNF) y menores puntuaciones en Mini-Cog (mediana de 2 puntos frente a 4 en los PNF). Los niveles de hemoglobina y colesterol LDL fueron similares en ambos grupos, pero los PF mostraron una menor tasa de filtración glomerular (TFG) (mediana de 57 mL/min/1,73 m² frente a 77 mL/min/1,73 m² en los PNF). Además, los PF presentaron un mayor número de vasos comprometidos (mediana de 3 vasos frente a 2 vasos en los PNF) y una menor fracción de eyección (mediana de 38% frente a 49% en los PNF).
Tabla 1 Características clínicas y sociodemográficas de los participantes del estudio
| Característica | Frágil, n (%) (n=35) | No frágil, n (%) (n=77) | Total, n (%) (n=112) |
|---|---|---|---|
| Edad* | 78 (75-80,5) | 73,0 (69,0-76,0) | 75,0 (70,8-78,0) |
| Sexo femenino | 18 (51,4) | 33 (42,9) | 51 (45,5) |
| Estrato socioeconómico | |||
| 1 (más bajo) | 12 (34,3) | 22 (28,6) | 34 (30,4) |
| 2 | 12 (34,3) | 23 (29,9) | 35 (31,3) |
| 3 | 10 (28,6) | 26 (33,8) | 36 (32,1) |
| 4 | 1 (2,9) | 4 (5,2) | 5 (4,5) |
| 5 | 0 (0) | 2 (2,6) | 2 (1,8) |
| 6 (más alto) | 0 (0) | 0 (0) | 0 (0) |
| Diagnóstico | |||
| SCA sin elevación del ST | 19 (54,3) | 37 (48,1) | 56 (50,0) |
| SCA con elevación del ST | 15 (42,9) | 33 (42,9) | 48 (42,9) |
| Angina Inestable | 1 (2,9) | 7 (9,1) | 8 (7,1) |
| Tiempo desde inicio de síntomas hasta sala de hemodinamia* | 48 (18-72) | 46 (24-72) | 48 (24-72) |
| Mini-Cog* | 2,0 (2,0-3,0) | 4,0 (3,0-5,0) | 3,50 (2,00-5,00) |
| GRACE* | 185 (162-217) | 137 (122-158) | 145 (127-177) |
| Comorbilidades | |||
| Diabetes mellitus | 11 (31,4) | 23 (29,9) | 34 (30,4) |
| Dislipidemia | 17 (48,6) | 34 (44,2) | 51 (45,5) |
| Tabaquismo | 17 (48,6) | 42 (54,5) | 59 (52,7) |
| Falla cardiaca | 1 (2,9) | 1 (1,3) | 2 (1,8) |
| Enfermedad renal crónica | 4 (11,4) | 5 (6,5) | 9 (8,0) |
| Fibrilación auricular | 1 (2,9) | 1 (1,3) | 2 (1,8) |
| Historia de enfermedad cardiovascular | |||
| Enfermedad coronaria | 5 (14,3) | 12 (15,6) | 17 (15,2) |
| Accidente cerebrovascular | 5 (14,3) | 0 (0) | 5 (4,5) |
| Antecedente de revascularización quirúrgica | 0 (0) | 2 (2,6) | 2 (1,8) |
| Antecedente de revascularización con estents | 3 (8,6) | 8 (10,4) | 11 (9,8) |
| Fracción de expulsión* | 38,0 (31,0-50,5) | 49,0 (38,0-56,0) | 46,5 (35,0-55,0) |
| Vaso culpable | |||
| Sin lesiones | 3 (8,6) | 2 (2,6) | 5 (4,5) |
| Arteria descendente anterior | 19 (54,3) | 36 (46,8) | 55 (49,1) |
| Arteria coronaria derecha | 9 (25,7) | 24 (31,2) | 33 (29,5) |
| Arteria circunfleja | 3 (8,6) | 12 (15,6) | 15 (13,4) |
| Tronco principal izquierdo | 1 (2,9) | 1 (1,3) | 2 (1,8) |
| Posterolateral | 0 (0) | 1 (1,3) | 1 (0,9) |
| Diagonal | 0 (0) | 1 (1,3) | 1 (0,9) |
| Número de vasos* | 3,00 (1,50-3,00) | 2,00 (1,00-3,00) | 2,00 (1,00-3,00) |
| Hemoglobina* | 12,8 (12,0-14,0) | 13,6 (12,1-15,0) | 13,4 (12,0-14,6) |
| Colesterol LDL* | 95 (66-125) | 107 (80,8-126) | 100 (74-127) |
| Creatinina* | 1,00 (0,740-1,40) | 0,910 (0,760-1,10) | 0,945 (0,748-1,20) |
| TFG* | 57,0 (40,5-83) | 77,0 (62,0-88,0) | 74,0 (54,0-87,0) |
* Los valores mostrados corresponden a la mediana y al rango intercuartílico (Q1-Q2).
En la Tabla 2 se describen las características relacionadas con la intervención. El 51,4% de los PF fueron tratados de manera conservadora, en comparación con el 95,5% de los PNF, quienes fueron tratados de forma invasiva. La mayoría de los pacientes se revascularizó de manera percutánea, el acceso más frecuente fue el radial, y el 41,1% requirió infusión de tirofiban. No hubo diferencias entre los grupos en el número de estents implantados.
Tabla 2 Características relacionadas con la intervención
| Característica | Frágil, n (%) (n=35) | No frágil, n (%) (n=77) | Total, n (%) (n=112) |
|---|---|---|---|
| Manejo médico | 18 (51,4) | 4 (5,2) | 22 (19,6) |
| Revascularización | |||
| Quirúrgica* | 2 (5,7) | 8 (10,4) | 10 (8,9) |
| Angioplastia con balón + estent | 15 (42,8) | 65 (84,4) | 80 (71,4) |
| Acceso | |||
| Radial | 26 (74,2) | 63 (81,8) | 89 (79,4) |
| Femoral | 6 (17,1) | 14 (18,2) | 20 (17,9) |
| Radial + femoral | 3 (8,6) | 0 (0) | 3 (2,7) |
| Número estents** | 2 (1-3,25) | 2 (1-3) | 2 (1-3) |
| Tirofiban | 13 (37,1) | 33 (42,9) | 46 (41,1) |
* 1 paciente del grupo frágil y 2 del grupo no frágil se llevaron inicialmente a revascularización percutánea y posteriormente a revascularización quirúrgica.
** Los valores mostrados corresponden a la mediana y al rango intercuartílico (Q1-Q2).
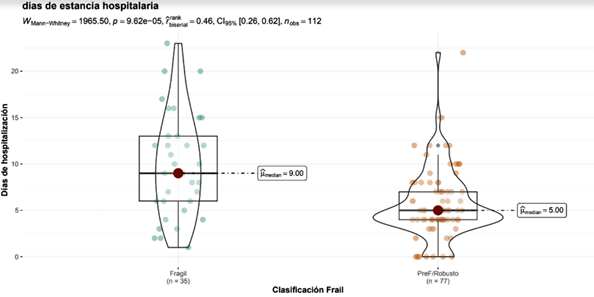
La Tabla 3 muestra la frecuencia de los desenlaces adversos intrahospitalarios y su asociación con la fragilidad. La ocurrencia del desenlace primario en los PF fue del 22,8% frente al 4,8% en los PNF. La fragilidad se asoció con un mayor riesgo de desenlace primario en el análisis ajustado (RR ajustado 19,00, IC 95%: 5,04-72,61; p < 0,001). También se observó un aumento del riesgo de presentar el desenlace compuesto (RR ajustado 4,57, IC 95%: 2,56-8,34; p < 0,001). Adicionalmente, como se muestra en la Figura 2, los PF tuvieron estancias hospitalarias más prolongadas (mediana de 9 días frente a 5 días en los PNF; rbiserial rango = 0,46, IC 95%: 0,26-0,62). En el Material suplementario se detallan los desenlaces y las causas específicas de mortalidad.
Tabla 3 Desenlaces adversos intrahospitalarios y asociación con fragilidad
| Desenlace | Frágil | No frágil | RR ajustado* | IC 95 % | Valor de p |
|---|---|---|---|---|---|
| Mortalidad a 30 días ** | 8/35 (22,9%) | 1/77 (1,3%) | 19,00 | 5,04-72,61 | <0,001 |
| Desenlace compuesto*** | 27/35 (77%) | 14/77(18,2%) | 4,57 | 2,56-8,34 | <0,001 |
| Nefropatía inducida por contraste | 11/35(31,4%) | 5/77 (6,5%) | 6,52 | 1,56-35,39 | 0,015 |
| Complicaciones vasculares**** | 7/35 (20%) | 6/77 (7,8%) | 1,36 | 0,32-5,69 | 0,671 |
| Sangrado intrahospitalario**** | 11/35(31,4%) | 1/77(1,3%) | 25,54 | 3,5-815 ,53 | 0,009 |
| Falla cardiaca aguda**** | 9/35(25,7%) | 2/77(2,6%) | 11,00 | 2,18-93,93 | 0,009 |
| Hospitalización a 30 días**** | 7/35(20%) | 3/77(3,9%) | 1,38 | 0,23-8,08 | 0,720 |
| Choque cardiogénico**** | 11/35 (31,4%) | 1/77 (1,3%) | 30,07 | 7,93-196,81 | <0,001 |
RR: riesgo relativo. IC: intervalo de confianza.
* Modelo ajustado por edad, sexo, antecedente de enfermedad coronaria, tabaquismo, diabetes, estrato socioeconómico y manejo médico.
** Detalle de cada causa de muerte se presenta en el Material suplementario.
*** El desenlace compuesto incluyó: mortalidad a 30 días, nefropatía inducida por contraste, cualquier complicación vascular, cualquier sangrado, falla cardiaca aguda, hospitalización a 30 días y choque cardiogénico. Este desenlace se calculó como riesgo relativo mediante un modelo quasi-Poisson, con estimación quasi-verosímil de los parámetros del modelo
**** Para nefropatía por contraste, complicaciones vasculares, sangrado intrahospitalario, falla cardiaca aguda y choque cardiogénico se presenta el RR estimado mediate modelo quasi-Poisson.
Se realizó un análisis exploratorio sobre la estrategia de manejo (invasiva vs. conservadora) y los desenlaces según el grado de fragilidad (Material suplementario). Los PF manejados de manera conservadora, en comparación con los tratados con una estrategia invasiva, presentaron menos complicaciones relacionadas con sangrado (16,7% vs. 47,1%), choque cardiogénico (22,2% vs. 41,2%), mortalidad a los 30 días (16,7% vs. 29,4%) y menor duración de la estancia hospitalaria (mediana de 8 días frente a 12 días). En los PNF, la ocurrencia de complicaciones fue baja y la única muerte ocurrió en un paciente con infarto evolucionado (>48 h) complicado con choque cardiogénico.
Discusión
En este estudio se encontró asociación entre la fragilidad y el riesgo de desenlaces adversos intrahospitalarios y a 30 días en pacientes mayores de 65 años con síndrome coronario agudo (SCA). Así, el 31,3% de los pacientes fueron clasificados como frágiles y no hubo diferencias en las comorbilidades, excepto por el antecedente de accidente cerebrovascular (ACV) y la tasa de filtración glomerular (TFG), que fue más baja en los pacientes frágiles. La fragilidad se asoció de manera independiente con mortalidad intrahospitalaria y a 30 días, mayor duración de la estancia hospitalaria, complicaciones relacionadas con sangrado, nefropatía inducida por contraste (NIC), insuficiencia cardíaca aguda y choque cardiogénico.
Los resultados del presente estudio son consistentes con los informados en otras cohortes, aunque la ocurrencia del desenlace primario en el grupo frágil fue mayor de lo esperado (22,8% frente a 4,8 % en el grupo no frágil). En 2011, Ekerstad et al. fueron los primeros en informar la asociación entre fragilidad y mortalidad intrahospitalaria y a 30 días en pacientes con SCA, con incidencias de mortalidad del 10,1 y 15,4% en los pacientes frágiles, respectivamente 9. Resultados similares se observaron en la cohorte de Kang et al. (2015) y Alonso Salinas et al. (2016), quienes informaron la relación entre fragilidad y mortalidad a corto plazo 8,11. En 2018, Patel et al. publicaron los resultados de una cohorte australiana de 3944 pacientes mayores de 65 años con SCA, evidenciando la asociación entre fragilidad y mortalidad intrahospitalaria (10% frente a 4,9% en pacientes no frágiles) 10.
A diferencia de otras cohortes, no se encontraron diferencias significativas en las comorbilidades de los pacientes. Generalmente, los pacientes frágiles presentan más comorbilidades y complicaciones 23. Esto podría deberse al tamaño limitado de nuestra muestra y a las características de la escala FRAIL, en la cual las comorbilidades solo representan 1 de los 5 ítems. No obstante, la asociación entre fragilidad y desenlaces adversos se mantuvo, lo que apoya la idea de que la fragilidad abarca otros factores más allá de las comorbilidades. Además, la fragilidad se asoció con un mayor deterioro cognitivo; en esta cohorte, los pacientes frágiles presentaron puntajes más bajos en el Mini-Cog. El deterioro cognitivo es común en ancianos con SCA y se asocia con una mayor probabilidad de eventos adversos en el primer año 24.
En cuanto a las características angiográficas, los pacientes frágiles presentaron más vasos comprometidos y fueron tratados con manejo conservador con mayor frecuencia (51,4% frente a 4,5%). Los pacientes frágiles con SCA sin elevación del segmento ST (SCASEST) presentan características angiográficas más complejas y graves, independientemente de la edad, lo que aumenta su riesgo de mortalidad, revascularización urgente, infarto y sangrado durante el seguimiento 25. Aunque las guías recomiendan una estrategia invasiva temprana en grupos de alto riesgo, los pacientes frágiles con SCA tienden a verse afectados de manera desproporcionada por estas características de alto riesgo. En esta cohorte, los pacientes frágiles tuvieron un puntaje GRACE más alto, y se ha demostrado una correlación entre el grado de fragilidad y este puntaje 26. Sin embargo, el puntaje GRACE puede sobreestimar el riesgo en pacientes mayores de 65 años. La reclasificación del riesgo según el grado de fragilidad podría mejorar la precisión de las predicciones 27.
El manejo invasivo en pacientes ancianos sigue las mismas recomendaciones que en la población general; sin embargo, deben considerarse variables como la gravedad de las comorbilidades, el deterioro cognitivo y la expectativa de vida. En el estudio de Patel et al., aproximadamente el 40% de los pacientes frágiles fueron manejados de manera conservadora, lo que concuerda con los resultados de esta cohorte 10. En cuanto al SCASEST, cinco estudios clínicos aleatorizados han evaluado la eficacia de la estrategia invasiva en pacientes ancianos, pero solo dos consideraron la fragilidad y las comorbilidades. Cuatro estudios no encontraron diferencias, mientras que uno reportó una reducción en la recurrencia de infartos y la necesidad de revascularización urgente 28. En los pacientes con SCA con elevación del segmento ST, un metaanálisis demostró que la revascularización percutánea reduce la mortalidad, el reinfarto y los ACV, aunque ningún estudio consideró la fragilidad 28. Además, los pacientes frágiles presentan un mayor riesgo de complicaciones vasculares, hemorrágicas, NIC, infecciones y complicaciones relacionadas con el procedimiento. Asimismo, el metaanálisis mostró que los pacientes mayores de 70 años tratados con un manejo invasivo tienen mayor riesgo de sangrado (Odds ratio [OR] 2,19, IC 95%: 1,12-4,28) 29, y los mayores de 75 años sometidos a arteriografía coronaria tienen un mayor riesgo de desarrollar NIC (OR 1,99, IC 95%: 1,75-2,27) 28. Nuestros datos coinciden con estudios previos que muestran que los pacientes frágiles con SCA presentan peores desenlaces a corto plazo.
Al analizar los desenlaces según la estrategia de manejo, los pacientes frágiles tratados con un enfoque invasivo presentaron más desenlaces adversos. Sin embargo, estos datos no son generalizables debido a que la comparación no fue planificada a priori, lo que podría introducir un error tipo I, además del tamaño reducido de la muestra. Finalmente, la principal causa de muerte en esta cohorte fue el choque cardiogénico. Los pacientes ancianos con SCA tienen una mayor prevalencia de choque cardiogénico y peor pronóstico, comparado con los pacientes más jóvenes. Además, este subgrupo es menos propenso a intervenciones invasivas y más vulnerable a complicaciones derivadas de la enfermedad crítica, como infecciones, arritmias y sangrados gastrointestinales 30.
Dado que la fragilidad es un concepto emergente, no existe una definición universalmente aceptada ni una escala estandarizada para su evaluación. En este estudio se eligió la escala FRAIL por su facilidad de aplicación; asimismo, ha sido validada en México y utilizada en investigaciones locales 13-16. Independientemente del método empleado, la fragilidad se ha asociado consistentemente con desenlaces adversos, lo que resalta la necesidad de una mayor evaluación en este campo 28.
El presente estudio tiene varias limitaciones. Al tratarse de un estudio unicéntrico con una muestra pequeña y su naturaleza observacional, está sujeto a sesgos, principalmente de confusión y medición, dado que algunos desenlaces dependían de los registros clínicos. La tasa de recolección fue menor a la esperada, lo que explica los amplios intervalos de confianza y limita la precisión de los resultados. El reducido número de pacientes también se debió al tiempo limitado para la recolección de datos. Además, el estudio se realizó en un centro de alta complejidad que no se limita a enfermedades cardiovasculares y con un muestreo por conveniencia, lo que impide la generalización de los resultados. La escala FRAIL, que incluye cuatro ítems autoinformados, podría estar sesgada por la subjetividad del paciente. La falta de una escala estandarizada para evaluar la fragilidad también podría limitar la extrapolación de los resultados. Sería importante ampliar estas observaciones aplicando la misma escala a una muestra más grande y con un seguimiento a largo plazo, lo que posiciona este estudio como un punto de partida para futuras investigaciones.
En conclusión, en la presente cohorte, un número significativo de pacientes mayores de 65 años con SCA fueron clasificados como frágiles. La fragilidad se asoció con desenlaces adversos, tanto intrahospitalarios como a 30 días. El grado de fragilidad podría ser un marcador pronóstico importante en pacientes ancianos con SCA, por lo que su evaluación de rutina podría impactar significativamente en la toma de decisiones clínicas.