INTRODUCCIÓN
Entre las actividades fundamentales y económicamente importantes en el Perú destaca la producción avícola, la cual es reconocida por su alta productividad respecto a la proteína animal (carne y huevos) a nivel nacional, encontrándose en continuo crecimiento (MINAGRI, 2019). Este incremento tiene una estrecha relación con los insumos y demanda de piensos destinados para el consumo animal, que representa no menos del 60% del costo producción total (Ravindran, 2013).
La presencia e incremento de hongos en los alimentos se encuentra favorecida en climas tropicales ya que desfavorecen la estabilidad de los insumos (Guerre, 2016). Factores ambientales, como el tiempo de almacenamiento, temperatura, pH, oxígeno y humedad promueven su crecimiento y, posteriormente, la producción de micotoxinas (Kana et al., 2013). Esto conlleva a una importante problemática por el riesgo sanitario en productos como el huevo y la carne de animales que consumieron piensos contaminados (Tolosa et al., 2017), pudiendo provocar intoxicaciones severas, tanto en animales como humanos (Alshannaq y Yu, 2017; Toso et al., 2018).
Entre los hongos capaces de producir micotoxinas en productos para el consumo se puede mencionar a especies de los géneros Penicillium, Fusarium y Aspergillus (Marin et al., 2013). Asimismo, las toxinas de mayor frecuencia en el alimento, piensos y cultivos son las ocratoxinas (OTs), aflatoxinas (AFs), zearalenona (ZEN), fumonisinas (FBs) y tricotecenos, que incluyen a la toxina T-2 y el deoxynivalenol (Yang et al., 2020). Las micotoxinas en el alimento ocasionan cuantiosas pérdidas económicas a nivel comercial, debido a la disminución del rendimiento productivo al afectar clínica o sub clínicamente a los animales (Gimeno y Martins, 2011; Murugesan et al., 2015). La exposición a micotoxinas puede ocasionar alteraciones histopatológicas, tanto en hígado, riñón e intestinos, alterando la supervivencia y el crecimiento, generando inmuno-toxicidad y merma de los índices reproductivos (Rawal et al., 2010; Yang et al., 2020).
Se recomienda realizar análisis cuantitativos para detectar agentes que contaminen los alimentos, tales como el recuento de bacterias, identificación de patógenos y la cuantificación de hongos (Da Silva et al., 2013). Por otra parte, un método para analizar micotoxinas con mayor regularidad, validado por diversas matrices de alimentos, de ejecución sencilla, rápida y especifica, viene a ser la prueba de ELISA (Pereira et al., 2014).
Los problemas frecuentes en la crianza avícola en la amazonia peruana relacionados principalmente con la alteración en los parámetros productivos e infecciones secundarias, hace necesario la implementación de un sistema de monitoreo del alimento destinado a los pollos. Por tal razón, la finalidad de este estudio fue cuantificar la presencia de hongos y micotoxinas en alimento balanceado procedente de granjas avícolas de la provincia Coronel Portillo, Ucayali, Perú.
MATERIALES Y MÉTODOS
Lugar y Tiempo del Estudio
La investigación se desarrolló en la provincia de Coronel Portillo, región Ucayali, Perú. la cual tiene una temperatura ambiental entre 26 y 34 °C, humedad relativa de 85 ± 5% y precipitación anual de 2682 msnm. Se trabajó con muestras de alimento balanceado balanceado de 36 granjas destinadas a la crianza de pollos de engorde (etapas de inicio, crecimiento o engorde) y de 4 granjas de aves de postura (proporción 9:1), (85% del total de establecimientos de la provincia).
El análisis de las muestras se llevó a cabo en la Unidad de Diagnóstico del Laboratorio de la Sección de Sanidad Animal de la Estación IVITA (Pucallpa), de la Facultad de Medicina Veterinaria, Universidad Nacional Mayor de San Marcos, entre 2018 y 2019, con las consideraciones necesarias de bioseguridad por vacío sanitario para la visita a los establecimientos.
Caracterización de las Granjas y Condiciones del Alimento Balanceado
Las granjas tuvieron fines comerciales, con capacidad instalada de crianza para aves en un rango de 2500 a 50 000 para engorde y de 8000 a 35 000 para postura. Las granjas de engorde estuvieron ubicadas en los distritos de Campo Verde, Yarinacocha, Manantay, Callería y Nueva Requena, mientras que las granjas de postura estuvieron ubicadas en los distritos de Campo Verde y Yarinacocha.
Algunas empresas avícolas tenían molino de alimento, por lo cual compraban sus insumos y preparaban el balanceado, llevándolo a su granja por camión en contenedores o a granel; otras granjas avícolas compraban directamente el alimento balanceado a tres grandes empresas comercializadoras de alimento. Los insumos del balanceado como el maíz proveían de otros departamentos como Ica, La Libertad, San Martín o Lima; a diferencia de la torta de soya que provenía de Argentina o Bolivia.
En las granjas, l balanceado se almacenaba en zonas aledañas a los galpones (áreas de concreto con techos del mismo material o de calamina). Los sacos eran arrumados sobre parihuelas o conservados en contenedores de plástico. El balanceado se conservaba en el almacén por un periodo de hasta una semana en las granjas de aves de engorde y hasta por 15 días en aves de postura, usualmente a temperatura ambiente (periodo de lluvias, durante el estudio). No se observó roedores en los almacenes al momento del muestreo, pero había diverso tipo de insectos y en tres granjas tenían otras especies de animales.
Muestreo y Análisis de Muestras
El muestreo se ejecutó siguiendo las recomendaciones del Servicio Nacional de Sanidad Agraria (SENASA), que dispone un procedimiento para el manejo de muestras de alimentos (SENASA, 2017). Se recolectó una muestra representativa de 1000 g de alimento balanceado con una sonda de metal introducida en forma inclinada en el saco. La muestra total se redujo en algunos casos hasta 500 g, con un separador mediante el método de cuarteo. Las muestras fueron rotuladas y transportadas en una caja de poliestireno expandido (Tecnopor) hasta el laboratorio, y fueron conservadas en un lugar fresco y seco (temperatura ≤ 16 °C y humedad ≤ 14%) hasta su procesamiento.
El recuento de hongos se hizo dentro de los tres días posteriores a la colecta. Se utilizó metanol para la extracción de la muestra y se conservó entre 2 y 4°C hasta su procesamiento mediante el método de ELISA. Se procesaron 13-15 muestras por vez para optimizar la cantidad de kits disponibles, y para no prolongar el tiempo desde la obtención de la muestra y el análisis en laboratorio. Se llevaron a cabo dos procedimientos para el análisis de las muestras:
El conteo en placa para mohos (hongos) y levaduras en alimento, descrito por la American Public Health Association (APHA), metodología referida por Da Silva et al. (2013).
La prueba de ELISA Directa Competitiva para la detección de micotoxinas, frecuentemente nocivas en la producción avícola, según Yang et al. (2020) en alimento balanceado, utilizando kits de Veratox®.
Se usaron kits de Veratox® Aflatoxina (USDA-GIPSA2012-010.AOAC-RI 050901. ISO 9001:2000), Veratox® Ochratoxina A (ISO 9001:2000), Veratox® Toxina T-2/HT-2 (ISO 9001:2000), Veratox® Fumonisina (AOAC Official Method #2001.06) y Veratox® Zearalenona (ISO 9001:2000) de la empresa fabricante NEOGEN.
Comparación de Resultados
Los resultados del recuento de hongos en alimento fueron comparados con los parámetros descritos por Gilbert et al. (2000), quienes clasificaban la condición del alimento según la cantidad de unidades formadoras de colonias por gramo (UFC/g) en satisfactorio (<104), aceptable (104 -105) e inaceptable (>105). En el caso de las micotoxinas, la comparación con los límites máximos permisibles (LMP) se basó con lo descrito por The European Commision (2006) y Gimeno (2009) (Cuadro 1).
Cuadro 1. Concentraciones máximas tolerables (ppb, microgramos/kg) de micotoxinas en alimento para aves (con 12% de humedad)
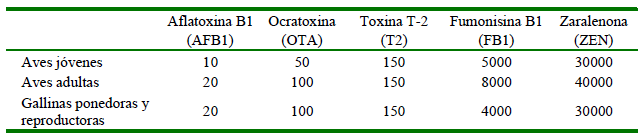
Fuente: European Commision (2006); Gimeno (2009)
Análisis de Datos
Los resultados se presentan mediante estadística descriptiva, con cuadros que describen las frecuencias y porcentajes de la calidad o condición de las muestras según tipo de alimento y procedencia. Asimismo, gráficos que describen las cantidades en los recuentos o micotoxinas halladas en las muestras. Se utilizo la prueba de Chi-cuadrado para determinar diferencias entre la calidades o condiciones de las muestras en las etapas de crianza o distritos y un análisis no paramétrico para muestras independientes (prueba de Kruskal-Wallis) para determinar la diferencia entre los promedios de las cantidades de hongos y aflatoxinas en las muestras por tipo de alimento o procedencia. En todos los casos se utilizó un nivel de significancia de p<0.05.
RESULTADOS
El 25% de las muestras de alimento balanceado tuvo calidad inaceptable (10/40) para el conteo de hongos, encontrándose las mayores frecuencias en el alimento de postura (2/4, 50%) e inicio (4/12, 33.3%) a diferencia de los demás tipos de alimento, aunque sin diferencias significativas (Cuadro 2).
Cuadro 2. Frecuencias y porcentajes totales de calidad o condición del alimento balanceado para aves de engorde (broilers) y de postura (gallinas) según el periodo de crianza en granjas de Ucayali (Pucallpa, Perú)
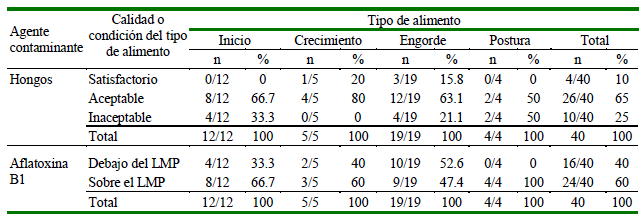
LMP: Límite máximo permisible
Se encontró mayor frecuencia de muestras contaminadas con AFB1 (sobre el LMP) con respecto a las demás micotoxinas evaluadas, aunque esta diferencia no fue estadísticamente significativa con respecto a las demás micotoxinas (p>0.05). Asimismo, se encontró mayor frecuencia de muestras contaminadas con AFB1 (sobre los LMP) en la etapa de postura (100%, 4/4) (Cuadro 2; p<0.05).
En el distrito de Yarinacocha se encontró mayor frecuencia de muestras contaminadas con AFB1 (sobre los LMP) (75%, 9/12), pero sin diferencia significativa con las frecuencias encontradas en los demás distritos (Cuadro 3; p<0.05). Por otra parte, si bien la mayor cantidad de muestras procedió del distrito de Campo Verde, el porcentaje y frecuencia de alimentos contaminados en ese distrito fue bajo (25%, 4/16) (Cuadro 3).
Cuadro 3. Frecuencias y porcentajes totales de calidad o condición del alimento balanceado para aves de engorde (broilers) y de postura (gallinas) según el distrito de crianza en granjas de Ucayali (Pucallpa, Perú)
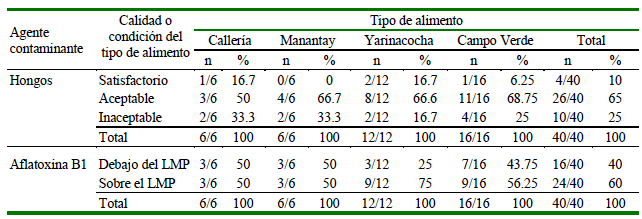
Límite máximo permisible (LMP) de hongos para materias primas y piensos para animales (UFC/g): satisfactorio <104, aceptable 104-105, insatisfactorio >105 (Gilbert et al., 2000)
Concentraciones máximas tolerables de aflatoxinas B1 (ppb, microgramos/kg) de acuerdo a lo descrito en el Cuadro 1
El alimento de postura tuvo el promedio más elevado en el recuento de hongos (1.68 x 105 [5.8 x 104 -4.2 x 105]), mientras que el promedio más elevado de concentraciones de aflatoxinas se encontró en las muestras de alimento de inicio (46.17 ppb [ND -124.6]). Por otra parte, el distrito de Manantay tuvo el alimento con el promedio más alto en el recuento de hongos (1.11 x 105 [4.1 x 104 2.8 x 105]), mientras que, el alimento de Callería presento la media más alta de concentraciones de aflatoxinas de las muestras (44.71 ppb [ND -124.6]). No obstante, los rangos en los valores para ambos parámetros en todas las etapas fueron muy variables (Figura 1), no encontrándose diferencias significativas entre las cantidades de hongos y aflatoxina B1 en las muestras de alimento para aves por tipo y por distrito (p>0.05).
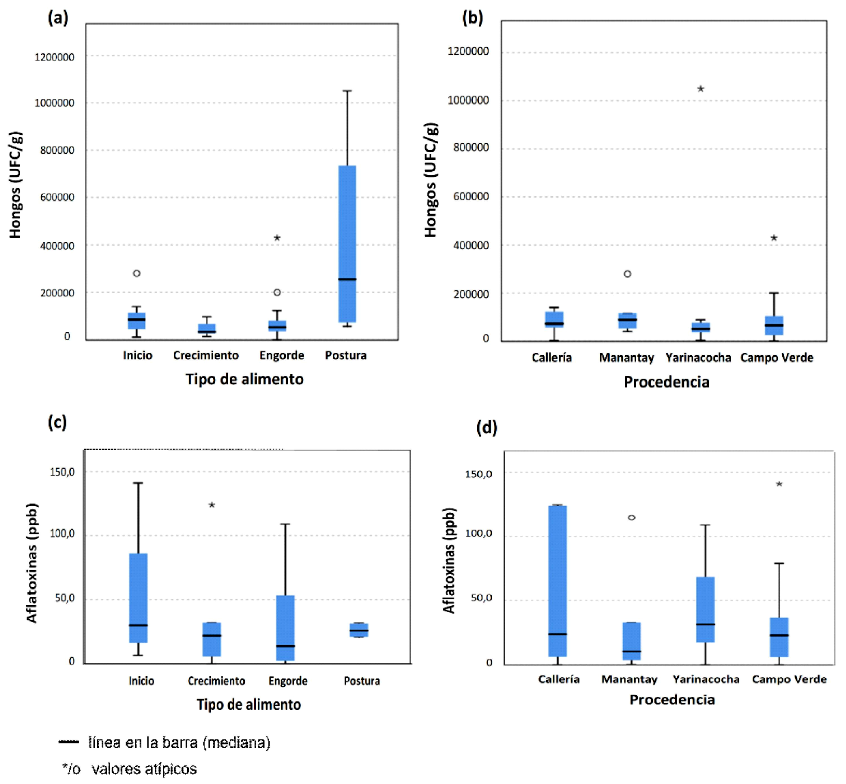
Figura 1. Diagramas de cajas de las cantidades de hongos y aflatoxinas B1 en las muestras de alimento para aves por tipo y procedencia de las granjas avícolas en Coronel Portillo, Ucayali (2018-2019). (a). Recuento de hongos (UFC/g) en muestras por etapa de crianza, (b). Recuento de hongos (UFC/g) en muestras por distrito, (c). Cantidad de aflatoxina B1 (ppb) en muestras por etapa de crianza, (d). Cantidads de aflatoxina B1 (ppb) en muestras por distrito
Las otras micotoxinas evaluadas en el estudio presentaron concentraciones menores al LMP. Los promedios más elevados de ocratoxina A se encontraron en el distrito de Manantay (7.233 ppb, [1.6 -23.9]) y en la etapa de engorde (3.16 ppb, [0.90 -23.90]). Para Fumonisina B1 los promedios más elevados se presentaron en Yarinacocha (2.48 ppm, [0.3 -4.3]) y en la etapa de postura (2.03 ppm, [1.30 -2.50]), para la toxina T-2/ TH-2 fueron en Campo Verde (19.02 ppb, [0 -123.90]) y en alimentos de la etapa de engorde (21.08 ppb, [0.0 -123.9]), en tanto que para Zearalenona se encontraron en Yarinacocha (145.40 ppb, [58.9 -290.1]) y en la etapa de postura (199.4 ppb, [59.80 -290.10]).
DISCUSIÓN
La alta temperatura y humedad en la región Ucayali pueden promover de manera constante la formación de hongos y micotoxinas en los alimentos. Consecuentemente, el manejo inadecuado en el almacenamiento y limpieza de los equipos de preparación, junto con la falta de control de calidad, si no es realizado a tiempo, puede afectar la calidad del producto, lo que puede generar problemas de contaminación y de intoxicación por micotoxinas (Buzby, 2003; Santin, 2014), factores que podrían señalarse causales de los hallazgos en el presente estudio.
Si bien solo se determinó un 25% de muestras de alimento con calidad inaceptable, este valor no fue proporcional al porcentaje de muestras con aflatoxinas por encima a los LMP (60%; Cuadro 2). Estos valores contrastan con los descritos en Argentina por Monge et al. (2013), quienes encontraron hongos en cantidades menores al LMP (1 x 104UFC/g), aunque reportaron latoxinaHT2, Fumonisina B1 y T-2 en el total de muestras. Esto puede demostrar que, el nivel de micotoxinas en el alimento no está necesariamente relacionada a la presencia de hongos (Zain, 2011).
El mayor porcentaje de muestras inaceptables en Campo Verde (4/16, 25%) no fue significativamente mayor a los porcentajes de los otros distritos (Cuadro 3), a pesar de ser un distrito eminentemente rural; además, se encontró mayor promedio en el recuento de hongos de las muestras de Manantay (con un amplio rango); sin embargo, no hubo asociación entre la calidad del alimento y la etapa de crianza, y entre la calidad y la procedencia.
Los hongos del género Aspergillus spp. pueden relacionarse con la presencia y formación de aflatoxinas. Así, Iram et al. (2019) en Pakistán investigaron la presencia de Aspergillus flavus y aflatoxinas en alimento para gallinas ponedoras encontrando el 64.7% de las muestras de alimento contaminadas, estando el 31% por encima del LMP. Esto indicaría que el hongo fue incluido en alguna etapa de producción o que las condiciones de almacenamiento eran inadecuadas (Marin et al., 2013; Pereira et al., 2014).
Aunque se hayan obtenido resultados diversos luego del análisis de las muestras recolectadas (Cuadro 2, Figura 1), la elevada contaminación en el alimento de postura, sugiere un efecto acumulativo de hongos y micotoxinas por el mayor tiempo de almacenamiento en las granjas; además, sus altos niveles en el alimento de inicio donde a pesar de no encontrarse diferencia significativa, podría deberse a una mayor cantidad de insumos energéticos, que se requieren para su preparación (Gimeno y Martins, 2011).
En referencia a la cuantificación de micotoxinas en el alimento, los promedios de aflatoxina B1 en todos los periodos de crianza y la mayor frecuencia de muestras con cantidades sobre los LMP (24/40, 60 %) (Figura 1) fue superior a lo descrito por Caballero et al. (2001) para Lima Metropolitana. Estos niveles podrían conllevar a alteraciones subclínicas y afectar los parámetros productivos en las aves en el caso que el consumo ocurra por periodos prolongados, lo cual, podría estar ocurriendo en algunos establecimientos del estudio.
Los resultados de la presente investigación con respecto a la contaminación de aflatoxinas es contrastado a lo indicado por Flores et al. (2006) en México, quienes hallaron 18.7% de piensos contaminados con micotoxinas; sin embargo, los porcentajes encontrados en Argentina por Dieser (2014), en alimento comercial para gallinas ponedoras fue mayor (77.8% por encima a los LMP), en tanto que Greco et al. (2014) indicaron que el déficit nutricional de aves en el 90% de muestras (44/49) fue debido a la presencia de aflatoxinas y otras micotoxinas.
A nivel internacional; Shar et al. (2014) e Iram et al. (2019) en Pakistán revelaron que los niveles de aflatoxinas en el alimento de aves ponedoras y de engorde se encontraba por encima de los LMP en el 31 y 42% de las muestras, respectivamente. Asimismo, Nishimwe et al. (2019) en Ruanda y Akinmusire et al. (2019) en Nigeria indicaron que más del 50 y el 83% de muestras procesadas se encontraban contaminadas por aflatoxinas, respectivamente. Esto evidencia que, la presencia de aflatoxinas es muy relevante y se extiende en zonas tropicales, influido por el clima que promueven su continuo desarrollo (Santin, 2014; Ayofemi, 2020).
Las bajas cantidades de ocratoxinas (OTA) en las muestras pudo deberse a la escasa presencia de cebada, trigo y subproductos de cereales susceptibles a esta micotoxina en el balanceado (Gimeno y Martins, 2011). No obstante, se tienen reportes de mayor frecuencia de esta micotoxina en el alimento de aves en granjas avícolas (Flores et al., 2006; Fareed et al., 2014). A pesar de estas diferencias, se debe tener en cuenta que solo escasas concentraciones de OTA pueden conllevar en el organismo animal a alteraciones tanto morfológicas como funcionales a nivel del hígado yriñón (Malir et al., 2013).
Las mínimas concentraciones halladas de fumonisina B1, toxina T-2/TH-2 y zearalenona fueron semejantes a los reportes de Franco et al. (2019) en Brasil, Monge et al. (2013) en Argentina y Flores et al. (2006) en México. Esto sugiere la posibilidad de la inactivación de Fusarium spp. en vegetación de campo e insumos húmedos ante procedimientos químicos o ecológicos, influenciados en gran medida por el proveedor y en mínima probabilidad por el avicultor; no obstante, su resistencia a procedimientos físicos y termo químicos pueden conllevar a su presencia en el alimento (Marín et al., 2013).
Finalmente, los resultados evidencian contaminación del alimento en las granjas avícolas en Ucayali de forma parcial, sugiriendo que, diversos factores, entre ellos; condiciones de almacenamiento y conservación, pudieron conllevar a la contaminación de los mismos, como lo menciona Milani (2013); sin embargo, es necesario investigar si otros factores externos pudieron contribuir al crecimiento de hongos y formación de micotoxinas, desde la siembra y recolección de insumos, hasta la elaboración del alimento (Zhu et al., 2016).












 uBio
uBio 


