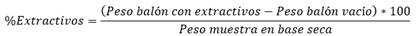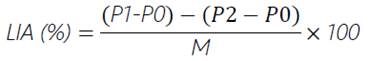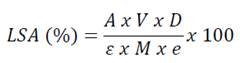1. Introducción
El concepto de biorrefinería se refiere a los procesos integrados, tanto químicos como bioquímicos, que transforman biomasa en bioproductos como biocombustibles, biocompuestos, alimentos para animales y biopolímeros (Sampaolesi et al., 2023). Esta biomasa lignocelulósica (BLC) está compuesta por una variedad de constituyentes, que incluyen celulosa (40% - 60%), hemicelulosa (20% - 40%) y lignina (10% - 24%) y en menor proporción, pectina y proteínas, así como extractivos (taninos, lípidos, resinas, esteroides, terpenos, terpenoides, flavonoides y compuestos fenólicos) (Mujtaba et al., 2023).
El interés en convertir materiales lignocelulósicos, como la celulosa, en productos de alto valor ha aumentado significativamente tanto en la academia como en la industria (Ahmad et al., 2023). La celulosa, caracterizada por su capacidad de atraer agua, biodegradabilidad, no toxicidad y facilidad de modificación, puede ser procesada para formar nanomateriales o nanocelulosa, lo que potencia aún más sus propiedades (Aoudi et al., 2022). La nanocelulosa se presenta principalmente en dos formas: nanocristales de celulosa (CNC) y nanofibras de celulosa (CNF). Aunque químicamente similares, estas formas difieren en sus propiedades físicas y métodos de extracción, los cuales pueden involucrar procesos mecánicos, químicos, o una combinación de ambos. Estos nanomateriales preservan la renovabilidad y abundancia de la celulosa, y ofrecen ventajas como baja densidad, alta superficie, gran resistencia a la tracción, excelente rigidez e inercia química (Trache et al., 2020) y se estima que el mercado de nanocelulosa alcanzará los 783 millones de dólares para 2025 (Zhang et al., 2023).
Por otro lado, la nanocelulosa bacteriana (BNC), consiste en nanofibras ultrafinas, puras y en forma de cinta con 20 a 100 nm de diámetro y longitudes micrométricas, que se entrelazan para producir una red tridimensional como sello distintivo. Este tipo de nanocelulosa se produce normalmente a partir de bacterias, identificándose a las del género Glucona cetobacter como excelentes productoras de BNC en medios de cultivo estáticos. De tal modo que, uno de los principales desafíos en la producción de celulosa bacteriana es encontrar fuentes de carbono adecuadas que sean baratas, abundantes y que no compitan con la producción de alimentos (Dórame-Miranda et al., 2019). Por tal motivo, BLC como piel de uva, cáscara de mango, plátano, granada entre otros, han sido analizados y utilizados como fuente de carbono (Gorgieva et al., 2023; Hasanin et al., 2023; Kumari et al., 2023; Ogrizek et al., 2021; Ul-Islam et al., 2023). Sin embargo, es necesario investigar nuevas fuentes de carbono.
De igual manera, biomasa lignocelulósica (BLC) de bajo costo también ha sido objeto de estudio en la producción de polihidroxialcanoatos (PHA) (De Souza et al., 2020), dado el creciente interés comercial y de investigación en polímeros ecológicos. Estos polímeros destacan por sus propiedades favorables, como alta biocompatibilidad, excelente biodegradabilidad, estructura química diversa y la posibilidad de ser fabricados a partir de recursos de carbono renovables (Sharma et al., 2021). Los PHA, poliésteres de base biológica, se sintetizan intracelularmente en más de 300 microorganismos, siendo los géneros Alcaligenes, Azotobacter, Bacillus, Rhizobium, Rhodospirillum y Pseudomonas los más comunes (Vaishnav & Choudhary, 2021). No obstante, se está investigando un grupo alternativo de microorganismos halófilos, debido a las ventajas que ofrecen en la producción de PHA (Daoud & Ali, 2020). Para una síntesis efectiva de PHA, es necesario cumplir dos condiciones: limitar la fuente de nitrógeno y proporcionar un exceso de fuente de carbono. En relación con esta última condición, se ha investigado la incorporación de biomasa de bajo costo con alto contenido de azúcares (Mahato et al., 2023).
No obstante, la diversidad composicional y las propiedades fisicoquímicas de la BLC influyen en su viabilidad para su aplicación en procesos de biorrefinería (Saba et al., 2023). Por esta razón, es fundamental comprender su composición estructural para estandarizar los procesos de producción de nanopolisacáridos y polihidroxialcanoatos.
Por lo anteriormente expuesto, el objetivo de esta investigación fue caracterizar composicional y estructuralmente once tipos de BLC, para evaluar su potencial uso en la obtención de nanopolisacáridos y producción de polihidroxialcanoatos, así como su posible aplicación industrial.
2. Metodología
Acondicionamiento de la biomasa lignocelulósica
Once tipos de BLC, procedente de empresas agroindustriales de la región La Libertad, Perú: brácteas de alcachofa (BA), cáscara de espárrago (CE), semilla de palta (SP), cáscara de yuca (CY), cáscara de limón (CL), cáscara de naranja (CN), cáscara de maracuyá (CM), cáscara de papa (CP), cáscara de arroz (CA), paja de arroz (PA) y bagazo de caña de azúcar (BC) con no más de 24 horas de haber sido procesados, fueron secados en estufa (Memmert, UF110 Plus, Alemania) a 40 ± 2 °C hasta peso constante, posteriormente fueron molidos y tamizados usando tamiz N° 70 , envasados herméticamente y almacenados a temperatura ambiente hasta su posterior análisis.
Análisis composicional de la biomasa lignocelulósica
Se determinó el contenido de humedad y sólidos totales (Sluiter et al., 2008a), ceniza (Sluiter et al., 2005) y proteína (Hames et al., 2008) a cada una de las muestras de BLC. El contenido de proteína fue calculado a partir del nitrógeno total empleando factor de conversión: 6,25 (Reyes et al., 2017).
Cuantificación de extractivos
Los extractivos (compuestos no estructurales) fueron cuantificados utilizando un equipo Soxhlet y etanol al 96% como solvente. Tras 24 horas de reflujo, se eliminó el solvente residual por filtración y se lavó la muestra con etanol. La muestra libre de extractivos se secó en estufa (Memmert, UF110 Plus, Alemania) a 40 ± 2 °C hasta peso constante y se almacenó en bolsas herméticas. El filtrado recolectado se concentró en un evaporador rotatorio (Dlab, RE100-PRO, China) para retirar el solvente y luego se secó en estufa (Memmert, UF110 Plus, Alemania) a 40 ± 2 °C durante 24 horas hasta peso constante para medir el contenido de extractivos (Ecuación 1) (Sluiter et al., 2008b).
Cuantificación de carbohidratos estructurales y lignina
La BLC libre de extractivos se sometió a dos hidrólisis consecutivas con soluciones de ácido sulfúrico (72%, 1 h, 30 °C; 4%; 1 h, 121 °C). Posteriormente fue enfriada a 25 °C, para luego ser filtrada a vacío y el sobrenadante se empleó para la cuantificación de lignina insoluble en ácido (LIA), lignina soluble en ácido (LSA) y lignina total (LT), así como carbohidratos estructurales (CE) (Sluiter et al., 2008a) (Figura 1).
Para la cuantificación de LIA, los sólidos o residuo insoluble en ácido (AIR) retenidos en el papel filtro se transfirieron a un crisol y se secaron en estufa (Memmert, UF110 plus, Alemania) a 105 ± 3 °C durante 24 horas. Posteriormente, se incineraron los crisoles en el horno de mufla (Hornos Felix, HM 010, Perú) a 575 ± 25 °C durante 5 horas. El contenido de LIA de la muestra en una base libre de extractivos fue determinado con la ecuación 2.
Donde P1: peso crisol + residuo insoluble; P0: peso crisol vacío; P2: Peso crisol + cenizas; M: peso muestra libre de extractivos.
La lignina soluble en ácido (LSA) se determinó a partir del hidrolizado filtrado al vacío empleando método espectrofotométrico. Se midió la absorbancia de la muestra a una longitud de onda 205 nm en un espectrofotómetro UV-Visible (Thermo Scientific, Orion AquaMate 8000, USA). Se diluyó la muestra con agua desionizada para llevar la absorbancia al rango de 0,7 - 1,0. La lignina soluble en ácido (LSA) se determinó mediante la ecuación 3.
Donde A: Absorbancia de la muestra; V: Volumen del hidrolizado; D: Dilución; Ɛ: Absortividad de biomasa a una longitud de onda específica (110 L/g-cm); M: peso muestra libre de extractivos; e: distancia que recorre la luz UV-Visible a través de la celda (1 cm).
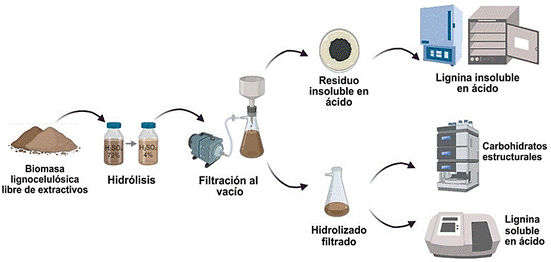
Figura 1 Proceso de cuantificación de lignina insoluble en ácido, lignina soluble en ácido y carbohidratos estructurales.
La cuantificación de carbohidratos estructurales se realizó por cromatografía líquida de alta resolución (HPLC) (Thermo Scientific, Ultimate 3000, USA) equipado con un detector de aerosol cargado o CAD (Thermo Scientific, Corona Veo RS, USA) (Sluiter et al., 2008a). Las condiciones cromatográficas se muestran en la Tabla 1; se empleó un kit de azúcares (glucosa, xilosa, galactosa, arabinosa y manosa (Sigma Aldrich, pureza 99,5%), en un rango de 50 a 1000 ug/ml por triplicado para poder construir curvas de calibración logarítmicas (Tabla MS1, Material Suplementario). Se utilizaron están dares de verificación (CVS) a 800 ug/ml para evaluar la calidad y estabilidad de las curvas de calibración.
Tabla 1 Condiciones de HPLC y CAD para carbohidratos estructurales
| Parámetros HPLC | Valor |
|---|---|
| Columna | Shodex Sugar SP0810 y SP-G-6B |
| Volumen de inyección | 10 µl |
| Fase móvil | Acetonitrilo 11% en fase acuosa |
| Tasa de flujo | 0,700 ml/min |
| Temperatura de columna | 80 °C |
| Parámetros CAD | Valor |
| Temperatura del detector | 50 °C |
| Filtro | 5 s |
| Recolección de datos | 10 Hz |
| Tiempo de ejecución | 25 minutos |
Análisis estadístico
Los valores se citan en el texto como medias ± DE. Para evaluar la similitud de la BLC, en función a su análisis composicional, se elaboró un dendrograma, observándose la formación de conglomerados con una disimilitud del 50%. Para la analítica de datos se utilizó el software R 4.3.1 con los paquetes "factoextra" (Kassambara & Mundt, 2020) y "tydiverse" (Wickham et al., 2019).
3. Resultados y discusión
Análisis composicional de la biomasa lignocelulósica
El análisis composicional de la BLC es presentado en la Figura 2 (Tabla MS2, Material Suplementario) y proporciona información clave para orientar de manera específica el aprovechamiento de la BLC en la obtención de nanopoliscáridos y producción de polihidroxialcanoatos. La humedad inicial varió entre el 6,32% y el 14,19% para BC (Figura 2d) y CE (Figura 2e), respectivamente. Es cru cial destacar que concentraciones superiores al 15% de humedad en la biomasa resultan inadecuadas para la determinación precisa de carbohidratos, ya que podrían influir en la concentración del ácido uti lizado en la hidrólisis posterior (Sluiter et al., 2008a).
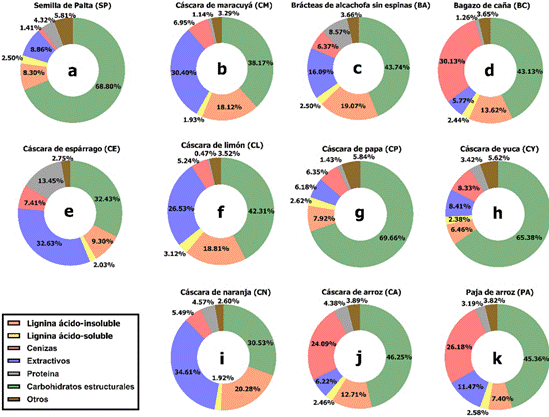
Figura 2 Caracterización composicional y estructural de semilla de palta (SP), cáscara de maracuyá (CM), brácteas de alcachofa sin espinas (BA), bagazo de caña de azúcar (BC), cáscara de espárrago (CE), cáscara de limón (CL), cáscara de papa (CP), cáscara de yuca (CY), cáscara de naranja (CN), cáscara de arroz (CA), paja de arroz (PA).
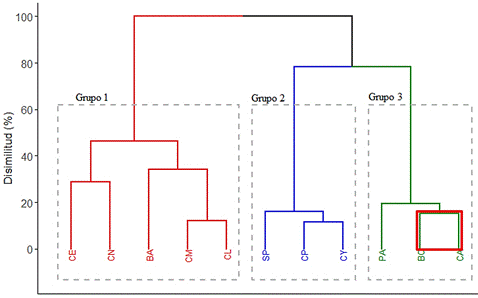
Figura 3 Dendograma presentado tres conglomerados, grupo 1: cáscara de espárrago (CE), cáscara de naranja (CN), brácteas de alcachofa sin espinas (BA), cáscara de maracuyá (CM), cáscara de limón (CL), grupo 2: semilla de palta (SP), cáscara de papa (CP), cáscara de yuca (CY), grupo 3: paja de arroz (PA), bagazo de caña de azúcar (BC), cáscara de arroz (CA).
En cuanto al contenido de cenizas, se observó que el BC (Figura 2d) exhibió el valor más alto entre los diferentes tipos de BLC analizados, alcanzando un 30,13%. Este fenómeno podría atribuirse a los procesos previos de transformación a los que fue sometida la materia prima (Phonphuak & Chindaprasirt, 2015). En lo que respecta al contenido de proteína, osciló entre 0,47% y 13,45% para CL (Figura 2f) y CE (Figura 2e) respectivamente, cifras que difieren de las reportadas por Mhgub et al. (2018) y Goñi et al. (2024). Por otro lado, en cuanto a los extractivos, que comprenden materiales no estructurales, los valores se situaron entre el 5,77% (BC) (Figura 2d) y el 34,61±1,40 (CN) (Figura 2i), sugiriendo la presencia de aceites esenciales, pectinas, gomas y compuestos fenólicos en la BLC (Ortiz-Sanchez et al., 2021). Estas discrepancias entre los once tipos de BLC evaluadas podrían atribuirse principalmente a diferencias en la variedad de biomasa, las regiones de cultivo y los procesos mecánicos y químicos a los que se somete la materia prima durante su procesamiento y transformación. Según MacLellan et al. (2017), es esencial tener en cuenta el contenido de proteína, ya que concentraciones elevadas podrían afectar su uso en procesos subsiguientes de sacarificación y fermentación.
La cantidad de lignina, polímero de estructura aleatoria y cuya presencia aporta protección y rigidez a las plantas (Bilal et al., 2024) es variable en la biomasa evaluada debido principalmente a que el contenido difiere según su ubicación, como cáscaras, tallos y hojas, encontrándose el menor contenido de lignina total en CY (8,84%) (Figura 2h) y el mayor en CN (22,2%) (Figura 2i), los cuales deberán ser removidos para aprovechar los carbohidratos y otros componentes presentes en la BLC (Ayala et al., 2021).
El análisis del contenido de carbohidratos estructurales presenta gran interés en la investigación científica debido a su potencial para ser revalorizado en diversos procesos industriales y biotecnológicos. En este contexto, la CP (69,66%) (Figura 2g), SP (68,8%) (Figura 2a) y CY (65,38%) (Figura 2h) exhiben los mayores niveles de carbohidratos estructurales, destacándose como candidatos prometedores para procesos fermentativos. No obstante, es crucial tener en cuenta que estos carbohidratos podrían estar parcialmente asociados con la presencia residual de almidón (Sandoval-Contreras et al., 2023). Por otro lado, la CN presenta la menor concentración de carbohidratos estructurales (30,53%) (Figura 2i), lo que podría atribuirse a su elevado contenido de pectinas y otros componentes solubles en su composición (Turan et al., 2024).
En el dendrograma mostrado en la Figura 3, se identifican tres conglomerados. El primer grupo, compuesto mayoritariamente por cáscaras (CE, CN, BA, CM y CL), se caracteriza por un contenido promedio de extractivos más alto (16,09%-34,61%) y una mayor concentración de lignina total (11,33%-22,02%) en comparación con los grupos 2 y 3. El contenido de extractivos en este grupo podría estar asociado con la presencia de una amplia gama de compuestos, incluyendo grasas, ceras, proteínas, terpenos, gomas, resinas, fenólicos, aceites esenciales, pectinas, mucílagos y saponinas, así como ácidos grasos, esteroles y flavonoides (Pecha & Garcia-Perez, 2020).
En el caso de CE (32,63%) (Figura 2e), los extractivos podrían tener valor comercial significativo, debido a la probable presencia de compuestos bioactivos y extractos con capacidad antioxidante, ricos en flavonoides y saponinas (Alcaide et al., 2023). La CN (34,61%) (Figura 2i) exhibe un alto potencial de compuestos extraíbles que podrían ser aprovechados, como azúcares solubles, oligosacáridos y polímeros de ácidos urónicos. Además, contiene una fracción insoluble compuesta principalmente por grasas, ceras y aceites esenciales (Turan et al., 2024). Las BA (16,09%) (Figura 2c) representa una fuente de com puestos bioactivos, destacando los polifenoles (Órbenes et al., 2021) y otros compuestos de interés alimentario, como la inulina (Ruiz-Aceituno et al., 2016). La CM (30,40%) (Figura 2b) contiene componentes de alto interés para la industria alimentaria, como pectinas (Inayati et al., 2018), así como compuestos fenólicos bioactivos (Pereira et al., 2021). Finalmente, en CL (26,53%), (Figura 2f), los extractivos están compuestos principalmente por pectinas, gra sas, azúcares solubles y aceites esenciales (Mamma & Christakopoulos, 2014), destacando el limoneno, que tiene amplias aplicaciones en las industrias de fragancias, farmacéutica, alimentos y bebidas (Lopresto et al., 2018).
En el caso de CE (32,63%) (Figura 2e), los extractivos presentan un valor comercial significativo debido a la presencia de compuestos bioactivos y antioxidantes, ricos en flavonoides y saponinas (Alcaide et al., 2023). Por su parte, CN (34,61%) (Figura 2i) muestra un alto potencial en compuestos extraíbles, como azúcares solubles, glucooligosacáridos y polímeros de ácidos urónicos. Además, su fracción insoluble está compuesta principalmente por grasas, ceras y aceites esenciales (Ayala et al., 2021). Finalmente, en CL (26,53%) (Figura 2f), los extractivos estarían conformados principalmente por pectinas, grasas, azúcares solubles y aceites esenciales, con el limoneno destacando por su importancia en las industrias de fragancias, farmacéutica, alimentaria y de bebidas (Núñez-Gómez et al., 2024).
Por otro lado, la lignina, como un recurso renovable clave, se destaca por su amplia disponibilidad, siendo el segundo componente más abundante en la BLC. Su estructura, rica en compuestos aromáticos e hidroxilos fenólicos, ha despertado un considerable interés en diversas aplicaciones (Baite et al., 2023). Las propiedades de la lignina, que incluyen actividad antioxidante, antimicrobiana, no toxicidad, estabilidad térmica, biodegradabilidad y capacidad para bloquear rayos UV, resultan especialmente atractivas para su uso en la formulación de envases para alimentos, productos farmacéuticos y otras aplicaciones industriales (Priyadarshi et al., 2024).
Los tres tipos de BLC que componen el segundo grupo (SP, CP y CY), se caracterizan por su alto contenido de carbohidratos estructurales en forma de celulosa, hemicelulosas o almidón, oscilando entre el 65,38% y el 69,66%. Esta fracción sería de gran interés debido a su potencial de valorización, ya que permite la extracción de nanopolisacáridos, almidones y oligosacáridos, así como la obtención de sustratos para la producción de azúcares fermentables. Estos azúcares podrían ser utilizados en diversos bioprocesos, como producción de etanol, biosíntesis de celulosa bacteriana (CB) y producción de bioplásticos, como los polihidroxialcanoatos (PHA).
La SP, con un contenido de carbohidratos del 68,80% (Figura 2a), se destaca como la BLC más prometedora, dado que entre el 33,17% y el 67,5% de estos carbohidratos son almidones. Estos almidones pueden emplearse en procesos alimentarios o, mediante hidrólisis química o enzimática, transformarse en glucosa para su uso en procesos fermentativos posteriores (Sandoval-Contreras et al., 2023). En cuanto a la CP (Figura 2g) y la CY (Figura 2h), con contenidos de carbohidratos del 69,66% y 65,38%, respectivamente, presentan composición similar. La CP podría ser apta para procesos fermentativos y ser usada en la producción de etanol y ácidos orgánicos (Liang & McDonald, 2015), mientras que la CY, mediante hidrólisis enzimática, podría generar hidrolizados ricos en azúcares fermentables (Ona et al., 2019).
En un tercer grupo (PA, BC y CA), se observa un mayor contenido de cenizas, que varía entre el 24,09% y el 30,13%, junto con un contenido moderado de carbohidratos estructurales, como celulosa y hemicelulosa, con valores de 43,13%, 45,36% y 46,25% en BC (Figura 2d), CA (Figura 2e) y PA (Figura 2f), respectivamente. Estos carbohidratos estructurales ofrecen diversas posibilidades de valorización. Además, la fracción de cenizas, notablemente rica en sílice, confiere a estos materiales un valor especial para aplicaciones en la fabricación de adsorbentes para metales pesados y colorantes, así como en la producción de aerogeles y materiales de construcción (Goodman, 2020).
Análisis de carbohidratos estructurales
En la Figura 4 se muestra los resultados del análisis de carbohidratos estructurales en los once tipos de BLC, observándose variabilidad significativa de glucano, xilano, galactano, arabinano y manano, considerados como componentes clave de la pared celular (Marx & Radebe, 2018).
Como se muestra en la Figura 4, el glucano es el carbohidrato polimérico más abundante, con valores entre 14,73% y 61,87%. Este glucano se deriva principalmente de polisacáridos no pécticos, como la celulosa o el almidón, presentes en las muestras de SP, CP y CY (Wang et al., 2016). Por otro lado, el mayor contenido de xilano se identificó en BC, alcanzando 12,102%, mientras que no se detectó en SP. El xilano, que es un componente principal de la hemicelulosa, está formado por largas cadenas de residuos de xilopiranosa unidas por enlaces β-1,4 (Senthilkumar et al., 2005). Este carbohidrato tendría potencial para aplicaciones en procesos químicos, como la producción de xilitol, y en procesos biotecnológicos, como la producción de etanol, ácidos orgánicos y polihidroxialcanoatos (Hermiati et al., 2024).
El contenido de galactano (4,32% - 14,15%) y arabinano (0,52% - 8,55%) parece estar relacionado tanto con la estructura de las sustancias pécticas (Rahmani et al., 2020) como con los componentes característicos de la hemicelulosa (Narisetty et al., 2022). En particular, el alto contenido de galactanos en SP (14,15%) puede estar asociado con las pectinas en la pared celular, que influyen en la firmeza del fruto (Tateishi et al., 2007). De manera similar, los mayores niveles de arabinano se registran en CL (8,55%) y CN (7,53%), lo que podría deberse a la presencia de pectinas en las cáscaras de estos cítricos (John et al., 2017). En cuanto al manano, su presencia es mínima, con CN (1,74%) y CL (1,73%) mostrando las mayores concentraciones. Esta presencia estaría probablemente vinculada a fracciones hemicelulósicas o residuales de pectinas características de las cáscaras de cítricos (Mhgub et al., 2018).
Potenciales aplicaciones
Extracción y producción de nanopolisacáridos
En la última década, ha surgido un creciente interés en la conversión de celulosa, considerada un recurso altamente versátil, para sustituir materiales derivados del petróleo. La celulosa destaca por su disponibilidad, estabilidad, baja densidad, naturaleza no abrasiva, renovabilidad y biodegradabilidad (Ahmad et al., 2023). Se han desarrollado varios derivados solubles en agua, como carboximetilcelulosa, metilcelulosa, hidroxipropilmetilcelulosa, acetato de celulosa, hidroxietilcelulosa, entre otros (Li et al., 2018).
La estructura lineal y semirrígida de la celulosa, impulsada por enlaces de hidrógeno, confiere una resistencia excepcional. Su arquitectura jerárquica única, que incluye fibrillas y cristalitos a nanoescala, permite la extracción de nanoconstituyentes mediante métodos mecánicos, químicos o una combinación de ambos (Li et al., 2018). Estos nanoconstituyentes incluyen las nanofibras (NFC) de celulosa, largas, delgadas y flexibles, y los nanocristales (CNC) de celulosa, partículas cristalinas en forma de varilla (Chieng et al., 2017).
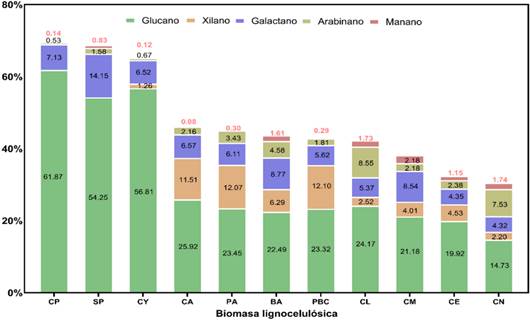
Figura 4 Análisis de carbohidratos estructurales en semilla de palta (SP), cáscara de maracuyá (CM), brácteas de alcachofa sin espinas (BA), bagazo de caña de azúcar (BC), cáscara de espárrago (CE), cás cara de limón (CL), cáscara de papa (CP), cáscara de yuca (CY), cáscara de naranja (CN), cáscara de arroz (CA), paja de arroz (PA).
Las NFC, según la norma ISO/TS 20477:2017, son fi bras con un diámetro de entre 3 nm y 100 nm y una longitud de hasta 100 μm. Se producen mediante métodos mecánicos como homogeneización a alta presión, microfluidización o molienda (Xu et al., 2023). Las propiedades distintivas de las NFC, como su resistencia mecánica y capacidad de absorción, han promovido su producción y uso desde 1983.
Por otro lado, los CNC, son nanopartículas altamente cristalinas con una pureza del 90% y generalmente, se obtienen separando la celulosa para preservar su región cristalina (Ahmad et al., 2023). Estos nanomateriales pueden ser extraídos de diver sas fibras naturales y se destacan por su bajo costo, disponibilidad y biodegradabilidad. Una vez aislados, pueden ser utilizados en una amplia gama de aplicaciones en varios campos, incluyendo nanocompuestos, materiales de construcción, envases inteligentes, superficies funcionales, entre otros (Nascimento et al., 2021).
La producción de celulosa bacteriana (BNC) ha captado considerable atención debido a sus propiedades excepcionales y su producción sostenible. La BNC, caracterizada por su estructura de cinta retorcida, posee propiedades físicas y mecánicas notables (Cazón & Vázquez, 2021). La BNC se produce utilizando residuos agroindustriales como fuentes de carbono no convencionales, lo que ha permitido reducir costos y aumentar su producción (Barja, 2021).
Producción de polihidroxialcanoatos
Los polihidroxialcanoatos (PHA) son biopolímeros que poseen una amplia gama de propiedades deseables para diversas aplicaciones industriales y biomédicas. Una de las propiedades más destacadas de los PHA es su biodegradabilidad, que les permite descomponerse de manera natural en el medio ambiente, reduciendo así la acumulación de desechos plásticos y contribuyendo a la preservación del ecosistema (Koller, 2017). Esta propiedad es aprovechada en la elaboración de indumentaria sanitaria y equipos de protección personal de un solo uso (Lo et al., 2024), que significó una marcada contaminación ambiental en tiempos de pandemia por el COVID-19 debido a su alta demanda. En productos relacionados a la cosmética y cuidado personal también se incorporan como material alternativo para encapsular antioxidantes para mejorar la apariencia de la piel (Phothong et al., 2024). El PHA también es una alternativa para sustituir los productos a base de petróleo en aplicaciones en agricultura y horticultura como los maceteros empleados para trasplantar los plantines hacia los campos de cultivo, permitiendo enterrar la planta junto con el macetero para evitar maltratar las raíces (Oliver-Ortega et al., 2024).
Además de su biodegradabilidad, los PHA también exhiben termoplasticidad, lo que significa que pueden ser moldeados y transformados a través de técnicas de procesamiento térmico, como la extrusión y la inyección, para fabricar una amplia variedad de productos plásticos. Esta propiedad los hace adecuados para aplicaciones en la industria de envases, donde se requiere flexibilidad en el diseño y la fabricación de productos. Se ha logrado elaborar biopelículas con características de barrera al oxígeno y al dióxido de carbono empleando PHA junto con otros polímeros (Iglesias-Montes et al., 2022); de igual manera se puede mejorar las características del material para mantener la calidad, sabor, color y frescura de las bebidas, y mejorar la seguridad del producto, inhibiendo la degradación hasta que el empaque sea desechado (Stoica, 2020).
Otra propiedad importante de los PHA es su biocompatibilidad, con baja probabilidad de causar reacciones adversas en el cuerpo humano. Esta característica los hace ideales para su uso en aplicaciones biomédicas, como la fabricación de implantes médicos (Ye et al., 2022) y dispositivos de sutura (Li et al., 2020).
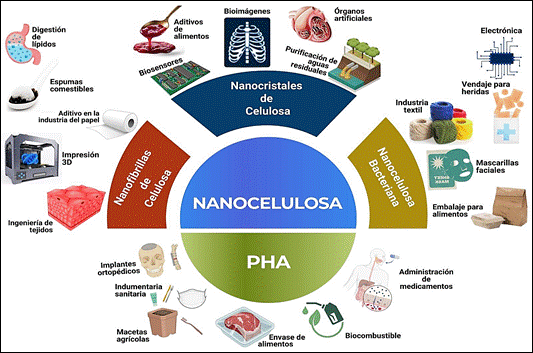
La Figura 5 resume las posibles aplicaciones de los nanopolisacáridos y polihidroxialcanoatos obtenidos a partir de la biomasa lignocelulósica evaluada.
4. Conclusiones
Este estudio proporciona una caracterización detallada de once tipos de BLC de la región de La Libertad, Perú, destacando la variabilidad en su composición y estructura. Se identificaron muestras con altos contenidos de extractivos, como la cáscara de maracuyá, brácteas de alcachofa y cáscaras de diversas frutas cítricas, lo que sugiere la presencia de una amplia gama de compuestos. Por otro lado, muestras como la semilla de palta, cáscara de papa y de yuca, junto con el bagazo de caña de azúcar y residuos de arroz, exhibieron contenidos significativos de carbohidratos estructurales y lignina. Además de su caracterización, se exploró el potencial de esta biomasa para la extracción y síntesis de nanopolisacáridos y producción de polihiroxialcanoatos, lo que abre perspectivas prometedoras en diversas industrias, desde la alimentaria hasta la ingeniería de materiales. Estos hallazgos subrayan la importancia de aprovechar los recursos naturales locales de manera sostenible y ofrecen nuevas oportunidades para el desarrollo de aplicaciones innovadoras como emul siones pickering, envases biodegradables, aerogeles e hidrogeles, y alimentos funcionales. Estas aplicaciones prometen ser áreas prometedoras para futuras investigaciones y desarrollo tecnológico.