INTRODUCCIÓN
La sacroileítis infecciosa (SII) fue descrita por primera vez por Poore en 1878 y, desde entonces, la literatura sobre esta infección proviene principalmente de informes de casos y pequeñas series de pacientes.1La incidencia del SII es relativamente baja, aprox. 1%. Representa el 2% de todos los casos.
Un caso de artritis séptica.2,3. Esto puede deberse a varias razones diferentes, causas que incluyen enfermedades degenerativas, traumatismos, embarazo, uso de drogas intravenosas, terapia inmunosupresora, trastornos de la hemoglobina, enfermedades inflamatorias e infecciones como endocarditis y del tracto urinario o dermatitis; sin embargo, estos factores de riesgo sólo pueden estar presentes en pacientes del 55% al 60% de los casos identificados1. La sacroileítis unilateral debe guiar el diagnóstico de la SII4, aunque la sacroileítis unilateral se asocia con espondiloartropatías (artritis psoriásica, espondilitis anquilosante reactiva, temprana), lo que supone un desafío diagnóstico.
La contaminación puede ser producto de una bacteriemia, debido a una infección contigua, o por inoculación directa, como en el caso de las infiltraciones articulares.7
Las infecciones pueden ser causadas por organismos piógenos y tuberculosis.5-8
Los síntomas iniciales inespecíficos y los hallazgos variables del examen físico dificultan el diagnóstico y a menudo se pasan por alto desde el principio. Las manifestaciones clínicas son diferentes, pero el dolor más común es en la zona lumbar y en los glúteos, que empeora al caminar. La resonancia magnética de imagen (MRI) de la pelvis es el estándar de oro para diagnosticar el SII.6
El tratamiento con antibióticos a largo plazo, que dure más de cuatro semanas, se considera un tratamiento adecuado.9
CASO CLÍNICO
Se presenta el caso de una paciente femenina de 83 años, con antecedentes de enfermedad cerebrovascular, hipertensión arterial, diabetes mellitus tipo 2 e infección de vías urinarias. La paciente presentó, de forma brusca, dos días antes de su ingreso, dolor en flanco derecho tipo cólico de moderada intensidad, debilidad de hemicuerpo izquierdo, disartria y cuadros febriles intermitentes. Al examen físico de ingreso, en cuanto a los signos vitales se encontró: PA: 140/70, T: 38.2°. Con respecto a piel y faneras, se evidenció edemas de miembros inferiores y fóvea (+). A nivel respiratorio, el murmullo vesicular pasaba disminuido en ambos campos pulmonares. En cuanto al aparato CV, se auscultó un soplo holosistólico. Además, en lo que respecta al abdomen, había dolor a la palpación en hipogastrio y en cuanto al SNC, había hemiparesia izquierda.
Respecto al examen físico somático, se realizó prueba de flexión, abducción y rotación externa (FABERE), positivo, Prueba de Gaenslen-Mennel, positivo; Test Log Roll de la cadera izquierda, negativo; signos de irritación radicular negativos sin adenopatías inguinales palpables.
Los exámenes de laboratorio revelaron: glucosa basal en 537, urea de 170, leucocitosis de 18000, plaquetopenia de 38 000, abastados de 3%, segmentados en 80%, linfocitos de 10%, T de protrombina de 17.3. Además, contó con un examen de orina patológico (proteínas 2+, nitritos +, sangre +, leucocitos +; en cuanto al sedimento urinario: glóbulos rojos en 139.92/ uL. y glóbulos blancos en 640.20/uL).
Se realizó una TEM cerebral sin contraste, la cual evidenció signos tomográficos en relación a ACV isquémico subagudo fronto parieto temporal derecho, dependiente del territorio de la ACM derecha. Asimismo, se hizo un EKG con diagnóstico de fibrilación auricular con respuesta ventricular controlada y una ecografía abdominal completa con diagnóstico de litiasis renal izquierda e hidronefrosis grado II.
Debido a persistencia de cuadros febriles intermitentes con foco a determinar, se realizan exámenes de laboratorio seriado control a los siete días, los cuales revelaron glucosa basal de 221 mg/dL, urea de 211 mg/dL, PCR de 23.28, creatinina de 3.30 mg/dL, leucocitos de 13 380 xmm3, plaquetas de 42 000, abastonados de 4%, segmentados en 88% y linfocitos en 6%.
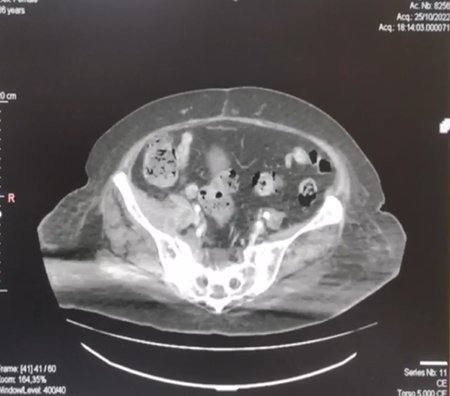
Debido a la clínica destacable, pruebas de examen físico probables y exámenes ecográficos con resultados poco esclarecedores, se decide realizar una TEM de abdomen con contraste completo, con vistas a encontrar afección sacroiliaca con compromiso retroperitoneal; dichas imágenes evidenciaron a nivel de la articulación sacroiliaca una colección densa heterogénea con contenido aéreo asociado a erosión cortical que se extiende anteriormente a músculos psoas e iliacos y hacia posterior al músculo piramidal, así como signos tomográficos en relación a artromielitis sacroiliaca con zonas de colección abscedada en músculo psoas iliaco y piramidal ipsilateral (Figura 1)
Se planteó el diagnóstico de absceso retroperitoneal, por lo cual se realizó una laparotomía exploratoria + drenaje de absceso + dren mixto. En cuanto a los hallazgos operatorios, se menciona que a la apertura de la fascia de Todd se evidenció abombamiento de psoas derecho debido a líquido purulento de aproximadamente 100mL.
DISCUSIÓN
El SII es una enfermedad rara que se manifiesta con síntomas inespecíficos, lo que a menudo provoca un retraso en el diagnóstico. La presentación inicial puede indicar afecciones más comunes, como dolor de espalda, ciática, abscesos dentro o fuera de la pelvis, infección abdominal, cálculos renales o pielonefritis. La SII suele ser unilateral. Los síntomas típicos incluyen febrícula, dolor lumbar (ocurre hasta en el 100% de los pacientes), dolor en la cintura y parte posterior del muslo y dificultad para caminar del lado afectado. Sorprendentemente, más de la mitad de los casos notificados se diagnosticaron 10 días o más después de la aparición de los síntomas2,9.
El examen físico temprano reveló hallazgos específicos que incluyen sensibilidad en la región posterior del ASI y dolor causado por la compresión de la pelvis posterior, pero la palpación directa del ASI fue difícil, debido a su ubicación anatómica, lo que requirió un examen provocativo para replicar el dolor y los síntomas: Gaenslen (flexión forzada de cadera contralateral e hiperextensión forzada de cadera ipsilateral con el paciente en decúbito supino) y una prueba FABERE positiva hasta en el 91,7% de los pacientes10,11. Estas pruebas han demostrado ser confiables con sensibilidad, especificidad y valor predictivo positivo (60%), para determinar el origen del dolor, pero no se realizan comúnmente en el entorno clínico actual, debido a un bajo índice de sospecha.
Berthelot y Laslett12reportaron que, en el examen clínico de la ASI, ningún signo clínico podría indicar claramente el dolor, pero que la probabilidad de dolor articular o periarticular aumenta cuando tres de las cinco pruebas de provocación más confiables son positivas:
Maniobra de distracción de las alas ilíacas
Maniobra de compresión de las alas ilíacas
Compresión directa en el sacro
Prueba de Gaenslen
Prueba de Mennell (prueba de Gaenslen con el paciente en decúbito lateral)
Estas pruebas deben ser realizadas sobre una superficie dura, con la duración y fuerza suficientes para movilizar la articulación y reproducir el dolor. El riesgo de complicaciones, recurrencia y secuelas, como dolor crónico, aumenta con el retraso en el diagnóstico.13
Aproximadamente, el 50% de los pacientes también pueden tener leucocitosis14, pero las pruebas de laboratorio más confiables son los marcadores de inflamación, incluidos VSG y PCR, y aunque estos marcadores son sensibles, no son específicos para el diagnóstico o el tratamiento.3
En la fisiopatología de la SII, la infección puede ser causada por diseminación hematógena de bacterias desde fuentes distantes del SIA, la circulación subcondral en el lado ilíaco de la articulación, donde terminan las arterias, puede servir como punto de entrada para los microorganismos y extenderse posteriormente a la articulación. Otras vías son a través de infección adyacente, ya sea muscular o intestinal, o por inoculación directa, como en la infiltración.7,11
La TC se puede utilizar para el diagnóstico temprano, porque muestra cambios inflamatorios y una apariencia compatible con la SII. La resonancia magnética es la modalidad de imagen con mayor sensibilidad y especificidad (95% y 100%, respectivamente) y se considera la prueba de referencia confirmación de la SII.11La resonancia magnética combina una buena visualización de la compleja anatomía de la ASI con la capacidad de identificar diversos grados de inflamación y daño articular, como la presencia de derrames articulares y periarticulares, edema de la médula ósea, abscesos musculares, erosiones óseas y secuestro y capsulitis articular o ensanchamiento del espacio articular.
El edema de la médula ósea en la espondiloartritis sacroileítis se produce principalmente en la cadera, mientras que en la SII se produce principalmente en el sacro o se distribuye uniformemente.12En la resonancia magnética con contraste, se observa un aumento unilateral de la captación tres días después del inicio de los síntomas.6,11-13
El diagnóstico microbiológico definitivo puede basarse en hemocultivos, toma de muestras de líquido por punción percutánea guiada por radiografía o TAC o aseo quirúrgico. La aspiración de la ASI es técnicamente difícil, debido a su ubicación.
Bajo la guía radioscópica, se ubica una aguja de calibre suficiente para tomar una muestra de tejido y aspiración de la ASI, para enviarlas a estudio histopatológico, cultivos corrientes, y de tuberculosis.14El S. Aureus es el microorganismo aislado con más frecuencia, entre el 45% y el 83,3% de los casos, según distintos autores, seguido por Staphylococcus coagulasa negativo, Streptococcus del grupo B, Streptococcus pneumoniae, Enterobacterias, como Escherichia coli, y especies de Salmonella, mycobacterium catarrhalis, mycobacterium tuberculosis, haemophilus influenzae, especies de brucella, y pseudomona aeruginosa 2,17, 27, 28). Sin embargo, en el 27% al 40% de los casos, los cultivos son negativos.14
El retraso en el diagnóstico y/o tratamiento inadecuado de la SII puede llevar a consecuencias graves, tales como bacteriemia, shock séptico, osteomielitis o formación de abscesos.13,14
En la actualidad, no existe un consenso sobre la duración del tratamiento antibiótico; la habitual es de 4 a 6 semanas, aunque algunos autores15,16proponen de 4 a 8 semanas, y otros como Matt et al.17reportaron que la ausencia de recaídas clínicas observada en su grupo de 18 pacientes, después de un seguimiento mínimo de 6 meses, sugiere que 6 a 12 semanas de tratamiento antibiótico son suficientes para obtener una cura. La elección del antibiótico se basa en el cultivo y el antibiograma.
La intervención quirúrgica se reserva para la falla del tratamiento conservador y la presencia de complicaciones como abscesos y osteomielitis.18,19
El seguimiento de los pacientes es prolongado; la ausencia de los síntomas es el primer elemento a considerar, además de la normalización de los parámetros inflamatorios. En cuanto al seguimiento imagenológico, es importante tener en cuenta que el edema óseo persiste hasta veinte meses después de completado el tratamiento.20
CONCLUSIÓN
La SII es una enfermedad rara, pero sus complicaciones pueden tener consecuencias graves y funcionales. Un alto índice de sospecha permite un diagnóstico precoz y un rápido inicio del tratamiento.
Aunque algunos diagnósticos requieren el aislamiento de microorganismos en hemocultivos o aspirados articulares, se considera que el cuadro clínico de un episodio agudo, afectación unilateral y dolor intenso en las nalgas, acompañado de fiebre respaldan el diagnóstico de SII.
Los estudios de imágenes, especialmente la resonancia magnética, deben realizarse lo antes posible para ayudar en el diagnóstico temprano. No existe consenso sobre la duración de la terapia con antibióticos, pero lo más apropiado es un ciclo de 4 a 6 semanas.
La información actual se basa en reportes y series de casos, por lo que se necesitan estudios con muestras significativas para determinar el diagnóstico, la duración mínima del tratamiento y el seguimiento necesario para controlar esta condición.











 texto en
texto en