1. INTRODUCCIÓN
La producción de agua potable a partir de fuentes superficiales de agua generalmente incluye una etapa de coagulación-floculación para eliminar la turbidez. Este proceso también se aplica en el tratamiento postsecundario de aguas residuales municipales. La eficiencia en la obtención del nivel deseado de calidad del agua depende, entre otros factores, del coste y disponibilidad de los agentes coagulantes y floculantes. Comúnmente, se utilizan sales metálicas de aluminio y hierro en conjunto con polímeros orgánicos sintéticos como floculantes.
La utilización de coagulantes metálicos y floculantes sintéticos en el tratamiento del agua plantea preocupaciones significativas en términos ambientales y de salud pública. El aluminio residual, derivado de la coagulación y presente en el agua tratada descargada a sistemas acuáticos, puede provocar efectos tóxicos en organismos vivos por acumulación a largo plazo [1]. Es posible que concentraciones anormales de aluminio en el agua provengan de una coagulación deficiente con coagulantes a base de aluminio [2]. La importancia de minimizar la cantidad de aluminio residual en el agua destinada al consumo humano se debe a las implicaciones para la salud, ya que altas concentraciones de aluminio pueden representar un riesgo para la salud humana, incluyendo trastornos cerebrales asociados con la enfermedad de Alzheimer [2]. Aunque los coagulantes de aluminio son efectivos para remover partículas o materia orgánica durante la coagulación, la cantidad de aluminio residual puede ser considerable. Algunos estudios han sugerido que el aluminio residual podría ser una causa significativa de la enfermedad de Alzheimer, lo que destaca la importancia de reducir las concentraciones de aluminio residual para asegurar la calidad del agua [3].
Los floculantes inorgánicos, aunque utilizados en el tratamiento del agua, conllevan inconvenientes significativos debido a su sensibilidad a los cambios de pH y su tendencia a generar grandes volúmenes de lodo. Esta generación excesiva de lodos, rica en iones metálicos, representa un desafío ambiental considerable al infiltrarse en las aguas subterráneas [4]. Adicionalmente, los floculantes orgánicos sintéticos, a pesar de su capacidad para lograr eficiencias aceptables en dosis reducidas, presentan problemas de biodegradabilidad y toxicidad [5]. Estos desafíos se ven agravados por el hecho de que, más allá de su uso predominante en la industria, tales floculantes no son biodegradables, resultando en soluciones tanto ineficaces como costosas [6]. Esta situación subraya la necesidad imperante de explorar alternativas más seguras y sostenibles en la práctica de floculación.
En los últimos años ha habido un interés creciente en el uso de biopolímeros (floculantes) como sustitutos de los floculantes sintéticos. El uso de biopolímeros o floculantes orgánicos que coadyuven al proceso de coagulación - floculación con sales metálicas resulta ventajoso con respecto a la floculación con polímeros sintéticos floculantes por las siguientes razones: los floculantes orgánicos no son tóxicos, por lo que una desviación en la dosificación de estos floculantes orgánicos, no representa riesgos tan elevados en comparación con un floculante sintético, esto posibilita que el proceso de dosificación sea más flexible y menos especializado. Otra ventaja importante es que la adición de floculante en el proceso de coagulación - floculación evita que las dosis requeridas de coagulantes sean mayores, obteniendo las mismas eficiencias de remoción turbiedad usando dosis menores de coagulante, lo que hace que se genere menos aluminio residual y al tener un componente orgánico el lodo generado, posibilita su biodegradabilidad. El factor económico también es relevante ya que los biopolímeros pueden resultar menos costosos en comparación con los floculantes sintéticos debido principalmente a la gran disponibilidad de algunos productos orgánicos con potencial floculante.
2. ANTECEDENTES
Actualmente, entre los diversos materiales base utilizados en las investigaciones de floculantes a base de biopolímeros, los más utilizados son el quitosano, el almidón, la celulosa y la lignina. Con respecto al almidón este es un polímero compuesto por unidades de α-D-glucosa [1], es un tipo de glicano soluble en agua con una fuerte regeneración [2]. En informes recientes, las fuentes naturales de almidón son las siguientes: granos de mango [3], algas verdes [4], patatas [5], tubérculos [6], entre otros.
Con respecto al tratamiento de aguas en donde se usan biopolímeros podemos mencionar el trabajo de Acosta-Bastar y Hernández-Barajas (2021) [7], en su investigación de la dinámica de fluidos computacional del proceso de coagulación-floculación empleando almidón de malanga como floculante para potabilización de agua tienen como objetivo realizar una simulación CFD (Dinámica de Fluidos Computacional) para evaluar el desempeño del almidón extraído de malanga (Colocasia esculenta) como agente floculante en el proceso de coagulación-floculación, donde también se analiza la reducción de la dosis de agente coagulante cuando se emplea este almidón como agente floculante. Inicialmente, los tubérculos de malanga fueron cuidadosamente lavados, pesados, pelados y cortados en cubos. Luego, estos cubos se remojaron en agua fría antes de ser licuados para formar una pasta. Esta pasta fue filtrada, y el líquido resultante se trasladó a un recipiente donde se dejó reposar por tres horas para facilitar la sedimentación. El sobrenadante se eliminó mediante decantación, dejando una pasta blanca que se conservó en refrigeración por 24 horas. Posteriormente, esta pasta se secó en un deshidratador a 40 °C, luego se molió, trituró y se pasó por un tamiz No. 270 de la escala ASTM para obtener un polvo fino de almidón, el cual se almacenó en bolsas herméticas para su conservación. Los resultados de este proceso meticuloso mostraron que el uso de 0.5 mg/L de almidón de malanga permitía reducir la dosis óptima de sulfato de aluminio de 24 mg/L a 12 mg/L, alcanzando eficiencias de remoción de turbidez y color del 93.1% y 94.7%, respectivamente. Este detallado procedimiento no solo evidencia el potencial del almidón de malanga como un floculante eficaz y sostenible, sino que también garantiza la reproducibilidad del estudio, destacando la importancia de una metodología rigurosa en la investigación aplicada al tratamiento de aguas.
Otro estudio relevante es el de Quino-Quispe (2019) [8], cuya investigación tiene como propósito evaluar la posibilidad técnica y ambiental de utilizar coagulantes-floculantes naturales en la remoción de la turbidez de las aguas del Río Jillusaya (Bolivia) a tres diferentes temperaturas (19°C, 22°C y 25°C). Para ello, utiliza floculantes a base de cáscara de papa, pencas de tuna y semillas de durazno. Respecto al almidón obtenido de la cáscara de papa, para su obtención se realizó la desinfección a las cáscaras, se secó la muestra en la estufa a 105°C, para pasar a una moledora manual y morteros, y, por último, ser pasado por un tamiz. Los resultados obtenidos en este estudio muestran que los parámetros físicos mostraron mejores resultados con el sulfato de aluminio a 25°C sin embargo se obtuvo resultados similares con el almidón de cascara de papa a 19°C.
El estudio de Anastasakis K., Kalderis D. y Diamadopoulos E. [9] tiene como objetivo evaluar el comportamiento floculante a partir de mucílagos de Malva sylvestris (malva) e Hibiscus esculentus (okra) para la remoción de turbidez de efluentes sintéticos. El método de obtención de estos floculantes orgánicos fue sencillo e inició con lavado de impurezas, seguido del secado a 110°C durante 6 horas, para pasar a la etapa de trituración, y luego pasar a un molino de micropercusión y finalizar en la tamización. Los resultados obtenidos en este estudio muestran que Hibiscus esculentus es más eficiente que Malva sylvestris en la remoción de turbidez de aguas residuales sintéticas.
3. METODOLOGÍA
3.1. OBTENCIÓN DEL FLOCULANTE
Extracción del almidón
Para la extracción de almidón, se utilizó Solanum tuberosum variedad comercial papa blanca y Solanum tuberosum variedad comercial papa amarilla y también Colocasia esculenta (pituca). Estas 3 especies se utilizaron como materia prima, un kilogramo y medio de cada una de ellas. La materia prima se lavó cuidadosamente para eliminar la suciedad e impurezas adheridas en su superficie. Posteriormente, se pelaron y cortaron en cubos de 2 cm de arista para su posterior trituración. La trituración se realizó con una licuadora comercial, donde se utilizó una proporción de 1:4 de agua (1g/4ml) para las papas y 1:1 para la pituca, y se trituró durante 20 segundos para asegurar su completa desintegración y liberar el almidón contenido. La mezcla triturada se lavó tres veces con la misma agua de remojo utilizando un colador metálico mediano sobre una tela de tocuyo crudo, con excepción de la pituca, que se lavó solo una vez. Esta etapa permitió la separación del almidón de otras partículas finas y residuos más grandes. En el caso de las papas, el almidón se sedimentó durante una hora en vasos precipitados, mientras que el de la pituca se centrifugó por 5 minutos a 8500 revoluciones por minuto y a una temperatura de 25°C con un centrifugador marca Biobase. Tras el tiempo de sedimentación, el líquido sobrante se retiró cuidadosamente y el sedimento, que contenía el almidón, se trasladó a placas Petri de vidrio para su posterior secado en estufa universal UN30 a 45 °C por 24 horas. Finalmente, los almidones una vez secos, se pulverizaron para obtener un polvo homogéneo y fino. Este polvo fue posteriormente tamizado mediante un tamiz microhammer de 100 µm para garantizar la consistencia en la granulometría. Una vez tamizado, el polvo fue almacenado en recipientes de plástico debidamente etiquetados para asegurar su correcta identificación, conservación y posterior uso en experimentos [13] [14].
Preparación del floculante
Se pesaron 10 gramos de almidón utilizando una balanza analítica KERN ABS 220-4N. Paralelamente, se calentaron 250 ml de agua destilada hasta alcanzar una temperatura de 60 °C en una olla. Una vez alcanzada la temperatura deseada, se añadieron los 10 gramos de almidón directamente al agua caliente, agitando constantemente la mezcla para facilitar la disolución del almidón y prevenir la formación de grumos, esta mezcla se calentó hasta la ebullición. Una vez disuelto el almidón por completo, la mezcla fue trasladada a un vaso precipitado para su posterior uso [13] [14].
3.2. EVALUACIÓN DEL FLOCULANTE
Coagulación del agua superficial
El agua superficial se obtuve de una quebrada denominada “El Naranjal” las características iniciales se muestran en la Tabla 1. El agua superficial pasó por un proceso de coagulación, para ello en primer lugar se añadió una solución de potasa caustica concentrada para subir el pH inicial hasta un valor cercano a 9, posteriormente se añadió sulfato de aluminio tipo A hasta bajar el pH de la muestra a un valor cercano a 6.9, valor de pH en donde el coagulante de sulfato de aluminio es más eficiente [10].
Dosificación del floculante
Para evaluar el poder floculante de los almidones, se consideraron las dosis de 0.3 ml y 0.5 ml de la solución de 10 g de almidón en 250 ml de agua destilada para cada almidón (papa amarilla, blanca y pituca) [3] como se muestra en la Tabla 2.
Tabla 2 Evaluación del floculante para diferentes fuentes de almidón y dosis
| Tratamiento | Dosis (ml) | ||
| T0 | Solo coagulante | D0 | 0 |
| T1 | Coagulante + almidón de papa amarilla | D1 | 0.3 |
| D2 | 0.5 | ||
| T2 | Coagulante + almidón de papa blanca | D1 | 0.3 |
| D2 | 0.5 | ||
| T3 | Coagulante + almidón de pituca | D1 | 0.3 |
| D2 | 0.5 | ||
A estos resultados se le aplicó un ANOVA para determinar la influencia de los tratamientos y las dosis y se realizó una prueba de Tukey para identificar los grupos estadísticos para cada parámetro fisicoquímico.
3.3. ANÁLISIS FISICOQUÍMICO
Los parámetros físicoquímicos se evaluaron antes de la coagulación, como se muestra en la Tabla 1, después de la coagulación y después de la adición de los floculantes de almidón.
Lodos
Los lodos se determinaron de la siguiente manera, en un vaso precipitado de un litro se añadió agua superficial coagulada, posteriormente se le añadieron los floculantes de almidón de papa amarilla, blanca y de pituca a las diferentes dosis descritas en la Tabla 2, este litro de agua con floculante se añadió al cono Imhoff y después de 30 minutos se registró el volumen de lodos generados.
Turbiedad
El agua de la parte superior del cono Imhoff, después de los 30 minutos se vertió en un envase de 250 ml, garantizando que sea el agua clarificada la que se vierte a este envase, de esa agua clarificada se tomaron 10 ml y se midió la turbiedad en un el turbidímetro HACH 2100Q.
Demanda Bioquímica de Oxigeno (DBO)
Para determinar la DBO se midió la cantidad de oxígeno disuelto inicial y a los 5 días de incubación con un oxímetro HANNA HI9146. En una botella de 300 ml pintada de negro se añadió 30 ml del agua clarificada, lo que representa un factor de siembra del 10%, la mezcla se guardó en una cámara de incubación a una temperatura de 25°C y a los 5 días se hizo la lectura de DBO5 [11], la fórmula es la siguiente:
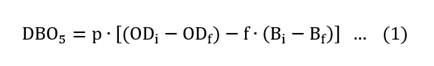
Donde:
DBO5 es la Demanda Bioquímica de Oxígeno a los 5 días.
p es la proporción del volumen total al volumen de la mezcla.
ODi es el oxígeno disuelto inicial de la mezcla de agua residual con agua destilada.
ODf es el oxígeno disuelto final de la mezcla de agua residual con agua destilada.
Bi es la concentración inicial de oxígeno disuelto del agua destilada.
Bf es la concentración final de oxígeno disuelto del agua destilada.
f es el factor de siembra o dilución.
pH, conductividad, sólidos disueltos y potencial redox
Finalmente, para los parámetros de pH, conductividad, sólidos disueltos y potencial redox, se utilizó un equipo multiparámetro HANNA HI991301, el agua en la que se hizo estas mediciones fue del agua clarificada [11]
4. ANÁLISIS DE RESULTADOS
4.1. INFLUENCIA DE LOS TRATAMIENTOS Y DOSIS EN LAS PROPIEDADES FISICOQUÍMICAS DEL AGUA
Influencia en la turbiedad
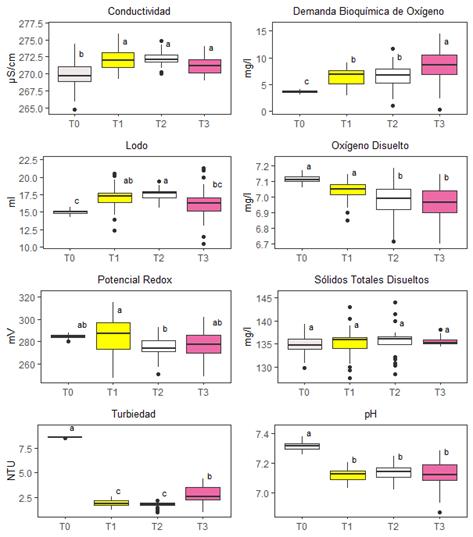
Como se muestra en la Tabla 3 y la Figura 1, en base a los datos presentados, hay diferencias estadísticamente significativas en la reducción de la turbiedad entre los diferentes tratamientos (p-valor < 0.01). El tratamiento en donde solo se añadió coagulante (T0) resultó en una turbiedad de 8.57 ± 0.01 NTU, que es significativamente mayor en comparación con los otros tratamientos. Por otro lado, la combinación de coagulante con almidón de papa amarilla (T1), papa blanca (T2) y pituca (T3) redujeron la turbiedad a 1.92 ± 0.06 NTU, 1.79 ± 0.05 NTU y 2.81 ± 0.18 NTU, respectivamente.
Estas reducciones de turbiedad representan eficiencias mayores al 95% para los tres floculantes analizados, esto también es comparable al estudio [12] sobre el uso de M. oleífera (también llamado Moringa) como floculante orgánico para el tratamiento de agua superficial. Como se puede observar, en la investigación mencionada, se hace uso de un floculante orgánico y los autores muestran una notoria disminución de turbidez, la cual desciende de 126.6 NTU a 4.1 NTU.
Asimismo, en la Tabla 4 y Figura 2, se observa una notoria disminución en la turbidez luego de añadir los floculantes orgánicos. Este resultado es similar al obtenido [13] en su investigación sobre el uso de M. oleífera (también llamado Moringa) como floculante orgánico para el tratamiento de agua superficial. Como se puede observar, en la investigación mencionada, se hace uso de un floculante orgánico y los autores muestran una notoria disminución de turbidez, la cual desciende de 126.6 NTU a 4.1 NTU, lo cual representa una eficiencia del 96.8%.
Tabla 3 Promedio de los parámetros fisicoquímicos ± el error estándar para cada tratamiento, las agrupaciones estadísticas del test de Tukey se muestran como letras entre paréntesis (a), (b), (c) y (d)
| Parámetro | Unidad | T0 | T1 | T2 | T3 | p-valor |
| Conductividad | µS/cm | 269.78 ± 0.70 (b) | 272.08 ± 0.30 (a) | 272.28 ± 0.19 (a) | 271.26 ± 0.25 (a) | <0.01 |
| DBO | mg/l | 3.68 ± 0.08 (c) | 6.43 ± 0.31 (b) | 6.49 ± 0.43 (b) | 8.49 ± 0.65 (a) | <0.01 |
| Lodo | ml | 15.01 ± 0.11 (c) | 17.06 ± 0.31 (ab) | 17.48 ± 0.17 (a) | 16.22 ± 0.42 (bc) | <0.01 |
| Oxígeno Disuelto | mg/l | 7.11 ± 0.01 (a) | 7.04 ± 0.01 (a) | 6.97 ± 0.02 (b) | 6.96 ± 0.02 (b) | <0.01 |
| Potencial Redox | mV | 284.43 ± 0.59 (ab) | 284.63 ± 2.98 (a) | 274.61 ± 1.73 (b) | 277.79 ± 2.41 (ab) | <0.01 |
| STD | mg/l | 134.77 ± 0.69 (a) | 135.04 ± 0.62 (a) | 135.51 ± 0.60 (a) | 135.50 ± 0.17 (a) | 0.767 |
| Turbiedad | NTU | 8.57 ± 0.01 (a) | 1.92 ± 0.06 (c) | 1.79 ± 0.05 (c) | 2.81 ± 0.18 (b) | <0.01 |
| pH | 7.31 ± 0.01 (a) | 7.12 ± 0.01 (b) | 7.14 ± 0.01 (b) | 7.13 ± 0.02 (b) | <0.01 |
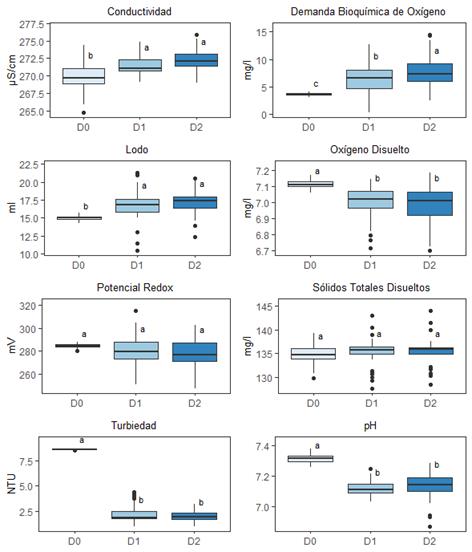
Al considerar las diferentes dosis, en la Tabla 4 y Figura 2, se observaron diferencias significativas en la turbiedad (p-valor < 0.01). La dosis de 0 ml (D0) resultó en una turbiedad de 8.57 ± 0.01 NTU, mientras que las dosis de 0.3 ml (D1) y 0.5 ml (D2) redujeron la turbiedad a 2.34 ± 0.14 NTU y 2.01 ± 0.08 NTU, respectivamente.
De acuerdo a la Tabla 4 y Figura 2, es posible que la falta de diferencia significativa en la remoción de turbiedad entre las dosis D1 y D2 se deba a que se alcanzó un límite en la eficiencia del almidón para reducir la turbiedad. Este fenómeno a menudo se conoce como "efecto de saturación" [15]. En contextos como este, el efecto de saturación ocurre cuando aumentar la dosis de almidón no mejora significativamente la remoción de turbiedad. Esto podría ser porque la cantidad de almidón en la dosis D1 ya es suficiente para interactuar con la mayor parte o todas las partículas que contribuyen a la turbiedad. Si este es el caso, agregar más almidón en la dosis D2 no tendría un impacto significativo porque ya no hay suficientes partículas libres para interactuar con el almidón adicional. Por lo que podríamos decir que la dosis óptima de floculante es D1.
Influencia en Ph
Tabla 4 Promedio de los parámetros fisicoquímicos ± el error estándar para cada dosis, las agrupaciones estadísticas del test de Tukey se muestran con letras entre paréntesis
| Parámetro | Unidad | D0 | D1 | D2 | p-valor |
| Conductividad | µS/cm | 269.78 ± 0.70 (b) | 271.46 ± 0.20 (a) | 272.28 ± 0.21 (a) | <0.01 |
| DBO | mg/l | 3.68 ± 0.08 (c) | 6.41 ± 0.41 (b) | 7.86 ± 0.40 (a) | <0.01 |
| Lodo | ml | 15.01 ± 0.11 (b) | 16.79 ± 0.30 (a) | 17.05 ± 0.24 (a) | <0.01 |
| Oxígeno Disuelto | mg/l | 7.11 ± 0.01 (a) | 6.99 ± 0.01 (b) | 6.98 ± 0.02 (b) | <0.01 |
| Potencial Redox | mV | 284.43 ± 0.59 (a) | 279.78 ± 1.97 (a) | 278.25 ± 2.16 (a) | 0.279 |
| STD | mg/l | 134.77 ± 0.69 (a) | 135.24 ± 0.43 (a) | 135.47 ± 0.40 (a) | 0.697 |
| Turbiedad | NTU | 8.57 ± 0.01 (a) | 2.34 ± 0.14 (b) | 2.01 ± 0.08 (b) | <0.01 |
| pH | 7.31 ± 0.01 (a) | 7.12 ± 0.01 (b) | 7.14 ± 0.01 (b) | <0.01 |
En la Tabla 3 y Figura 1, se observó una disminución significativa en el pH al pasar del tratamiento solo con coagulante (T0: 7.31 ± 0.01) a los tratamientos que incluyen los almidones (T1: 7.12 ± 0.01, T2: 7.14 ± 0.01, T3: 7.13 ± 0.02). Esto podría estar asociado con las propiedades ácidas de los almidones, que podrían haber reducido el pH del agua. Además, las diferencias entre los tres tipos de almidón no fueron significativas (todos pertenecen al mismo grupo estadístico), lo que indica que todos los almidones tuvieron un efecto similar en la reducción del pH. Este efecto podría ser atribuido a la capacidad de los almidones para liberar grupos hidroxilo durante su interacción con el agua, lo cual ha sido reportado en estudios previos [16]
En la Tabla 4 y Figura 2 se observó una disminución en el pH al aumentar la dosis de almidón, con valores de pH de 7.31 ± 0.01 para D0, 7.12 ± 0.01 para D1 y 7.14 ± 0.01 para D2. Esta disminución podría ser explicada por la mayor cantidad de grupos hidroxilo liberados con la mayor dosis de almidón, lo cual ha sido demostrado en estudios previos [17]. Es interesante notar que la diferencia entre D1 y D2 no fue significativa (grupo estadístico b), lo que sugiere que un aumento en la dosis de almidón por encima de cierto umbral no produce una disminución adicional significativa en el pH.
En la evaluación del pH, se observó que luego de aplicar los tratamientos, este parámetro disminuye ligeramente (de 7.31 a 7.13 en promedio). Esta característica no es compartida por (Herrera, 2015) debido a que en su investigación sobre el uso de almidón de papa en el tratamiento de agua residuales el pH aumenta (de 7.34 a 7.56). Tal vez la variación de valores respecto a la investigación de [18] se pueda explicar en que este último utiliza agua residual, mientras que en este estudio se utiliza agua superficial con turbidez. Es decir, las características físicas y químicas del agua en ambos estudios son diferentes y por lo tanto pueden haber influenciado en el aumento o disminución del pH.
Influencia en la Conductividad, Potencial Redox y Sólidos Totales Disueltos
Los valores de conductividad, que mide la capacidad del agua para conducir la electricidad, de acuerdo con la Tabla 3 y Figura 1 variaron significativamente entre los tratamientos (p < 0.01). Los tratamientos con floculantes presentaron valores más altos en comparación con el tratamiento solo con coagulante (T0: 269.78 ± 0.70 µS/cm). Por ejemplo, en el tratamiento T1, la conductividad fue de 272.08 ± 0.30 µS/cm. Este aumento podría ser debido a la adición de los almidones, que poseen grupos funcionales como hidroxilos capaces de ionizarse y aumentar la capacidad conductiva del agua [16].
Asimismo, el resultado de conductividad obtenido es diferente al que obtuvo [7], debido que los mencionados autores en su evaluación de la malanga (o pituca) como floculante registró un descenso de la conductividad (de 273.8 μS/cm a 253.6 μS/cm). Los valores de potencial redox, que es un indicador del equilibrio redox en el agua, de acuerdo con la Tabla 3 y Figura 1 también mostraron variaciones significativas entre los tratamientos (p < 0.01). En el tratamiento T1, el potencial redox fue de 284.63 ± 2.98 mV, y para el T2 fue de 274.61 ± 1.73 mV. Estas diferencias podrían estar relacionadas con la diferente composición de los almidones, que pueden interactuar con el coagulante y afectar la capacidad redox del sistema [19].
Sólidos totales disueltos (STD). De acuerdo con la tabla 3 y figura 1, no hubo diferencias significativas en los valores de STD entre los diferentes tratamientos (p = 0.767), lo que indica que la adición de almidón no afectó la cantidad de sólidos disueltos en el agua. Esto se alinea con la literatura, que muestra que los almidones, al ser biopolímeros, no contribuyen a aumentar la concentración de sólidos disueltos [20]
Los sólidos totales disueltos (STD) en este estudio tuvieron un ligero aumento luego de la administración de los floculantes orgánicos. A partir de lo anterior, [8] comparte esta característica debido a que en su investigación de coagulación-floculación empleando el almidón de la cáscara de papa la concentración de STD también aumenta. Pero este aumento, según su investigación, solo ocurre mientras el almidón de cáscara de papa se encuentre a tempera ambiente (25°C), pero de encontrarse a bajas temperatura (22 °C o 19°C, como analiza en su estudio) los STD aumentan.
En la Tabla 4 y Figura 2 se observa que, al aumentar la dosis de floculante, los valores de conductividad aumentaron (p < 0.01). Por ejemplo, al pasar de la dosis D1 (271.46 ± 0.20 µS/cm) a D2 (272.28 ± 0.21 µS/cm). Este aumento puede ser atribuido a la mayor cantidad de almidón que puede ionizarse y aumentar la conductividad. No se observaron diferencias significativas en los valores de potencial redox con respecto a las dosis (p = 0.279). Esto sugiere que la cantidad de almidón añadido no tiene un efecto considerable en el equilibrio redox del sistema. Similar al caso de los tratamientos, no hubo diferencias significativas en los STD entre las dosis (p = 0.697), lo que indica que la cantidad de almidón añadido no afectó los sólidos disueltos en el agua. Por lo tanto, la conductividad y el potencial redox son afectados tanto por el tipo de almidón como por la dosis, mientras que los STD parecen ser independientes de estos factores. Sin embargo, estos resultados deben ser interpretados en el contexto de otros parámetros como la turbidez y el volumen de lodos, que también mostraron diferencias significativas entre tratamientos y dosis y están relacionados con la eficacia de la floculación. Además, es importante destacar que estos resultados son específicos para el tipo de agua superficial estudiada y podrían variar con diferentes fuentes de agua.
4.2. CARGA ORGÁNICA
Influencia en la DBO
Analizando los datos obtenidos, en la Tabla 3 y Figura 1 se observan diferencias significativas entre los tratamientos (p-valor <0.01). El tratamiento T0 (solo coagulante) tuvo la DBO más baja, con 3.68 ± 0.08 mg/l (c). En contraste, el tratamiento con almidón de pituca (T3) tuvo la DBO más alta, con 8.49 ± 0.65 mg/l (a). Los tratamientos con almidón de papa amarilla y blanca (T1 y T2 respectivamente) mostraron valores intermedios de DBO, ambos con una categorización de (b) en la agrupación de Tukey. Estos resultados indican que la adición de almidón a los tratamientos aumenta la DBO, siendo más pronunciado en el caso del almidón de pituca.
Es posible que este incremento en la DBO con la adición de almidones esté relacionado con la introducción de materia orgánica adicional en el agua durante el proceso de coagulación-floculación. Los almidones pueden proporcionar una fuente de carbono para las bacterias, lo que incrementaría su actividad y, por ende, la DBO [9]. Además, la centrifugación adicional realizada durante la extracción del almidón de pituca podría haber llevado a la retención de más materia orgánica, lo que explica su mayor DBO comparada con los almidones de papa.
En cuanto a las diferentes dosis, en la Tabla 4 y Figura 2 también se observan diferencias significativas en la DBO (p-valor <0.01). La dosis D0 (0 ml, solo coagulante) tuvo la DBO más baja, con 3.68 ± 0.08 mg/l (c), mientras que la dosis D2 (0.5 ml) mostró la DBO más alta, con 7.86 ± 0.40 mg/l (a). La dosis D1 (0.3 ml) presentó un valor intermedio de DBO, con 6.41 ± 0.41 mg/l (b). Estos resultados sugieren que una mayor dosis de floculante conduce a una mayor DBO. Como se mencionó en anteriormente, la carga orgánica expresa en DBO aumenta con coagulante y almidón de papa amarilla (T1), papa blanca (T2) y pituca (T3). Particularmente, T1, T2 y T3 aumentan aproximadamente en un 50%, 50% y más del 100% respectivamente, esta característica lo comparte la investigación realizada por Anastasakis et al, (2009) [9] . Éstos últimos, centran su atención en la floculación mediante el uso del mucílago de malva, determinando que la carga orgánica en términos de carbono orgánico total (COD) aumentó en un 80% debido a la presencia de sustancias orgánicas de estos floculantes.
4.3. GENERACIÓN DE LODOS
Influencia en la generación de lodos
En la Tabla 3 y Figura 1, observando las medias y los errores estándar, el tratamiento T0 (solo coagulante) generó la menor cantidad de lodos, con un valor de 15.01 ± 0.11 ml. Por otro lado, el tratamiento T2 (Coagulante + almidón de papa blanca) resultó en la mayor generación de lodos, con un valor de 17.48 ± 0.17 ml. Estas diferencias son estadísticamente significativas, ya que el p-valor es menor a 0.01. Cuando se añadió el almidón de papa amarilla (T1), se observó una producción de lodos de 17.06 ± 0.31 ml, mientras que la adición de almidón de pituca (T3) generó 16.22 ± 0.42 ml de lodos. Las letras de la agrupación de Tukey indican que estos dos tratamientos no se diferencian significativamente entre sí, pero ambos son diferentes del tratamiento T0 y T2.
En cuanto a las dosis, la Tabla 4 y Figura 2 muestran que la generación de lodos aumentó de manera significativa con la dosis. A una dosis de 0 ml (D0), la producción de lodos fue de 15.01 ± 0.11 ml. Esta producción aumentó a 16.79 ± 0.30 ml cuando se utilizó una dosis de 0.3 ml (D1) y llegó a 17.05 ± 0.24 ml a una dosis de 0.5 ml (D2). Estas diferencias son significativas, con un p-valor menor a 0.01. Los cambios en la producción de lodos pueden estar directamente relacionados con la turbidez medida. La turbidez disminuyó significativamente con la adición de floculante y con el aumento de la dosis (p-valor <0.01 en ambos casos), lo que sugiere que los sólidos suspendidos se estaban aglomerando y sedimentando como lodo. Por ejemplo, el tratamiento T2 redujo la turbidez a 1.79 ± 0.05 NTU y generó 17.48 ± 0.17 ml de lodo, mientras que el tratamiento T0 resultó en una turbidez más alta de 8.57 ± 0.01 NTU y generó solo 15.01 ± 0.11 ml de lodo.
CONCLUSIONES
De acuerdo con los resultados obtenidos, se puede concluir que la adición de floculantes orgánicos, específicamente almidones de papa amarilla, papa blanca y pituca, mejora significativamente la eficiencia de remoción de turbiedad en el tratamiento de agua, alcanzando impresionantes eficiencias de remoción de turbiedad superiores al 95%. Este hallazgo es particularmente notable dado que supera la eficacia del tratamiento solo con coagulante, que resultó en una turbidez significativamente mayor de 8.57 NTU.
Sin embargo, esta mejora en la remoción de turbiedad viene con un aumento significativo en la demanda bioquímica de oxígeno (DBO), con el tratamiento con almidón de pituca alcanzando la DBO más alta de 8.49 mg/l, lo que indica un aumento en la carga orgánica del agua. Este aumento en la DBO puede estar relacionado con la introducción de materia orgánica adicional en el agua durante el proceso de coagulación-floculación.
Además, la adición de floculantes orgánicos también resultó en una mayor generación de lodos. El tratamiento con almidón de papa blanca generó la mayor cantidad de lodos, con un valor de 17.48 ml, lo cual es significativamente mayor que el tratamiento solo con coagulante, que generó 15.01 ml de lodos. Este aumento en la generación de lodos puede estar directamente relacionado con la reducción de la turbidez, ya que los sólidos suspendidos se aglomeran y sedimentan como lodo.
Finalmente, es importante destacar que la eficacia de los almidones como floculantes parece tener un límite. Aumentar la dosis de almidón más allá de 0.3 ml no mejoró significativamente la remoción de turbidez, un fenómeno conocido como "efecto de saturación". Este hallazgo sugiere que existe una "dosis óptima" de almidón que maximiza la eficacia de la reducción de la turbidez, más allá de la cual no se obtienen beneficios adicionales.