Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista Peruana de Biología
On-line version ISSN 1727-9933
Rev. peru biol. vol.19 no.2 Lima Aug. 2012
TRABAJOS ORIGINALES
Patógenos introducidos al Perú en post larvas de Litopenaeus vannamei importadas
Pathogen introduced to Peru by trade in postlarvae of Litopenaeus vannamei
Mervin Guevara y Rubén Alfaro
Laboratorio de Sanidad Acuícola, Instituto del Mar del Perú (IMARPE), Sede Tumbes. Panamericana Norte Km. 1249, Zorritos, Tumbes, Perú.
E-mail Mervin Guevara: mguevara@imarpe.gob.pe
E-mail Rubén Alfaro: ralfaro@imarpe.gob.pe
Resumen
El comercio internacional de animales acuáticos es uno de los factores más importantes en la introducción involuntaria de patógenos a una región libre de estos. Los patógenos introducidos han sido causa de enormes pérdidas económicas en organismos bajo cultivo y daños ecológicos en poblaciones silvestres. En este trabajo, utilizando la técnica de la PCR se analizaron postlarvas de Litopenaeus vannamei importadas desde Ecuador para ser utilizada en los cultivos de langostinos en Tumbes. La finalidad fue detectar patógenos como el virus de la mancha blanca (WSV), virus de la cabeza amarilla (YHV), virus de la necrosis hipodérmica y hematopoyética infecciosa (IHHNV), Baculovirus penaei (BP), virus del síndrome de Taura (TSV) y la bacteria de la hepatopancreatitis necrotizante (NHPB). Se analizaron 177 muestras de postlarvas en el año 2009 y 274 en el 2010. En el año 2009 se encontraron cuatro patógenos infecciosos en las postlarvas analizadas, siendo más frecuente el IHHNV (9,60%). En el año 2010 la frecuencia de aparición de postlarvas infectadas con IHHNV fue mayor (16,79%). Tanto en el 2009 como en el 2010 se encontraron postlarvas positivas a NHPB, BP y TSV.
Palabras Clave: Frecuencia, Litopenaeus vannamei, patógenos, postlarva.
Abstract
International trade of aquatic animals is the most important source for pathogens introduction in new areas, beginning cause of huge economic losses in growing animals and ecological damage. In this paper, we analyze Litopenaeus vannamei postlarvae imported for shrimp farming companies of Tumbes from Ecuador, in order to detect pathogens such as the white spot virus (WSV), yellow head virus (YHV), infectious hypodermal and haematopoietic necrosis virus (IHHNV), Baculovirus penaei (BP), Taura syndrome virus (TSV) and necrotizing hepatopancreatitis bacterium (NHPB). For this purpose, 177 samples of postlarvae in 2009 and 274 in 2010 from different larviculture laboratories of Ecuador were processed by the technique of PCR. In 2009, four infectious pathogens were present in postlarvae. In 2010 the frequency of occurrence of IHHNV –infected postlarvae was higher (16.79%). Both in 2009 and 2010 were found positive postlarvae NHPB, BP and TSV.
Keywords: Frequency, Litopenaeus vannamei, pathogens, postlarvae.
Introducción
De acuerdo con la Organización Mundial de Sanidad Animal, (OIE), durante la década pasada, la producción mundial de especies acuícolas se ha visto afectada por numerosas enfermedades infecciosas, las que han impactado severamente el desarrollo y sustentabilidad de la acuicultura convirtiéndose en una restricción primaria para su desarrollo (OIE 2010).
La causa principal de brotes de enfermedades y epidemias, está dada por la transferencia de agentes infecciosos vía transporte de organismos vivos (OIE 2009, Lightner & Redman 1994, Lightner 1996, Tang et al. 2003, Briggs et al. 2005). La actual tendencia del libre comercio y el deseo de los países de generar nuevas alternativas para el desarrollo social y económico son factores que pueden incrementar el riesgo sanitario y que de no ser considerados oportunamente pueden hacer fracasar la acuicultura.
Entre los factores que deben tomarse en cuenta para el control del riesgo se incluyen el estado sanitario de las especies que deseamos introducir, los problemas sanitarios que las aquejan, el riesgo de transferencia en la zona donde las vamos a introducir y los problemas sanitarios de la zona receptora que pueden afectar a la nueva especie (Frelier et al. 1993, Lotz et al. 2002 Nunan et al. 2003).
Algunos países líderes en el cultivo de especies acuáticas, han desarrollado políticas relativamente precisas para evitar la transmisión de enfermedades, estos lineamientos se han agrupado en el Código Sanitario para los Animales Acuáticos y en el Manual de Pruebas de Diagnóstico para los Animales Acuáticos de la OIE. De la misma manera, países productores a menor escala, han desarrollado lineamientos sanitarios propios para evitar la transferencia de enfermedades a su territorio. Sin embargo, pese al arduo trabajo, estos lineamientos no han sido eficaces en la prevención de la diseminación de patógenos virales exóticos (Jiménez et al. 1997, Nielsen et al. 2005, Briggs et al. 2005).
En América Latina la realidad es muy similar, porque aun cuando se cuenta con lineamientos y normas sanitarias que regulan la entrada de especies acuícolas, en varios casos se ha dado la diseminación de muchos patógenos exóticos. (Wyban et al. 2004, Lightner 2006, Senapin et al. 2007, Aguado et al. 2008).
En ciertos patógenos, como el virus de la Mancha blanca (WSV, white spot virus) y la Necrosis hipodérmica y hematopoyética infecciosa (IHHNV, Infectious hypodermal and haematopoietic necrosis virus) el mecanismo de transmisión transovum, es una importante fuente de contaminación de huevos (Lo et al. 1997, OIE 2010). Así mismo, existe la posibilidad de transmisión vertical del virus del síndrome de Taura (TSV, Taura syndrome virus) y virus de la mionecrosis infecciosa (IMNV, infectious mionecrosis virus) que no han sido confirmadas experimentalmente (Brock 1997, Lightner 1996, OIE 2009). En el caso de contagio por Baculovirus (BP, Baculovirus penaei) de los reproductores a su progenie, se puede producir mediante contaminación fecal de huevecillos al eclosionar, por tanto sin las medidas profilácticas adecuadas en la larvicultura, inevitablemente las larvas cultivadas, serán infectadas. (Overstreet et al. 1998). Así mismo, está ampliamente documentado que el agua es un vehículo de transmisión horizontal de agentes patógenos a los diferentes estadios larvarios de peneidos (OIE 2009).
Existen muchos ejemplos de propagación de enfermedades de animales acuáticos en el mundo, entre los casos más relevantes, se puede reportar como ejemplo lo ocurrido con el TSV; este patógeno se identificó inicialmente en Ecuador, (país en el cual causó gran mortalidad a los langostinos cultivados) se dispersó rápidamente a Perú, Colombia, países de Centroamérica, Estados Unidos, Hawai, Brasil y países de Asia, probablemente a través de la transferencia regional e internacional de post larvas y reproductores de L. vannamei infectados con el virus (Lightner 1996, Tu et al. 1999, Briggs et al. 2005, OIE 2009).
Otro caso es el ocurrido con el IHHNV; este patógeno tuvo su origen en Asia y se sospecha que su ingreso al continente americano fue producto de la importación de Penaeus monodon a Hawai y posteriormente diseminado a otros países de Latinoamérica por el movimiento transfronterizo sin certificación sanitaria adecuada (Tang et al. 2003). La particularidad de este virus de producir infecciones latentes en sus hospederos, le permite una mayor transmisión de la infección a su progenie y a otras poblaciones susceptibles (Madhavi et al. 2002).
Con la aparición del WSV en Perú en el año 1999, el sector gubernamental mediante Decreto Supremo Nº 009-99-PE, decide suspender por un periodo de 180 días la importación de nauplios, post larvas y reproductores de langostino Litopenaeus sp. Posteriormente esta suspensión fue levantada bajo la condición de llevar a cabo un estricto cumplimiento de la certificación sanitaria de organismos acuáticos de importación, para asegurar que las larvas importadas ingresaban al país libre de YHV y WSV.
El Laboratorio de Sanidad Acuícola del IMARPE-Sede Tumbes mediante Resolución Ministerial Nº 393-2001-PE es el órgano facultado para realizar los análisis que certifiquen el estatus sanitario de post larvas y reproductores de los crustáceos que ingresan al territorio peruano. Con este certificado, PRODUCE a través de la oficina del SANIPES levanta un acta de conformidad con el que se da inicio a la importación. Este trámite se realiza con el fin de evitar el ingreso de nuevos patógenos como YHV o incrementar la incidencia de infecciones endémicas por WSV en los centros de cultivo de langostinos o en los ambientes naturales, que pongan en riesgo la producción de langostinos y el estatus poblacional de las diferentes especies de peneidos silvestres presentes en el Perú .
En el presente trabajo informamos sobre la frecuencia de los patógenos IHHNV, NHPB, BP, TSV, YHV y WSV en las post larvas de Litopenaeus vannamei importados al Perú en los años 2009 y 2010.
Material y métodos
Área de estudio.- Se analizaron post larvas importadas de L. vannamei, procedentes de laboratorios de maduración de Ecuador, ubicados en los poblados de Mar Bravo, Punta Carnero, Ayangue y San Pablo, de la provincia de Santa Elena.
Muestras de post larvas.- Entre febrero y diciembre del año 2009 se colectaron al azar 177 muestras y entre enero y diciembre del año 2010, 274.
Las post larvas rutinariamente son remitidas al Laboratorio de Sanidad Acuícola del IMARPE - Sede Tumbes, para el análisis obligatorio de WSV e YHV (agentes patógenos de notificación obligatoria, según la OIE) con la finalidad de obtener el certificado que indique que están libres de tales patógenos y poder ingresarlas al país.
Extracción de ácidos nucleicos.- Las extracciones de ADN se realizaron individualmente, utilizando el método estándar CTAB-DTAB (Gustincich et al. 1999, modificado para tejidos de langostinos). Se pesó 25 mg de macerado de post larvas, en un microtubo de 1,5 mL y se le agregó 600 µL de solución DTAB (dodeciltrimetilamonio bromuro 8%, NaCl 1,5 M, Tris HCl 100 mM pH 8,8 y EDTA 50 mM). Con la ayuda de un micromacerador de plástico se homogeneizó el tejido, para luego incubarlo a 75 °C por 5 minutos. Después de la incubación, se agregó 0,7 mL de cloroformo HPLC, se mezcló con un agitador automático y se centrifugó en una microcentrífuga a 12000 rpm por 5 minuto. El sobrenadante (250 µL) fue transferido a un microtubo de 1,5 mL que contenía 100 µL de solución CTAB (5% cetiltrimetilamonio bromuro, 0,4 M NaCl) y 900 µL de agua destilada autoclavada, se mezcló, incubó a 75 °C por 5 minutos y centrifugó a 12000 rpm por 10 minutos; el sobrenadante fue descartado y el pellet resuspendido en 150 µL de solución disolvente (NaCl 1,2 M) se incubó a 75 °C por 5 minutos y centrifugó a 12000 rpm por 5 minutos. La solución fue transferida a un nuevo microtubo con 300 µL de etanol al 95%, se mezcló y centrifugó nuevamente a 12000 rpm por 5 minutos, el pellet fue lavado con etanol al 75%, secado por 10 minutos y resuspendido con buffer TE (10 mM Tris-HCl, 1 mM EDTA pH 8).
Las extracciones de ARN se realizaron con un kit de extracción de ARN de IQ 2000® siguiendo las indicaciones del fabricante.
Cebadores específicos para el análisis por PCR.- Los cebadores usados para la realización de la PCR fueron específicos para cada patógeno evaluado y están recomendados tanto en el manual de la OIE como en artículos científicos actuales (Tabla 1)

Análisis por PCR.- El análisis de las muestras de post larvas fue realizado mediante la técnica de la PCR simple, para el descarte de los agentes patógenos causantes de las enfermedades "Hepatopancreatitis necrotizante" (NHP), "Necrosis hipodérmica y hematopoyética infecciosa" (IHHN), "Baculovirosis tetraédrica" y "Síndrome de Taura" (TS), además de la enfermedad de las manchas blancas (WSD) y cabeza amarilla (YHD). Los productos de amplificación para cada patógeno están detallados en la Tabla 1.
Para la detección de NHPB, las reacciones se realizaron en mezclas de 20 µL, que contenían 2,0 µL de buffer Taq 10X (100 mM Tris-HCl pH 8,8, 500 mM KCl y 0,8% de Nonidet P-40), 1,5 mM de MgCl2, 0,125 mM de cada dNTPs, 1,25 U de Taq ADN polimerasa (Fermentas), 10 pmol de cada cebador y 2 µL de ADN extraído. El perfil de la PCR se realizó en un termociclador (9800 Fast Thermal Cycler, Applied Biosystems, USA) y constó de 35 ciclos de 94 °C por 30 s, 58 °C por 30 s, 72 °C por 1 minuto y una extensión final a 72 °C por 5 minutos.
Para la detección de IHHNV, se utilizó un volumen de reacción final de 20 μL, constituida por 2,0 μL de buffer Taq 10X, 2,0 mM de MgCl2, 0,2 mM de cada dNTPs, 1,25 U de Taq ADN polimerasa , 150 ng de cada cebador y 2 μL de ADN extraído. El programa de la PCR (termociclador 9800 Fast Thermal Cycler, Applied Biosystems, USA) constó de un ciclo de 94 °C por 5 minuto, 35 ciclos de 95 °C por 30 s, 55 °C por 30 s, 72 °C por 1 minuto y una extensión final a 72 °C por 5 minuto.
Para la detección de BP el análisis fue realizado en un volumen de reacción de 20 μL, constituido por 2 μL de buffer Taq 10X, 1,5 mM de MgCl2, 0,2 mM de cada dNTPs, 1 U de Taq ADN polimerasa, 5 pmol de cada cebador y 2 μL de ADN extraído. La PCR (termociclador 9800 Fast Thermal Cycler, Applied Biosystems, USA) se realizó con un ciclo de 95 °C por 5 min, 30 ciclos de 94 °C por 30 s, 58 °C por 45 s, 72 °C por 45 s y una extensión final a 72 °C por 5 min.
Se utilizó nested PCR para detección de WSV, con los cebadores específicos para la primera y segunda reacción (Tabla 1). El volumen final de cada reacción fue 50 μL, constituido por 5 μL de buffer Taq 10X, 1,5 mM de MgCl2, 0,2 mM de cada dNTPs, 1 U de Taq ADN polimerasa 10 pmol de cada cebador y 1 μL de ADN extraído. La PCR fue realizada en un termociclador (Thermolyne Amplitron II, USA) y consta un ciclo de 94 °C por 5 min, seguido de 30 ciclos de 94 °C por 30 segundos, 52 °C por 30 segundos y 72 °C por 45 segundos y una extensión final a 72 °C por 5 minutos.
En el caso de la detección de TSV, se usó el kit de detección Concepto Azul, siguiendo las indicaciones del fabricante.
Los productos de amplificación fueron verificados en geles de agarosa al 1%, teñido con bromuro de etidio (0,5 g/mL) y por electroforesis en buffer TAE 1X (Tabla 1).
Análisis de datos.- Los parámetros que se determinaron basados en la información obtenida fueron:
-
- Frecuencia anual de muestras positivas por agente patógeno.
-
- Frecuencia mensual de muestras positivas por agente patógeno.
Resultados
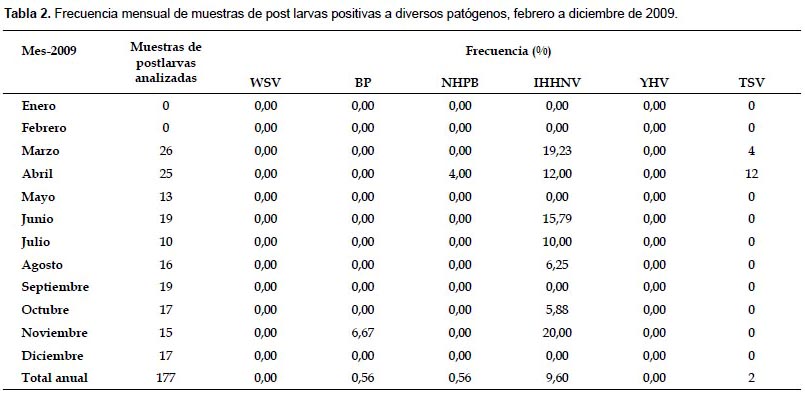
Frecuencia anual de muestras positivas a diferentes agentes infecciosos.- En el año 2009, se obtuvieron muestras positivas al IHHNV con una frecuencia de 9,60%, para los patógenos BP y NHPB fue de 0,56% y del 2% para el TSV. Las mayores frecuencias de detección del IHHNV se produjeron dentro del periodo febrero-marzo (19,2%) y en el mes de diciembre (17,6%). Los patógenos BP y NHPB se detectaron en abril y noviembre respectivamente (Tabla 2).
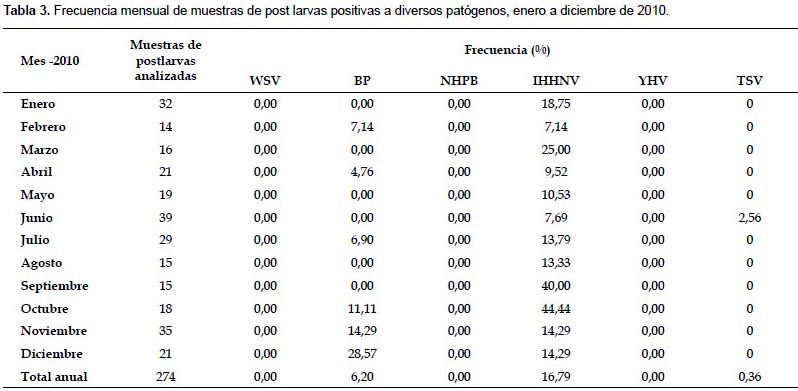
En el 2010, se obtuvo muestras positivas al IHHNV y BP, siendo su frecuencia de detección 16,79% y 6,20% respectivamente y de 0,36% para el TSV (Fig. 1). Cabe señalar que se encontraron muestras de post larvas positivas a IHHNV durante todo el año, siendo el valor más alto encontrado de 44,4% correspondiente al mes de octubre (Tabla 3).
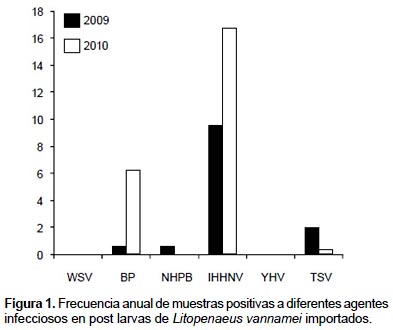
Todas las muestras de post larvas de importación analizadas en este periodo (2009 – 2010) resultaron negativas a WSV e YHV.
Discusión
El Perú cuenta con normativa (Decreto Supremo Nº 0202001-PE) destinada a impedir la entrada de organismos acuáticos (crustáceos, poliquetos u otros invertebrados) positivos a YHV y WSV, exigiéndose el certificado sanitario de importación extendido por laboratorios autorizados, a pesar de esto existe la introducción ilegal de post larvas por parte de empresas informales. En los años 2007 y 2009 la DIREPRO (Dirección Regional de la Producción) detectó 2400 y 4000 millares de post larvas respectivamente, ingresadas de forma ilegal provenientes de Ecuador; además la Aduana de Tumbes informó sobre 3000 millares en el 2007, 2000 millares en el 2008, y 1000 millares de post larvas en el 2009 que iban a ser ingresadas a territorio peruano y que al no contar con las certificaciones sanitarias fueron incineradas.
El Laboratorio de Sanidad Acuícola del IMARPE está facultado (Resolución Ministerial Nº 393-2001-PE), para certificar, en las post larvas de importación, la ausencia de los patógenos causantes de la enfermedad de la cabeza amarilla (YHD) y de la enfermedad de las manchas blancas (WSD). Sin embargo las empresas informales burlan estas medidas sanitarias obligatorias poniendo en riesgo a toda la actividad langostinera de Tumbes.
Según nuestros resultados, se encontró que para el 2010 la frecuencia de muestras positivas al IHHNV y BP se incremento con respecto al año anterior. Teniendo en cuenta que el éxito de las producciones de langostino está condicionado a disponer de una fuente confiable de post larvas y preferentemente producidas en laboratorios locales (FAO 2004), son preocupantes estos resultados que indicarían una amenaza a la industria del cultivo de L. vannamei en Perú.
Al parecer, las empresas langostineras no prestan la importancia debida al estado sanitario de las post larvas que importan, debido a factores como el costo adicional de los servicios de diagnóstico, el desconocimiento de las normas vigentes o porque están seguros que ciertos patógenos en las post larvas no involucran mayores pérdidas en la producción final del cultivo. Tal es el caso del IHHNV, agente etiológico que no es mortal para L. vannamei y que causa retardo en el crecimiento y ocasionalmente deformidad externa (rostrum o segmentos abdominales). La infección experimental con IHHNV reduce significativamente las mortalidades de los langostinos tras la exposición con WSV, a esto se le denomina "interferencia viral". Según este concepto la presencia de dos o más virus en un hospedero causará la inhibición de la replicación de uno de ellos (Tang et al. 2003, Namikoshi et al. 2004, Witteeveldt et al. 2004, Bright et al. 2005, Melena et al. 2006); de esta manera los langostinos positivos al IHHNV no mueren cuando son atacados por el WSV, debido a la protección que brinda el IHHNV frente a la infección por WSV.
Sin embargo, esto no debe justificar su presencia en post larvas de importación, porque el IHNNV presenta una alta tasa evolutiva y una amplia diversidad genética en las cepas aisladas (Robles et al. 2010), existiendo el riesgo latente de aparición de cepas más virulentas, que pueden poner en peligro a los cultivos de L. vannamei y las poblaciones silvestres de L. stylirostriss, especie para la cual el IHHNV es mortal.
Frente a los riesgos mencionados es necesario contar con estrategias que permitan evitar el ingreso al Perú de nuevas cepas virulentas de patógenos, aplicándose recomendaciones precisas, como las especificadas por la FAO y la OIE, entre ellas desarrollar normativas estrictas; sistemas de supervisión y las capacidades para la aplicación de control y registro de las importaciones de organismos vivos y evitar así el contrabando; obligar al registro de empresas langostineras informales; organizar talleres de manejo sanitario en enfermedades para difundir información; crear un directorio de los laboratorios que ofrecen organismos certificados libres de enfermedades; desarrollar y aplicar las buenas prácticas para el manejo en langostineras; establecer laboratorios de referencia nacional de patologías para los procesos de intercalibración y asegurar la calidad de los diagnósticos; establecer programas de reproducción de ciclo cerrado para producir semilla SPF (libres de patógenos específicos) y SPR (resistentes a patógenos específicos); y financiar programas de investigación en estos temas.
Literatura citada
Aguado García N, Boada M, de Donato M. 2008. Detección del virus del síndrome de Taura (TSV)en Litopenaeus vannamei (Boone) del occidente de Venezuela. Revista científica, FCV-LUZ. XVIII, (2): 134 – 141 pp.
Briggs M, Funge-Smith S, Subasinghe R, Phillips M. 2005. Introducciones y movimiento de dos especies de camarones en Asia y el Pacífico. FAO Documento Técnico de Pesca. 476: 86 pp.
Brock J. 1997. Special topic review: Taura syndrome, a disease important to shrimp farms in the Americas. World J. Microbiol & Technol. 13: 415-418 pp.FAO 2004. Manejo sanitario y mantenimiento de la bioseguridad de los laboratorios de post larvas de camarón blanco (Penaeus vannamei) en América Latina. Documento Técnico de Pesca. No. 450. Roma, FAO. 2004. 66p.
Gustincich S, Manfiolett G, Del Sal G, Schneider C, Carnici P. 1991. A fast method for high quality genomic DNA extraction from whole human blood. Biotechniques. 11 (3): 298-302.
Jiménez R, Barniol R, Machuca M. 1997. An epizootic of an intra cellular bacterium in cultured penaeid shrimp (Crustacea, Decapoda) in the Gulf of Guayaquil, Ecuador. In: Flegel T, MacRae I. Diseases in Asian Aquaculture III. 305-311 pp.
Lightner D, Redman R. 1994. An epizootic of Necrotizing Hepatopancreatitis in cultured penaeid shrimp (Crustacea: De capoda) in northwestern Peru. Aquaculture 122:9-18 pp.
Lightner D. 1996. A handbook of shrimp pathology and diagnostic procedures for diseases of cultured penaeid shrimp. World Aquaculture Society. Baton Rouge. Louisiana. USA. 304 pp.
Lightner D.V. 2006. The penaeid shrimp viral pandemics due to IHHNV, WSSV, STV and YHV: History in the Americas and current status. 1995. Proc. Special Session on Shrimp Farming. Aquaculture 95 San Diego. World Aquatic Soc. On Line: Http://www.Lib.noaa/gov/japan/aquaculture/proceedings/reporte32/lightner/corrected.pdf.
Lo C, Ho C, Chen C, Liu K, Chiu Y, Yeh P, Peng S, Hsu H, Liu H, Chang C, Su M, Wang C, Kou G. 1997. Detection and tissue tropism of white spot syndrome baculovirus (WSBV) in captured brooders of Penaeus monodon with a special emphasis on reproductive organs. Diseases of Aquatic Organisms. 30(1): 53-72 pp.
Lotz J, Soto M. 2002. Model of White Spot Syndrome virus (WSSV) epidemics in Litopenaeus vannamei. Dis Aquat Org 50:199–209 pp.
Madhavi R, Janakiram P, Jayasree L, Murthy P. 2002. Occurrence of concurrent infections with multiple viruses in Penaeus monodon from culture ponds of north coastal Andhra Pradesh. Current Science. 82 (11): 1397-1400 pp.
Melena J. 2005. Estudio de la co-infección viral IHHNV-WSSV en el camarón blanco L. vannamei. Boletín Informativo Nº 130. Disponible en http://www.cenaim.espol.edu.ec/publicaciones/quincenal/bquinc130.pdf.
Melena J, Bayot B, Betancourt I,Amano Y, Panchana F,Alday V, Calderón J, Stern S, Roch Ph y Bonami JR. 2006. Pre-exposure to infectious hypodermal and haematopoietic necrosis virus or to inactivated white spot syndrome virus (WSSV) confers protection against WSSV in Penaeu vannamei (Boone) postlarvae. Journal of Fish Diseases. 29: 589-600.
Morales V, Cuéllar J. 2008. Guía técnica - Patología e inmunología de camarones peneidos. Programa CYTEC Red II-D Vannamei. Panamá. 270 pp.
Namikoshi A, Wu J, Yamashita T, Nishizawa T, Nishioka T,Arimoto M y Muroga K. 2004. Vaccination trials with Penaeus japonicus to induce resistance to white spot syndrome virus. Aquaculture 229: 25-35.
Nielsen L, Sang-oum W, Cheevadhanarak S, Flegel T. 2005. Taura syndrome virus (TSV) in Thailand and its relationship to TSV in China and the Americas. Dis Aquat Org. 63: 101-106 pp.
Nunan L, Noble B, Le Groumellec M, and Lightner D. 2003. Experimental infection of Penaeus vannamei by a rickettsia-like bacterium (RLB) originating from Penaeus monodon. Diseases of Aquatic Organisms 54:43–48 pp.
Oie. 2009. Manual de pruebas de diagnóstico para los animales acuáticos. Disponible en http://www.oie.int/esp/normes/fmanual/e_SUMMRY.HTM
Oie. 2010. Manual de pruebas de diagnóstico para los animales acuáticos. Disponible en http://www.oie.int/esp/normes/fmanual/e_SUMMRY.HTM
Overstreet R, Stuck K, Krol R, Hawkins W. 1988. Experimental infections with Baculovirus penaei in the white shrimp Penaeus vannamei as a bioassay. J. World Aquaculture Soc. 19: 175-187 pp.
Robles-Sikisaka R, Bohonak AJ, McClenaghan LR Jr, Dhar AK (2010) Genetic Signature of Rapid IHHNV (Infectious Hypodermal and Hematopoietic Necrosis Virus) expansion in wild Penaeus shrimp populations. PLoS ONE 5(7): e11799. doi:10.1371/journal.pone.0011799
Senapin S, Phewsaiya K, Briggs M, Flegel T. 2007. Outbreaks of infectious myonecrosis virus (IMNV) in Indonesia confirmed by genome sequencing and use of an alternative RT-PCR detection method. Aquaculture. 266: 32-38.
Tang K, Poulos B, Wang J, Redman R, Hsiu-Hui S, Lightner D. 2003. Geographic variations among infectious hypodermal and hematopoietic necrosis virus (IHHNV) isolates and characteristics of their infection. DisAquat Org. 53: 91-99 pp.
Tang K, Durand S, White B, Redman R, Mohney L, y Lightner D. 2003 Induced resistance to white spot syndrome virus infection in Penaeus stylirostris through pre-infection with infectious hypodermal and hematopoietic necrosis vírus – a preliminar study. Aquaculture 216: 19-29.
Tu C, Huang H, Chuang S, Hsu J, Kuo S, Li N, Hsu T, Li M, Lin S. 1999. Taura syndrome in Pacific white shrimp Penaeus vannamei cultured in Taiwan. Dis Aquat Org. 38:159-161 pp.
Witterveldt J, Vlak J, van Hulten M. 2004. Protection of Penaeus monodon against white spot syndrome virus using a WSSV subunit vaccine. Fish and Shellfish Immunology 16: 571-576.
Wyban J, White B, Lightner D. 2004. TSV Challenges Advance selective breeding in Pacific White Shrimp. Global Aquaculture Advocate.
Presentado: 23/01/2012
Aceptado: 04/08/2012
Publicado online: 10/11/2012













