Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista Peruana de Biología
On-line version ISSN 1727-9933
Rev. peru biol. vol.24 no.3 Lima Sept./Dec. 2017
http://dx.doi.org/10.15381/rpb.v24i3.13902
TRABAJOS ORIGINALES
Presencia de genes rhlAB, rhlR y rhlC en Pseudomonas aeruginosa nativas sobreproductoras de ramnolípidos
Detection of rhlAB, rhlR and rhlR genes in Pseudomonas aeruginosa natives overproducers of ramnolipids
Roger A. Palomino 1, Guillermo Romero 1, Abigail González-Valdez 2, Gloria Soberón-Chávez 2, Susana M. Gutiérrez 1* y Fernando A. Merino 1
1 Universidad Nacional Mayor de San Marcos. Facultad de Ciencias Biológicas, Laboratorio de Microbiología y Biotecnología Microbiana. Av. Venezuela cdra. 34, Ciudad Universitaria, puerta 1, Lima, Perú.
2 Universidad Nacional Autónoma de México. Instituto de Investigaciones Biomédicas, Departamento de Biología Molecular y Biotecnología. Circuito Mario de la Cueva s/n, Coyoacán, Ciudad Universitaria, Apartado Postal 70228, 04510 Ciudad de México, CDMX, México.
*Autor para correspondencia
Email Roger Palomino: micro_roger@hotmail.com
Email Guillermo Romero: romerogguillermo@gmail.com
Email Abigail González: abigaila@biomedicas.unam.mx
Email Gloria Soberon-Chávez: gloria@biomedicas.unam.mex
Email Fernando Merino: fmerinor@unmsm.edu.pe
Email Susana Gutiérrez: sgutierrezm@unmsm.edu.pe
Resumen
Se realizó la caracterización molecular de los genes asociados a la producción de ramnolípidos (RL), en 61 cepas bacterianas de la colección del Laboratorio de Microbiología y Biotecnología Microbiana (LAMYBIM) de la Universidad Nacional Mayor de San Marcos, Perú. Las cepas provenian de entornos peruanos contaminados con hidrocarburos y fueron catalogadas como sobreproductoras de RL(n= 21), productoras de RL (n=20) y no productoras de RL (n= 20). Las 61 cepas fueron identificadas bioquímicamente con el sistema API 20 NE. La identificación molecular se realizó empleando el gen del RNAr 16S. Se encontró que Pseudomonas aeruginosa fue el microorganismo de mayor prevalencia en los estratos sobreproductores y productores de ramnolípidos. Además, se encontraron: Burkholderia cepacea, Pseudomonas fluorescens, Aeromonas hydrophila y Chryseobacterium indologenes. Los microorganismos no productores de ramnolípidos, también fueron caracterizados bioquímicamente. Mediante amplificación de PCR y electroforesis en gel de agarosa, estandarizados por la UNAM, se evidenció que las cepas seleccionadas poseen los genes: rhlA, rhlB, rhlR y rhlC. Para el secuenciamiento de la región génica rhLABR, se seleccionaron cuatros especies: Pseudomonas aeruginosa T2X-2, Pseudomonas aeruginosa IIIT1P2, Pseudomonas aeruginosa 6K-11 y Pseudomonas aeruginosa ATCC 9027, siguiendo metodología estandarizada por la UNAM y fueron comparados con Pseudomonas aeruginosa PAO1. Nuestros resultados muestran que los genes estudiados en las cepas seleccionadas son sinónimas de sus homólogos en la cepa patrón Pseudomonas aeruginosa PAO1, por lo que las diferencias genotípicas que expliquen la sobreproducción de ramnolípidos deberían hallarse en otros marcadores moleculares no cubiertos en el presente estudio.
Palabras clave: Pseudomonas aeruginosa; biosurfactantes; ramnolípidos; rhlAB; rhlR; rhlC.
Abstract
Genes associated to rhamnolipids production were molecularly characterized in 61 bacterial strains from LAMYBIM bacterial collection (Laboratorio de Microbiología y Biotecnología Microbiana, Universidad Nacional Mayor de San Marcos, Perú). Strains were isolated from peruvian environments hydrocarbons polluted and were classified as RL overproducers (n= 21), RL producers (n = 20) and non-producers (n = 20) producers. Molecular identification using the 16S rRNA gene was preceded by the biochemical identification of 61 strains selected with the API 20 NE system. Pseudomonas aeruginosa was the most prevalent strain of the RL overproducers and RL producers. Species such as Burkholderia cepacea, Pseudomonas fluorescens, Aeromonas hydrophila and Chryseobacterium indologenes, were found too. In the same way, non-producers microorganisms were also characterized. The PCR amplification and agarose gel electrophoresis techniques, standarized by the UNAM laboratory, showed that the selected strains had the genes: rhlA, rhlB, rhlR and rhlC. For the sequencing of the rhLABR gene region, four strains were selected: Pseudomonas aeruginosa T2K2, Pseudomonas aeruginosa III T1P2, Pseudomonas aeruginosa 6K-11 and Pseudomonas aeruginosa ATCC 9027, applying the methodology standardized by the UNAM and were compared with Pseudomonas aeruginosa PAO1. Our results show that the genes studied in the selected strains are synonymous with their homologues in Pseudomonas aeruginosa PAO1 standard strain. Therefore, genotypical differences that explain the overproduction of rhamnolipid might be found in other molecular markers not covered in this study.
Keywords: Pseudomonas aeruginosa; biosurfactants; rhamnolipids; rhlAB; rhlR; rhlC.
Introducción
En el Perú, numerosos estudios de la diversidad microbiana de ambientes contaminados por petróleo, han señalado a Pseudomonas aeruginosa como la especie de mayor prevalencia convirtiéndose en una prometedora herramienta biotecnológica en futuros procesos de biorremediación microbiana, evaluando su capacidad degradadora, emulsificante y productora de biosurfactante de tipo ramnolípidos (Norman et al. 2002, Hernández 2012, Arenas 1999, Renteria y Miranda 1998) Tabuchi (2014) previamente a la optimización del uso en agar CTAB/MB para selección de cepas productoras de ramnolípidos, reactivó cepas aisladas de ambientes contaminados por petróleo, determinando que el 30% de éstas, pertenecían al género Pseudomonas sp.
Los biosurfactantes del tipo ramnolípidos en comparación con sus equivalentes sintetizados químicamente tienen muchas ventajas como ser biodegradables, menos tóxicos, no peligrosos, altamente selectivos y de amplia aplicabilidad (Tejeda 2012, Singh et al. 2007) Diferentes especies de Pseudomonas son capaces de producir grandes cantidades de ramnolípidos de diferentes sustratos (De Lima et al. 2009) y constituye uno de los géneros que mayor potencial aplicativo engloba (Giraldo 2012). Se ha descrito que Pseudomonas aeruginosa produce típicamente biosurfactante de tipo ramnolípido (RL) (Perfumo et al. 2013, Soberón-Chávez et al. 2005) y corresponde al mayormente investigado (Du Plessis 2005). La mayoría de cepas de esta especie producen dos tipos de RL (Grosso et al. 2016), uno de ellos el mono-ramnolípido conteniendo una molécula de L-ramnosa y el di-ramnolipido que contiene dos moléculas de L-ramnosa (Aguirre et al. 2012, Croada 2011), el cual está controlado por el mecanismo de regulación génica denominada quorum sensing (Dobler et al. 2016).
En la biosíntesis de ramnolípidos, es necesario tener presente la via del dTDP-L-ramnosa y la síntesis de novo de los ácidos grasos. La via de la del dTDP-L-ramnosa, produce la fracción azúcar de éstos glicolípidos, en forma de dTDP-L-ramnosa (Reis et al. 2011). La síntesis de ramnolípidos se lleva a cabo en 3 reacciones enzimáticas principales (Dobler et al. 2016, Toribio et al. 2010) y la participación de dos ramnosiltrasferasas: RhlA que cataliza la dimerización de intermediarios de la biosíntesis de ácidos grasos para producir los β-hidroxialcanoil-β- hidroxialcanoatos (HAAs) mientras que RhlB (ramnosiltrasferasa 1) transfiere a los HAAs una primera molécula de ramnosa a partir de la dTDP-L-ramnosa (Aguirre M. 2013, Delgado 2009, Déziel et al. 2003) para formar el mono-ramnolípido, el cual se convierte en sustrato de RhlC (ramnosiltransferasa 2) agregando una segunda molécula de ramnosa, usando también una molécula de dTDP-L-ramnosa como precursor, obteniendo finalmente di-ramnolípido (Bazire & Dufour 2014, Rahim et al. 2001)
La producción de ramnolípidos en P. aeruginosa está fuertemente controlada por regulación genética (transcripcional y postranscripcional) en los operones rmlBDAC y rhlAB que responde a una amplia variedad de condiciones ambientales y señales fisiológicas (Reis et. al 2013)
El próposito de nuestra investigación fue determinar la presencia de los genes rhlA, rhlB, rhlR y rhlC (asociados a la producción de ramnolípidos) en especies nativas de Pseudomonas aeruginosa con capacidad de sobreproducción de este biosurfactante, los cuales provienen de ambientes contaminados por petróleo en el Perú.
Material y métodos
Microorganismos usados.- Bajo la técnica de muestreo subjetivo por decisión razonada (Quezada 2010) nosotros seleccionamos una muestra aleatoria de 61 microorganismos provenientes de una población perteneciente al género Pseudo-monas sp (n= 749), en base a lo hallado por Tabuchi 2014, de un universo de 2516 microorganismos que conforman el cepario del Laboratorio de Microbiología y Biotecnología Microbiana (LAMYBIM) de la Facultad de Ciencias Biológicas-UNMSM. Tabuchi clasificó en estratos o categorías, de acuerdo al área de halo en agar CTAB/MB modificando el método de Pinzón y Ju, convirtiéndola en herramienta semicuantitativa para selección de microrganismos de ramnolípídos.
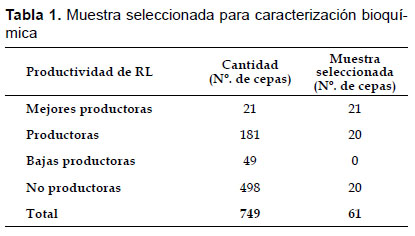
La muestra se seleccionó de la siguiente forma: sobreproductoras de RL (n= 21), productoras de RL (n= 20) y no productoras de RL (n= 20); no se seleccionaron microorganismos del estrato baja productoras de RL (Tabla 1).
Para la caracterización molecular, se seleccionaron 7 microorganismos. Además se emplearon como controles la cepas Pseudomonas aeruginosa ATCC 9027 y Pseudomonas aeruginosa PAO1 (Tabla 2). A partir del DNA purificado de estas cepas, se eligió a 3 de ellas en base en los trabajos de Tabuchi (2014) sobre la producción de ramnolípidos, encontrándose estos microorganismos dentro de las 5 mejores productoras de RL.
Kits de extracción de ADN.- La extracción y purificación del ADN cromosómico se realizó mediante los kits Ultra Clean Microbial DNA Isolation Kit Sample (Mio Bio Laboratories, Inc) y Gene JET Genomic DNA Purification Kit (Thermo Scientific).
Cebadores oligonucleótidos.- Los cebadores específicos utilizados tanto para la amplificación y secuenciamiento del gen ribosomal 16S de Pseudomonas aeruginosa, como para la amplificación de los genes y regiones génicas relacionados a la producción de ramnolípidos (rhlAB, rhlABR y rhlR, rhLC), se presentan en la Tabla 3. Se purificaron los productos de PCR, con los kits QI Aquick Gel Extracción (QIAGEN) y QI Aquick PCR Purification (QIAGEN).
Células competentes y plásmidos utilizados.- Con el fin de obtener mayor cantidad de ADN para el posterior secuenciamiento, se ligaron los genes rhlAB y rhlR con los vectores de clonación Kit CloneJet PCR cloning (Thermo Scientific) y pGEM-T Easy Vector Systems (Promega), respectivamente, en células competentes de Escherichia coli TOP 10. La purificación de plásmidos se realizó siguiendo las indicaciones de QIAprep Spin Miniprep Kit Protocol. Se verificó la direccionalidad y peso molecular mediante una digestión con la enzima HindIII (New England Biologics).
Identificación bioquímica.- Se identificaron taxonómicamente las cepas seleccionadas mediante uso del sistema de identificación rápida API 20 NE (Biomérieux), siguiendo las indicaciones dadas por el proveedor.
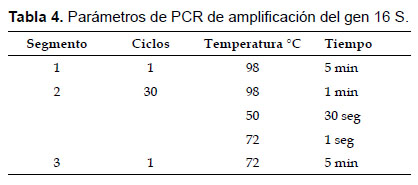
Amplificación del gen ribosomal 16S.- Se realizó la amplificación del gen ribosomal 16S mediante la reacción en cadena de la polimerasa (PCR) usando la enzima Phusion Hot Start II siguiendo las recomendaciones del proveedor y como molde el ADN cromosomal de los microorganismos seleccionados, preparándose la mezcla de la reacción como sigue: 10 μL de Buffer 5X Phusion Green HF, 1 uL dNTPs [10 mM], 0.5 μL de oligonucleótido 27F [10 mM], 0.5 μL de oligonucleótido 1942R [10 mM], 0.5 μL DNA obtenido, 37 μL de agua (grado milliphore) y 0.5 μL de enzima. La mezcla de la reacción fue transferida al termociclador, programado con los parámetros que se detallan a continuación (Tabla 4).
Amplificación de rhlAB, rhlABR y genes rhlR y rhlC.-La amplificación de las regiones rhlAB, rhlABR, se llevaron a cabo mediante la reacción en cadena de la polimerasa (PCR) siguiendo las recomendaciones del proveedor utilizando la enzima Phusion Hot Start II y como molde el ADN cromosomal de los microorganismos seleccionados, preparándose la mezcla de la reacción como sigue: 10 µL de Buffer 5X Phusion Green HF, 1 uL dNTPs [10 mM], 0.5 µL de oligonucleótido forward [10 mM], 0.5 µL de oligonucleótido reverse [10 mM], 0.5 µL DNA obtenido (en caso de rhlAB), 1,0 µL DNA obtenido (en caso de rhlABR), 37 µL de agua grado milliphore (en caso de rhlAB), 36.5 µL de agua grado milliphore (en caso de rhlABR) y 0.5 µL de enzima.
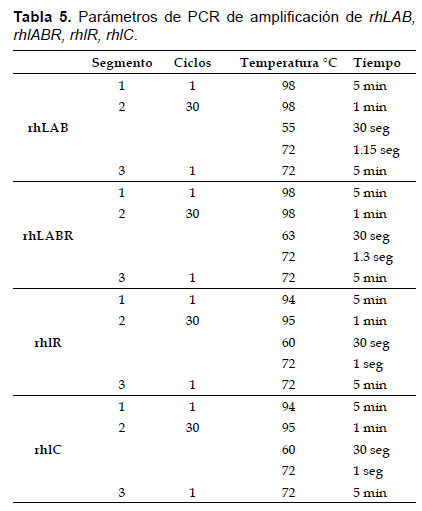
La amplificación de los genes rhlR y rhlC se llevó a cabo mediante la reacción en cadena de la polimerasa siguiendo las recomendaciones del proveedor utilizando la enzima Go Taq Polimerasa y como molde el ADN cromosomal de los microorganismos seleccionados, preparándose la mezcla de la reacción como sigue: 10 µL de Buffer 5X Green Go Taq, 1 µL dNTPs [10 mM], 1 µL de oligonucleótido forward [10 mM], 1 µL de oligonucleótido reverse [10 mM], 4 µL de MgCl2 25 mM , 1 µL DNA obtenido, 18.5 µL de agua (grado milliphore) y 0.5 µL de enzima. La mezcla de la reacción se transfiere al termociclador utilizándose los parámetros que se detallan a continuación (Tabla 5).
Inducción de células competentes y transformación de células.- Se realizó la reacción de ligación en células competentes de Escherichia coli TOP 10 basada en los protocolos de: pGEM T and pGEM T Easy Vector Systems, Thermo Scientific CloneJet PCR Cloning Kit y el protocolo de Chung, et al (1989), modificada por el Laboratorio de Biotecnología Molecular 7 de la UNAM como sigue: Se desarrolló una ligación a 22 °C por 30 minutos. Posteriormente se mantuvo la mixtura de la ligación en hielo durante 15 minutos. Se dio un choque de calor de 1 minuto a 42 °C, luego un choque de frio en hielo por 5 minutos. Se adicionó 900 µL de Caldo LB, y se procedió a incubar con agitación: 37 °C a 250 rpm por un tiempo de 40 minutos. Se centrifugó a 14000 rpm por 1 minuto, eliminando el sobrenadante y sembrando por diseminación la cantidad de 100 µL, haciendo uso de espátula de Drigalsky en placas de agar LB mas solución stock de carbenelina (50 mg/mL), en caso del vector CloneJET, para una concentración final de 100 µg/mL y placas de agar LB mas solución stock de X Gal (40 mg/mL), en caso del vector PGEM-T, para una concentración final de 100 µg/ mL. Las placas se incuban a 37 °C toda la noche.
Obtención de clonas y purificación de plásmidos.-Se seleccionó de 2 a 4 clonas (colonias) de cada placa con células transformadas. Con ayuda de palillos mondadientes estériles se procedió a cultivar en matraces conteniendo 15 mL de medio Luria Bertini (LB) mas solución stock de carbenicilina (50 mg/ mL) para una concentración final de 100 µg/mL, finalmente se incubó toda la noche a 37 °C con agitación de 220 rpm. Después de 12 horas, se purificaron los cultivos crecidos en matraces, distribuyendo en dos tubos eppendorf de 1 y 5 mL, y se centrifugó a 14 000 rpm por 2 minutos. De este pellet se procedió a la purificación de plásmidos, utilizando la metodología indicada en QIAprep Spin Miniprep Kit Protocol (QIAGEN).
Análisis de restricción.- Los análisis de restricción se realizaron con la enzima Hind III-HF 20 000 U/mL (New Englands Biolabs) siguiendo las instrucciones del fabricante.
Secuenciamiento.-Las secuencias del gen ribosomal 16S, como de las regiones génicas rhlABR fueron enviadas a la Unidad de Síntesis y Secuenciación de DNA (USSDNA) del Instituto de Biotecnología de la Universidad Autónoma de México (UNAM), Cuernavaca, Estado de Morelos, para su secunciamiento. Las lecturas de los cromatogramas de estas secuencias fueron realizadas con el software FinchTV.
Análisis bioinformático.- Las secuencias nucleotídicas obtenidas fueron alineadas junto a trece (13) secuencias nucleotídicas de referencia mediante el programa MUSCLE (Edgar 2004). Posteriormente, se realizaron análisis evolutivos en MEGA6. Las distancias evolutivas fueron calculadas usando el método de Jukes-Cantor (1969), y la variación entre los sitios fue modelada con una distribución gamma. Finalmente, se infirió la historia evolutiva del conjunto mediante el método de Neighbour-Joining (Saitou & Nei 1987), aplicando posteriormente la prueba de bootstrap con 2000 réplicas (Felsenstein 1985).
Resultados y discusión
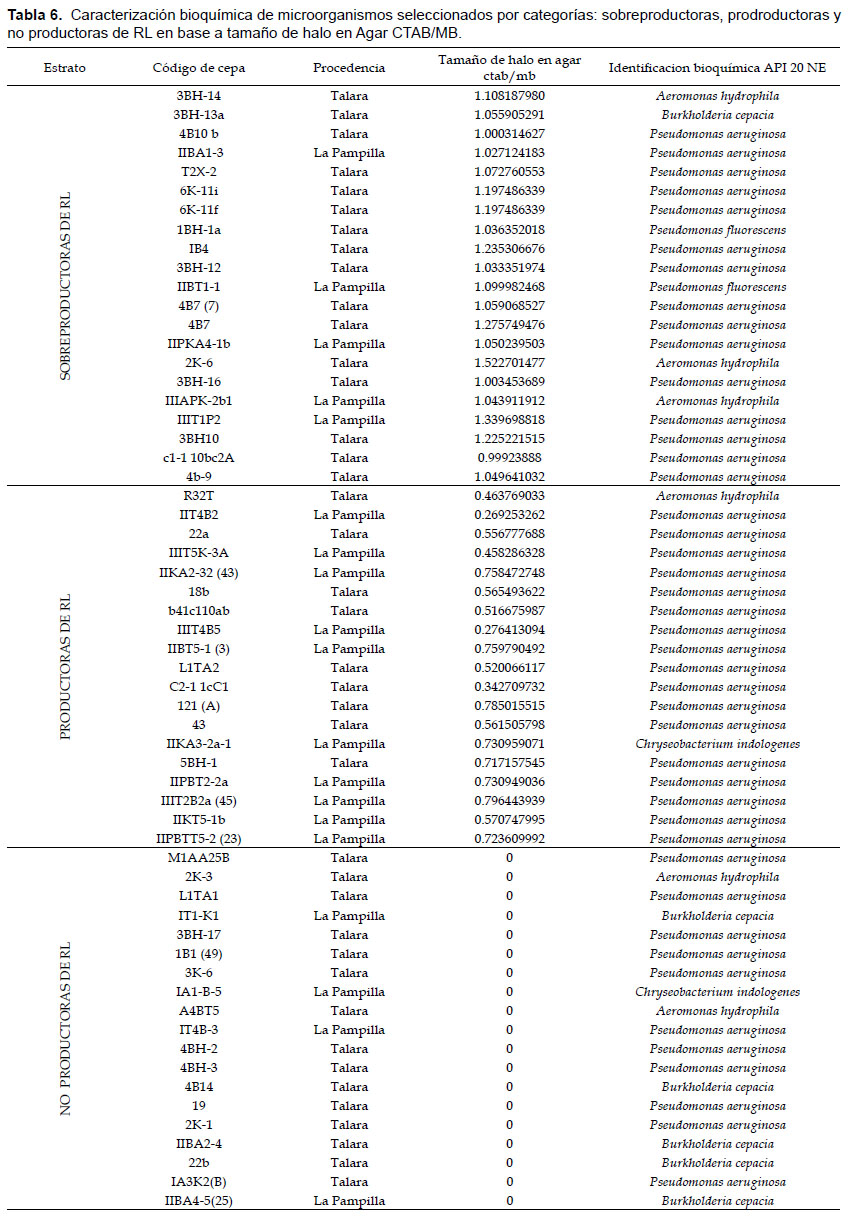
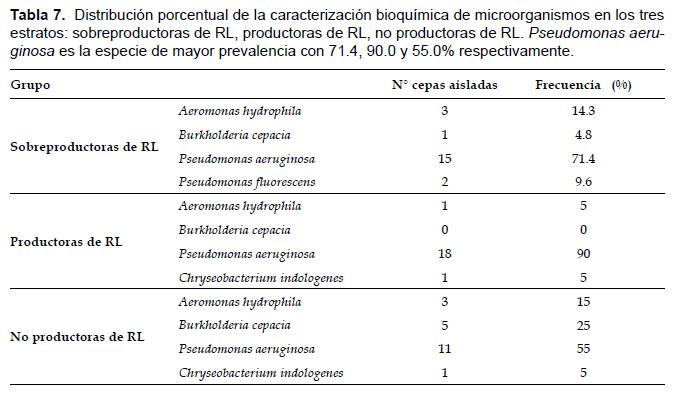
Identificación bioquímica y molecular de microorganismos.-Mediante la identificación bioquímica con el sistema API 20 NE de una muestra aleatoria de 61 microorganismos provenientes de una población de 749 especies del género Pseudomonas spp. (Tabla 6). Se encontró que el microorganismo de mayor prevalencia en los tres estratos evaluados (sobreproductoras de RL, productoras de RL y no productoras de RL), corresponde a la especie Pseudomonas aeruginosa, con 71.4, 90.0 y 55.0% respectivamente. En menor proporción se identificaron las especies: Aeromonas hidrophyla, Pseudomonas fluorescens, Burkolderia cepacea y Chryseobacterium indologenes (Tabla 7). Chryseobacterium indologenes se evidenció sólo en los estratos productoras de RL (Código IIKA3-2a-1)y no productoras de RL (Código IA1-B-5).
El 95.7% de las cepas correspondientes al estrato sobreproductoras de RL, pertenecen a especies del género Pseudomonas (P. aeruginosa P. fluorescens) y Burkohlderia cepacea, especie fenotípicamente cercana a Pseudomomas spp. Arenas (1999) halló una frecuencia de 30.91% de cepas del género Pseudomonas de una muestra de 55 microorganismos identificados. El 88.24 % cepas de este género correspondió a la especie Pseudomonas aeruginosa.
Ajustando los datos de Tabuchi (2014) mediante identificación bioquímica obtuvimos una frecuencia estimada de 19.8% de cepas correspondientes al género Pseudomonas del total de microorganismos del cepario de LAMIBYM (n= 2517). Este resultado es menor al reportado por Arenas (1999) que obtuvo un 30.91% en su estudio, sin embargo su población muestral (n= 55) y sus métodos de aislamiento fueron distintos a los nuestros.
A la luz de nuestros resultados, la frecuencia ponderada de cepas de Pseudomonas spp fue del 66.5%, valor que se eleva a 83.2 % cuando se incluye a B. cepacia. Observamos que nuestro estudio presenta un porcentaje de mayor prevalencia para especies del grupo Pseudomonas, y específicamente de P. aeruginosa, lo cual corrobora lo planteado por Norman et. al. (2002) que indican que Pseudomonas es el género con mayor frecuencia que se aísla de ambientes contaminados con hidrocarburos. Además concordamos con Pérez et al. (2008) quienes mediante pruebas bioquímicas clásicas, caracterizaron cepas bacterianas aisladas de suelos contaminados con petróleo de alrededores de una refinería de Santiago de Cuba, determinando que 5 de ellas corresponden a Pseudomonas aeruginosa. Narvaéz-Flores et al. 2008 seleccionaron bacterias con capacidad degradadora de hidrocarburos, aisladas de sedimentos del Caribe colombiano, identificadas con el sistema bioquímico BBL Cristal y API 50CH/E como: Klebsiella sp, Chhromobacterium sp., Flavimonas orizihabitans, Enterobacter cloacae, Pseudomonas aeruginosa, Bacillus brevis, B. pumillus y B. cereus. Por su parte, Pucci et al. (2010) estudiaron la diversidad bacteriana con capacidad de degradar hidrocarburos en la playa de Caleta Córdova (Argentina), utilizando el sistema FAMEs, identificaron como los género de mayor frecuencia: Pseudoalteromonas, Bacillus, Psychrobacter y Shenewanella; además de Pseudomonas sp., Aeromonas sp. y Burkholderia cepacea, entre otras. Arrieta et al. (2012) realizaron la caracterización fenotípica y molecular de poblaciones bacterianas de un suelo contaminado con diésel, diferenciándolos molecularmente en los siguientes géneros: Enterobacter, Bacillus, Arthrobacter, Sanguibacter, Staphyococcus y Flavobacterium.
Basados en el trabajo de Tabuchi (2014), tenemos un total de 21 microorganismos sobreproductores de RL, nosotros seleccionamos 8 de ellos: 7 cepas identificadas con API 20 NE como Pseudo-monas aeruginosa: 2K1,T2X-2, II PKA41b, 3Bh-16, IIIT1P2, 4B7 (7), 6K11 y una especie identificada como Burkholderia cepacea 3Bh13a, a fin de realizar la amplificación del gen ribosomal 16 S (16 S ADNr) mediante técnica de PCR y de electroforesis en gel de agarosa, para una posterior selección al secuenciamiento respectivo. Se consideraron como controles positivos, Pseudomonas aeruginosa ATCC 9027 y Pseudomonas aeruginosa PAO1.
Para el secuenciamiento se seleccionaron 4 microrganismos: Pseudomonas aeruginosa T2X-2, Pseudomonas aeruginosa III T1P2, Pseudomonas aeruginosa 6K-11 y Pseudomonas aeruginosa ATCC 9027. Las secuencias obtenidas el gen ribosomal 16 S fueron analizadas y comparadas con el Gen Bank, encontrándose que los cuatro microorganismos aislados tienen correspondencia génica con Pseudomonas aeruginosa PAO1. Las secuencias de 16S obtenidas permite identificarlas como miembros de la especie Pseudomonas aeruginosa.
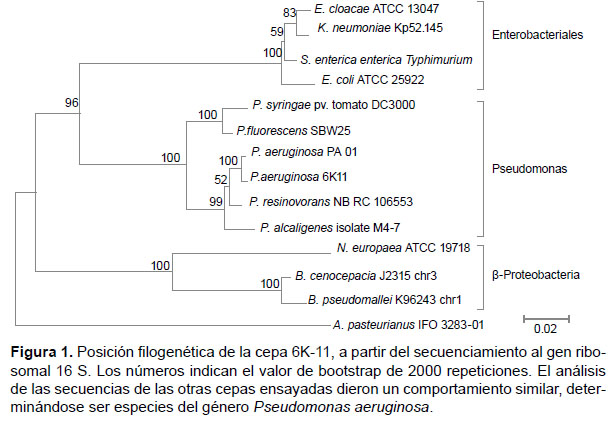
Las secuencias obtenidas a partir de 4 cepas problema seleccionadas presentan una alta similitud con las regiones homólogas codificadas en el genoma de Pseudomonas aeruginosa PAO1. Además las secuencias aminoacídicas predichas para estas secuencias noveles resultan sinónimas de la registrada para la cepa patrón (Fig. 1)
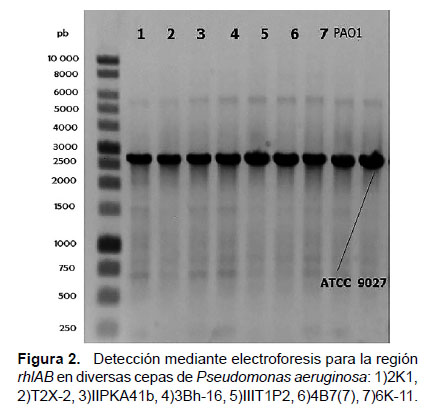
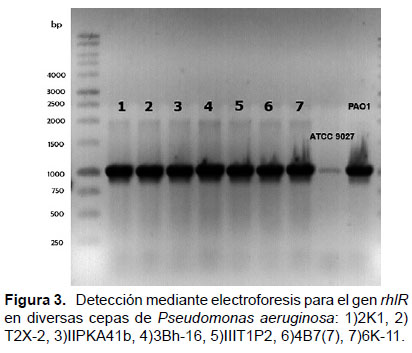
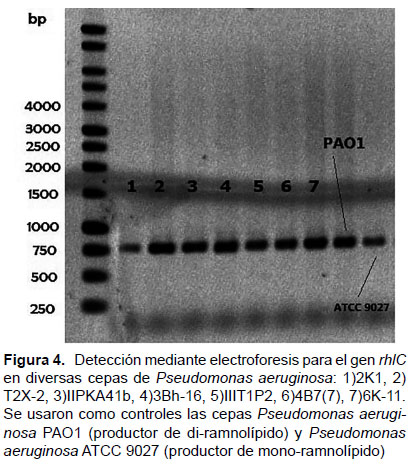
Caracterización molecular de genes asociados a la producción de ramnolípidos. - Luego de amplificar mediante PCR las secuencias y regiones génicas rhlAB, rhlABR, rhlR y rhlC, los productos de amplificación fueron separados en gel de agarosa mediante electroforesis. Luego fueron secuenciados los productos de amplificación de la región rhlABR de las cepas Pseudomonas aeruginosa T2X-2, Pseudomonas aeruginosa IIIT1P2, Pseudomonas aeruginosa 6K-11, Pseudomonas aeruginosa ATCC 9027 y comparados con la cepa Pseudomonas aeruginosa PAO1. En las pruebas de electroforesis realizadas a las siete cepas mencionadas previamente, se determinó la presencia de los genes: rhlA, rhlB y rhlC, como se observa en las Figuras 2 a 4, las cuales codifican respectivamente:
a. la 3-(3-hidroxialcanoiloxi)alcanoato sintetasa (Abdel-Mawgoud et al. 2011), responsable de la síntesis de HAAs y la fracción dimérica de los ácidos grasos de loa ramnolípidos (Dobler et al. 2016, Reis et al. 2011, Soberón-Chávez et al. 2005).
b. la enzima ramnosiltransferasa 1, responsable de la biosíntesis de momo-ramnolípido y
c. la enzima ramnosiltransferasa 2, responsable de la biosíntesis de di-ramnolípido (Bazire & Dufour 2014, Déziel et al. 2003, Soberón-Chávez et al. 2005) respectivamente.
Asimismo también se determinó la presencia del gen rhlR, como se muestra en la Figura 4, que codifica el regulador transcripcional RhlR que tiene un papel central en la respuesta de detección del quórum (Medina et al. 2003)
Al no encontrar diferencias significativas en la caracterización molecular de genes y regiones génicas asociadas a la producción de ramnolípidos, planteamos la hipótesis que se deba a la presencia de regiones altamente conservadas en el genoma de Pseudomonas aeruginosa. Esto fue demostrado por Wolgang et al. 2003, al utilizar microarrays de ADN de genoma completo para determinar el contenido genomico de 18 cepas de Pseudomonas aeruginosa, 13 aisladas de infecciones humanas más comunes y 5 de fuentes ambientales; encontrando una remarcable conservación de genes incluidos aquellos que codifican casi todos los factores de virulencia conocidos, concluyendo que cepas de Pseudomonas aeruginosa poseen un genoma altamente conservado que codifica genes importantes para la supervivencia en numerosos ambientes. Asimismo, Grosso et al. (2014), quienes al secuenciar cuatro aislados no humanos de Pseudomonas aeruginosa (3 ambientales y un aislado de estómago de delfin), y comparados frente a 12 aislados clínicos y uno proveniente de rizósfera de melón cepa M18, afirmaron que estos aislados estudiados tienen una larga proporción de sus genomas conservados entre ellos (núcleo genómico); concluyendo que la variabilidad genética de todas las cepas de Pseudomonas aeruginosa cuyos genomas han sido secuenciados, es extremadamente bajo.
En el análisis detallado de la secuencia de los genes dependientes del QS (rhlA, rhlB, rhlR, rhlI, etc), Grosso et al. (2014) demostraron que los cuatro aislados de Pseudomonas aeruginosa (ID 4365, M10, IGB83, 148) resultaron ser idénticos; de igual forma nosotros encontramos los mismos resultados para nuestras cepas de Pseudomonas aeruginosa T2X-2, IIIT1P2, 6K-11, ATCC 9027 (Figs. 5 y 6)
Es importante destacar que el análisis molecular de genes asociados a la producción de ramnolípidos solo contempló los genes del sistema rhl. Al no haber hallado diferencias genéticas en la región estudiada, debemos hallar las bases moleculares de las diferencias fenotípicas (nivel de producción de ramnolípidos) en otras regiones del genoma.
Agradecimientos
Los autores manifiestan su agradecimiento a los investigadores del Instituto de Investigaciones Biomédicas de la Universidad Autónoma de México (UNAM), a la Unidad de Síntesis y Secuenciación de DNA (USSDNA) del Instituto de Biotecnología de la UNAM, sede Cuernavaca, Estado de Morelos. Al Programa Nacional de Innovación para la Competitividad y Productividad (Innóvate Perú) bajo el contrato Nº238-FINCyT-IA-2013.
Literatura citada
Abdel-Mawgoud A.M., R. Hausmann, F. Lépine, et al. 2011. Rhamnolipids: detection, analysy, biosynthesis, genetic regulationand bioengineering of production. En: Biosurfactants.Microbiology Monographs 20. DOI: [ Links ]
Abdel-Mawgoud A.M., R. Hausmann, F. Lépine, M.M. Müller, E. Déziel. 2011. Rhamnolipids: Detection, Analysis,Biosynthesis, Genetic Regulation, and Bioengineering ofProduction. In: Biosurfactants. Springer, Berlin, Heidelberg. (Microbiology Monographs). p. 13–55. http://dx.doi.org/10.1007/978-3-642-14490-5_2. [ Links ]
Aguirre M., G. Medina, A. González, et al. 2012. The Pseudomonas aeruginosa rmlDBAC operon, encondind dTDP-L- rhamnose biosynthetic enzymes, is regulated by the quorumsensing transcriptional regulator RhlR and the alternative sigma factor σs. Microbiology 158: 908-916. DOI: http://dx.doi.org/10.1099/mic.0054726-0. [ Links ]
Aguirre M. 2013. Regulación del operon rmlBDAC por el sistema sensor de quórum RhL en Pseudomonas aeruginosa. Tesis, Doctor en Ciencias Bioquímicas. Facultad de Química,Programa de Maestris y Doctorado en Ciencias Bioquímicas, Universidad Nacional Autónoma de México. México D.F. 47 p. [ Links ]
Arenas S. 1999. Aislamiento y caracterización de bacterias de ambientescontaminados por petróleo en la Refinería La Pampilla-Lima.Tesis, Biólogo con mención Microbiología y Parasitología. Facultad de Ciencias Biológicas, Universidad NacionalMayor de San Marcos. Lima-Perú [ Links ].
Arrieta O.M., A.P. Rivera, B. Rojano, et al. 2012. Caracterización fenotípica y molecular de poblaciones bacterianas aisladas deun suelo contaminado con diésel y sometiodo a dos tecnologías de biorremediación. Gestión y Ambiente 15(3):65-76. http://www.bdigital.unal.edu.co/35842/1/36281-1560601-PB.pdf. [ Links ]
Bazire A. & A. Dufuor. 2014. The Pseudomonas aeruginosa rhlG and rhlAB genes are inversely regulated and RhlG is not requiredfor rhamnolipid synthesis. BMC Microbiology 2014, 14: 160. DOI: http://dx.doi.org/10.1186/1471-2180-14-160. [ Links ]
Croada G. 2011. Caracterización de la regulación transcripcionaldel gen rhlR en Pseudomonas aeruginosa por Vfr. Tesis,Doctor en Ciencias (Bioquímicas). Programa de Maestría en Ciencias Bioquímicas, Facultad de Química, UniversidadNacional Autónoma de México. México D.F. 95 p. [ Links ]
Delgado V. 2009. El papel de la proteína RhlA en la síntesis de ramnolípidos (rhl´s)y polihidroxialcanoatos (PHA´s)en Pseudo-monas aeruginosa. Tesis, Maestro en Ciencias Bioquímicas. Universidad Autónoma de México. Mexico D.F. 123 p. [ Links ]
Déziel E., F. Lépine, S. Milot, et al. 2003. rhlA is required for the production of a novel biosurfactant promoting swarming motility in Pseudomonas aeruginosa: 3-(3-hydroxyalkanoyloxy) alkanoic acids (HAAs), the precursors of rhamnolipids. Microbiology 149:2005–2013. DOI: http://dx.doi.org/10.1099/mic.0.26154-0 [ Links ]
Dobler L., L.F. Vilela, R.V. Almeida, et al. 2016. Rhamnolipids in perspective: gene regulatory pathways, metabolic engineering, production and technological forecasting. Review.New Biotechnology. 33(1):123-135 DOI: http://dx.doi.org/10.1016/j.nbt.2015.09.005. [ Links ]
Du Plessis D.J.F. 2005. Regulation rhamnolipid biosynthesis in the Pseudomonas aeruginosa PAO1 biofilm population. Tesis, Magister en Ciencias. Facultad de Ciencias Naturales yAgrícolas, Departamento de Mkicrobiología y Patología de Plantas. Universidad de Pretoria. Sudafrica. 112 p. [ Links ]
Edgar R. C. 2004. Muscle: multiple sequence alignment with high accuracy and high throughput. Nucleic Acids Research32(5):1792-1797. DOI: http://dx.doi.org/10.1093/nar/gkh340. [ Links ]
Felsenstein J. 1985. Confidence limits on phylogenies: An approach using the bootstrap. Evolution 39(4):783-791. http://dx.doi.org/10.2307/2408678 [ Links ]
Giraldo J.D. 2012. Producción de ramnolípidos por Pseudomonas aeruginosa Pb25: evauación de su actividad emulsificante y remoción de metales pesados. Tesis, Biólogo, MenciónMicrobiogía y Parasitología. Facultad de Ciencias Biológicas,Universidad Nacional Mayor de San Marcos. Lima-Perú. 58 p. [ Links ]
Grosso, M.V., C. Santos, A. González, et. al. 2014. Pseudomonas aeruginosa and environmental isolates constitute a single population with high phenotypic diversity. BCM Genomics 15:318. DOI: http://dx.doi.org/10.1186/1471-2164-15-318. [ Links ]
Grosso, M.V., A. González, M.J. Granados, et. al. 2016. Pseudomonas aeruginosa ATCC 9027 is a non virulent strain suitable for mono-rhamnolipids production. Applied Microbiology andBiotechonology 100 (3):9995-10004. DOI: http://dx.doi.org/10.1007/s00253-016-7789-9. [ Links ]
Hernández D. 2012. Incremento de la producción de ramnolípidos en la cepa modelo Pseudomonas aeruginosa PAO1. Tesis, Químico Farmaceútico Biólogo. Facultad de Química, Universidad Nacional Autónoma de México. México D.F. 46 p. [ Links ]
Medina, G., K. Juárez, R. Díaz, et. al. 2003. Transcriptional regulationof Pseudomonas aeruginosa rhlR, encoding a quorumsensing regulatory protein. Microbiology 149(11):3073-81. [ Links ]
Medina G., Juárez K., Díaz R., Soberón-Chávez G. 2003. Transcriptional regulation of Pseudomonas aeruginosa rhlR,encoding a quorum-sensing regulatory protein. Microbiology 149:3073–3081. DOI: http://dx.doi.org/10.1099/mic.0.26282-0 [ Links ]
Narváez-Flores S., M.L. Gómez, M.M. Martínez. 2008. Selección de Bacterias con capacidad degradadora de hidrocarburos aisladas a partir de sedimentosdel caribe colombiano. Boletíndel Instituto de Investigaciones Marinas y Costeras (INVEMAR), 37(1):61-75. ISSN 0122-9761. http://www.scielo.org.co/pdf/mar/v37n1/v37n1a04 [ Links ]
Norman R.S., R. Frontera-Suau, P.J. Morris. 2002. Variability inPseudomonas aeruginosa lipopolisaccharyde expresiónduring crude oil degradation. Applied and Environmental Microbiology, October 2002, p. 5096-5103. DOI: http://dx.doi.org/10.1128/AEM.68.10.5096–5103.2002. [ Links ]
Perfumo A., M. Rudden, T. Smyth, et al. 2013. Rhamnolipids are conserved biosurfactants molecules: implications for their biotechnological potencial. Applied Genetics and Molecular Biotechnology 97:7297-7306. DOI: http://dx.doi.org/10.1007/s00253-013-4876-z. [ Links ]
Pucci N., A. Acuña, N. Tonin, et. al. 2010. Diversidad de bacterias cultivables con capacidad de degradar hidrocarburos de la playade la Caleta, Argentina. Revista Peruana de Biología 17(2): 237-244. DOI: http://dx.doi.org/10.15381/rpb.v17i2.34. [ Links ]
Quezada N. 2010. Metodología de la Investigación. Estadísticaaplicada en la investigación. Editora Macro E.I.R.L. Lima-Perú. 334 p. [ Links ]
Rahim R., U.A. Ochsner, C. Olvera, M. Graninger, et. al. 2001. Cloning and functional characterization of the Pseudomonas aeruginosa rhlC gene that encodes rhamnosyltransferase 2, an enzyme responsable for di- rhamnolipid biosynthesis.Molecular Microbiology 40(3):708-718. DOI: http://dx.doi.org/10.1046/j.1365-2958.2001.02420.x. [ Links ]
Reis R.S., S. L. Gonc¸alves, D.A. Chapeaurouge,et al. 2010. Effects of carbon and nitrogen sources on the proteome of Pseudomonas aeruginosa PA1 during rhamnolipid production. Process Biochemistry 45(9):1504-1510. DOI:http://dx.doi.org/10.1016/j.procbio.2010.05.032. [ Links ]
Reis R.S., A.G. Pereira, B.C. Neves, et. al. 2011. Gene regulation of rhamnolipid production in Pseudomonas aeruginosa-A review. Bioresource Technology 102:6377-6384. DOI: http://dx.doi.org/10.1016/j.biortech.2011.03.074. [ Links ]
Reis R.S., G.J. Pacheco, A.G. Pereira, D.M.G. Freire. 2013. Biosurfactans: Production and Applications. En: Biodegradation-Lifeof Science, Chapter 2. Chamy R. & F. Rosenkranz. EditoresIntech Open Acces Publications 378 p. DOI: http://dx.doi.org/10.5772/56144. [ Links ]
Saitou N. & M. Nei. 1987. The neighbor-joining method: A new method for reconstructing phylogenetic trees. MolecularBiology and Evolution 4(4):406-425. [ Links ]
Pérez R.M., M.I. Camacho, J.M. Gómez, et al. 2008. Aislamiento y selección de una cepa bacteriana degradadora de hidrocarburos a partir de suelos contaminados con petróleo. CENIC-Ciencias Biológicas, 39(1):44-51,. http://www.redalyc.org/html/1812/181214889004/ [ Links ]
Singh A., J. Van Hamme, & O. Ward. 2007. Surfactans in microbiology and biotechnology. Part 2. Application aspects.Biotechnology Advances 25:99-121. doi:10.1016/j.biotech.adv.2006.10.004. [ Links ]
Soberón-Chávez G., F. Lépine & E. Déziel. 2005. Production of rhamnolipids by Pseudomonas aeruginosa. Mini-Review. AppliedMicrobiology and Biotechnology 68:718-725. DOI: http://dx.doi.org/10.1007/s00253-005-0150-3. [ Links ]
Tabuchi T. 2014. Optimización del uso de agar con cetiltrimetilamonio bromuro y azul de metileno para la selección de cepas de Pseudomonas spp. productoras de ramnolípidos. Tesis, Biólogo Genetista Biotecnólogo. Facultad de Ciencias Biológicas, Universidad Nacional Mayor de San Marcos.74 pp. [ Links ]
Tejeda V. 2012. Efecto de RhlA en la producción de ramnolípidos y polihidroxialcanoatos en Pseudomonas aeruginosa (PAO1) Tesis, Biólogo. Fascultad de Estudios Superiores Zaragoza, Universidad Nacional Autónoma de México. México D.F. 36 p. [ Links ]
Toribio J., A. Escalante & G. Soberón-Chávez. 2010. Rhamnolipids: Production in bacteria other than Pseudomonas aeruginosa.Review Article. European Journal of Lipid Science and Technology 112:1082-1087. DOI: http://dx.doi.org/10.1002/ejlt.200900256. [ Links ]
Wolfgang M.C., B. R. Kulasekara, X. Liang, et al. 2003. Conservation of genome content of virulence determinants among clinical and environmental isolates of Pseudomonas aeruginosa. Proceedings of the National Academy of Sciences. 100(14):8484- 8489. DOI: http://dx.doi.org/10.1073/pnas.0832438100. [ Links ]
Presentado: 09/01/2017
Aceptado: 26/07/2017
Publicado online: 28/10/2017
Información sobre los autores: RP, AG, FM: diseñaron el experimento. RP, AG: realizaron la parte experimental. RP, GR: analizaron los datos. RP: redactó el manuscrito. GSC, FM, SG: asesoramiento en la ejecucion de la investigación. Todos los autores revisaron y aprobaron el manuscrito.
Los autores no incurren en conflictos de intereses.
Fuentes de financiamiento: FINCyT contrato N°238-FINCyT-IA-2103.