INTRODUCCIÓN
El fósforo (Pi) es uno de los cationes divalentes más importantes del organismo por la gran variedad de funciones que cumple: Es esencial para los procesos energéticos celulares, forma parte de la estructura de huesos, dientes, y es necesario en la estructura y función de la membrana celular. Este ion es regulado por el riñón y la parathormona (PTH) así como por una molécula identificada en el año 2000 como factor de crecimiento fibroblástico 23 (FGF- 23).1-4) En el riñón la PTH modula la absorción y excreción de calcio y fósforo mientras que en el hueso se encarga del recambio de estos minerales según las necesidades del organismo.4
La concentración sérica de fosfato menor a 0,80 mmol/L en adultos se define como hipofosfatemia y menos de 0,30 mmol/L se clasifica como hipofosfatemia severa.5 Existen tres mecanismos de hipofosfatemia: La disminución de la absorción intestinal, el aumento de las pérdidas urinarias y el paso desde el espacio extra al intracelular.(4 La hipofosfatemia de aparición en la infancia temprana se debe a problemas hereditarios y se caracteriza por la disminución de la reabsorción tubular renal de fosfato. Sus principales manifestaciones clínicas son el raquitismo y la osteomalacia.(6
La forma más frecuente de la hipofosfatemia familiar es heredada como un rasgo dominante ligado al cromosoma X y se le conoce como raquitismo hipofosfatémico ligado al cromosoma X o hipofosfatemia ligada a X, esta alteración comprende casi 80 % de los casos de raquitismo hipofosfatémicos hereditarios.(6,7 La imposibilidad de inhibir el FGF-23 produce una incapacidad para la reabsorción tubular del Pi y reduce la actividad alfa- 1-hidroxilasa, lo que resulta en niveles séricos reducidos de 1.25-dihidroxivitamina D, hiperfosfaturia e hipofosfatemia.8 Existen formas oligosintomáticas que se solo manifiestan algunos síntomas como dolor óseo o debilidad.
El raquitismo hipofosfatémico es una condición poco frecuente en nuestro medio y muchas veces difícil de reconocer en aquellos con signos o síntomas subclínicos por lo que el objetivo de este reporte de caso es presentar el espectro de presentación, diagnóstico y opciones de manejo de dos pacientes (madre-hijo) con raquitismo hipofosfatémico ligado al cromosoma X.(9
PRESENTACIÓN DEL CASO
La madre de nacionalidad peruana-española tiene 36 años y diagnóstico de raquitismo hipofosfatémico desde los 2 años. Debutó con debilidad muscular, retardo del crecimiento y retraso en la aparición de los dientes. Con el tiempo desarrolló deformaciones en varo en extremidades inferiores que dificultaron la movilización afectando su calidad de vida. La madre recibió hasta los 15 años calcitriol 1.2 mcg/d y fósforo 1936 mg 2 tab cada 8 h, en la actualidad persiste con las malformaciones esqueléticas, presenta talla corta, dolor en articulación de cadera, rodilla y limitación parcial al movimiento. Fue evaluada por otorrinolaringología y no presentó alteraciones auditivas. La madre actualmente recibe como terapia calcitriol 1.5 mcg/ día y Solución de Joulie (ácido orto fosfórico 85% 5.45g fosfato disódico 18.75g) 60 ml cada 8 horas.
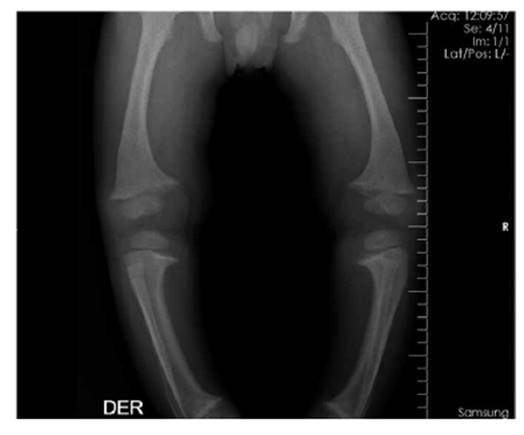
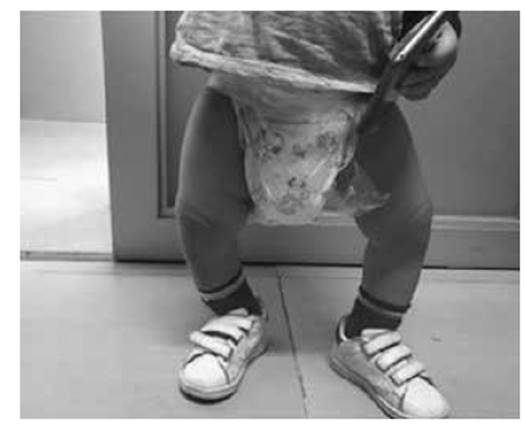
El hijo fue evaluado por el antecedente materno de raquitismo hipofofosfatémico, tiene 15 meses de edad y recibe tratamiento con aporte de fósforo Solución de Joulie 7 ml 4 veces/día (aporte de fósforo 52 mg/kg/d) y calcitriol 1 ug/día (0.5 ug C/12 horas) desde los 4 meses. A pesar del tratamiento y de tener una curva de crecimiento adecuado para edad tiene un retraso en la aparición de dientes y deformaciones en extremidades inferiores como se aprecian en las imágenes 1 y 2. Los exámenes auxiliares de la madre y el hijo al momento de la evaluación clínica inicial se muestran en la tabla 1.
Tabla 1 Exámenes auxiliares de la madre y el hijo al momento de la evaluación clínica inicial
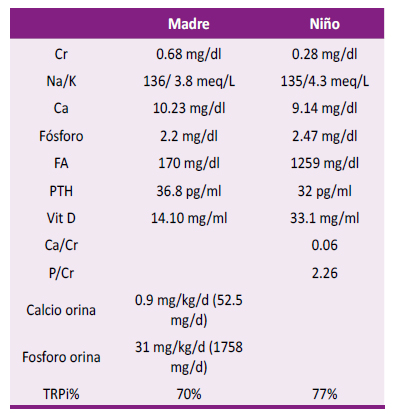
FA: fosfatasa alcalina (U/L), PTH: paratohormona (pg/ml), Vit D: 25 OH vitamina D (ng/ml), Ca: calcio (mg/dl), Cr: creatinina (mg/dl), TRP%: tasa de reabsorción de fósforo
En el caso de la madre se pudo hacer la colecta de orina de 24 horas, en el caso del hijo se utilizó la relación de electrolitos y creatinina en orina de una muestra aislada por la dificultad en recolectar orina de 24 horas y donde la hiperfosfaturia expresada en la baja tasa de reabsorción de fósforo en ambos pacientes es el hallazgo más representativo.
La madre fue sometida a un estudio genético en España para identificar la mutación puntual, dando como resultado: Mutación del Gen PHEX, variante patogénica tipo Splicing en hemicigosis: rs886041839:g.22190443 G>A Mutación previamente descrita como HGMD CS126536 confirmando el diagnóstico materno de raquitismo hipofosfatémico ligado al cromosoma X.
DISCUSIÓN
El raquitismo hipofosfatémico forma parte de un grupo de tubulopatías hereditarias caracterizadas por la pérdida excesiva de fósforo a través del riñón como defecto primario y donde el raquitismo hipofosfatémico ligado al cromosoma X (RHLX) tiene una incidencia de aproximadamente 1:20000 representando el 80 % de raquitismos hipofosfatémicos. Es la forma heredada más común de raquitismo en niños con 86-87 % de casos de herencia familiar y 57-72 % de casos esporádicos.9,10
La mutación del gen PHEX con pérdida de función (deleción del extremo 3’) conduce al aumento de FGF-23. El FGF-23 inhibe la transcripción de la 1 alfa hidroxilasa y es además una hormona fosfatúrica que requiere la presencia del cofactor Klotho. Las endopeptidasas PHEX (del inglés Phosphate regulating gene with Homologies to Endopeptidases on the X chromosome) y DMP1 controlan los niveles sanguíneos de FGF-23.(8
En condiciones normales, PHEX degrada el FGF-23 en fragmentos inactivos, evitando de esta manera el aumento excesivo de la excreción de fosfatos y el desarrollo de hipofosfatemia. Sin embargo, las mutaciones en PHEX en los pacientes con RHLX permiten que se mantengan niveles elevados del FGF-23, esto induce alteraciones de la reabsorción tubular renal de fosfatos y desarrollo de hipofosfatemia.(9 Las manifestaciones clínicas ocurren después del primer año de vida con retraso en el crecimiento, raquitismo y deformidades óseas: Piernas curvadas, manifestaciones neurológicas, malformación de Arnold Chiari, craneosinostosis, sordera neurosensorial, tinnitus, vértigo.10,11 Otras manifestaciones incluyen: abscesos dentales, artritis y calcificaciones de los tendones y ligamentos (entesopatía), estenosis del canal espinal y artropatía degenerativa.(11
Se ha observado nefrocalcinosis entre el 22 % y 100 % de los pacientes con XLH. Esta variación se puede atribuir parcialmente a los estudios de pequeño tamaño y a la alta variabilidad de pacientes y tratamientos. En el caso de los pacientes aquí presentados ninguno desarrollo nefrocalcinosis ni litiasis renal.(10
Los hallazgos de laboratorio más frecuentes incluyen: hiperfosfaturia, hipofosfatemia, calcio en sangre normal, calcio en orina bajo, 25 OH Vitamina D normal, 1,25 OH Vitamina D normal o baja, Fosfatasa alcalina alta, PTH normal o alta y FGF-23 alta.(11
La hipofosfatemia grave induce el raquitismo y compromete la apoptosis de los condrocitos hipertróficos en la placa de crecimiento del hueso, generando las malformaciones óseas características de esta condición.(9-11
El tratamiento se basa en la suplementación de fósforo: 40-100 mg/kg/día, calcitriol 15-60 ng/kg/día y últimamente Burosumab (inmunoglobulina humana recombinante que antagoniza los efectos y FGF-23). Esta última sustancia muestra resultados prometedores en la presente condición pudiendo ser un tratamiento seguro y clínicamente útil de los pacientes con enfermedades hipofosfatémicas relacionadas con el FGF23. Este hecho sentaría las bases para el establecimiento de una terapia única.11
En un paciente con hipofosfatemia no dependiente de la hormona PTH o de la vitamina D y de presentación familiar debe considerarse el diagnóstico de raquitismo hipofosfatémico ligado al cromosoma X.