Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Scientia Agropecuaria
Print version ISSN 2077-9917
Scientia Agropecuaria vol.5 no.3 Trujillo 2014
http://dx.doi.org/10.17268/sci.agropecu.2014.03.04
ARTÍCULOS ORIGINALES
Influencia de la temperatura y tiempo de extracción en la fuerza de gel y rendimiento de gelatina obtenida a partir de piel de tollo (Mustelus mento)
Influence of temperature and extraction time on gel strength and yield of gelatin from speckled smooth-hound skin (Mustelus mento)
Alberto Miano1, Carmen Rojas2, Gabriela Barraza3
1 Escuela de Ingeniería Agroindustrial y Comercio Exterior, Facultad de Ingeniería, Universidad César Vallejo, Av. Larco cuadra 17, Trujillo, Perú.
2 Escuela de Ingeniería Agroindustrial, Facultad de Ciencias Agropecuarias, Universidad Nacional de Trujillo, Av. Juan Pablo II s/n, Ciudad Universitaria, Trujillo, Perú.
Resumen
En el presente trabajo se determinaron los parámetros de temperatura y tiempo de extracción para obtener mayor rendimiento y fuerza de gel de gelatina a partir de piel de tollo (Mustelus mento) por hidrólisis alcalina. Se empleó el diseño compuesto central rotacional (DCCR) realizando en total 11 ensayos experimentales con temperaturas entre 60ºC y 95ºC, y tiempo de extracción entre 30 y 240 min. Se concluyó que a mayores tiempos de extracción se obtiene mayor rendimiento de gelatina y a menor temperatura de extracción mayor es la fuerza de gel. Para obtener mayor rendimiento (27% – 28%) y mayor fuerza de gel de gelatina (130 – 150g Bloom), se tendría que utilizar tiempos entre 220 y 240 minutos, y temperaturas entre 60 y 65ºC.
Palabras clave: gelatina, tollo, fuerza de gel, Bloom.
Abstract
In the present study was determined the parameters of temperature and extraction time to achieve higher yield and gel strength of gelatin from speckled smooth-hound skin (Mustelus mento) by alkaline hydrolysis. It was used the central composite rotational design (CCRD) with 11 experiments with temperatures between 60ºC and 95°C and extraction time between 30 minutes and 240 min. It was concluded that with higher extraction times, higher yield percentage will get, and with lower extraction temperature, higher gel strength will get. For obtaining higher yield (27% – 28%) and greater gelatin gel strength (130 - 150g Bloom), we used 220 and 240 minutes, and temperatures between 60 and 65 °C.
Keywords: gelatin, speckled smooth-hound, gel strength, Bloom.
1. Introducción
La gelatina viene siendo extraída mayoritariamente a partir de piel de cerdo (46%), pieles de bovino (29,4%), huesos (23,1%) y otras fuentes (1,5%) (GME, 2008). Sin embargo, a pesar de que la gelatina tiene múltiples aplicaciones (espesante, emulsificante, etc.), aún existen preocupaciones de parte de los consumidores con respecto a su origen (Asher, 1999). Esto se debe principalmente a las creencias religiosas (tanto el judaísmo y el Islam prohíben el consumo de productos provenientes de cerdo, mientras que los hindúes del ganado vacuno), como la tendencia hacia el vegetarianismo en todo el mundo (Wilesmith et al., 1991). Existe gran interés por parte del mercado europeo de sustituir la gelatina del ganado bovino por otras fuentes como la proveniente de recursos marinos debido a que no está asociado con riesgo de Encefalopatía Espongiforme Bovina (EEB) (Badii y Howell, 2006) y por razones religiosas (Gilsen y Ross-Murphy, 2000). Una alternativa para la obtención de gelatina es la derivada de pescado y aves de corral. El pescado es una fuente de gelatina pero su producción comercial es alrededor de 1% en el mundo (Jamilah y Harvinder, 2002). Se espera que en un futuro aumente la producción de gelatina procedente de esta materia prima, ante ello se debe investigar y buscar nuevas tecnologías para mejorar el bajo rendimiento y fuerza de gel del que actualmente se obtiene (Schrieber y Gareis, 2007). La obtención de gelatinas procedentes del colágeno de pescado tiene un gran impacto económico y social, debido principalmente a problemas de índole religiosa moral y de salud. Desde el punto de vista ambiental, el aprovechamiento de residuos hidrobiológicos mantendría los mares, ríos y lagunas con menor contaminación (Badii y Howell, 2006).
El procesamiento de los recursos pesqueros producen una gran biomasa residual como piel, huesos y aletas que generalmente es descartado aproximadamente 7,3 millones de toneladas por año en el mundo (Kelleher, 2005). La venta de pescado para el consumo humano directo en los mercados, producen aún más desechos que las empresas pesqueras, debido al ineficiente uso de esta materia prima, generándose 35% de desperdicios, que pueden ser destinados a la fabricación de ensilado (empleando vísceras) y gelatina (empleando pieles y huesos). Alrededor del 30% de ese subproducto está constituido de piel y hueso con alto contenido de colágeno (Muyonga et al., 2004).
La extracción de gelatina a partir de diversas especies de pescado ha sido reportada por varios autores como Schriebery y Gareis (2007), Jamilah y Harvinder (2002) y Gudmundsson y Hafsteinsson (1997) quienes demostraron su viabilidad. En el Perú, el tollo (Mustelus mento) es un pez aprovechado en la culinaria y la piel actualmente no tiene ninguna transformación que genere valor agregado. Por este motivo, en el presente trabajo de investigación se planteó determinar los parámetros de temperatura y tiempo de extracción para obtener mayor rendimiento y fuerza de gel de gelatina.
2. Material y métodos
Se empleó piel de tollo (Mustelus mento) proveniente de pescado fresco comprado en el mercado. Las pieles de tollo se lavaron con agua potable y se cortaron en cuadrados de 1cm de lado, se sometieron a pre tratamiento con una solución de Hidróxido de Sodio 0,1N en la proporción piel/solución de 1:3 (p/v) a temperatura de 10°C por 48 horas. Luego se lavaron con agua destilada y se neutralizaron con ácido clorhídrico 0,05N.
En la etapa de extracción se colocaron en un vaso de precipitación 150 g de piel pre tratadas, con agua destilada en la proporción 1:4 (p/v) y fueron expuestas a temperaturas que oscilaron entre 60ºC a 95ºC por tiempos 30 min a 240 min, según los tratamientos del diseño propuesto. Se filtró la suspensión y se obtuvo la parte liquida (gelatina en solución). Esta solución se congeló por 24 horas; el agua excedente se separó por descongelación a 20ºC. Los geles de gelatina fueron colocadas en un secador por aire caliente a 60ºC por 12 horas para obtener láminas de gelatina deshidratada. Se determinó la humedad y cenizas (AOAC, 2000) con los métodos 950.46 y 920.153 respectivamente en la piel de tollo y la gelatina extraída. Para la determinación del porcentaje de rendimiento se expresó los gramos de gelatina seca por cada 100 g de piel fresca limpia y para la determinación de la fuerza de gel se empleó el Gelómetro tipo Bloom (AOAC 948.21, 2006).
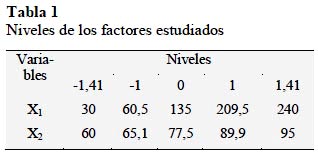
Se empleó el diseño rotacional central compuesto (DCCR) de segundo orden con resultados en superficies de respuesta. El planeamiento factorial fue del tipo 2k + 2*k +3 pc = 11 experimentos (pc: puntos centrales). En la Tabla 1 se muestran los niveles de las variables independientes (X1: tiempo de extracción en minutos; X2: temperatura en ºC).
Se construyeron modelos del tipo:
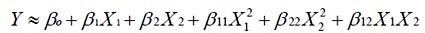
(Donde βo, β1, β2, β11, β22, y β12: Coeficientes de regresión; Y: Respuesta, en función de los coeficientes significativos para cada respuesta (rendimiento y fuerza de gel). Luego, se realizó ANVA para los modelos y el cálculo de los coeficientes de determinación (R2), pruebas que permiten validar estadísticamente los modelos. Finalmente, se generaron superficies de respuesta con el Software Statistica 7.0, donde se buscaron las regiones de interés.
3. Resultados y discusión
Resultados experimentales de los tratamientos
A partir de piel de tollo, se obtuvo gelatina con diferentes rendimientos expresados en porcentaje y fuerza de gel (g Bloom), valores que se muestran en la Tabla 2.
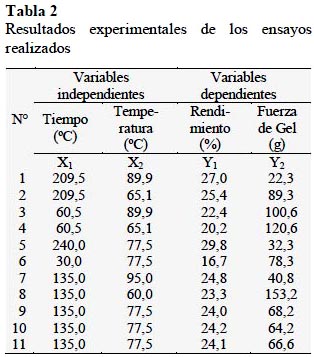
Se encontró humedad de 29,72 % + 2,2 y 3,98 % + 0,48 de contenido de cenizas. Con el tratamiento 5 (240 min a 77,5 °C) se logró obtener mayor rendimiento. El tratamiento 8 (135 min a 60 °C) obtuvo un valor de fuerza de gel (153,2 g Bloom). Se demuestra que tiempos largos permiten obtener mayores rendimientos y bajas temperaturas de extracción permiten obtener gelatinas con mayor fuerza de gel. Los rendimientos en base seca encontrados en esta experiencia oscilan en el rango de 16,7% y 29,8%, valores bastante aceptables si consideramos que Rahman et al. (2008) reportaron rendimientos de 18% de gelatina extraída a partir de atún de aleta amarilla concluyendo que el rendimiento y calidad de la gelatina no sólo están influenciados por la especie o tejido del cual es extraída, sino también por el proceso de extracción. Mohtar et al. (2010), reportaron un rendimiento de 17,4% de gelatina extraída a partir de hoki (Macruronus novaezelandiae) a 49 °C por 60 min en solución de NaCl 0,75 M. Lo que no se especifica es si el rendimiento reportado es para gelatina purificada (decolorada y deodorizada) o gelatina bruta.
Los rendimientos de gelatina que han sido reportados varían entre las diferentes especies especialmente por el diferente contenido de colágeno en la composición de la piel y por el método de extracción empleado (Gómez-Guillén et al., 2002; Jamilah y Harvinder, 2002; Muyonga et al., 2004; Jongjareonrak et al., 2006). También existe pérdida del colágeno a consecuencia de los sucesivos lavados a la piel y por desnaturalización insuficiente del colágeno soluble durante la extracción por el alto grado de entrecruzamiento de los enlaces covalentes que puede hacer decrecer la solubilidad del colágeno (Foegeding et al., 1996).
Con respecto a la fuerza de gel, se obtuvieron valores entre 22,3 y 153,2 g Bloom que se pueden considerar valores razonablemente aceptables. La fuerza de gel es uno de los más importantes indicadores de calidad de gelatina, siendo su rango comercial entre 100 a 300 g Bloom, rango deseable para la industria y entre 250 a 260 g Bloom para su uso en la industria alimentaria de yogurt, embutidos, gomitas, etc. (Holzer, 1996). Karim y Bhat (2009) y Gilsenan y Ross-Murphy (2000) establecieron que la mayoría de gelatinas extraídas de pescado presentan una fuerza de gel entre 0 y 270 g Bloom valores menores a la fuerza de gel que presentan la gelatina bovina y porcina (entre 200 y 240 g Bloom). Sin embargo, Cho et al. (2005) reportaron una fuerza de gel de 426 g Bloom a partir de gelatina extraída de atún de aleta amarilla. Gelatinas provenientes de especies de agua fría generalmente tienen valores de fuerza de gel menores y siendo el tollo un pez cartilaginoso de aguas frías, la gelatina extraída de esta especie no gelificaría bien a temperaturas mayores a 10 °C y presentaría baja fuerzas de gel (Norland, 1990); a diferencia de los peces de agua caliente que exhiben valores altos de fuerzas de gel muy cercanos a los de gelatina porcina (Gudmundsson y Hafsteinsson, 1997). La diferencia en la fuerza de gel podría atribuirse al menor contenido de prolina e hidroxiprolina encontrados en gelatina de pescado (16-18%) comparado con la gelatina proveniente de mamíferos (24%).
Los diferentes orígenes de la materia prima y las condiciones de extracción también afectan la fuerza de gel debido a los cambios conformacionales del colágeno (Karim y Bhat, 2009). Esto ha sido también demostrado por Zhou et al. (2006) en el estudio que realizaron de extracción de gelatina con diferentes concentraciones de hidróxido de sodio y ácido acético.
Modelado matemático
El análisis de regresión (Tabla 3) demuestra que para la variable rendimiento los coeficientes no fueron significativos (p > 0,05); mientras que los valores del coeficiente de determinación R2 (91,34%) y R2-ajustado (82,68%) fueron superiores al 85 y 75% respectivamente.
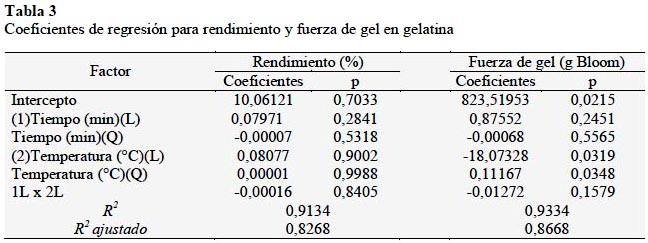
El modelo de regresión encontrado para el rendimiento sigue la siguiente ecuación:
Y1 = 10,06 + 0,079 X1 – 0,00007 X12 + 0,081 X2 + 0,0001 X22 – 0,0001 X1 X2
Donde Y1: porcentaje de rendimiento; X1: tiempo de extracción en minutos; y, X2: temperatura de extracción en ºC.
Para el caso de la variable fuerza de gel sólo se reporta coeficientes de regresión significativos (p < 0,05) para intercepto, temperatura lineal y la temperatura cuadrática. Al eliminar los coeficientes de regresión no significativos, el valor de coeficiente de determinación disminuyó a 61,2%, por lo que se consideró presentar los coeficientes de regresión en su totalidad para aumentar la capacidad de predicción del modelo, obteniendo un coeficiente de determinación R2 de 93,34% y un R2-ajustado de 86,68%. El modelo de regresión encontrado para la fuerza de gel siguió la siguiente ecuación:
Y2 = 823,5 + 0,8755 X1 – 0,0007 X12 – 18,073 X2 + 0,112 X22 – 0,0127 X1 X2
Donde Y2: Fuerza de gel (g Bloom).
En la Tabla 4 se muestra el análisis de varianza de la regresión.
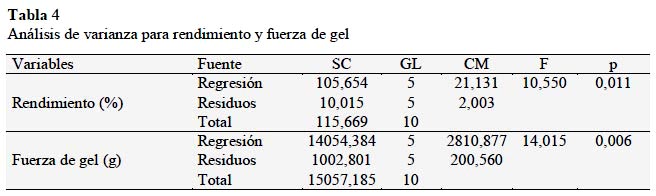
Tal como se observa, los modelos propuestos para rendimiento y fuerza de gel fueron significativo (p < 0,05), además presentaron coeficientes de determinación elevados de 91,34 y 93,34%, respectivamente. En las figuras 4 y 5 se presentan los diagramas de Pareto, empleados para evaluar el efecto de la temperatura y tiempo de extracción en el rendimiento y fuerza del gel de gelatina extraída a partir de piel de tollo respectivamente.
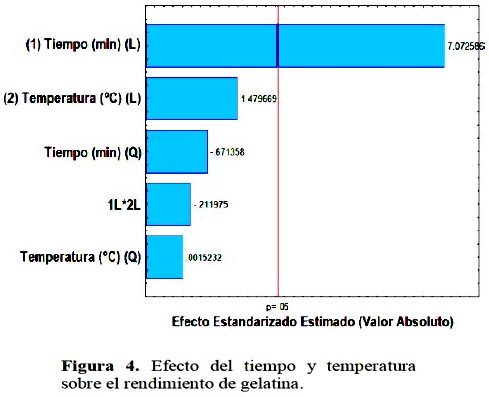
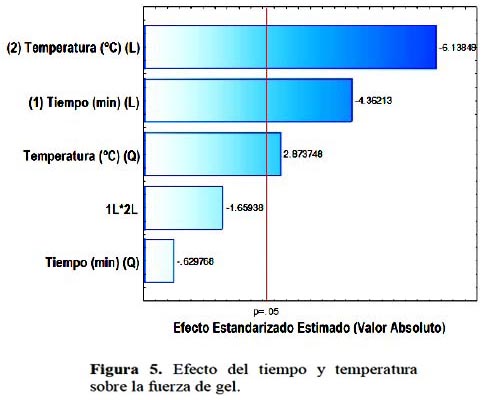
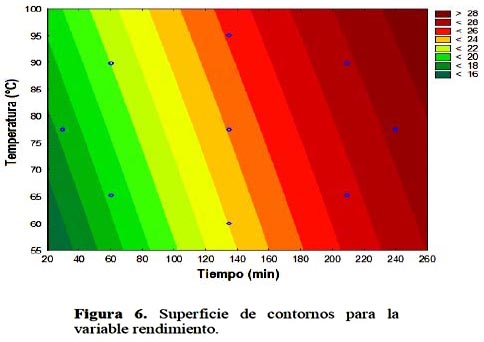
Se observa que existe sólo un efecto lineal significativo del tiempo de extracción en el rendimiento de la gelatina extraída, efecto significativo lineal del tiempo y temperatura y cuadrático de la temperatura de extracción en la fuerza del gel de la gelatina extraída a partir de piel de tollo. En la Figura 6 se presenta superficie de contornos para la variable rendimiento, donde se observa que el rendimiento se incrementa al incrementarse el tiempo de extracción, mientras que el efecto de la temperatura es en menor cuantía.
En la Figura 7 se presenta la superficie de contornos para la variable fuerza de gel.
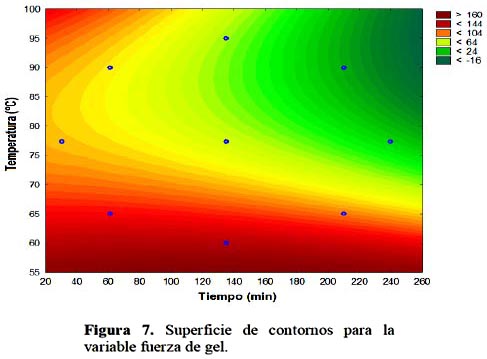
Se observa que a bajas temperaturas se puede obtener una gelatina de alto Bloom sin que el tiempo le afecte, efecto similar se lograría a altas temperaturas, pero en tiempos cortos. Esto se puede explicar por lo mencionado por Djabourov et al., (1993) quienes establecieron que las temperaturas mayores a 40 ºC destruyen los puentes de hidrógeno y rompen muchos enlaces covalentes que ayudan a desestabilizar la triple hélice y convirtiéndola en gelatina soluble; pero las temperaturas mucho más altas (superiores a 80 ºC) pueden romper demasiados enlaces, debilitando la fuerza de gel.
La superficie de contornos, muestra un leve incremento de la fuerza de gel a temperaturas mayores de 85 ºC, lo cual puede contradecir lo dicho anteriormente. Sin embargo, según Intarasirisawat et al. (2007), algunas proteasas termoestables endógenas de la piel están involucradas en la degradación de las moléculas de gelatina (especialmente las cadenas α y β) durante el proceso de extracción a elevadas temperaturas lo que contribuye a obtener gelatinas de bajo Bloom. Estas proteasas ayudan en la disminución de la fuerza de gel de la gelatina, pero las temperaturas superiores a 85ºC comienzan a inactivar dichas enzimas, aumentando la probabilidad de obtener gelatinas de mayor Bloom.
Al realizar una superposición de gráficas de contornos (Figura 8), se observa que a tiempos entre 220 y 240 minutos, y temperaturas entre 60 y 65 ºC (valores dentro de los rangos estudiados), se obtiene la zona óptima de operación, donde existe alto rendimiento y valores elevados de fuerza de gel. Karim y Bhat (2009), demostraron que el proceso de extracción realizado puede influenciar en la longitud de las cadenas polipeptídicas y propiedades funcionales de la gelatina. Esto dependería de los parámetros de proceso (temperatura, tiempo y pH), el pre tratamiento que se haya efectuado y el acondicionamiento y la preservación que se le haya dado a la materia prima.
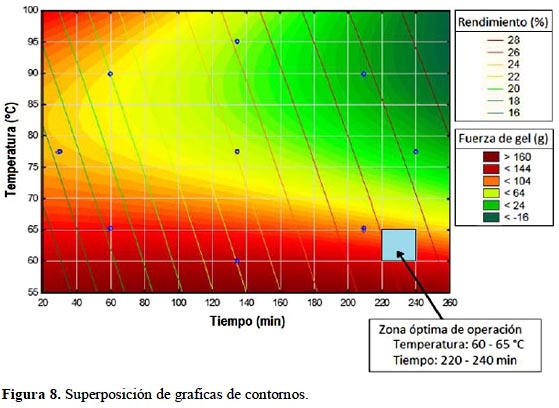
Se ha demostrado en este estudio que existe influencia de tiempo y temperatura pero también se debe considerar que existen otros factores como los mencionados por Karim y Bhat (2009).
La gelatina obtenida en estas condiciones de extracción, presentó un contenido de cenizas promedio de 2,19 ± 0,11 %. Según la RTCR 9 (1956), el porcentaje de cenizas máximo que debe presentar la gelatina comestibles es del 2%. La gelatina que se extrajo tuvo un contenido superior debido probablemente, a la falta de desmineralización que reduce el contenido de cenizas.
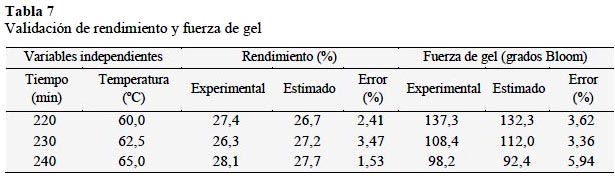
Validación del modelo
Al determinar la zona óptima de operación por superposición de graficas de contornos: tiempo (220 - 240 min) y temperatura (60 - 65 °C) de extracción, se procedió a realizar la validación de los resultados, para lo cual se comparó los valores de rendimiento y fuerza del gel estimados con los modelos propuestos, con los valores experimentales de la gelatina extraída con los parámetros de tiempo y temperatura de la zona óptima, presentando un error menor al 10%, por lo que ambos modelos presentarían una buena capacidad de predicción y podrían ser empleados dentro del rango de parámetros de extracción establecidos en el presente trabajo de investigación, puesto que presentan errores porcentuales entre 1,53% y 5,94% (Gutiérrez y De la Vara, 2009).
4. Conclusiones
Se encontró influencia de la temperatura y tiempo de extracción en el rendimiento y fuerza de gel de gelatina obtenida a partir de piel de tollo (Mustelus mento), donde a mayores tiempos de extracción mayor rendimiento de gelatina y a menor temperatura de extracción, mayor fue la fuerza de gel. Se obtuvo gelatina con una fuerza de gel entre 22,3 y 153,2 g Bloom y rendimientos de 16,7 y 29,8% en los diferentes ensayos realizados. De acuerdo a este estudio para obtener rendimiento entre 27 - 28% y mayor fuerza de gel (130 a 150 g Bloom) se debería utilizar los rangos de 220 y 240 minutos y, 60 y 65ºC, respectivamente. Por lo tanto, se demuestra que utilizando los parámetros obtenidos de tiempo y temperatura hallados en la presente investigación, la piel de tollo (Mustelus mento) es una alternativa para obtener gelatina con fuerza de gel aceptable comercialmente para sustituir la gelatina de ganado bovino y porcino por la proveniente de recursos marinos.
5. Referencias bibliográficas
AOAC. 2000. Official Methods of Analysis (17 th ed.) Association of Official Analytical Chemists. Washington, D.C. [ Links ]
AOAC. 2006. Official Methods of Analysis 925.10. Association of Official Analytical Chemists. Washington, D.C. [ Links ]
Asher, D. 1999. The transmissible spongiform encephalopathy agents: concerns and responses of the United States regulatory agencies in maintaining the safety of biologics. Developments in Biological Standardization 100: 103–118. [ Links ]
Badii, F.; Howell, N.K. 2006. Fish gelatin: structure, gelling properties and interaction with egg albumen proteins. Food Hydrocolloid 20: 630-640. [ Links ]
Cho, S.; Gu, Y.; Kim, S. 2005. Extraction optimization and physical properties of yellowfin tuna (Thunnusal bacares) skin gelatin compared to mammalian gelatins. Food Hydrocolloids 19: 221–229. [ Links ]
Djabourov, M.; Lechaire, J.; Gaill, F. 1993. Structure and rheology of gelatin and collagen gels. Biorheology 30: 191–205. [ Links ]
Foegeding, E.; Lanier, T. ; Hultin, H. 1996. Characteristics of edible muscle tissues. In: Fennema ,O.R. (Ed). Food Chemistry. Marcel Dekker, New York. [ Links ]
Gómez-Guillén, M.C.; Turnay, J.; Fernández-Díaz, M.D.; Ulmo, N.; Lizarbe, M.; Montero, P. 2002. Structural and physical properties of gelatin extracted from different marine species: a comparative study. Journal of Food Hydrocolloids 16: 25-34. [ Links ]
GME. 2008. Gelatin Manufacturers of Europe. http://www.gelatine.org/ [ Links ]
Gilsenan, P.M.; Ross-Murphy, S.B. 2000. Rheological characterization of gelatins from mammalian and marine sources. Food Hydrocolloids 14: 191-195. [ Links ]
Gudmundsson, M.; Hafsteinsson, H. 1997. Gelatin from cod skins as affected by chemical treatments. Journal of Food Science 62: 37–47. [ Links ]
Gutierrez, H ; De la Vara, R. 2009. Control Estadístico de la Calidad y Seis Sima Segunda edición. Editorial McGraw-Hill. Interamericana Editores. [ Links ]
Holzer, D. 1996. Gelatin production. US patent: 5,484,888. [ Links ]
Intarasirisawat, R.; Benjakul, S.; Visessaguan, W.; Prodpran, T.; Tanaka, M.; Howell, N. 2007. Autolysis study of big eye snapper (Priacanthus macracanthus) skin and its effect on gelatin. Food Hydrocolloids, 21: 537–544. [ Links ]
Jamilah, B.; Harvinder, K. 2002. Properties of gelatins from skins of fish-blacktilapia (Oreochromis mossambicus) and red tilapia (Oreochromis nilotica). FoodChemistry 77: 81–84. [ Links ]
Jongjareonrak, A.; Benjakul, S.; Visessanguan, W.; Tanaka, M. 2006. Effects of plasticizers on the properties of edible films from skin gelatin of big eye snapper and brown stripe red snapper. European Food Research Technology 222: 229-235. [ Links ]
Karim, A.; Bhat, R. 2009. Fish gelatin: properties, challenges, and prospects as an alternative to mammalian gelatins. Food Hydrocolloids 23: 563-576. [ Links ]
Kelleher, K. 2005. Discards in the worlds marine fisheries. An update. FAO Fisheries Technical Paper N 470 (pp. 131). Rome. [ Links ]
Mohtar, N., Pereda, C.; Quek, S. 2010. Optimization of gelatine extraction from hoki (Macruronus novaezelandiae) skins and measurement of gel strength and SDS–PAGE. Food Chemistry 122: 307-313. [ Links ]
Muyonga, J.; Cole, C.; Duodu, K. 2004. Extraction and physicochemical characterization of Nile perch (Lates niloticus) skin and bone gelatin. Food Hydrocolloids 18: 581–592. [ Links ]
Norland, R. 1990. Fish gelatin. In M. N. Voight, & J. K. Botta (Eds.), Advances in fisheries technology and biotechnology for increased profitability. 325–333. Lancaster: Technomic Publishing Co. [ Links ]
Rahman, M.; Al-Saidi, G.; Guizani, M. 2008. Thermal characterization of gelatin extracted from yellowfin tuna skin and commercial mammalian gelatin. Food Chemistry 108: 472-481. [ Links ]
RTCR9. 1956. Norma general para gelatina comestible .La Gaceta digital. Diario oficial La Uruca, San José. Costa Rica. [ Links ]
Schrieber, R.; Gareis, H. 2007. Gelatin handbook. Theory and industrial practice. Wyley-VCH, Germany. [ Links ]
Wilesmith, J.; Ryan, J.; Atkinson, M. 1991. Bovine spongiform encephalopathy: epidemiological studies on the origin. Veterinary Record 128: 199–203. [ Links ]
Zhou, P,; Mulvaney, S.; Regenstein, J. 2006. Properties of Alaskan Pollock skin gelatin: a comparison with Tilapia and pork skin gelatins. Journal of Food Science 71: C313-C321. [ Links ]
* Autor para correspondencia
E-mail: crojasp@unitru.edu.pe (C. Rojas).
Recibido 16 enero 2013.
Aceptado 20 julio 2014.














