1. Introducción
El antropoceno es la alteración humana significativa del sistema de la Tierra, principalmente está relacionada con el consumo de combustibles fósiles, en los bosques tropicales sin embargo la evidencia arqueológica e histórica demuestra que los humanos influyeron en los sistemas físicos, químicos y biológicos a través de grandes regiones de bosques tropicales a partir de hace 45 mil años aproximadamente (Roberts et al., 2018). A nivel mundial la mayoría de los bosques son secundarios y se encuentran en diferentes etapas de sucesión, así evaluar la riqueza, similitud de especies y cuantificar la importancia de los procesos ecológicos estocásticos son esenciales para comprender los mecanismos de sucesión para la restauración forestal (Abbas et al., 2019). El Neotrópico abarca el sur de México, América Central y la mayor parte de América del Sur (Beck, 2019), posee una diversidad arbórea excepcional que ha sido formada por los factores ambientales y procesos históricos (Rezende et al., 2018), su cobertura está ligada a factores ambientales y cambio en el uso del suelo (Bernardi et al., 2016).
La deforestación de la amazonia debido a la expansión de la agricultura y plantaciones de árboles exóticos hoy conduce a una liberación futura de carbono con retraso en el tiempo, debido a la eventual descomposición de los productos forestales o de la tala que queda en el sitio (Rosa et al., 2016). Estas modificaciones antrópicas en los paisajes crean parches forestales que varían en tamaño y forma, lo que a su vez afecta a toda la biodiversidad regional (Macedo-reis et al., 2019), generando interrupción de los procesos de sucesión sin la transición de bosques secundarios a bosques maduros. (Lascurain-rangel et al., 2019), por ejemplo, se conoce la relevancia biológica de la cubierta forestal para los herbívoros, y su conservación en el paisaje circundante contribuye a la diversidad del bosque (Maua et al., 2020), mantenimiento sus servicios ecológicos (Macedo-reis et al., 2019), además, del rol en la regulación del clima local es clave, este servicio es importante para evitar enfermedades causadas por el calor y permitir la adaptación al cambio climático (Wol et al., 2018).
Ante la importancia y amenazas que sufren los bosques amazónicos, los inventarios forestales son una fuente significativa de información taxonómica a partir del cual se puede estimar la diversidad de los sitios a escalas regionales (Guitet et al., 2014), y pueden contribuir valiosamente a la detección de patrones de diversidad a gran escala cuando los sesgos están bien controlados y corregidos (Guitet et al., 2014). Ya desde hace tiempo el establecimiento y monitoreo de parcelas permanentes ha contribuido al entendimiento de la dinámica y biodiversidad de los bosques tropicales y su relación con el clima y suelo (Roberts et al., 2018), adicionalmente también se pueden entender los procesos ecológicos como la apertura de claros en el dosel de forma natural, por la caída de árboles mayores, debido a condiciones como lluvia, suelo y vientos (Jara Gavilán, 2018), que impulsan la regeneración del ecosistema y permite la estabilidad de la diversidad, y las funciones ecológicas en el bosque, por ello su conservación y restauración es prioritaria (Farneda et al., 2018).
La región amazónica de Madre de Dios en Perú, poseen una alta diversidad de especies de árboles (Monteagudo-Mendoza et al., 2020), como Bertolletia excelsa de familia Licytidaceae cuyo fruto es la castaña o nuez del Brasil muy abundante y de alto valor económico (Pardo-Molina et al., 2020). Por tanto, el objetivo del estudio fue evaluar la composición y diversidad arbórea, para lo cual, aplicando el método de inventario, se evaluó la estructura y composición florística, y posteriormente estimar los valores de biodiversidad y analizar las asociaciones entre especies.
2. Materiales y métodos
Área de estudio
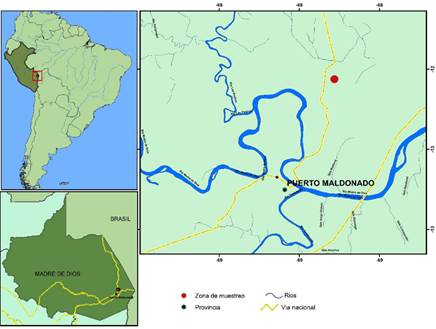
El estudio se realizó sobre en un del Rodal Semillero Fundo “El Bosque” con un área total de 425 Ha (Longitud -75°7’27”, latitud 12° 28’ 13”), propiedad de la Universidad Nacional Amazónica de Madre de Dios - UNAMAD, localizada a 30 minutos aproximadamente de la ciudad de Puerto Maldonado, en el sector Loboyoc, Distrito de las Piedras, Provincia de Tambopata, Departamento Madre de Dios, Perú (Figura 1). Es un de un bosque de terrazas o tierra firme, (terraza alta) (Araujo-Murakami et al., 2011). Actualmente se encuentra en estado de conservación; después que el 100% del área fuera sometida a tala selectiva de especies valiosas.
El rango de altitud esta entre los 200 y 210 m.s.n.m, son áreas poco inundables y presentan pendientes moderadas a bajas y pertenece a una zona de vida de Bosque húmedo sub tropical (BH-st) en transición a BHT (Holdridge & Tosi, 1967). La precipitación media anual es de 2000 mm, con una marcada estación seca de mayo a noviembre y una época lluviosa entre octubre y marzo (Pallqui, 2013). La temperatura media anual es de 25°C con presen cia de vientos fríos entre los meses de junio y agosto. En los suelos hay una variedad de clases, generalmente arcillo arenosos y de coloración rojiza, el material consiste en depósitos marinos del terciario, suelos profundos y bien drenados (Quispe Villafuerte, 2010).
Protocolo de muestreo
El muestreo se realizó durante los años 2016 - 2017 a través de bloques, siguiendo la metodología “BIOTROP” representada por 5 bloques (Vallejo-Joyas et al., 2005), en cada bloque, se establecieron dos parcelas rectangulares o transectos en banda de 20 m x 500 m, que se ubicaron perpendicularmente al alineamiento base y dispuestas en forma lineal generando un total de 10 sub-parcelas rectangulares de 1 hectárea en total (Reátegui Alván, 2015). Se registraron el diámetro, altura y especie de todos los individuos con dap ≥ 10 cm. Durante el inventario en campo, la determinación florística fue realizada a través de guías rápidas de identificación y apuntes sobre evaluaciones anteriores. Posteriormente, en el herbario Alwyn Gentry de la UNAMAD, las muestras botánicas de los individuos inventariados fueron identificadas hasta el nivel de especie (Quinto Mosquera & Moreno Hurtado, 2014).
Análisis de Datos
Para determinar la composición florística, los individuos fueron clasificados en familia y especie, en una lista general, cabe resaltar la importancia de la base de datos de identificación botánica del herbario Alwyn Gentry, que cuenta con una colección superior a 300 especies entre árboles, palmeras y arbustos.
En el caso de la estructura forestal, los datos de diámetros, altura fueron ordenadas en matrices de abundancia por parcela y especie, para generar un análisis conjunto; se graficó el histograma de la distribución de individuos por altura y clase diametrica para su interpretación; posteriormente, se calculó el índice de valor de importancia (IVI), que determina los pesos ecológicos en el bosque de las especies, valiéndose de la sumatoria de los registros de abundancia, frecuencia y dominancia de cada especie, que se expresan de manera relativa (Mijares-Santana & Pérez-Buitrago, 2018).
La diversidad arbórea alfa fue estimada aplicando el índice de alfa de Fisher “S” y Shannon-Wiener “H´” (Spellerberg & Fedor, 2003) por ser de los métodos más utilizados y confiables (Thukral, 2017; Diewert, 2013; Carmona & Carmona, 2014). Para la diversidad beta, se utilizó la distancia de Jaccard y el método de agrupación de Ward por cada 2 parcelas que conformó un bloque, representado en un dendrograma, que da un peso igual a todas las especies y valora la presencia de especies raras (Niwattanakul et al., 2013). Para el análisis computacional se utilizó el paquete Biodiversity R (Kindt & Coe, 2005), Vegan (Oksanen, 2019) y ggplot2 (Wickham, 2016) del software estadístico libre de R Project.
3. Resultados y discusión
Composición florística
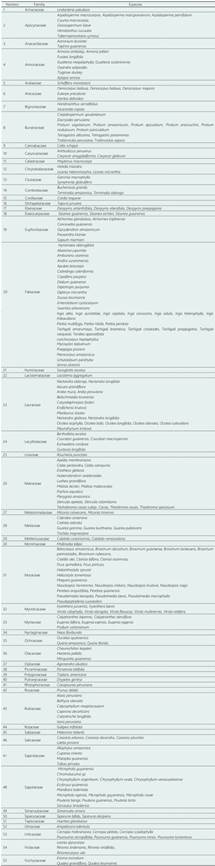
En las 10 parcelas de 1 ha, se identificaron un total de 4429 árboles ≥ 10 cm de DAP, distribuidos en 251 especies, 161 géneros y 55 familias. Las familias más abundantes con el mayor número de individuos, con mayor número de géneros y especies son: Moraceae, Arecaceae, Burseraceae, Fabaceae, Myristicaceae, Lauraceae, Urticaceae, Siparunaceae, Sapotaceae, Malvaceae y Annonaceae. Algunos de los géneros más abundantes estuvieron representados por. Pseudolmedia, Tetragastris, Euterpe, Iryanthera, Brosimum, Siparuna, Ocotea, Tachigali, Protium, Inga, Cecropia, Virola, Pourouma, finalmente Melisoma. Y en las especies más abundantes estuvieron representadas por: Tetragastris altissima, Euterpe precatoria, Iriartea deltoidea, Siparuna decipiens, Brosimum lactescens, Pseudolmedia laevis, Iryanthera laevis, Iryanthera juruensis, Cecropia sciadophylla, Tachigali vasquezii Pipoly, Pseudolmedia laevigata, el resumen de los datos se muestra en la Tabla 1 y Figura 3.
Esta composición y por tanto la diversidad, es producto de cambios en la comunidad vegetal, debido al ambiente y los gradientes geográficos como los impactos del hombre (Gentry, 1988). Por ejemplo, la estacionalidad de la humedad influye en la composición de la comunidad ya que las altas precipitaciones amplifican el nicho de espacio disponible para las plantas tolerantes a la sombra (Butt et al., 2008). En los bosques de terrazas de la región Madre de Dios dominan las familias Fabaceae, Moraceae y Arecaceae, estos tienen baja diversidad, pero elevada importancia por su amplia distribución, tal como fue evidenciado en estudios previos realizados por Dueñas y Garate-Quispe; esto es característico de los bosques húmedos tropicales, que a nivel mundial son dominados por la familia Fabaceaes y algunas leguminosas, como el género Inga también en bosques de llanuras aluviales (de Assis et al., 2017). Y comparte la mayoría de géneros más representativos del bosque de tierra firme en la provincia de Tambopata; así tienen una amplia distribución también en otros diferentes tipos de bosques de la región (Baez et al., 2017; Cueva-Altamirano, 2014).
Las especies Tachigali amarumayu, T. vasquezii y Tachigali poeppigiana Tul, son especies limitadas a los bosques amazónicos de Madre de Dios y las zonas aledañas de Bolivia y Brazil (Huamantupa et al., 2017 ), por otra parte, Ocotea bofo, es una especie de gran distribución en las zonas amazónicas tanto de bosques inundables como no inundables (Daza, 1998).
Estructura del bosque
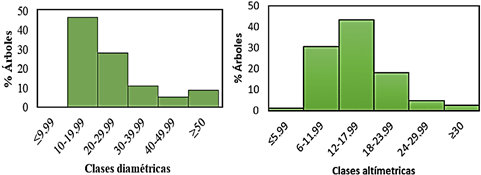
La estructura horizontal fue organizada en 6 clases diamétricas separadas cada 10 cm; donde las frecuencias relativos del número de individuos fueron: clase de 10 - 19,99 cm con 46,67%, clase de 20 - 29,99 cm con 28,04% y clase de 30 - 39,99 cm con 10,95%, como se observa en la parte izquierda de la Figura 2, hay una mayor cantidad de individuos jóvenes, y va decreciendo hacia las clases diamétricas mayores que representan a los individuos maduros, este patrón es diferente a los bosques del mismo tipo, pero mejor conservados (Pardo-Molina et al., 2020). La estructura vertical como se ve en la parte derecha de la misma figura, muestra 5 clases altimétricas; separadas cada 5 m; constituido por tres estratos principales, y las siguientes frecuencias relativas de números de individuos: clase de 6 -11,99 m con 30,41%, clase 12 - 17,99 m con 43,49%, clase de 18 - 23,99 m con 18,6%, en este caso se observa un patrón de distribución de altura diferente a una curva normal, con una asimetría positiva hacia la derecha, presentando un patrón ya conocido para los bosques tropicales, con mayor cantidad de árboles en las menores clases altimétricas (Marrero Mendoza, 2014). Esto posiblemente a que la deforestación a menudo no resulta en la pérdida inmediata de especies, y las comunidades pueden exhibir un proceso de "relajación" a su nuevo equilibrio con el tiempo (Rosa et al., 2016), este y otros impactos antrópicos son factores relevantes en la diversidad de árboles, hábitats tropicales (Janssen et al., 2018), y reestructura comunidades enteras (Norris, 2016).
Tabla 2 Estimación de Índices de diversidad alfa de Shannon-Wiener y α-Fisher para las 10 parcelas y el promedio de estas
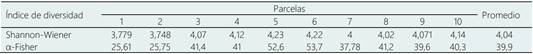
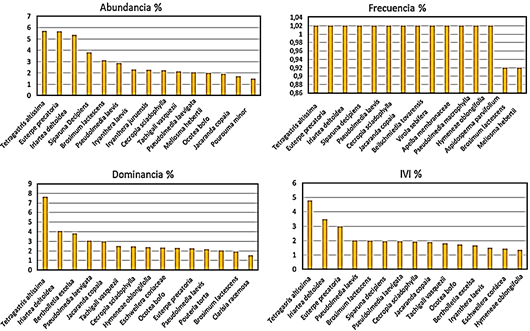
Figura 3 Histograma de las 15 especies más importantes según su abundancia relativa, frecuencia relativa, dominancia relativa e índice de valor de importancia relativa (IVI).
Del total del inventario, Fabaceae fue la familia más abundante. Solo nueve especies fueron muy abundantes en más de un área de estudio, mientras que 220 especies se registraron en una sola parcela. Las especies de mayor peso ecológico (IVI) o las que presentan un mejor desempeño crecimiento en la comunidad del bosque de tierra firme, se puede observar en la Figura 3. Como se observa en el análisis no siempre las especies más abundantes son las dominantes (Dueñas & Garate-Quispe, 2018).
Diversidad florística
La región de Madre de Dios, en Perú, es solo moderadamente diversa para los altos estándares de diversidad amazónicos, y compartiendo también especies catalogadas como comunes para bosques de terraza, como Pseudolmedia laevis muestra una dispersión efectiva en diferentes tipos de bosques, e Iriartea deltoidea una palmera, según la Figura 4 (Pitman et al., 2002). Tal como muestra la Tabla 2, a escala local la diversidad de especies y riqueza es menor comparado a otros sitios de la región amazónica peruana, que se encuentran en mejor estado de conservación (Villacorta-Flores, 2013). El impacto de las talas extractivas modificaron los parámetros estructurales indicando el predominio de bosque heterogéneo (García-Quintana et al., 2020), y con una homogenización de la comunidad florística favoreciendo especies de rápido crecimiento como la especies de Arecaceae como E. precatoria y I.deltoidea (Benjamin et al., 2015). Por tanto, el impacto de la actividad humana ha modelado la diversidad presente de los bosques en el mundo (Roberts et al., 2018, Walters et al., 2019), y es un indicador de la recuperación del bosque después de alguna actividad de aprovechamiento (Villa et al., 2018). Como en nuestro estudio, los coeficientes de diversidad de la Tabla 2 son menores en comparación a los reportes de Dueñas y Baez en bosques mejor conservados de la región Madre Dios.
De la Figura 4 presenta las siguientes características en los grupos de especies cercanas y lejanas por cada bloque:
En el bloque 1, la especie T. altissima está relacionado a las especies I. laevis, Siparuna decipiens, E. precatoria y también cercana la relación con las especies O. bofo, Jacaranda copaia, I. edeltoidea, C. scidophylla, Quiina Amazonica e Inga auristellae. Sin embargo, las especies T. vasquezii, Claricia racemosa, Virola sebifera, Aniba peruviana, Nectandra longifolia, Apeiba membranácea, Aspidosperma parvifolium, pertenecen a otro grupo más distante de T. altissima.
En el bloque 2, T. altissima, S. decipens, T. vasquezii, Psudolmedia laevigata, Ocotea aciphylla, E. precatoria, I. deltoidea, Brosimum lactescens, Iryanthera juruensis, Qualea grandiflora, P. laevis, A. membranacea están en el mismo grupo y un grupo cercano a este presenta las especies O. bofo, J. copaia, Beilschmiedia tovarensis, B. excelsa. Por otra parte, los grupos más distantes presentan las especies Aspirosperma parvifolium, C. racemosa, Hymenaea oblongifolia, Capirona decorticans, Rinoreo carpus, Inga heterophylla, Symphonia globulifera, Parkia pendula, Aspidosperma marcgravianum, Dipteryx micrantha y Xylopia serícea.
En el bloque 3, las especies P. laevigata, Neea floribunda, I. juruensis, Ocotea bofo, Brosimum lactescens, S. decipens, T. altissima, I. deltoidea, E. precatoria, T. vasquezii, C. sciadophylla son un grupo separado del resto por su elevada abundancia en las parcelas 5 y 6. Por otro lado, el resto de los grupos son más distantes y están conformados por: Meliosma hebertii, Virola sebifera, C. racemosa, B. excelsa, B. tovarensis, Eschweilera coriácea, A. membranaceae y J. copaia.
En el bloque 4, el grupo de T. altissima incluye a I. deltoidea y E. precatoria. El grupo más cercano está conformado por: J. copaia, Protium sagotianum, T. vasquezii, P. laevis, P. laevigata, C. sciadophylla, I. juruensis, Tachigali poeppigiana, A. membranácea, S. decipens y Meliosma hebertii. Los grupos más lejanos a T. altissima se conforman por: E. coriácea, Virola calophylla, V. sebifera, Nectandra longifolia, Clarisia biflora, Neea floribunda, Capirona decorticans e Inga alba.
En el bloque 5, en función al grupo de T. altissima, están presentes las especies: V. calophylla, J. copaia, Ocotea bofo, Neea floribunda, Pouruoma minor, Virola sebifera, Qualea grandiflora, B. lactescens, S. decipens, E. precatoria, P. laevis, Meliosma hebertii, I. deltoidea, I. juroensis, Inga auristellae, I. alba y P. sagotianum. Los grupos más alejados están conformados por: Aniba peruaviana, B. excelsa, Ficus gomelleira, A. parvifolium, Ocotea ovata, E. coriácea y Schefflera morototoni, A. membranácea y C. sciadophylla.
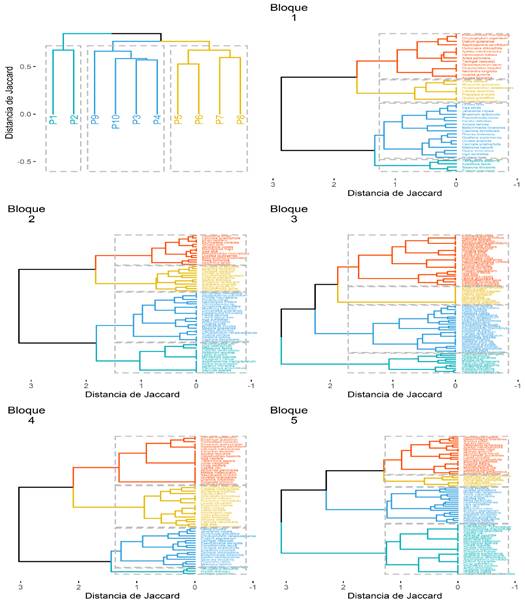
Figura 4 Dendrograma de las parcelas con el análisis de agrupamiento jerárquico utilizando el índice de disimilaridad de Jaccard y el método de agrupamiento Ward (Bloque 1: P1 - Parcela 1 / P2 - Parcela 2, Bloque 2: P3 - Parcela 3 / P4 - Parcela 4, Bloque 3: P5 - Parcela 5 / P6 - Parcela 6, Bloque 4: P7 - parcela 7 / P8 - parcela 8, Bloque 5: P9 - parcela 9 / P10 - parcela 10).
La evidencia que las parcelas fueron taladas en la Figura 4, donde una baja presencia de E. coriaceae, especialmente en los bloques 1 y 2 no se presenta, su presencia en los bloques 3, 4 y 5 es poco relevante, agrupándose con las especies raras de la parcela. El género Escheweilera es representativo de este tipo de bosque amazónico, debido talvez a que E. coriaceae puede habitar en zonas bajo estrés (Fernandes et al., 2020). Sin embargo, en la zona evaluada ya solo se encuentra una especie, que por la conservación de la zona empieza a dominar nuevamente el bosque (Bredin et al., 2020). También se observa en una alta frecuencia de T. altissima, E. precatoria e I. deltoidea en todos los bloques, esto se debe a una disposición suficiente de agua y nutrientes que, sumado a un incremento de luz, debido a talas modificaron el dosel y así promovieron el crecimiento y reclutamiento de individuos de palmeras y arboles rápido medianos (Sousa et al., 2020).
Por otra parte, la Figura 4 muestra que la diversidad de árboles recupera su exuberancia, con especies impactadas por la tala como B. lactescens y C. racemosa, que vieron limitado el reclutamiento de nuevos individuos, esto modifica profundamente su abundancia y frecuencia en los bloques (Marimon et al., 2020). La presencia de una gran diversidad de géneros como Aniba, Ocotea, Quiina, Aspidorsperma, Dypterix, Clarisia y Virola, distribuida de forma heterogénea. Estos patrones a escala global en la diversidad beta de los árboles se combinan con los cambios en la riqueza debido a la variación generada por el ensamblaje estocástico local (De Cáceres et al., 2012). Además, la abundancia y diversidad de especies pueden variar ampliamente en su fisonomía, composición de especies y ecología a pesar de que están bajo climas idénticos (Pennington et al., 2018), y probablemente, la elevada diversidad de estos bosques tropicales amazónicos, puede ser debido a su dinámica alta (Giacomotti & Reynel, 2018).
4. Conclusiones
El área de estudio es un bosque de amazónico de terrazas, que fue impactado por la tala selectiva. Posteriormente fue destinada para investigaciones forestales de la Universidad Nacional Amazónica de Madre de Dios, lo que permitió una recuperación de bosque y la mayor abundancia de especies pioneras. En total 4429 árboles se midieron, e identificaron 251 especies, 165 géneros y 55 familias.
La distribución de clases diamétricas y altura presenta patrones típicos de bosques intervenidos, en este caso por la extracción de madera décadas atrás. Las especies de mayor importancia ecológica fueron: Tetragastris altissima (Aubl.) Swart, Iriartea deltoidea Ruiz & Pav, Euterpe precatoria Mart., Tachigali vasquezii Pipoly, y Ocotea bofo Kunth, Bertholletia excelsa Bonpl, Eschweilera coriácea (DC.) S.A. Mori.
EL bosque inventariado tiene como promedio de los índices de biodiversidad son: Shannon-Wienner 4,039 ± 0,16 y α-Fisher 39,90 ± 9,23, por tanto, la información obtenida de los inventarios forestales es fundamental para el monitoreo, conservación y restauración de bosques amazónicos como medida de adaptación y mitigación al cambio climático.