Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Medica Herediana
versión impresa ISSN 1018-130Xversión On-line ISSN 1729-214X
Rev Med Hered v.19 n.4 Lima oct./dic. 2008
Choque cardiogénico en síndrome coronario agudo: causas, criterios diagnósticos, tratamiento y mortalidad en el Instituto Nacional del Corazón en Lima- Perú.
Cardiogenic shock in coronary acute syndrome: Causes, diagnostic criteria, treatment and mortality at the Instituto Nacional del Corazón in Lima – Peru.
Aranda Aguirre Ernesto Luis1, Reyes Díaz Jacqueline Vanessa1, Téllez Farfán David2.
1
Medico Cirujano. Facultad de Medicina Alberto Hurtado, Universidad Peruana Cayetano Heredia. Lima, Perú.2
Asistente del Servicio de Cardiología del Hospital Nacional Cayetano Heredia. Lima, Perú.
RESUMEN
Objetivo: Determinar las causas, criterios diagnósticos, tratamiento y mortalidad del choque cardiogénico (ChC) como complicación del síndrome coronario agudo (SCA) en el Instituto Nacional del Corazón, en Lima – Perú. Material y métodos: Se realizó un estudio observacional, descriptivo tipo serie de casos de fuentes secundarias en pacientes con diagnóstico de ChC por SCA del Instituto Nacional del Corazón desde febrero 2004 hasta 31 diciembre 2005. Para seleccionar los pacientes, se utilizaron las palabras clave: choque cardiogénico, balón intraaórtico (BIA) e infarto de miocardio agudo (IMA) más muerte. Los datos obtenidos de las historias clínicas seleccionadas, fueron procesados en el programa SPSS. Resultados: Se encontraron 24 pacientes. Veinte tuvieron ecocardiografía y 70,0%, presentaron disfunción ventricular izquierda (DVI) como causa de ChC, las demás fueron por complicaciones mecánicas. El 95% de pacientes tuvieron criterios clínicos (hipotensión o signos de hipoperfusión tisular); 11 tuvieron estudio hemodinámico, y cumplieron el criterio hemodinámico de choque. El tratamiento fue con vasopresores en 95,8% de los pacientes, inotrópicos en 66,7%, BIA en 50%. Trece pacientes tuvieron cinecoronariografia siendo revascularizados el 69,2%. Todos los pacientes fallecieron. Conclusiones: La causa principal de ChC fue DVI. El diagnóstico fue predominantemente clínico. El tratamiento en su mayoría fue médico y la tasa de mortalidad fue del 100%. Estos datos concuerdan con los descritos en otros estudios excepto que la mortalidad fue mayor en nuestro estudio. (Rev Med Hered 2008;19:138-144).
PALABRAS CLAVE: Choque cardiogénico, balón intraaórtico, infarto de miocardio, síndrome coronario agudo.
SUMMARY
Objective: To determine causes, diagnostic criteria, treatment and mortality of cardiogenic shock complicating coronary acute syndrome (CSCCAS), at the Instituto Nacional del Corazón Lima – Peru. Material and methods: Observational – descriptive (case series) study of secondary sources was conducted on patients with CSCCAS. To select patients we used key words: cardiogenic shock, intraaortic balloon pumping (IABP), myocardial infarction plus death. Data of clinic charts was analyzed in SPSS program. Results: We got 24 patients, 20 of them had echocardiographic study and 70% showed left ventricular dysfunction (LVD) as a cause of cardiogenic shock owing to coronary acute syndrome (myocardial infarction) and the rest were mechanical complications. 95% filled clinical criteria (including hypotension or signs of end organ hypoperfusion); 11 patients had hemodynamic study and all of them filled hemodynamic criteria. Treatment consisted on vasopressors in 95.8% of patients, inotropics in 66.7%, IABP in 50%. 13 patients had coronary angiographic study and 69.2% of them were revascularized. All the patients died. Conclusions: LVD was the main cause of CS. Diagnosis was predominantly clinical. Medical treatment were used in the majority of cases. Our results were similar to other studies except in mortality that was higher (100%). (Rev Med Hered 2008;19:138-144).
KEY WORDS: Cardiogenic shock, intraaortic balloon counterpulsation, myocardial infarction, coronary acute syndrome.
INTRODUCCIÓN
El síndrome coronario agudo (SCA) comprende un espectro de cardiopatías coronarias que incluyen angina inestable, infarto de miocardio con segmento ST elevado (IMASTE) e infarto de miocardio sin elevación del segmento ST (IMASTNE)(1). La complicación más temida del SCA es el choque cardiogénico (ChC), el cual es un estado de inadecuada perfusión tisular debido no sólo a una disfunción miocárdica sistólica, sino también a un síndrome de respuesta inflamatoria sistémica donde el óxido nítrico (NO) y sus derivados tienen efectos deletéreos (inhibición directa de la contractilidad miocárdica, supresión de la respiración mitocondrial en miocardio no isquémico, efectos en el metabolismo de la glucosa, efectos proinflamatorios, reducción de la respuesta de catecolaminas e inducción de vasodilatación sistémica)(2). Todo esto se da en el contexto de un infarto de miocardio agudo (IMA) (3).
El choque cardiogénico es la causa más común de muerte en pacientes hospitalizados con IMA, reportándose rangos de mortalidad que van del 50 al 80% (3) y afecta aproximadamente al 7% de pacientes con esta patología (4).
Los pacientes con ChC son a menudo de edad avanzada, hipertensos, diabéticos y tienen antecedente de IMA previo (5), lo que se refleja angiográficamente, demostrando enfermedad de tres vasos en 58%, dos vasos en 20% y enfermedad uniarterial en 22% (6). El ChC se asocia en un 55% a IMA anterior y 45% a otras localizaciones según el registro SHOCK (3,6).
Los criterios para el diagnóstico de ChC usados para el estudio SHOCK (SHould we emergently revascularize Occluded Coronaries for cardiogenic shocK) fueron:1) hipotensión, 2) evidencia clínica de hipoperfusión de órganos (oliguria, obnubilación del sensorio, frialdad y palidez de extremidades); 3) parámetros hemodinámicas y radiológicos confirmatorios: presión capilar pulmonar en cuña (PCWP) > 15 mmHg, índice cardiaco (IC) < 2,2 l/min/m2 (para IMA no anterior) o congestión pulmonar en una placa de tórax, con la confirmación hemodinámica para IMA anterior (5).
El ChC se da tanto en síndrome coronario agudo con segmento ST elevado (SCASTE) como ST no elevado (SCASTNE)(7,8). La incidencia de pacientes con SCASTE que desarrollaron ChC, en el estudio GUSTO II-b, fue casi el doble de los SCASTNE (4,43 y 2,56% respectivamente)(8).
Si bien en la gran mayoría de casos es causada por disfunción sistólica del ventrículo izquierdo, también puede ser causado por complicaciones mecánicas (regurgitación mitral aguda (RMA), ruptura de septum interventricular (RSIV), o ruptura de pared libre (RPL)), por infarto extenso del ventrículo derecho u otras causas. Es por eso que deben emplearse la ecocardiografía para definir anormalidades anatómicas y monitoreo hemodinámico invasivo.
La terapia para ChC está representada en la actualidad por tratamiento médico (inotrópicos y vasopresores), uso de balón intraaórtico (BIA), y revascularización de miocardio con angioplastía o cirugía cardiaca, ya que mejoran la sobrevida (9).
Por todo lo señalado, el ChC constituye la complicación más letal de los SCA y es un tema importante de salud pública. El Perú cuenta con un instituto especializado en el manejo de enfermedades cardiovasculares (INCOR), el cual se integra de una unidad de cuidados coronarios (UCC), unidad de cuidados intensivos post operatorio, unidad de hemodinámica . Sin embargo por motivo de logística, la sala de hemodinámica no atiende las 24 horas.
El objetivo del estudio fue determinar las causas, criterios diagnósticos, tratamiento y mortalidad del choque cardiogénico en pacientes con sindrome coronario agudo en el instituto Nacional del Corazón, en Lima, Perú.
MATERIAL Y MÉTODOS
Se realizó un estudio observacional, descriptivo tipo serie de casos de fuentes secundarias en pacientes mayores de 18 años que fueron diagnosticados de choque cardiogénico por SCA, hospitalizados en el Instituto Nacional del corazón (INCOR), desde 1º febrero del 2004 al 31 de diciembre del 2005. Se hizo una búsqueda en el libro de registro de la unidad de cuidados coronarios (UCC) y se seleccionó a los pacientes con las siguientes palabras claves: choque cardiogénico, uso de BIA e IMA más muerte. Se excluyeron a los pacientes con ChC de otras causas como miocarditis, cardiomiopatía terminal, contusión miocárdica, bypass cardiopulmonar prolongado, shock séptico con severa depresión miocárdica, insuficiencia aórtica aguda, regurgitación mitral aguda no causada por ruptura de músculo papilar, causas de obstrucción del tracto de salida y del llenado de ventrículo izquierdo. Se revisaron las historias clínicas de los pacientes seleccionados.
Los criterios para el diagnóstico de IMA fueron: criterios enzimáticos (creatinina fosfoquinasa isoenzima MB o troponina elevadas), más cualquiera de los siguientes criterios: síntomas isquémicos, cambios electrocardiográficos que indiquen isquemia o intervención arterial coronaria (10). Se utilizó la clasificación utilizada en los estudios SHOCK y GUSTO I para definir la localización electrocardiográfica: V1-V4 anterior; II, III, AVF inferior; V5-V6 apical; I, AVL lateral; V1-V2 posterior.
En todos los pacientes seleccionados se utilizó un formato similar a la historia clínica de la institución para la obtención de las características demográficas; examen clínico; exámenes auxiliares como electrocardiograma (ECG) (al momento del diagnóstico del infarto); ecocardiografía y coronariografía (luego del diagnóstico de ChC) ; forma en que se hizo el diagnóstico de ChC, ya sea por criterio clínico (hipotensión o signos de hipoperfusión tisular), criterio hemodinámico (PCWP > 15 y/o IC < 2,2 l/min./m2) o criterio radiológico como congestión pulmonar en IM anterior (tomado luego del diagnóstico de ChC); y tratamiento instalado.
Los datos recolectados fueron ingresados al programa Microsoft Excel para Windows usando una codificación para cada variable (la cual fue revisada por dos expertos), siendo luego analizados con el software estadístico SPSS, donde se logró obtener promedio de las variables continuas con su respectiva desviación standard y frecuencia de las variables discretas expresados en porcentaje.
RESULTADOS
Se seleccionaron 52 pacientes del libro de registro de la UCC del INCOR con las palabras claves: ChC, uso de BIA o IMA más muerte; durante el período 1º febrero 2004 a 31 de diciembre 2005. De ellos, 24 cumplieron los criterios para ChC por IMA.
El 75% de los pacientes fueron del sexo masculino. La edad promedio fue 71,3±9,2 siendo en edad promedio varones 72,5± 8,7 años y en mujeres 70,9±9,6 años, no encontrándose diferencia significativa.
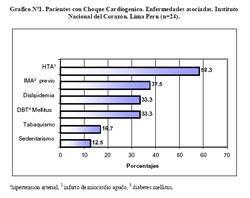
En el gráfico Nº1 se muestran los factores de riesgo para enfermedad coronaria, siendo hipertensión arterial (HTA), IMA previo, dislipidemia y diabetes mellitus (DM), los más frecuentes.
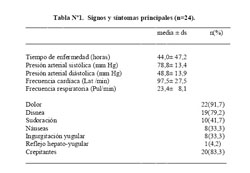
La tabla Nº1 muestra los síntomas y signos al ingreso. La presencia de dolor se observó en casi todos los pacientes a excepción de 2 en los que no hubo registro. El tiempo de instalación del choque fue de 44,0 horas en promedio.
El 62,5% de los pacientes con chC tuvo SCASTE y 37,5% SCASTNE.
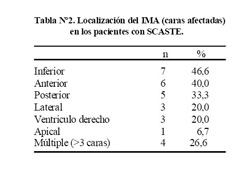
La tabla Nº2 muestra la localización del IMA en los pacientes con SCASTE.
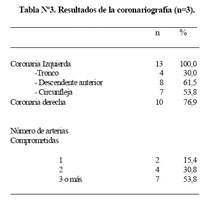
Se realizó coronariografía en 13 pacientes, de los cuales se presentó enfermedad multiarterial en la mayoría ( Tabla Nº3). En 11 pacientes no se realizó el estudio debido a inestabilidad hemodinámica o por limitaciones logísticas, por lo que ingresaron a la UCC donde desarrollaron disociación electromecánica y fallecieron.
En 20 pacientes (83,3%) se realizó ecocardiografía, la fracción de eyección fue 31,2 ±11,4%
La causa de ChC fue disfunción ventricular izquierda, en el 70% de los casos.
Seis pacientes presentaron complicaciones mecánicas (CM) post infarto de las cuales 3 presentaron ruptura del septum interventricular (con 87.3 horas como tiempo de enfermedad promedio) y fueron STE; 2 pacientes con regurgitación mitral aguda y uno con ruptura de pared libre.
El 95,8% cumplieron el criterio clínico para el diagnóstico de choque cardiogénico, siendo hipotensión el más frecuente (91,3%) ( Tabla Nº4). Sólo un paciente no fue contabilizado por tener malos registros, pero si cumplió el criterio hemodinámico.
Sólo 11 pacientes tuvieron estudio hemodinámico; el 100% presentó alteración en la presiòn capilar pulmonar en cuña (PCWP) 24,4 ± 12,8 en promedio del indice cardíaco 2,0 ± 0,5 en promedio.
Como criterio radiológico, congestión pulmonar fue documentada en un tercio de los pacientes, 50% de ellos presentó IM anterior.
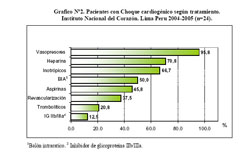
En el gráfico Nº2 se puede observar la distribución de los pacientes según el tratamiento recibido. En 23/24 (95,8%) se usaron vasopresores (dopamina, adrenalina o noradrenalina). Inotrópicos en 66,7% (dobutamina en 11 pacientes, levosimendán en 3 pacientes y ambos en 2 pacientes). BIA se utilizó en 50% de los pacientes, siendo el tiempo promedio de su uso 32,2 horas ± 25,9. En 5 pacientes se usó trombolíticos, 3 recibieron estreptoquinasa y 2 activador de plasminógeno tisular (t-PA).
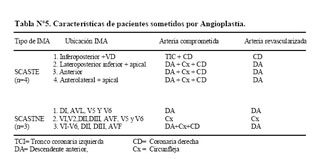
Nueve pacientes fueron sometidos a procedimientos de revascularización en 6 se practicó angioplastía, en 2 cirugía y en uno ambas. En los pacientes que se realizó cirugía, 2 presentaron como complicación mecánica ruptura del septum interventricular y el otro fue operado post angioplastía. De los cuatro que no fueron sometidos a revascularización: tres pacientes tuvieron descompensación hemodinámica durante el procedimiento, uno de los cuales hizo paro cardiaco en sala de hemodinámica y los 2 restantes pasaron a la UCC para su estabilización y cirugía ulterior, desarrollando disociación electromecánica y fallecieron. El otro paciente presentó lesión de tronco en un 90%, por lo que tuvo indicación quirúrgica.
En la tabla Nº5 se observa algunas características de los pacientes que fueron sometidos a angioplastía.
DISCUSIÓN
En nuestro estudio encontramos que muchos de los datos obtenidos concuerdan con los reportados en varios otros como SHOCK, PURSUIT, TRACE Y GUSTO I y GUSTO II, GUSTO III, sobretodo lo relacionado a causas, criterios de diagnóstico y tratamiento (farmacológico y uso de BIA)
La edad de presentación de los pacientes fue similar al encontrado en el SHOCK Registry (5). Se ha descrito que la edad avanzada es un factor de riesgo para el desarrollo de choque cardiogénico (11,12). Asimismo, en nuestro estudio encontramos que fue mas frecuente en el sexo masculino (75.0%) como sucedió también en el estudio mencionado (59,7%) (5). Un punto importante sobre las características demográficas halladas en nuestro trabajo es la similitud en frecuencia de pacientes con HTA (58,3%), DBM (33,3%), y IM previo (37,5%) comparado con el estudio SHOCK Trial Registry (5).
El tiempo promedio de la aparición de choque en post infarto de miocardio fue de 44 horas lo que es similar al encontrado en el registro de evaluación cardiaca Trandolapril (TRACE), donde 59% de los pacientes desarrollaron choque dentro de las 48 horas post infarto y 30% en 5 días (4).
La presión arterial sistólica promedio al ingreso y la frecuencia cardíaca encontradas en nuestro estudio estudio fue similar al hallado en el SHOCK Registry (5). En el ensayo de terapia trombolítica en IMA STE del GUSTO I y GUSTO III (12), estas dos variables fueron predictoras mayores de choque cardiogénico.
El tipo de infarto fue catalogado ST elevado en 62,5% coincidiendo con lo reportado por Holmes DR Jr, quien señala que la incidencia de ChC en IMA ST no elevado es menor, aproximadamente 50% de los vistos en el ST elevado (4,7,8).
Con respecto a la localización del infarto, los hallazgos de nuestro estudio difieren del registro del ensayo clínico SHOCK, donde las localizaciones fueron en su mayoría anterior (55%) inferior (46%) y lateral (32%) (3,6).
El compromiso multiarterial como lesión de tres o más arterias demostrado por angiografía fue lo mas frecuente en nuestro estudio (53,8%); valor similar al estudio de Hochman JS, quien encuentra enfermedad de tres vasos en 58%(6).
La literatura muestra que ChC debido a infarto de miocardio se da principalmente por disfunción ventricular izquierda en el 78,5%, seguido de complicaciones mecánicas, como se muestra en el estudio SHOCK (incluidos ambos grupos de pacientes del ensayo clínico como del registro) (5), lo cual es similar a nuestros hallazgos. La RSIV ocurrió en tres pacientes, dos con infarto de cara inferior y uno de cara anterior. Otros autores refieren que existe mayor frecuencia de RSIV en los tipos de infarto antes mencionados (13,14). En un estudio se encontró enfermedad de varios vasos (15) y otro mostró que 57% tenían lesión en un vaso (con mayor frecuencia la DA) (16). El tiempo de enfermedad de nuestros pacientes fue similar al encontrado en otros estudios (13,16).
La fracción de eyección promedio reportada en el SHOCK Trial Registry, la cual fue catalogada como inesperadamente alta, fue 31% (5), similar al encontrado en nuestro estudio.
En cuanto al criterio de diagnóstico empleado se pudo evidenciar que casi todos los pacientes en los que se documentó criterio hemodinámico (90,9%) tuvieron criterio clínico de ChC, por lo que cabría preguntarse si es necesario realizar cateterismo al corazón derecho para llegar al diagnóstico.
Hay que señalar que tanto en nuestro estudio como en el SHOCK Trial Registry(5) hipotensión no se presentó en la totalidad de los pacientes, sin embargo, tenían signos de hipoperfusión tisular (17); sugiriendo que esta se daría incluso sin hipotensión.
En cuanto al tratamiento, en los pacientes revascularizados, se encontró relación entre los hallazgos angiográficos y la arteria responsable del infarto. Como tratamiento farmacológico se usaron vasopresores en 95,8%, y dopamina en 100%; datos muy similares a los encontrados en el registro estudio SHOCK.
La tasa de mortalidad de los pacientes de nuestro estudio fue el 100%, diferente al estudio SHOCK. Como todo estudio descriptivo y retrospectivo de fuente secundaria, una limitante importante es la calidad de los registros de los pacientes.
REFERENCIAS BIBLIOGRÁFICAS
1. Braunwald E, Antman E, Hochman J, et al. ACC/AHA guidelines for the management of patients with unstable angina and non-ST- myocardial infarction. J Am Coll Cardiol 2001;38:294-5. [ Links ]
2. Judith S, Hochman M. Cardiogenic shock complicating acute myocardial infarction: Expanding the Paradigm. Circulation 2003;107:2998-3002. [ Links ]
3. Hochman J, Boland J, Sleeper L, et al. Current spectrum of cardiogenic shock and effect of early revascularization on mortality. Results of an International Registry. SHOCK Registry Investigations. Circulation 1995;91:873-81. [ Links ]
4. Holmes D. Cardiogenic Shock: A letal complication of acute myocardial infarction. Rev Cardiovasc Med 2003;4:131-135. [ Links ]
5. Hochman J, Buller C, Lynn A, et al. Cardiogenic shock complicating acute myocardial infarctionetiologies, management and outcome: a report from the SHOCK Trial Registry. JACC 2000;36(3)1063-1070. [ Links ]
6. Hochman J. Cardiogenic shock: Annual Scientific Sessions.Dallas,TX: American Heart Association; 1998. [ Links ]
7. Holmes D, Bates E, Kleiman N, et al. Contemporary reperfusion therapy for cardiogenic shock: the GUSTO-I trial experience. The GUSTO-I Investigators. Global Utilization of Streptokinase and Tissue Plasminogen activator for occluded coronary arteries. J Am Coll Cardio 1995;26:668-674. [ Links ]
8. Holmes D, Berger P, Hochman J, et al. Cardiogenic shock in patients with acute ischemic syndromes with and without ST-segment elevation. Circulation 1999; 100:2067-2073. [ Links ]
9. Bates E, Stomel R, Hochman J, Ohman E. The use of intraaortic balloon counterpulsation as an adjunct to reperfusion therapy in cardiogenic shock. International journal of cardiology 1998;65:S37–42. [ Links ]
10. Menon V, Hochman J. Management of cardiogenic shock complicating acute myocardial infarction. Heart 2002;88:531-537. [ Links ]
11. Kasper D, Braunwald E, Fauci A, Hauser S, Longo D, Jameson J. Harrisons principles of Internal Medicine. 15th ed. New York: McGrawl Hill; 2005. p.1448. [ Links ]
12. Hasdai D, Califf R, Thompson T, et al. Predictors of cardiogenic shock after thrombolytic therapy for acute myocardial infarction. J Am Coll Cardiol 2000;35:136. [ Links ]
13. Topaz O, Taylor A. Interventricular septal rupture complicating acute myocardial infarction: from pathophysiologic features to the role of invasive and noninvasive diagnostic modalities in current management. Am J Med 1992;93:683-688. [ Links ]
14. Mann J, Roberts W. Acquired ventricular septal defect during acute myocardial infarction: analysis of 38 unoperated necropsy patients and comparison with 50 unoperated necropsy patients without rupture. Am J Cardiol 1988;62:8-19. [ Links ]
15. Radford M, Johnson R, Daggert W, et al. Ventricular septal rupture: a review of clinical and physiologic features and an analysis of survival. Circulation 1981;64:545-553. [ Links ]
16. Crenshaw B, Granger C, Birnbaum Y, et al. Risk factors, angiographic patterns, and outcomes in patients with ventricular septal defect complicating acute myocardial infarction. Circulation 2000;101:27-32. [ Links ]
17. Menon V, Slater JN, White HD, et al. Acute myocardial infarction complicated by systemic hypoperfusion without hypotension: report of the SHOCK trial registry. Am J Med 2000;108:374. [ Links ]
Correspondencia
Jacqueline Vanessa Reyes Diaz
Correo electrónico: jvrd81@yahoo.com