Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Medica Herediana
versión impresa ISSN 1018-130Xversión On-line ISSN 1729-214X
Rev Med Hered vol.30 no.3 Lima jul. 2019
http://dx.doi.org/10.20453/rmh.v30i3.3587
REPORTE DE CASO
Uso de anhidrido carbónico como medio de contraste en la arteriografía y en ultrasonido intravascular en el implante endovascular de prótesis en aneurisma de aorta abdominal en paciente con insuficiencia renal. Reporte de caso
Use of carbon dioxide as a contrast medium for arteriography and intravascular ultrasound in endovascular prothesis of an abdominal aneurism in a patient with renal insufficiency. A case report
Fernando Bautista Sanchez 1,a, Carlos Zuñiga Luna 1,a, Daniel Silva Ñaupari 1,a, Wernher Cuya Ochoa 1,a, Oscar Soto Béjar 1,b
1 Servicio de Cirugía Cardiaca y Vascular Periférica, Hospital Nacional Guillermo Almenara Irigoyen, EsSalud. Lima, Perú.
a Asistente de Cirugía de Tórax y Cardiovascular; b Residente de Cirugía de Tórax y Cardiovascular.
RESUMEN
El EVAR (endovascular aortic replacement) es una técnica mínimamente invasiva para el tratamiento de los aneurismas de aorta abdominal (AAA). A pesar de ser una técnica muy útil en pacientes complicados, se ve restringida en pacientes con enfermedad renal crónica avanzada (ERCA) y en alérgicos a los medios de contraste yodados usados para el procedimiento. El objetivo del reporte fue describir el uso seguro y eficaz de la arteriografía con CO combinada con IVUS (intravascular ultrasound) en el implante de prótesis endovasculares para AAA en un paciente con ERCA y alérgico a los contrastes yodados. Se realizó la recopilación de datos de historia clínica para la descripción del procedimiento y resultados postoperatorios. El uso de la arteriografía con CO y el IVUS en el EVAR constituye una alternativa útil en pacientes que presentan AAA con ERCA y alérgicos al contraste yodado, con resultado post operatorio adecuado.
PALABRAS CLAVE: Procedimientos endovasculares, angiografía aortica, ultrasonografía intravascular. (Fuente: DeCS BIREME).
SUMMARY
The endovascular aortic replacement (EAR) is a minimally invasive technique for the treatment of abdominal aortic aneurisms. Despite of being a very useful technique it is restricted in patients with advanced chronic kidney disease and in patients allergic to iodine based contrast. The objective of this report is to describe the safe and effective use of arteriography using carbon dioxide combined to intravascular ultrasound in the endovascular aortic replacement of an aortic aneurism in a patient with renal insufficiency and history of allergy to iodine based contrasts. A review of the clinical chart of a patient who underwent this procedure was performed.
KEYWORDS: Endovascular procedures, aortic angiography, intravascular ultrasonography. (Source: MeSH NLM).
INTRODUCCIÓN
Un aneurisma de aorta abdominal (AAA) es definido como la dilatación de la arteria mayor al 50% de su diámetro normal medido en sentido antero- posterior o transverso (1). La prevalencia de los AAA está entre 4% y 7,2% en mayores de 65 años (1). La principal complicación de los aneurismas es la ruptura que lleva a una mortalidad perioperatoria de hasta 45% (2). La indicación de tratamiento quirúrgico de los aneurismas está establecida cuando el diámetro total se encuentra por encima de los 5,5 cm (3) o al presentar un crecimiento mayor de 1cm de diámetro por año, o desarrollo de sintomatología (1), mientras mayor sea el diámetro, mayor es el riesgo de ruptura (2).
Desde la descripción de Dubost en 1951 de la endoaneurismorrafia usando un injerto heterólogo y posteriormente con prótesis sintéticas, la reparación de los aneurismas evolucionó hasta fines del siglo pasado con la interposición de una prótesis endoluminal (stent recubierto) descrita por primera vez por Parodi en el año 1991, conocida por sus siglas como EVAR (Endovascular aortic replacement) (4), esta técnica utiliza contraste yodado para su visualización mediante fluoroscopia. Es una técnica mínimamente invasiva que en un principio permitía la reparación de aneurismas en pacientes principalmente con comorbilidades que aumentaban el riesgo de complicaciones y mortalidad perioperatoria empleando la técnica quirúrgica convencional. Sin embargo, como cualquier procedimiento quirúrgico o invasivo, no está exenta de complicaciones (5-7).
La insuficiencia renal avanzada puede verse empeorada con la exposición a medios de contraste yodados debido a la nefrotoxicidad asociada, aumentando la morbimortalidad o la necesidad de requerir diálisis de forma permanente (8-9).
El objetivo del reporte fue describir el uso del CO como medio de contraste alternativo para arteriografía, y del IVUS (ultrasonido intravascular) como un método imagenológico complementario en el implante de endoprótesis EVAR en un paciente con AAA infrarrenal y enfermedad renal crónica avanzada (ERCA) (10).
PRESENTACIÓN DEL CASO
Varón de 84 años natural y procedente de Lima, con factores de riesgo cardiovasculares hipertensión arterial (HTA), dislipidemia y sedentarismo, con antecedente de enfermedad arterial periférica desde hace 10 años, post operado de revascularización de miocardio hace 15 años, y de laparotomía por peritonitis secundaria a apendicitis aguda hace 10 años.
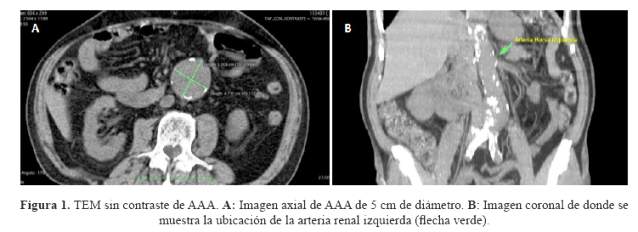
El paciente fue evaluado y seguido en consultorio externo de cirugía cardiovascular desde el 2010, presentando un AAA de 3,7 cm de diámetro, estable en su crecimiento. Tres años después, se evidenció un aneurisma de 4,1 cm, es decir un crecimiento de 0,4 cm (0,13cm/año), además se detectó aumento de la creatinina sérica hasta 1,92 mg/dl. Diez meses después, ingresó por emergencia por un cuadro de dolor abdominal, se le realizó TEM (tomografía espiral multicorte) sin contraste el cual mostró AAA infrarrenal de 5,0 cm de diámetro, correspondiente a un crecimiento de 0,9 cm/año (figura 1). Los exámenes de laboratorio mostraron: hemoglobina 12,9 g/dl, hematocrito 39,6%, creatinina 2,19 mg/dl, urea 56,8 mg/dl, y glucosa 89 mg/dl. El paciente fue hospitalizado en el Servicio de Cirugía Cardiaca y Vascular Periférica, sometido el caso a junta médica se decidió hacer el implante de una endoprótesis aórtica bifurcada bimodular con uso de CO2 como medio de contraste y con uso complementario de IVUS por presentar un abdomen hostil por antecedente quirúrgico e insuficiencia renal progresiva. El paciente fue intervenido en forma electiva.
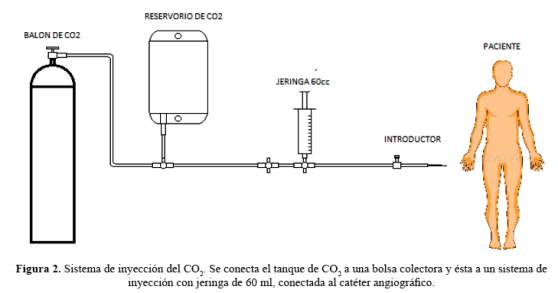
Se realizaron incisiones inguinales en ambos lados y por punción a visión directa de las arterias femorales comunes (AFC) se instalaron los introductores. A través la AFC derecha y con guía fluoroscópica se introdujo una guía de 0,035 pulgadas y 2,60 m, por donde se montó un catéter angiográfico tipo pig tail centimetrado de 5F; se ascendió hasta la aorta suprarrenal dejando una guía extra rígida de 0,035 pulgadas por 2,60 m para el soporte de la prótesis. Por el lado izquierdo se posicionó otro catéter pig tail centimetrado con un dispositivo de inyección adaptado. Para la aplicación del contraste se diseñó un dispositivo en base a una bolsa colectora de orina donde se coleccionó el gas, se aplicaron bolos de CO2 con una jeringa de 60 ml (figura 2). Por el lado izquierdo se introdujo una guía extra rígida de 0,035 por 2,60 m por donde se introdujo el catéter IVUS para verificar y marcar la imagen angiográfica de la posición exacta de los ostium de las arterias renales. Se reposicionó el catéter pig tail en el lado izquierdo para control angiográfico. Se procedió a retirar el introductor 7F del lado derecho para instalar un introductor 22F, por donde se desplegó el cuerpo de la prótesis de 31 mm por 150 mm por 14 mm.
Se realizó control angiográfico con CO2 para corroborar la posición de la prótesis con respecto a las arterias renales. Se retiró el introductor 8F y se intercambió por un introductor 12F para colocar la extensión de la prótesis de 14 mm por 120 mm.
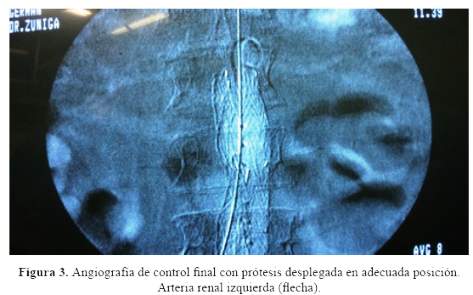
A través de la guía extra rígida se montó y desplegó un balón de acomodación a nivel de la zona de acople de los módulos de la prótesis y las zonas de anclaje aórtico e iliaco bilateral. Se realizó control radiológico obteniéndose un resultado posicional adecuado con lo cual se concluyó el procedimiento (figura 3).
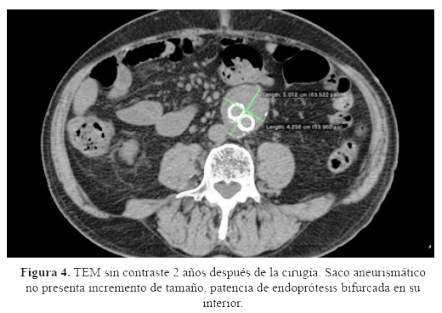
Los controles de laboratorio post operatorios fueron: creatinina 2,0 mg/dl, Hb 11,5gr/dl y leucocitos 14 200 sin desviación izquierda, cuyo valor se redujo a valores normales en el día 2 postoperatorio. El tiempo en la Unidad de cuidados intensivos (UCI) fue de un día y el alta se indicó al 4to día postoperatorio. En el seguimiento ambulatorio se evidenció ausencia de crecimiento del aneurisma a los 30 días y a los 2 años después de la cirugía, evaluado por TEM sin contraste (figura 4).
DISCUSIÓN
La insuficiencia renal es una comorbilidad importante que contribuye a aumentar la morbilidad y mortalidad luego del tratamiento del aneurisma de aorta abdominal, tanto por técnicas convencionales como endovasculares. Los mecanismos de injuria renal perioperatoria son múltiples, desde la manipulación de la aorta que desprende microémbolos a las arterias renales, clampaje suprarrenal en aneurismas yuxtarenales, ligadura de vena renal izquierda, caídas tensionales, stress oxidativo, apoplejía, politransfusión, síndrome de reperfusión, entre otros (11).
El EVAR, a pesar de que hace diez años era contraindicado en el manejo de pacientes con AAA y ERCA, explicado por la manipulación intraluminal, nefrotoxicidad por el contraste yodado, uso de medicamentos nefrotóxicos, deshidratación y manejo deficiente perioperatorio, ha sido revalidado por estudios recientes que han demostrado menor frecuencia de complicaciones agudas en comparación con la técnica convencional. Sin embargo, siempre existe el riesgo de agravar la ERCA y desencadenar un cuadro de insuficiencia renal aguda (IRA) (12).
La IRA ocurre entre 1,7% y 2,2% de pacientes sometidos a una arteriografía con contraste yodado, siendo los factores predisponentes el volumen del contraste, enfermedad renal previa y diabetes mellitus. Algunos estudios la consideran una complicación no benigna con una mortalidad en pacientes con enfermedad renal previa de 34% y en pacientes sin enfermedad renal 7% (13).
El paciente presentado tenía ERCA secundaria a HTA y a uropatía obstructiva (adenoma de próstata), sin criterios de hemodiálisis cuyos niveles de creatinina aumentaron en tres años de seguimiento. Las características anatómicas del AAA permitían evaluarlo con tomografías sin contraste.
Las consideraciones que se tuvieron en cuenta para decidir el tratamiento de urgencia por abordaje endovascular fueron: el paciente sintomático con una aorta de 5 cm de diámetro, y crecimiento del aneurisma de 1 cm/año (fase expansiva), asociado al antecedente de un abdomen hostil. Sin embargo, estaba de por medio el uso del contraste durante el implante.
El servicio tenía experiencia en el uso de CO2 para arteriografías periféricas diagnósticas, por lo que en junta médica se planteó su uso como medio de contraste y el apoyo con IVUS. El CO2 es un gas que puede ser usado como medio de contraste con mucha seguridad sin riesgos de alergia o nefrotoxicidad. Al aplicar CO2 la sangre es desplazada por el gas a diferencia del medio de contraste que se mezcla a esta, pueden inyectarse bolos de hasta 60 ml por disparo, para luego disolverse en la sangre 23 veces más rápido que el oxígeno, siendo eliminado rápidamente a través de los pulmones por difusión gaseosa. Síntomas neurológicos como convulsiones y pérdida de la conciencia, y paro respiratorio, son complicaciones que pueden presentarse por su uso, recomendándose no realizar angiografías por encima del diafragma (13).
Hawkins en 1982, describió por primera vez el uso del CO2 y la angiografía con sustracción digital con propósitos diagnósticos (14); sin embargo, la experiencia de esta técnica con propósitos terapéuticos aún no estaba bien establecida.
Chao (15) en el 2007, publica un estudio comparativo de 100 pacientes sometidos a EVAR, en un grupo con enfermedad renal (84 pacientes) en quienes usó CO2, y otro sin enfermedad renal en quienes uso contraste. Los resultados del implante fueron exitosos en ambos grupos sin variación de su creatinina en el postoperatorio inmediato y a 30 días (10), a pesar que en el grupo de ERCA se usó 27 ml de contraste para corroborar las imágenes obtenidas con CO2 de las arterias renales.
Morito (16) en el 2005, describió un caso de uso de IVUS y angiografía con CO2 para el implante de endoprótesis en un paciente con aneurisma inflamatorio y alérgico al contraste, con un resultado post operatorio adecuado. El IVUS ha sido reportado como una alternativa en el implante de endoprótesis que ayuda a reducir el volumen del contraste y la exposición a la radiación con una visualización de la anatomía endoluminal y la posición de las arterias permitiendo un adecuado implante.
Una vez realizada la angiografía con CO2 se corroboró el origen de las arterias renales con el IVUS, esto fue de mucha utilidad ya que permitió que lográramos desplegar la prótesis de forma segura y sin ocluir los ostium, con un tiempo operatorio de dos horas.
La revisión de la literatura y los resultados observados nos permite afirmar que EVAR con CO2 e IVUS, es una excelente alternativa en pacientes con enfermedad renal crónica avanzada o alérgicos al contraste, minimizando las complicaciones del uso del contraste yodado con una buena visualización y abordaje seguro de las estructuras vasculares.
REFERENCIAS BIBLIOGRÁFICAS
1. Moll FL,Powell JT, Fraedrich G, et al. Management of abdominal aortic aneurysms clinical Practice Guidelines of the European Society for Vascular Surgery. Eur J Vasc Endovasc Surg. 2011; 41:1-58. [ Links ]
2. Bowman MJ, Sutton NJ, Bell PRF, et al. A meta- analysis of 50 years of ruptured abdominal aortic aneurysm repair. Br J Surg. 2002; 89:714-730. [ Links ]
3. Ballard DJ, Filardo G, Fowkes G, Powell JT. Surgery for small asymptomatic abdominal aortic aneurysm. Cochrane Database Syst Rev. 2008;4: 1835. doi: 10.1002/14651858.CD001835.pub2 [ Links ]
4. Parodi JC, Palmaz JC, Barone HD. Transfemoral intraluminal graft implantation for abdominal aortic aneurysms. Ann Vasc Surg. 1991; 5:491-499. [ Links ]
5. Greenhalgh RM, Brown LC, Kwong GP, et al. Comparison of endovascular aneurysm repair with open repair in patients with abdominal aortic aneurysm (EVAR trial 1), 30-day operative mortality results: randomised controlled trial. Lancet. 2004; 364(4):843-8. [ Links ]
6. Prinssen M, Verhoeven EL, Buth J, et al. A randomixed trail comparing conventional and endovascular repair of abdominal aortic aneurysm. N Engl Med. 2004; 351:1607-18. [ Links ]
7. Lederle FA, Freishlag JA, Kyriakides TC, et al. Outcomes following endovascular vs open repair of abdominal aortic aneurysm: a randomized trial. JAMA. 2009; 302:1535-42. [ Links ]
8. Johnston KW. Multicenter prospective study of nonruptured abdominal aortic aneurysm; Part II:Variables predicting morbidity and mortality. J Vasc Surg. 1989; 9: 437-477. [ Links ]
9. Olsen PS, Schroeder M, Perko M, et al. Renal failure after operation for abdominal aortic aneurysm. Ann Vasc Surg. 1990; 4:580-583. [ Links ]
10. Chao A, Major K, Subramanyam RK, et al. Carbon doxide digital subtraction angiography-assisted endovascular aortic aneurysm in the azotemic patient. J Vasc Surg. 2007; 45:451-460. [ Links ]
11. Wijnen MH, Cuypers Ph, Buth J, et al. Differences in renal response between endovascular and open repair of abdominal aortic aneurysms. Eur J Vasc Endovasc Surg. 2001; 21:171-174. [ Links ]
12. Mehta M, Veith F, Lipsitz E, et al. Is elevated creatinine level a contraindication to endovascular repair? J Vasc Surg. 2004; 39: 118-123. [ Links ]
13. Eschelman D, Sullivan KL, Bonn J, Gardiner GA. Carbon dioxide as contrast agent to guide vascular interventional procedures. Am J Roentgenol. 1998; 171:1265-1270. [ Links ]
14. Hawkins IF. Carbon dioxide digital subtraction arteriography. Am J Roentgenol. 1982; 139:19-24. [ Links ]
15. Chao A, Major K, Kumar SR, et al. Carbon dioxide digital subtraction angiography-assisted endovascular aortic aneurysm repair in the azotemic patient. J Vasc Surg. 2007; 45(3):451-8. [ Links ]
16. Morito H, Katsuyuqui H, Hosaka A, et al. Endovascular surgery for inflamatory abdominal aortic aneurysm with contrast allergy-usefulness of carbon dioxide angiography and intravascular ultrasound: A case report. Ann Vasc Dis. 2012; 5:104-108. [ Links ]
Declaración de financiamiento y de conflictos de intereses: El estudio fue financiado por sus propios investigadores.
Contribución de autoría: FBS; CZL; DSÑ; WCO: concepción de la idea, participó del planeamiento, ejecución y seguimiento del paciente y la cirugía practicada. Participó en
Correspondencia:
Oscar Soto Béjar
Jirón Max Radiguetti 212, C-002,
Correo electrónico: osoto20@hotmail.com
Teléfono: 51 997111891
Recibido: 09/01/2017
Aceptado: 26/04/2019













