INTRODUCCIÓN
Desde su descubrimiento en 1963, la lipoproteína (a) (Lp (a)) presenta mayor relevancia en la práctica clínica debido a la sólida asociación entre el aumento de Lp (a) y la enfermedad cardiovascular (ECV)/ enfermedad coronaria y estenosis valvular aórtica calcificada 1. Esta lipoproteína está compuesta por una partícula similar a la LDL con una molécula de apolipoproteína B-100 (ApoB-100) y la apolipoproteína (a) (Apo (a)) 2,3.
Se han propuesto mecanismos fisiopatológicos subyacentes a su potencial efecto aterotrombótico, entre ellos destacan: 1) su infiltración directa en la íntima, uniéndose a la matriz extracelular a través de la ApoB-100 y la Apo (a); 2) aumenta la expresión de moléculas de adhesión y citoquinas proinflamatorias;3) la Lp (a) es más propensa a oxidarse, promoviendo la formación de células espumosas y el depósito de colesterol; 4) la inhibición de la cascada fibrinolítica; la Apo (a) inhibe la activación del plasminógeno bloqueando la formación de plasmina, y estimula la trombogénesis al bloquear la función del inhibidor de la vía del factor tisular 1,3,4,5. La Lp (a) es más aterogénica que la LDL porque contiene los componentes proaterogénicos de LDL, y la Apo (a), que potencia la aterotrombosis 4,5,6,7.
A pesar de que el papel de la Lp (a) como factor de riesgo cardiovascular es conocido, no se incluye su medición dentro del perfil lipídico convencional (3) y tampoco existen terapias específicas aprobadas en las guías de práctica clínica vigentes, lo cual podría cambiar con el desarrollo de tratamientos emergentes que se encuentran actualmente en fase de estudio 8.
Se reporta el caso de un varón de 49 años, sin factores convencionales de riesgo cardiovascular, que desarrolló infarto agudo de miocardio (IAM). Tras la evaluación, se identificó la elevación sérica de Lp (a) como único agente etiológico. El objetivo del reporte fue destacar la importancia de la detección y análisis de la Lp (a) para la evaluación del riesgo cardiovascular.
PRESENTACIÓN DEL CASO
Varón de 49 años, sin antecedentes de factores de riesgo cardiovascular, ingresó por dolor precordial de inicio brusco y de curso agudo. Al ingreso, el examen físico mostró a un varón de constitución mesomórfica (talla: 170 cm; peso: 73 kg; índice de masa corporal: 25,3 kg/m2). Se encontró PA: 130/90 mm Hg; FC: 105 lpm; FR: 20 rpm; Sat O2: 99% y T: 36,5°C. El resto de la exploración física no fue contributorio.
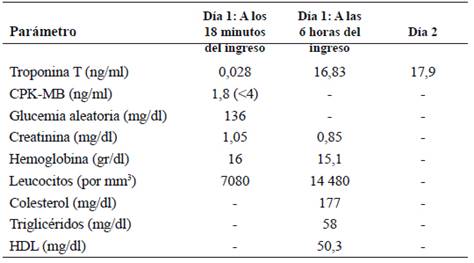
El primer electrocardiograma (ECG) (Figura 1) evidenció ondas T hiperagudas en V2-V4. La radiografía de tórax no mostró cambios significativos. El primer examen de laboratorio mostró hemoglobina 16 gr/dl, leucocitos 7 080 x mm3, creatinina 1,05 mg/ dl, glucemia (aleatoria) 136 mg/dl (había tomado desayuno una hora antes) y creatina quinasa MB (CK-MB) 1,8 ng/ml (tabla 1). El valor de troponina T ultrasensible (TnT-us) fue de 0,028 ng/ml (VN < 0,014 ng/ml). Se administró aspirina 200 mg; ticagrelor 180 mg y enoxaparina 80 mg. La cinecoronariografía mostró oclusión total proximal de la arteria descendente anterior (ADA), lesión ostial del 60% en la rama diagonal 1 (figura 2 (A)) y lesión del 70% en la arteria circunfleja. Se diagnosticó síndrome isquémico coronario agudo con elevación del ST (SICACEST): IAM anterior, por lo que se efectuó angioplastia e implante de stent medicado en la arteria descendente anterior (Figura 2 (B)).
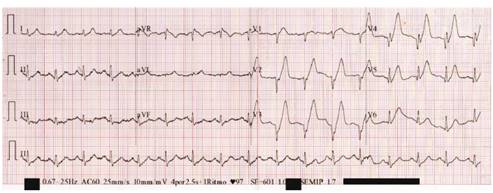
Figura 1 ECG de emergencia (A los 8 minutos del ingreso): FC:100. Ritmo sinusal regular. Eje QRS 60°. Intervalo PR: 160 ms. Complejo QRS:100 ms. QT: 360. QTc: 460 ms. Ondas T hiperagudas en V2-V4.
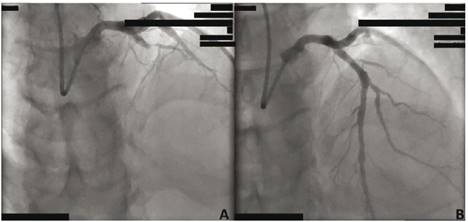
Figura 2 Cinecoronariografía (A la hora y 30 minutos del ingreso). (A): Oclusión total proximal de la arteria descendente anterior y lesión ostial de 60% en la rama diagonal 1. (B): Lesión perfundida post angioplastia e implante de stent medicado.
El paciente ingresó a la unidad de cuidados intensivos (UCI) en condiciones estables. El segundo ECG post angioplastia demostró leve elevación de ST y ausencia de ondas R en V1-V4 (Figura 3). En el segundo examen laboratorial mostró leucocitosis y el valor de TnT-us en 16,83 ng/ml (tabla 1). Al segundo día del ingreso, el valor de TnT-us mostró un pico de 17,9 ng/ml (Tabla 1); al tercer día, el ECG mostró ondas T invertidas en V2-V5, DI y aVL y ondas QS en V1-V4 (Figura 4). El ecocardiograma de reposo mostró una fracción de eyección de 42% con aquinesia del tercio medio y apical del septum.
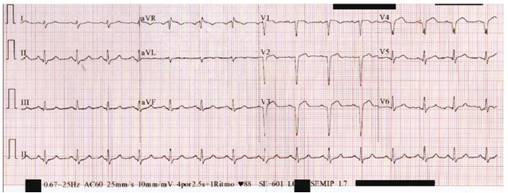
Figura 3 ECG Post angioplastia (A las 2 horas y 18 minutos del ingreso). FC: 93. Ritmo sinusal regular. Eje QRS 150°. Intervalo PR: 160 ms. Complejo QRS:100 ms. QT: 360 QTc: 460 ms. Elevación del ST en V1-V4. Ausencia de ondas R en V1-V4.
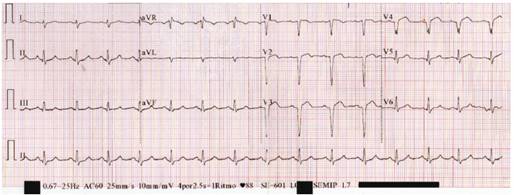
Figura 4 ECG al tercer día del ingreso. FC: 83 Ritmo sinusal. Eje QRS 60°. Intervalo PR: 160 ms. Complejo QRS:98 ms. QT: 340 QTc: 400 ms. Onda T invertida en V2-V5, DI y aVL.
El riesgo de ECV estimado de acuerdo a las guías de la Sociedad Europea de Cardiología (ESC)9 y el Colegio Americano de Cardiología (ACC)10 fue un bajo riesgo cardiovascular. Se le prescribió bisoprolol 5 mg c/24 h, valsartán 80 mg c/12 h, aspirina 100 mg c/24 h, ticagrelor 90 mg c/12 h y atorvastatina 80 mg; luego, fue dado de alta sin mayores complicaciones. Se buscó la presencia de factores de riesgo no convencionales por lo que se evaluó la Lp (a), mostrando valores elevados (71,2 mg/dl).
DISCUSIÓN
La Lp (a) es considerada un factor de riesgo de enfermedad vascular aterosclerótica, principalmente cuando sus concentraciones son >30 mg/dl. Los niveles de Lp (a) están determinados genéticamente en un 90%; mientras que la dieta y el ejercicio tienen un efecto mínimo sobre esta lipoproteína 4,11. Anteriormente, se creía que la Lp (a) no representaba un valor de riesgo cardiovascular cuando el C-LDL era controlado. Sin embargo, investigaciones recientes han demostrado que la Lp (a) elevada sigue siendo un factor de riesgo incluso en personas con un C-LDL <70 mg/dl 2,3,7.
Las calculadoras de riesgo cardiovascular de la ESC y el ACC presentan ciertas limitaciones ya que fueron elaboradas y validadas en poblaciones europeas y estadounidenses, respectivamente; sin embargo, las características de la población y de los factores de riesgo en América del Sur implican una sobreestimación o subestimación del resultado mediante el uso de estos algoritmos 9,10. La Organización Panamericana de la Salud (OPS) ha presentado recientemente una herramienta para calcular el riesgo cardiovascular, mediante una app disponible para celulares y computadoras. A diferencia de las calculadoras de la ESC y la ACC, estima el riesgo individual de incidencia en 10 años de IAM, ACV o muerte cardiovascular en las regiones de América (Andina, Caribe, Central, Norte y Sur) con la selección del país de procedencia y los datos de colesterol total en sangre, sexo, edad, tabaquismo, diabetes y presión arterial sistólica 12.
Se presenta un paciente varón con una estimación de bajo riesgo cardiovascular (2% de probabilidad de sufrir un evento cardiovascular en 10 años) según los algoritmos de estimación de riesgo de la OPS, ESC y ACC, diagnosticado de IAM anterior. Como único agente potenciador del riesgo cardiovascular, se identificó un nivel elevado de la Lp (a). Al alta, se le prescribió bisoprolol, valsartán, aspirina, ticagrelor y atorvastatina. De ellos, la atorvastatina (inhibidor de HMG-CoA reductasa o estatinas), es indispensable en la terapia aterosclerótica; sin embargo, su impacto sobre la Lp (a) es controvertido. Varios estudios muestran un incremento de la Lp (a) en 10-20% tras su administración 2,5,7,9.
Actualmente, existen fármacos que modifican las concentraciones de Lp (a). Entre estos, destacan IONIS-APO(a) y Mipomersen que pertenecen al enfoque prometedor de la terapia anti sentido. Estos son oligonucleótidos dirigidos contra el ARNm de Apo (a) en el núcleo de los hepatocitos, inhibiendo así su síntesis. Estudios de fase 1 y 2 mostraron tasas de reducción de Lp (a) de hasta el 80% 2,5,7.
Este reporte refuerza la recomendación en la guía de la ESC/EAS de 2019 en medir la Lp (a) una vez en la vida de cada persona dentro del perfil lipídico, para mejorar la precisión de los algoritmos de cálculo de riesgo cardiovascular y obtener un valor que refleje la probabilidad real de padecer un evento cardiovascular en aquellas personas con Lp (a) elevada. El enfoque actual para la atención de pacientes con esta alteración se basa en el control óptimo del perfil lipídico (LDL, colesterol no-HDL y triglicéridos), ya que las alternativas de tratamiento son limitadas. Asimismo, es necesaria la introducción de nuevas terapias farmacológicas emergentes en la práctica clínica para la disminución del riesgo de cardiopatía coronaria 7,9,13,14.