Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú v.31 n.3 Lima jul./set. 2011
GUÍA CLÍNICA
Guía de práctica clínica sobre el diagnóstico y tratamiento de la diarrea aguda infecciosa en pediatría Perú – 2011
Clinical practice guidelines on the diagnosis and treatment of infectious acute diarrhea in children Peru - 2011
Carlos Gonzales S.*
; Carlos Bada M.** ; Raúl Rojas G.* ; Guillermo Bernaola A.*** ; Carlos Chávez B.** Instituto Nacional de Salud del Niño
.** Hospital de Emergencias Pediátricas.
*** Hospital Suárez-Angamos, EsSalud.
RESUMEN
Guía de Práctica Clínica sobre el Diagnóstico y Tratamiento de la Diarrea Aguda Infecciosa en Pediatría del Perú es una información resumida sobre la definición criterios de inclusión y exclusión epidemiología y etiología de la diarrea infecciosa; considerando aspectos en el dignóstico y tratamiento (desidratación, tratamiento antibiótico, tratamientos de apoyo), soporte nutricional criterios de transferencias y alta y aspectos de prevención.
PALABRAS CLAVES: Diarrea Aguda infecciosa, pediatría, diagnóstico, tratamiento.
ABSTRACT
The Clinical Practice Guidelines cover the Diagnosis and Treatment of Acute Diarrhea in Pediatric Infectious is a consice information about definition, inclusion and exclusion criteria; epidemiology and etiology of infectious diarrhea. The guidelines cover aspects of diagnosis and treatment (dehydration, antibiotics, supportive therapy), nutritional support and other aspects of transferences and prevention.
KEYWORDS: Acute infectious diarrhea, pediatric, diagnosis, treatment.
1. RESUMEN
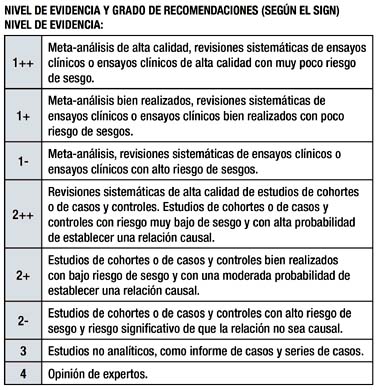
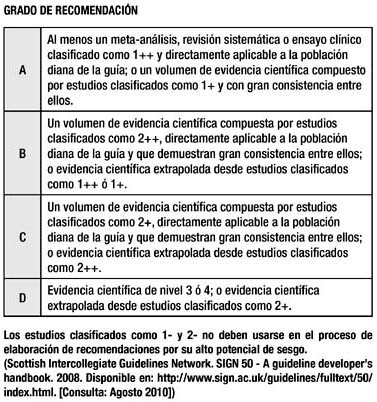
Las referencias están entre paréntesis y en superíndice. El nivel de evidencia en corchetes y el grado de recomendación está entre paréntesis con letras mayúsculas.
DEFINICIÓN: La Diarrea Aguda Infecciosa (DAI) se define como una disminución de la consistencia de las heces (blandas o líquidas) y/o un aumento en la frecuencia de las evacuaciones, con o sin fiebre o vómitos. La diarrea aguda suele durar menos de 7 días y no más de 14 días. En los primeros meses de la vida, un cambio en la consistencia de las heces es más indicativo de diarrea que el número de deposiciones.[3] Tener en cuenta que en niños con DAI los vómitos por lo general tiene una duración de 1-2 días, y en la mayoría se detiene en un plazo de 3 días.[3] Los términos enfermedad diarreica aguda, diarrea aguda infecciosa y diarrea infecciosa, se consideran sinónimos en el desarrollo de la presente guía.
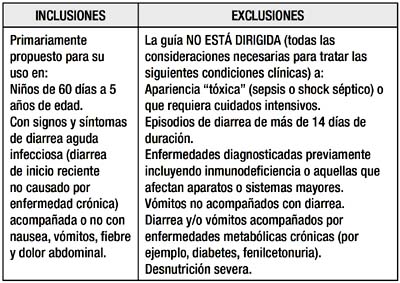
CRITERIOS DE INCLUSIÓN Y EXCLUSIÓN DE LA GUÍA: Criterios de Inclusión: Niños de 60 días a 5 años de edad, Con signos y síntomas de diarrea aguda infecciosa (diarrea de inicio reciente no causado por enfermedad crónica) acompañada o no con nausea, vómitos, fiebre y dolor abdominal. Criterios de Exclusión: La guía NO ESTÁ DIRIGIDA a pacientes con: Apariencia toxica o que requiera cuidados intensivos, episodios de diarrea de más de 14 días de duración, enfermedades diagnosticadas previamente incluyendo inmunodeficiencia o aquellas que afectan aparatos o sistemas mayores, vómitos no acompañados con diarrea, diarrea y/o vómitos acompañados por enfermedades metabólicas crónicas (por ejemplo, diabetes, fenilcetonuria), desnutrición severa.
RECOMENDACIONES
EPIDEMIOLOGÍA Y ETIOLOGÍA:
-
En diversos estudios a nivel mundial, el rotavirus fue el agente causal de diarrea más comúnmente aislado en todos los estudios. Las bacterias más frecuentes causantes de DAI fueron Campylobacter, E. coli y Salmonella. El Cryptosporidium fue el protozoario más detectado. [3]
-
En Europa: el rotavirus es el agente más frecuente de DAI. El agente bacteriano más común es el Campylobacter o Salmonella en función del país. [3]
-
En el Perú (estudio de cohortes, 1034 pacientes de 2 a 12 meses de edad, en 4 distritos de Lima) se aislaron con más frecuencia E. coli diarreogénica, Campylobacter y rotavirus (lactantes de ≥ 6 meses de edad). En niños mayores, E. coli difusamente adherente y E. coli enterotoxigénica fueron más frecuentemente aislados en muestras de diarreas que en los controles. [3]
-
En el Perú (2010), a la SE No 52 se han notificado 177 defunciones por episodios de diarrea aguda, en todas las edades. [3]
-
No hay evidencia suficiente para afirmar que las características clínicas del paciente y/o las macroscópicas de la diarrea sean de utilidad para el diagnóstico de la DAI. (B) Si bien un paciente con diarrea disentérica tiene alta probabilidad de ser portador de una diarrea de etiología bacteriana, también es cierto que no toda diarrea acuosa es de etiología viral.
-
En los pacientes con DAI, el uso rutinario del examen de heces no está recomendado.
Cuando se decide solicitar exámenes, la lactoferrina fecal es el de mayor rendimiento para determinar etiología bacteriana; al no contar con este examen en nuestro país, una alternativa es la suma de leucocitos fecales, la sangre oculta en heces o hematíes fecales y el estado clínico del paciente (A)
Si se sospecha un brote de diarrea viral, se debe solicitar exámenes para estudiarlo. (D) Cuando el estudio de la diarrea viral está indicado, la prueba de ELISA para rotavirus, es el examen de elección para el estudio de antígenos virales. (B)
DIAGNÓSTICO
CLÍNICA: GRADO DE DESHIDRATACIÓN, HOSPITALIZACIÓN Y SEVERIDAD
-
En pacientes con DAI, los signos que mejor rendimiento tienen para diagnosticar deshidratación son: mucosa oral seca, ojos hundidos, presencia del pliegue cutáneo, llenado capilar y alteración del estado de conciencia. (B) Dos o más signos hacen el diagnóstico.
-
Está indicada la hospitalización en cualquiera de las siguientes condiciones: shock, deshidratación severa (mayor de 9% de pérdida de peso corporal), alteración del estado de conciencia (letargia, convulsiones, etc.), vómitos intratables o biliosos, falla en la terapia de rehidratación oral, si los familiares no pueden proporcionar adecuado cuidado en casa y si en sospecha de patología quirúrgica. (B)
-
En los pacientes con DAI, son criterios de severidad: El llenado capilar prolongado, el signo del pliegue positivo, hipotensión arterial, las alteraciones del patrón respiratorio y del estado de conciencia. (B)
TRATAMIENTO
TRATAMIENTO DE LA DESHIDRATACIÓN
-
Está indicado iniciar la terapia de rehidratación oral en pacientes con DAI y en presencia de al menos dos signos clínicos de deshidratación. (A)
-
En pacientes con DAI y deshidratación, se recomienda hidratar por VO o por sonda nasogástrica (gastroclisis). (A)
-
Está indicada la terapia de hidratación endovenosa en pacientes pediátricos con DAI y deshidratación que presentan (B): Deshidratación severa/Deshidratación severa con Shock, deshidratación moderada e incapacidad de ser hidratado por vía enteral (vía oral o sonda nasogástrica) por vómitos persistentes o flujo de deposiciones "alto" (10mL/k/h), pacientes con co-morbilidades asociadas al tracto gastrointestinal (Intestino Corto, ostomías del intestino anterior), pacientes con íleo metabólico.
-
Cuando la hidratación por vía endovenosa está indicada, el volumen (cálculo de la pérdida de volumen de agua corporal), la solución y la duración de la hidratación (4 a 6 horas) son importantes para la recuperación del estado de hidratación del paciente. (A)
TRATAMIENTO ANTIBIÓTICO
-
La ciprofloxacina está indicada como terapia empírica de primera línea en los pacientes con sospecha de diarrea invasiva y además, deterioro del estado general. La azitromicina está indicada como terapia de segunda línea.(B)
-
La ciprofloxacina es el antibiótico de primera línea para los pacientes con DAI por Shigella. Son alternativas la azitromicina y la cefixima. (A)
-
La eritromicina es el antibiótico de primera línea (cuando está indicada) en pacientes con DAI por Campylobacter. (A)
-
La azitromicina es el antibiótico de primera línea en pacientes con DAI por Vibrio cholerae. (A)
-
No existe evidencia suficiente, para indicar de manera rutinaria, antibióticos en la DAI por Salmonella. (A)
-
La terapia antibiótica es controversial en pacientes con DAI por Escherichia coli enterohemorrágica. (A)
TRATAMIENTO COADYUVANTE
-
Existe evidencia suficiente para indicar Lactobacillus rhamnosus cepa GG y Saccharomyces boulardii como coadyuvantes en el manejo de la DAI. (A)
-
No hay evidencia suficiente que sustente el uso rutinario de racecadotrilo en pacientes con DAI. (A)
-
En zonas donde la mortalidad por DAI es importante, el zinc ha demostrado beneficios a dosis de 10 mg para menores de 6 meses y 20 mg en mayores, administrado por lo menos 14 días. (A)
-
En pacientes con DAI y vómitos persistentes, la administración de ondansetrón disminuye los vómitos, la necesidad de hidratación por vía EV y la necesidad de hospitalización. (A)
SOPORTE NUTRICIONAL
-
En los pacientes con DAI no se debe restringir la alimentación (lactancia materna, leche con lactosa, alimentos sólidos) ni alterar la calidad de los alimentos. (B)
CRITERIOS DE TRANSFERENCIA
-
El nivel de resolución del establecimiento de salud es importante para decidir la transferencia de un paciente con DAI. (D) La transferencia de un paciente con DAI a un nivel superior está indicada: Cuando hay signos o síntomas sugerentes de shock, cuando hay signos y/o síntomas que incrementan el riesgo de progresión hacia el shock, cuando las circunstancias sociales requieran supervisión de los profesionales de salud. [4]
CRITERIOS DE ALTA
-
El alta del paciente con DAI, se indica principalmente por criterios clínicos. (D)
-
El alta hospitalaria se puede considerar cuando: Se haya logrado la hidratación del paciente, lo cual se evidencia por la ganancia ponderal y la condición clínica, no se requieran fluidos endovenosos para hidratar al paciente, adecuada ingesta oral de fluidos para compensar las pérdidas, este asegurado un adecuado manejo por parte de los padres y el seguimiento médico sea factible.
PREVENCIÓN
-
El lavado de manos disminuye la prevalencia de diarrea en 50% y evita 1 millón de muertes anuales aproximadamente, la mejora en la calidad del agua y otras medidas higiénicas, deben ser aconsejados a los padres y cuidadores para evitar la DAI. (A)
-
La vacunación contra el rotavirus está aconsejada en los lactantes. (A)
-
Se debe recomendar: alimentar con lactancia materna exclusiva los primeros seis meses de vida, evitar el uso de biberones, mejorar las prácticas de manipulación de los alimentos y desechar las excretas de manera apropiada. (A)
EVIDENCIA E INFORMACIÓN DE APOYO PARA LAS RECOMENDACIONES
El Nivel de Evidencia y el Grado de recomendación utilizado se basaron en el SIGN. El proceso de toma de decisiones fue con la Metodología de grupo nominal en dos sesiones (paneles).
IMPLEMENTACIÓN, REVISIÓN Y ACTUALIZACIÓN
El Panel en su totalidad acordó adoptar el Plan de Implementación, Seguimiento y Actualización sugerido por el instrumento ADAPTE. El Plan de actualización se realizará a los 3 años (Actualización cada 3 años SIGN).
Ver la Guía completa para los detalles y evidencia de apoyo. La adherencia a las recomendaciones es voluntaria. La valoración final con respecto a la prioridad de cualquier procedimiento específico debe hacerse por el médico a la luz de las circunstancias individuales presentada por el paciente.

2. INTRODUCCIÓN
La tasa de Mortalidad infantil se utiliza como un indicador del nivel de calidad de vida de una población. Esta misma tasa, es la resultante del cuidado del bienestar en general y de la atención de la salud. Por ello, en el 2007, la Organización Mundial de la Salud (OMS – WHO de sus siglas en inglés), relaciona la tasa de mortalidad infantil con el nivel general de desarrollo de un país. (1)
La enfermedad diarreica constituye una de las primeras causas de mortalidad infantil en el mundo. En el 2008, la cantidad mundial de muertes por diarrea en niños menores de 5 años fue estimada en 1.87 millones (Intervalo de confianza al 95%: IC 95%: 1.56 – 2.19) lo cual constituye el 19% de las muertes en niños; las regiones de África y el Sureste asiático explican casi el 78% de las muertes (1.46 millones) de todas las muertes por diarrea ocurridas en el mundo en desarrollo; 73% de estas muertes, están concentradas sólo en 15 países. (2)[3]
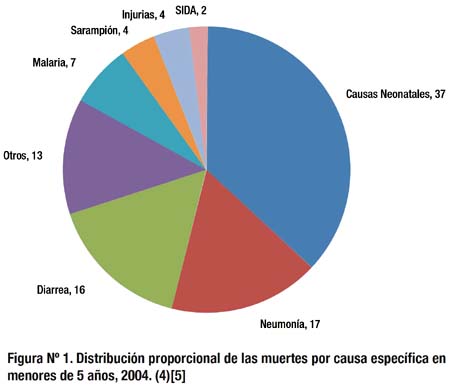
Cuando la mortalidad infantil en el mundo es distribuida por causas, se observa que las muertes atribuidas a la diarrea infecciosa ocupan los primeros lugares, luego de las causas neonatales. (3) Incluso, un análisis moderno como el relacionado a desarrollo ambiental, ubica a la diarrea infecciosa en primer lugar. (4)[5]
Las estadísticas del Ministerio de Salud (MINSA - Ofi cina General de Estadística e Informática) (5) reportan a la diarrea infecciosa como la tercera causa de consulta externa en todos los grupos etarios, hasta el año 2007. Por ello se entiende la importancia de contar con guías de práctica clínica de calidad que permitan mejorar la atención de nuestros pacientes pediátricos.
3. ALCANCE Y OBJETIVOS
La Guía de Práctica Clínica (GPC) tratará sobre la etiología, epidemiología, cuadro clínico, diagnóstico, tratamiento y prevención de la diarrea aguda infecciosa; en pacientes pediátricos de 2 meses a 5 años, en el ámbito de atención primaria y en el hospitalario a escala nacional.
OBJETIVO GENERAL:
-
Establecer recomendaciones basadas en evidencia para un adecuado diagnostico y manejo de la diarrea aguda infecciosa en el paciente Pediátrico.
OBJETIVOS ESPECIFICOS:
-
Optimizar la interpretación de los signos y síntomas clínicos.
-
Favorecer el uso apropiado de los métodos de ayuda diagnóstica.
-
Fomentar la adecuada categorización de la gravedad.
-
Identificar las complicaciones de la diarrea aguda infecciosa.
-
Mejorar la selección y el empleo apropiado de la terapia antibiótica.
-
Disminuir el porcentaje de pacientes con admisiones hospitalarias innecesarias.
-
Acortar los tiempos de estancia hospitalaria.
-
Disminuir la mortalidad por deshidratación causada por diarrea aguda infecciosa.
POBLACIÓN OBJETIVO:
USUARIOS OBJETIVO:
-
Personal Profesional y No profesional que atienden pacientes en los siguientes ámbitos:
-
Nivel Primario (Puestos y Centros de Salud)
-
Nivel Hospitalario (Consulta ambulatoria, Atención en Emergencia, Hospitalización)
4. METODOLOGIA PARA EL PROCESO DE ADAPTACIÓN
DESCRIPCIÓN DEL PROCESO DE ADAPTACIÓN
Se denomina Adaptación a la "aceptación parcial" (adecuación al contexto a ser empleado) de las GPCs, producidas en otro contexto (otros países o regiones) y Adopción a la "aceptación tal como está" de las mismas.(6) Así, en países donde los limitados recursos son un obstáculo para el desarrollo de GPCs, una opción es la adaptación de GPC conservando su calidad metodológica, con ello se evita duplicidad de esfuerzos en el mismo tema y es posible destinar los recursos disponibles a la gran labor de implementación de las mismas.
Se decidió por la adaptación de una GPC de gran nivel metodológico y aplicable a otro ámbito de salud, para respetar y conservar su alto nivel metodológico y obtener un material de gran calidad. En el proceso de adaptación la metodología se basó en el material proporcionado por la Colaboración ADAPTE, siendo el documento principal Resource Toolkit for Guideline Adaptation Version 2.0 que guió el desarrollo del proceso de adaptación.(7)
PREGUNTAS DE SALUD
POBLACIÓN: Pacientes con DAI (Edad: de 2 meses a 5 años, Género: ambos sexos. Condición clínica: pacientes con DAI con y sin deshidratación, Características clínicas: criterios de INCLUSIÓN y EXCLUSIÓN descritos).
INTERVENCIONES (Diagnóstico: clínico, Exámenes de laboratorio; Pronóstico: exámenes de laboratorio como reacción inflamatoria en heces, coprocultivo, hemograma, etc.; Tratamiento: medidas generales, hidratación, antibiótico; Prevención: inmunizaciones).
PROFESIONALES-PACIENTES (Asistenciales: médico general, médico residente de pediatría, pediatra, gastroenterólogo pediatra, infectólogo pediatra; Pacientes: diagnosticados con DAI, sin criterios de exclusión y sus familiares y/o representantes; Otros interesados: directores de hos pita les, jefes de departamento, autoridades de salud, etc.).
RESULTADOS (Pacientes: cura clínica, evitar casos de DAI, evitar complicaciones, uso racional de exámenes auxiliares, mejorar la adherencia al tratamiento; Sistema: disminuir la variabilidad en la práctica clínica, optimizar costos, mejorar la calidad de atención; Salud pública: disminuir la incidencia, disminuir la morbilidad, disminuir la mortalidad).
ÁMBITO (Nivel de atención: primario, consulta externa, hospitalización, emergencia; Contexto: nacional).
Las preguntas(22) se agruparon en 4 áreas principales para trabajar con las guías y plantear las respuestas a las mismas:
-
Epidemiología y Etiología (05)
-
Clínica
Tratamiento
Prevención
Preguntas planteadas según área de competencia:
DE EPIDEMIOLOGÍA Y ETIOLOGÍA:
-
Definición/definiciones de Diarrea Aguda Infecciosa (DAI).
-
¿Cuál es la Epidemiología de la DAI en Pediatría?
-
¿Son el grupo etario y/o las características macroscópicas útiles en la clasificación de la DAI?
-
En pacientes pediátricos con DAI ¿Cuándo solicitamos la reacción inflamatoria y/o antígeno viral? ¿Existe un punto de corte en reacción inflamatoria?
-
En pacientes pediátricos con DAI ¿Cuándo solicitamos cultivo en heces?
DE CLÍNICA:
-
En pacientes pediátricos con DAI ¿Cuáles son los signos de mejor rendimiento diagnóstico para determinar el grado de deshidratación?
-
En pacientes pediátricos con DAI ¿Cuáles son los criterios para hospitalización?
-
En pacientes pediátricos con DAI ¿Cuáles son los criterios de severidad?
DE TRATAMIENTO:
-
En pacientes pediátricos con DAI ¿Cuáles son los criterios para iniciar la Terapia de Rehidratación Oral (TRHO)?
-
En pacientes con DAI y deshidratación (DHT) ¿Cuáles son las indicaciones para la Terapia de Hidratación Endovenosa (THEV)?
-
¿La hidratación a través de Sonda Naso-gástrica (SNG) es tan efectiva como la THEV en pacientes con DAI y DHT Severa (DHTS)?
-
En pacientes con DAI y DHTS, ¿Cuál es el esquema de hidratación para la THEV?
-
En pacientes pediátricos con DAI ¿Cuándo iniciar tratamiento antibiótico empírico? ¿Qué antibiótico debería ser empleado de inicio?
-
En pacientes pediátricos con DAI ¿Se debe utilizar los Probióticos como terapia coadyuvante?
-
En pacientes pediátricos con DAI ¿Se debe utilizar los inhibidores de encefalinasa como terapia coadyuvante?
-
En pacientes pediátricos con DAI ¿Se debe utilizar los micronutriente (zinc) como terapia coadyuvante?
-
En pacientes pediátricos con DAI asociada a vómitos ¿Se debe utilizar los antieméticos como terapia coadyuvante?
-
En pacientes pediátricos con DAI ¿Se debe restringir algún tipo de alimento?
-
En pacientes pediátricos con DAI ¿Cuáles son los criterios de Transferencia, según nivel de atención?
-
¿Cuáles son los criterios de Alta en el paciente hospitalizado por DAI/DAI y DHT?
DE PREVENCIÓN:
-
¿Cuáles son las medidas higiénico-dietéticas deben impartirse para prevenir la DAI?
-
En pacientes pediátricos con DAI ¿Cuál es la efectividad y la disminución de la morbi-mortalidad con el empleo de la vacunación contra el rotavirus?
Estas preguntas buscan una respuesta al problema clínico desarrollado. La respuesta a tales preguntas son las RECOMENDACIONES de la Guía de Práctica Clínica.
BÚSQUEDA Y RECUPERACIÓN DE GUIAS DE PRÁCTICA CLÍNICA
Las guías recuperadas fueron seleccionadas teniendo en cuenta los siguientes criterios:
CRITERIOS DE INCLUSIÓN
-
Se seleccionaron guías basadas en evidencias.
-
Se seleccionaron guías nacionales o internacionales.
-
Se seleccionaron guías publicadas en los últimos 3 años, salvo que se trate de una guía de buena calidad metodológica y con buena presentación de la información.
-
Se seleccionaron guías escritas en cualquier idioma.
CRITERIOS DE EXCLUSIÓN:
-
Se excluyeron guías escritas por un solo autor.
-
Se excluyeron guías publicadas sin referencias.
La búsqueda de Guías de Práctica Clínica (GPC) se inició el 05-Agosto-2010 y terminó el 12-Agosto-2010.
Lo primero que se realizó fue la estrategia de búsqueda, la cual fue de la siguiente manera:
-
Determinación de las palabras claves. Las palabras claves que se emplearon fueron: Diarrhea, diarrhoea, gastroenteritis, "intestinal infections", dehydration, pediatr*, child*, infant*, toddler*, "Intravenous fl uid", "Ringers solution", "Saline solution", "Hypertonic solution", "Intravenous infusions" y "Hypotonic solution".
-
Selección de base de datos de Guías de Práctica Clínica. Priorizamos la búsqueda en bases de datos sugeridas por el manual ADAPTE y aquellas conocidas por su rigidez metodológica en la selección de sus datos. Las bases de datos consultadas fueron: SIGN (Scottish Intercollegiate Guidelines Network), NICE (National Institute for Health and Clinical Excellence) y se emplearon los siguientes buscadores: PubMed y Tripdatabase (Turning Research Into Practice).
-
Cuadro resumen de registros hallados. Se empleo una tabla para poder manejar con mayor facilidad las palabras clave y los enlaces hallados y poder visitarlos ante cualquier duda.
-
Búsqueda en las bases de datos. Basados en las palabras clave se procedió a realizar la búsqueda de las GPCs.
La búsqueda se inició en el SIGN (
http://www.sign.ac.uk/, revisado el 06 – Agosto – 2010) y en el NICE (http://www.nice.org.uk/, revisado el 07 – Agosto – 2010). Se emplearon los siguientes términos: Diarrhea, diarrhoea, gastroenteritis, tanto las palabras de manera aislada o la combinación de ellas. Por último, se buscó en el listado completo. En el SIGN no se hallaron GPCs sobre "gastroenteritis" o "diarrea" en pediatría. En el NICE se halló una GPC: National Institute for Health and Clinical Excellence. Diarrhoea and vomiting caused by gastroenteritis: diagnosis, assessment and management in children younger than 5 years. 2009.La búsqueda en PubMed (revisada el 10-Agosto-2010), se realizó con los siguientes términos: (Diarrhoea OR diarrhea OR Gastroenteritis OR "intestinal infections") AND (child* OR pediatr* OR infant* OR toddler*), que halló 51,200 documentos. Se aplicó el término: Type of article: Practice guideline, como límite y se obtuvieron 72 documentos. De estos documentos, 2 eran GPCs de utilidad con la búsqueda.
Registros recuperados de utilidad del PubMed:
-
European Society for Paediatric Gastroenterology, Hepatology, and Nutrition/European Society for Paediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe. Guarino A, Albano F, Ashkenazi S, Gendrel D, Hoekstra JH, Shamir R, Szajewska H; European Society for Paediatric Gastroenterology, Hepatology, and Nutrition; European Society for Paediatric Infectious Diseases. J Pediatr Gastroenterol Nutr. 2008 May; 46 Suppl 2:S81-122.
-
An evidence and consensus based guideline for acute diarrhoea management. Armon K, Stephenson T, MacFaul R, Eccleston P, Werneke U. Arch Dis Child. 2001 Aug; 85(2):132-42. Review (Resumen del documento original).
De igual forma se realizó la búsqueda en Tripdatabase (revisada el 11-Agosto-2010), con los siguientes términos: (Diarrhoea OR diarrhea OR Gastroenteritis OR "intestinal infections") AND (child* OR pediatr* OR infant* OR toddler*) mostró 1410 registros. Estos, al ser fi ltrados con el término "Guideline" mostró: Para "Australia & N Zelanda" 02 registros, para "Canada" 05 registros, para "Reino Unido" 19, "Norteamérica" 15 y "Otros" 02 registros, totalizando 44 registros.
Registros recuperados de utilidad del Tripdatabase:
-
En Reino Unido:
– An evidence and consensus based guideline for acute diarrhoea management. Armon K, Stephenson T, MacFaul R, Eccleston P, Werneke U. Arch Dis Child. 2001 Aug; 85(2):132-42. Review (Documento original). -
En Norteamérica:
– Cincinnati Childrens Hospital Medical Center. Evidence-based clinical care guideline for acute gastroenteritis (AGE) in children aged 2 months through 5 years. Cincinnati (OH): Cincinnati Childrens Hospital Medical Center; 2006 May. 15 p.
Los demás resultados no se consideraron debido que no eran del grupo etario (pediátrico).
A pesar de la fecha de elaboración de la GPC "An evidence and consensus based guideline for acute diarrhoea management" (2001) se seleccionó debido a su gran calidad metodológica. Ello no ocurrió con la GPC del Cin cinnati (2006).
Se elaboró una tabla resumen con las GPCs seleccionadas, para el tratamiento más práctico de las mismas.
EVALUACIÓN DE LA CALIDAD METODOLÓGICA DE LAS GUIAS
El resumen de la valoración con el instrumento AGREE (2001 – The Collaboration AGREE) es el siguiente:
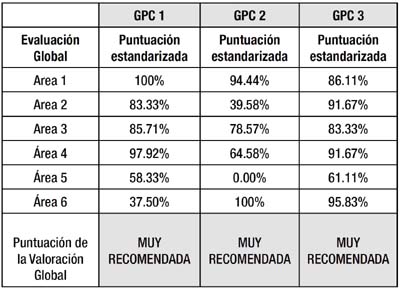
GUIA DE PRÁCTICA No 1: National Institute for Health and Clinical Excellence. Diarrhoea and vomiting caused by gastroenteritis: diagnosis, assessment and management in children younger than 5 years. London: NICE, 2009.
GUIA DE PRÁCTICA No 2: European Society for Paediatric Gastroenterology, Hepatology, and Nutrition/European Society for Paediatric Infectious Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe. 2008 May.
GUIA DE PRÁCTICA No 3: Armon K el al. An evidence and consensus based guideline for acute diarrhoea management. 2001 Aug. Arch Dis Childhood. Actualización 2005.
EVALUACIÓN DEL CONTENIDO Y CONSISTENCIA DE LAS GUIAS
Se construyó la matriz de recomendaciones con las preguntas clínicamente relevantes, teniendo en cuenta las 3 guías seleccionadas.
Cada guía usó un sistema diferente de clasifi cación de los niveles de evidencia y grados de recomendación. Para reclasificar la evidencia en el proceso de adaptación, se procedió a la lectura y valoración de los estudios que sustentan cada una de las recomendaciones, y se usó el sistema de clasificación del SIGN.
SELECCIÓN Y APROBACIÓN DE LAS RECOMENDACIONES
Para seleccionar, contextualizar y aprobar las recomendaciones se empleó la Técnica de Grupo nominal, un proceso de consenso formal, teniendo en cuenta tres vertientes de la evidencia: Investigación, Experiencia clínica y Situación de Salud. (8)
Los participantes del panel fueron seleccionados basado en los criterios recomendados por la bibliografía: Opinión aceptada en DAI, conocimiento en la investigación base y el interés en participar.
Se tuvo el cuidado suficiente para poder obtener y atender cualquier nueva evidencia que modificara las recomendaciones a plantearse. Las recomendaciones eran susceptibles a pequeñas modificaciones teniendo en cuenta tres criterios:
-
Vigencia del tema
-
Actualidad de la información sobre el tema
-
Relación con el ámbito de adaptación
La reunión de consenso para trabajar las recomendaciones permitió la discusión de las mismas, para ser incluidas en la presente Guía. Según se plantea en el documento ADAPTE, una vez construida la matriz de recomendaciones, el panel podía concluir lo siguiente: la GPC puede Rechazar la totalidad de la GPC, Aceptar la totalidad de la GPC, Aceptar las evidencia pero rechazar las interpretaciones derivadas, Aceptar recomendaciones específicas y Modificar recomendaciones específicas.
En el caso del proceso de adaptación de la presente Guía, se aceptó recomendaciones específicas y otras se modificaron a la luz de los conocimientos actuales, las características propias del ámbito de adaptación y opinión sustentada con elementos bibliográficos por los integrantes del panel.
Al final se construyó un proyecto de Guía adaptada, según formato sugerido por el documento ADAPTE. El producto final fue una Guía de Práctica Clínica de gran valor metodológico (9) y de ayuda a la toma de decisiones en DAI en pediatría.
5. RECOMENDACIONES
DEFINICIÓN, EPIDEMIOLOGÍA Y ETIOLOGÍA
a. DEFINICIÓN. La Diarrea Aguda Infecciosa (DAI) se define como una disminución de la consistencia de las heces (blandas o líquidas) y/o un aumento en la frecuencia de las mismas, con o sin fiebre o vómitos. (10,11) La diarrea aguda suele durar menos de 7 días y no más de 14 días. En los primeros meses de la vida, un cambio en la consistencia de las heces es más indicativo de diarrea que el número de deposiciones. [3] Tener en cuenta que en niños con DAI los vómitos por lo general tiene una duración de 1-2 días, y en la mayoría se detiene en un plazo de 3 días. [3] Los términos gastroenteritis enfermedad diarreica aguda, diarrea aguda infecciosa y diarrea infecciosa, se consideran sinónimos en el desarrollo de la presente guía.
b. ¿CUÁL ES LA EPIDEMIOLOGÍA DE LA DIARREA AGUDA INFECCIOSA (DAI) EN PEDIATRÍA? La DAI es la segunda causa de muerte en niños menores de 5 años y es responsable por la muerte de 1.5 millones de niños cada año, a nivel mundial. Los niños malnutridos o con la inmunidad comprometida tienen mayor riesgo de morir por diarrea. En los países en desarrollo, se reportan en niños menores de 3 años, un promedio de 3 episodios de diarrea por año. (12)
Aunque los resultados de diferentes estudios muestran la variación en la proporción de niños con DAI, se detectó que el rotavirus es la causa más común en los niños en todos los estudios. Los patógenos más frecuentes causantes de DAI bacteriana fueron Campylobacter, E. coli y Salmonella. El Cryptosporidium es el protozoario más detectado. En Europa: el rotavirus es el agente más frecuente de DAI. El agente bacteriano más común es el Campylobacter o Salmonella en función del país. (13) [3] En el 2003 se publicaron los resultados del Programa SENTRY. Este informe mostró, 1479 aislamientos bacterianos de infecciones gastrointestinales colectadas en Europa y América Latina, cuyo resultado mostró los siguientes agentes patógenos: Salmonella spp. (834; 56%), Shigella spp. (311; 21%), Campylobacter spp. (182; 12%) y Aeromonas spp. (72; 5%). (14)
En el 2004, en Cuba, en un estudio realizado en 960 pacientes menores de 5 años hospitalizados por diagnóstico de diarrea aguda, aproximadamente el 12% fue catalogada como diarrea con sangre. La Salmonella sp fue el enteropatógeno más frecuentemente detectado en el grupo de menores de 1 año. La Shigella predominó en los niños mayores de 1 año, también fue predominante, en ambos grupos etarios, en los niños que desarrollaron la diarrea persistente. (15)
En el Perú, se realizó un estudio de cohorte que involucró 1034 pacientes de 2 a 12 meses de edad, en 4 distritos de Lima. Las muestras de heces de control fueron de niños sin diarrea seleccionados de forma aleatoria. Las especies de E. coli diarreogénica, Campylobacter y rotavirus fueron los más frecuentemente aislados en lactantes de ≥ 6 meses de edad. En niños mayores, E. coli difusamente adherente y E. coli enterotoxigénica fueron más frecuentemente aislados en muestras de diarreas que en el control (P<0.05). En niños de ≥ 6 meses de edad quienes fueron infectados con E. coli enterotoxigénica tuvieron un riesgo incrementado de diarrea de 4.56 veces (IC 95%, 1.20–17.28), comparado con niños menores. La diarrea persistente fue más común en lactantes de < 6 meses (13.5% vs 3.6%; P < 0.001). Entre niños con muestras positivas a E. coli diarreogénica, las co-infecciones con otros patógenos fueron más comunes en niños con diarrea que en los controles (40.1% vs 15.6%; P < 0.001). (16) [3]
Según la Encuesta Nacional Demográfica y de Salud Familiar (ENDES – 2009), en el Perú, la prevalencia de la DAI en menores de 5 años fue del 14% no hallando diferencias en cuanto a sexo, área urbana o rural o educación y sí en cuanto a edad: De 12 a 23 meses (22.7%) mayor que de 48 a 59 meses (7.1%). Durante el 2005 se registraron 1 millón 222 mil 327 episodios de la DAI (incidencia acumulada de 4373.77 episodios por cada 100 mil habitantes). (17) La diarrea con sangre se presentó en el 1.3% de los menores de 5 años, pero sube alrededor del 5% en Loreto y Pasco. (17)
En el 2000, se registraron 441 muertes y en 2001 se contaron 401. En 1999 fue la tercera causa de muerte en menores de 5 años (535 fallecidos). (18) En el 2010, según la Dirección General de Epidemiología (DGE) del Ministerio de Salud (MINSA), los episodios de diarrea aguda a la Semana Epidemiológica (SE) No 52 fueron 623,004 (189,977 en menores de 1 año y 433,027 de 1 a 4 años). Además, 14 departamentos muestran mayor incidencia acumulada de episodios de diarrea aguda con respecto al nivel nacional, siendo las más altas: Amazonas (730,8), Pasco (718,4), Madre de Dios (651,0), Moquegua (647,0), Ucayali (622,8), Lo-reto (558,4), Arequipa (549,4), Tacna (490,1), Callao (459,1), Huancavelica (436,8), Huánuco (426,3) Apurímac (335,9), La Libertad (320,6) y Ancash (320,2).
A la SE No 52 se han notificado 177 defunciones por episodios de diarrea aguda, en todas las edades. (19) [3]
c. NO HAY EVIDENCIA SUFICIENTE PARA AFIRMAR QUE LAS CARACTERÍSTICAS CLÍNICAS DEL PACIENTE Y/O LAS MACROSCÓPICAS DE LA DIARREA SON DE UTILIDAD PARA EL DIAGNÓSTICO ETIOLOGICO DE LA DAI. (B)
No hay evidencia que las combinaciones de las características clínicas puedan con certeza predecir una etiología viral o bacteriana. (13) [2+]
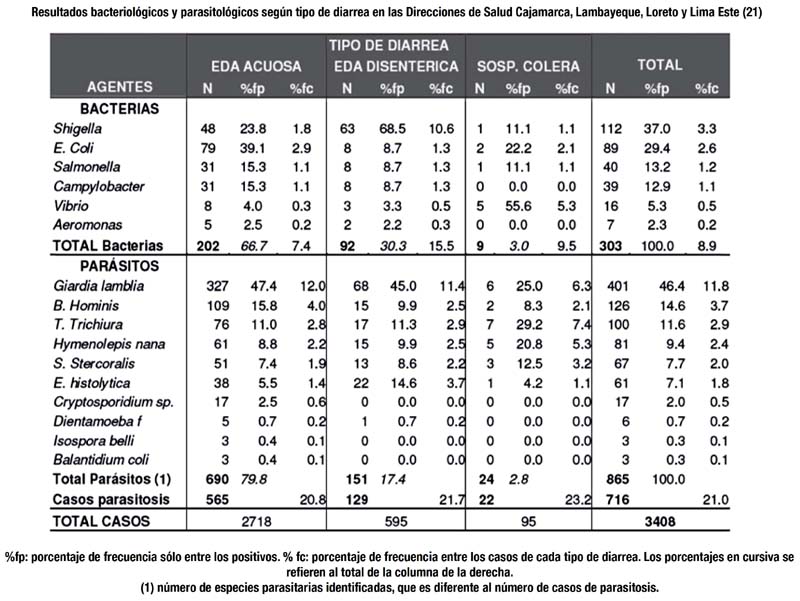
Si bien un paciente con diarrea disentérica tiene alta probabilidad de ser portador de una diarrea de etiología bacteriana, también es cierto que no toda diarrea acuosa es de etiología viral, como se demuestra en el estudio de etiología de la Diarrea Infecciosa en las Direcciones de Salud Cajamarca, Lambayeque, Loreto y Lima Este (20,21) [2+]
d. EN LOS PACIENTES CON DAI, EL USO RUTINARIO DEL EXAMEN DE HECES NO ESTÁ RECOMENDADO. (B)
LA INVESTIGACIÓN MICROBIOLÓGICA PARA EL DIAGNÓSTICO ETIOLÓGICO ESTÁ INDICADO EN LAS SIGUIENTES CONDICIONES (D):
-
– Si hay sangre y/o moco en las heces.
-
– Si el paciente tiene menos de 3 meses (por riesgo de bacteriemia).
-
– Si se sospecha de sepsis de origen gastrointestinal.
-
– Si hay incertidumbre en el diagnóstico etiológico de DAI.
-
– Si se sospecha de brote de DAI (en guarderías y salas de hospitalización): Para identificar el germen y conocer la epidemiologia.
-
– Si es un niño inmunocomprometido (debe ser evaluado fuera del alcance de la presente guía).
-
– Si la diarrea no ha mejorado a los 7 días o se considera que evoluciona desfavorablemente.
-
– Si el niño ha estado en zonas endémicas de DAI. (11) [4]
CUANDO SE DECIDE SOLICITAR EXAMENES, LA LACTOFERRINA FECAL ES EL DE MAYOR RENDIMIENTO PARA DETERMINAR ETIOLOGIA BACTERIANA; AL NO CONTAR CON ESTE EXAMEN EN NUESTRO PAIS, UNA ALTERNATIVA ES LA SUMA DE LEUCOCITOS FECALES, LA SANGRE OCULTA EN HECES O HEMATÍES FECALES Y EL ESTADO CLINICO DEL PACIENTE. (A)
No se debe solicitar exámenes de heces rutinariamente a todos los pacientes, puesto que el mayor porcentaje de episodios tienden a auto-limitarse.
La prueba de leucocitos fecales (reacción inflamatoria) aislada, tiene un pobre valor diagnostico (22) [1+].
La prueba de leucocitos fecales parece tener un rendimiento diagnostico aceptable, comparable a la lactoferrina fecal, solo en países desarrollados. (23) [1+].
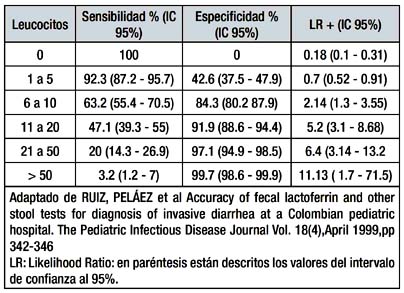
Un valor de los leucocitos fecales de 6 – 10 tienen una sensibilidad de 63.2% y especificidad 84.3%. Los leucocitos fecales 11 – 20 tienen una sensibilidad 47.1% y especificidad 91.9 %.(24,25) [2+]
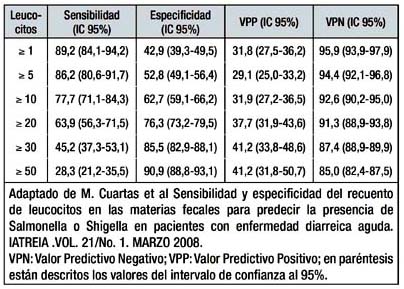
SI SE SOSPECHA UN BROTE DE DIARREA VIRAL, SE DEBE SOLICITAR EXÁMENES PARA ESTUDIARLO. (D) CUANDO EL ESTUDIO DE LA DIARREA VIRAL ESTÁ INDICADO, LA PRUEBA DE ELISA PARA ROTAVIRUS, ES EL EXÁMEN DE ELECCIÓN PARA EL ESTUDIO DE ANTÍGENOS VIRALES. (B)
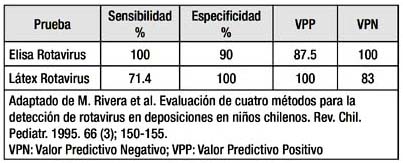
La prueba de LATEX tiene una sensibilidad 91.4% y Especifi cidad 98.2%.(11)
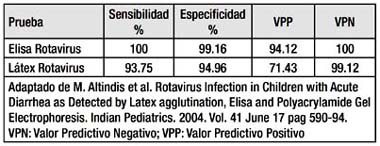
En un estudio Chileno, ELISA para Rotavirus mostró un mejor rendimiento de sensibilidad (sensibilidad del 100% y especificidad del 90%) comparado con LATEX (sensibilidad 71.4% y especifi cidad 100%). (26) En comparación, con otro estudio en Turquía, ELISA para Rotavirus mostró una mejor sensibilidad y especificidad (sensibilidad 100% y especifi ci-dad 99.16%) comparado con LATEX (sensibilidad 93.75% y especifi cidad 94.96%). (27)
CLÍNICA
EVALUACION DEL GRADO DE DESHIDRATACIÓN
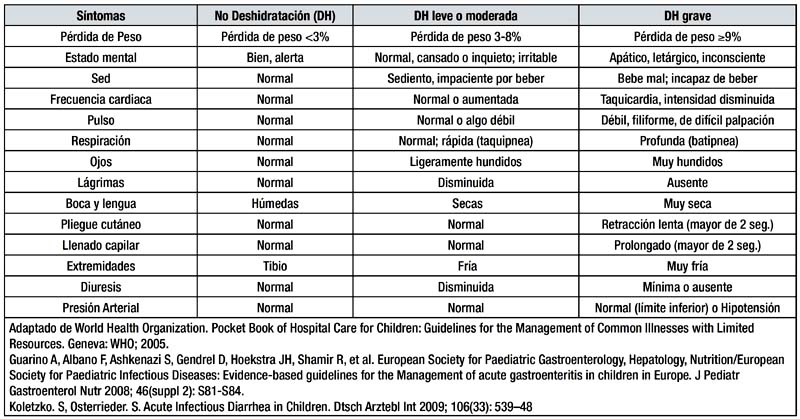
a. EN PACIENTES CON DAI, LOS SIGNOS QUE MEJOR RENDIMIENTO TIENEN PARA DIAGNOSTICAR DESHIDRATACIÓN SON: MUCOSA ORAL SECA, OJOS HUNDIDOS, PRESENCIA DEL PLIEGUE CUTÁNEO, LLENADO CAPILAR > 2 SEGUNDOS Y ALTERACIÓN DEL ESTADO DE CONCIENCIA. (B)
En niños entre 3 y 18 meses de edad, la presencia del pliegue cutáneo, mucosa oral seca, ojos hundidos y alteración del estado neurológico, se correlacionan mejor con la severidad de la deshidratación (según aumento de peso, posterior a rehidratación). Dos o más signos hacen diagnostico de deshidratación, si además presenta alteración del estado neurológico se trata de deshidratación severa, y si además presenta hipotensión y pobre perfusión periférica (llenado capilar > 2 segundos, piel marmórea), estamos frente a una deshidratación severa con shock. (28) [2+] En general, en menores de 4 años, la disminución de la turgencia de piel, disminución de la perfusión periférica y la respiración acidótica parecen ser los mejores signos clínicos de deshidratación. (28) [2+] Tienen alto riesgo de deshidratación aquellos niños: Menores de 6 meses de edad, que presentan más de 8 deposiciones abundantes y aquellos que presentan más de 4 vómitos abundantes, estos dos últimos en menos de 24 hs.(10) [4]
(Ver tabla adjunta y Anexo 1 para el rendimiento de los signos clínicos en la deshidratación por DAI)
INDICACIONES PARA LA HOSPITALIZACIÓN
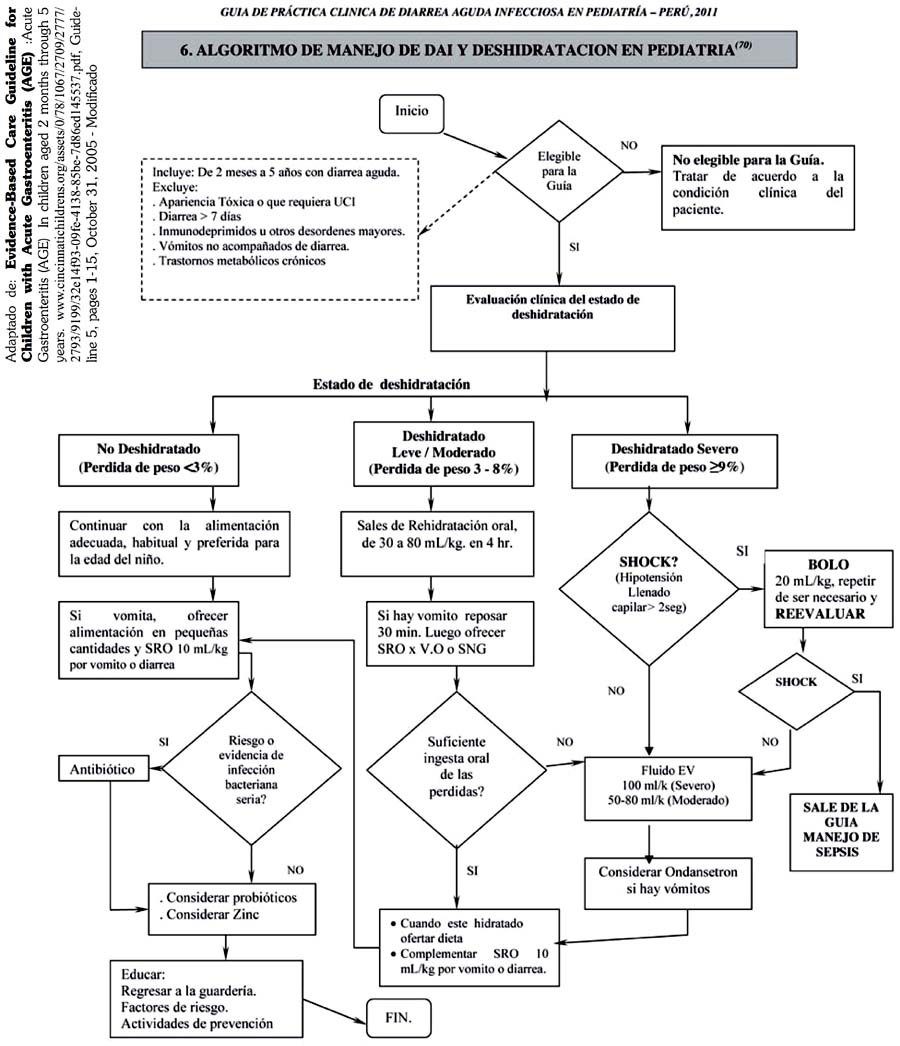
a. ESTÁ INDICADA LA HOSPITALIZACIÓN EN CUALQUIERA DE LAS SIGUIENTES CONDICIONES: SHOCK, DESHIDRATACIÓN SEVERA (MAYOR DE 9% DE PÉRDIDA DE PESO CORPORAL), ALTERACIÓN DEL ESTADO DE CONCIENCIA (LETARGIA, CONVULSIONES, ETC.), VÓMITOS INTRATABLES O BILIOSOS, FALLA EN LA TERAPIA DE REHIDRATACIÓN ORAL, FLUJO DE DEPOSICIONES "ALTO" (MAYOR DE 10 ML/K/HORA), SI LOS FAMILIARES NO PUEDEN PROPORCIONAR ADECUADO CUIDADO EN CASA Y EN SOSPECHA DE PATOLOGÍA QUIRÚRGICA.(28,29,30)(B)
b. EN LOS PACIENTES CON DAI, SON CRITERIOS DE SEVERIDAD: EL LLENADO CAPILAR PROLONGADO, EL SIGNO DEL PLIEGUE POSITIVO, LA HIPOTENSIÓN ARTERIAL, LA ALTERACIÓN DEL PATRÓN RESPIRATORIO Y DEL ESTADO CONCIENCIA. (B)
La severidad de la deshidratación está dada por la presencia de los siguientes parámetros: el porcentaje de pérdida de peso ≥ 9%, llenado capilar prolongado (> 2 segundos), signo del pliegue positivo, alteración del patrón respiratorio, alteración del estado neurológico e hipotensión arterial. (10) [2+]
Las membranas mucosas secas, ojos hundidos, la turgencia de la piel disminuida (signo del pliegue ≥ 2 segundos), alteración del estado neurológico y la respiración profunda (acidótica) están presentes con pérdidas del 3-8%. Con pérdida mayor del 9% los signos clínicos son más marcados y se presenta con colapso circulatorio (hipotensión) y pobre perfusión. (10) [2+]
Cuando hay signos de deshidratación es poco probable que la pérdida de peso sea menor al 3%.(10) [2+]
TRATAMIENTO
TRATAMIENTO DE LA DESHIDRATACIÓN
-
ESTÁ INDICADO INICIAR LA TERAPIA DE REHIDRATACIÓN ORAL (TRHO) EN PACIENTES CON DAI Y EN PRESENCIA DE AL MENOS DOS SIGNOS CLÍNICOS DE DESHIDRATACIÓN. (A)
-
La TRHO es el tratamiento de elección para niños con deshidratación leve-moderada secundaria a DAI.(11,31) [1+]. En una revisión sistemática de ensayos clínicos, donde se compararon la hidratación por VO con la EV, la primera se asoció a una menor estancia hospitalaria (-1.2 días; IC 95%: -2.38 a -0.02 días). El volumen, la duración de la diarrea y el riesgo de vómitos fueron menores con la hidratación VO. (11) [1+]
-
El empleo de las Sales de Rehidratación Oral (SRO) de osmolaridad reducida (Contiene Sodio 75 mEq/L de solución preparada), disminuye la necesidad de emplear Terapia de Hidratación EV (THEV). (11) [1+]
-
Dar SRO 50 mL/kg para reemplazar el déficit de líquidos en alrededor de 4 horas, frecuente y en pocas cantidades. (11) [4]
-
En lactantes con DAI sin deshidratación, el retiro de la lactancia materna durante el episodio diarreico, se asoció a incremento en el riesgo de deshidratación. Además, el proporcionar líquidos caseros en pocas cantidades redujo el riesgo de deshidratación. (11) [2+]
-
(Ver Anexo 3 para el esquema de hidratación oral en pacientes deshidratados)
-
EN PACIENTES CON DAI Y DESHIDRATACIÓN, SE RECOMIENDA HIDRATAR POR VO O POR SONDA NASOGÁSTRICA (GASTROCLISIS). (A)
-
Cuando la hidratación oral no es posible, la hidratación enteral por SNG es tan efectiva (sino mejor) como la THEV. (10,32) [1+]
-
Los procedimientos usados en los estudios sugieren que los niños con DAI y deshidratación severa pueden ser adecuadamente hidratados con TRHO luego de hidratarlos inicialmente con THEV. Luego de iniciada la THEV, la TRHO fue usualmente iniciada dentro de las 2-4 hs de iniciada la hidratación. (33) [4]
-
En niños con deshidratación severa, sin íleo metabólico, no hubo diferencias significativas en cuanto al riesgo de falla de hidratación, tanto en la hidratación por gastroclisis como la EV. La incidencia de hipernatremia, hiponatremia o hiperkalemia fue la misma en la hidratación por gastroclisis y la EV. (11) [1+]
-
ESTÁ INDICADA LA THEV EN PACIENTES PEDIÁTRICOS CON DAI Y DESHIDRATACIÓN QUE PRESENTAN (B):
-
Deshidratación severa / Deshidratación severa con Shock. [1+]
-
Deshidratación moderada e incapacidad de ser hidratado por vía enteral (VO o sonda nasogástrica) por vómitos persistentes o flujo de deposiciones "alto" (10mL/k/h). [1+]
-
Pacientes con co-morbilidades asociadas al tracto gastrointestinal (intestino corto, ostomías del intestino anterior). [4]
-
Pacientes con íleo metabólico. [4]
-
CUANDO LA HIDRATACIÓN POR VÍA EV ESTÁ INDICADA, EL VOLUMEN (CÁLCULO DE LA PÉRDIDA DE VOLUMEN DE AGUA CORPORAL), LA SOLUCIÓN Y LA DURACIÓN DE LA HIDRATACIÓN (4 A 6 HORAS) SON IMPORTANTES PARA LA RECUPERACIÓN DEL ESTADO DE HIDRATACIÓN DEL PACIENTE. (A)
Los pacientes tributarios de recibir THEV lo harán de la siguiente manera:
-
Volumen y Duración:
-
- Deshidratación severa / Deshidratación severa con shock:
-
Si presenta shock iniciar bolo de 20 mL/kg de NaCl al 0.9%, pasar en 5 a 10 min.; de ser necesario puede repetirse otro bolo de 20 mL/kg, hasta mejorar el estado hemodinámico (corregir Hipotensión, llenado capilar <2 seg). Si en la primera hora el paciente requiere un volumen total > 40 mL/kg, y continúa con inestabilidad hemodinámica, replantear los diagnósticos y el tratamiento, ya que se trataría de un Shock Séptico (exclusión de la presente guía).(34,35) [1+]
-
Luego de lograr la estabilidad hemodinámica, continuar la hidratación con 100 mL/kg en 4 a 6 horas.(10,36,37) [2+]
-
A partir de las 2 horas de hidratación EV, se puede ofrecer SRO por vía enteral (VO o SNG).(11,35) [4]
-
- Deshidratación moderada e incapacidad de ser hidratado por vía enteral (VO o SNG):
-
* Hidratar por vía EV según el cálculo del porcentaje de pérdida de peso (3-8% de pérdida) y reponer por lo tanto 30 a 80 mL/ kg en 4 horas. Luego de una hora de tratamiento EV, ofrecer SRO por vía enteral (VO o SNG).(11) [4]
-
Solución a emplear:
-
- Pacientes deshidratados con DAI sin sospecha de cólera(34,35,37) [1+]:
-
* Solución de NaCl al 0.9%; o Solución de NaCl al 0.9% (500cc) + D5% en AD (500cc) + KCl (20meq/L).(38) [1+]
-
- Pacientes deshidratados con DAI con sospecha de cólera(34,35,37,39) (B):
* Solución Polielectrolítica Estándar.
- Solución a emplear en la aplicación del "bolo"(35) [1+]:
* Solución de NaCl al 0.9%.
TRATAMIENTO ANTIBIÓTICO
-
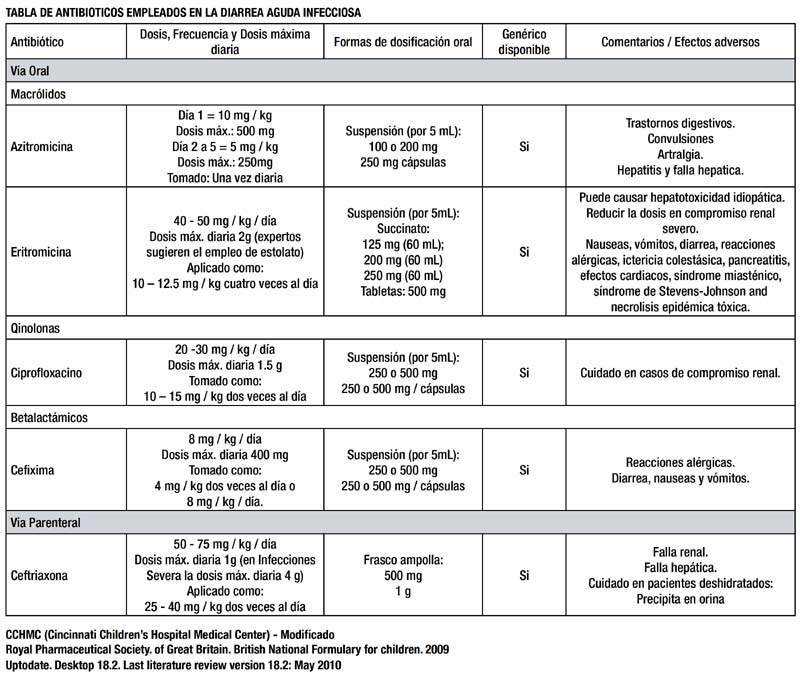
LA CIPROFLOXACINA ESTA INDICADA COMO TERAPIA EMPÍRICA DE PRIMERA LÍNEA EN LOS PACIENTES CON SOSPECHA DE DIARREA INVASIVA Y ADEMÁS, DETERIORO DEL ESTADO GENERAL. LA AZITROMICINA ESTA INDICADA COMO TERAPIA DE SEGUNDA LÍNEA (13,40) (B) Dar tratamiento antibiótico en diarrea invasiva severa y fiebre. Las causas comunes de diarrea invasiva son: Shigella, Campylobacter y Salmonella. El antibiótico de elección depende de la prevalencia del germen causal. (11,13,40) [4] Es preferible dar antibióticos parenterales si el paciente:
-
No tolera la VO;
-
Tiene enfermedad inmunodeficiente subyacente y tiene DAI y fi ebre;
-
Luce en mal estado general o se sospecha de bacteriemia, y
-
Lactantes menores de tres meses. (13) [4]
-
LA CIPROFLOXACINA ES EL ANTIBIÓTICO DE PRIMERA LÍNEA PARA LOS PACIENTES CON DAI POR shigella. SON ALTERNATIVAS LA AZITROMICINA Y LA CEFIXIMA. (A) La terapia antibiótica está indicada en la shigellosis sospechada o demostrada por cultivo. (13)[1+] El tratamiento oral de primera línea es la ciprofl oxacina. Son alternativas azitromicina o cefixima por 5 días.(13,40) [1+] El tratamiento parenteral de primera línea es la ceftriaxona por 5 días. (11,13) [1+]
-
LA ERITROMICINA ES EL ANTIBIÓTICO DE PRIMERA LÍNEA (CUANDO ESTÁ INDICADA) EN PACIENTES CON DAI POR Campylobacter. (A) La eritromicina es el antibiótico de primera línea (negativización del coprocultivo en menor tiempo). (11,13,41) [1+] El tratamiento con eritromicina reduce la duración media de las heces de consistencia anormal. (11,13) [1+] Solo debería tratarse las formas "disentéricas" para reducir la transmisión a contactos cercanos. Se pueden reducir los síntomas si el tratamiento se instala dentro de los 3 primeros días. (11,13) [1-]
-
LA AZITROMICINA ES EL ANTIBIÓTICO DE PRIMERA LÍNEA EN PACIENTES CON DAI POR Vibrio cholerae.(A) La eritromicina y la ciprofloxacina son una buena alternativa como terapia de segunda línea. (42) [1+] Una dosis única de azitromicina fue tan efectiva como un tratamiento estándar de eritromicina y adicionalmente, presentaron menos vómitos los pacientes. (43) [1+]
-
NO EXISTE EVIDENCIA SUFICIENTE, PARA INDICAR DE MANERA RUTINARIA, ANTIBIÓTICOS EN LA DAI POR Salmonella. (A) Los antibióticos no deben ser usados de manera rutinaria, en la DAI por Salmonella, pues pueden favorecer la aparición de estados de portador sanos. (13) [1+] No parece existir ninguna evidencia de un benefi cio clínico del tratamiento con antibióticos, en niños y adultos básicamente sanos, con diarrea no severa por Salmonella. Los antibióticos parecen aumentar los efectos adversos y también tienden a prolongar la detección de Salmonella en heces. (44) [1++] Los antibióticos están sugeridos en pacientes en riesgo de bacteriemia e infección extra intestinal: Pacientes con inmunodeficiencia subyacente, asplenia anatómica o funcional, terapia inmunosupresora o corticoidea, enfermedad inflamatoria intestinal o acloridia y neonatos o lactantes menores de 3 meses. (13) [4] La ampicilina EV protege contra las recaídas y el estado de portador, en relación a la ampicilina VO, la amoxicilina o el placebo. (11,13) [1+]
-
LA TERAPIA ANTIBIÓTICA ES CONTROVERSIAL EN PACIENTES CON DAI POR Escherichia coli enterohemorrágica. (A) Es controversial si el tratamiento antibiótico eleva la posibilidad de aparición de síndrome urémico hemolítico en los pacientes con DAI causada por E. coli enterohemorrágica. (45) [1+]
TRATAMIENTO COADYUVANTE
-
EXISTE EVIDENCIA SUFICIENTE PARA INDICAR Lactobacillus rhamnosus cepa GG Y Saccharomyces boulardii COMO ADYUVANTES EN EL MANEJO DE LA DAI. (A)
-
Un meta-análisis de ensayos clínicos aleatorizados demostró eficacia del Lactobacillus rhamnosus cepa GG y Saccharomyces Boulardii. El beneficio de acortar la duración de la diarrea se comparó con placebo y mostró una diferencia a favor del probiótico (-20.1 horas (IC al 95%: -26 a -14) y -25 (IC al 95%: -32 a -18) respectivamente). (46) [1+]
-
Una revisión sistemática reciente muestra que los probióticos (Lactobacillus rhamnosus GG, Lactobacillus bulgaricus, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus reuteri, Lactobacillus bifi dus, Bifi dobacterium bifidum, B. lactis, Streptococcus faecium, Streptococcus Thermophilus, S. boulardii) reducen la duración de la diarrea aguda infecciosa (diferencia de medias 24.76 horas; IC 95% 15.9, 33.6 horas; n=2367, ensayos=35). (47) [1+]
-
NO HAY EVIDENCIA SUFICIENTE QUE SUSTENTE EL USO RUTINARIO DE RACECADOTRILO EN PACIENTES CON DAI. (A) El racecadotrilo solo ha demostrado disminución del volumen de las heces (en DAI por rotavirus) las primeras 48 horas, comparado con placebo. Al 3, 4 y 5to día, no se encontró diferencia significativa contra placebo. (48,49) [1+]
-
EN ZONAS DONDE LA MORTALIDAD POR DAI ES IMPORTANTE, EL ZINC HA DEMOSTRADO BENEFICIOS A DOSIS DE 10 mg/día PARA MENORES DE 6 MESES Y 20 mg/día EN MAYORES, ADMINISTRADO POR LO MENOS 14 DÍAS. (A)
-
Una revisión sistemática mostró que el zinc reduce la duración de la diarrea aguda infecciosa (diferencia de medias 12.27 horas; IC 95% 1.52, 23.02 horas; n=2741, ensayos=9, comparaciones=13). Además, la misma revisión mostró menos pacientes con diarrea en el día 7 de tratamiento (RR=0.71, IC 95% 0.51, 0.98; 4087 niños, ensayos=7, comparaciones=10). Cuando se estratificó por edad no hubo beneficio en menores de 6 meses en ambos casos. Esta revisión sistemática consideró 4 ensayos clínicos que incluyeron niños con desnutrición. (50) [1+]
-
La UNICEF y la OMS recomiendan suplemento de zinc (10 mg en menores de 6 meses, y 20 mg para niños mayores por 10-14 días) como tratamiento universal para niños con diarrea. [4] Teniendo en cuenta la recomendación de la OMS, se debe administrar zinc a todo niño desnutrido. (51)
-
El meta-análisis de cinco ensayos clínicos que evaluaron zinc en el tratamiento de la diarrea aguda, y que excluyeron a los niños con desnutrición severa, mostró que no hubo diferencia estadísticamente signifi cativa en la duración media de la diarrea entre los que recibieron zinc (n=903) y los que recibieron placebo (n=821) (diferencia de medias=-4.4 horas; IC 95% -15.9 a 7.2 horas). (52) [1+]
-
El meta-análisis de cuatro ensayos clínicos que evaluaron zinc en el tratamiento de la diarrea aguda, y que excluyeron a los niños con desnutrición severa, muestra que no hubo diferencia estadísticamente significativa en la frecuencia de deposiciones entre los que recibieron zinc (n=1056) y los que recibieron placebo (n=1079) (diferencia de medias -0.32; IC 95% -0.8 a 0.17). (11) [1+]
-
d. EN PACIENTES CON DAI Y VÓMITOS PERSISTENTES, LA ADMINISTRACIÓN DE ONDANSETRÓN DISMINUYE LOS VÓMITOS, LA NECESIDAD DE HIDRATACIÓN POR VÍA EV Y LA NECESIDAD DE HOSPITALIZACIÓN. (A)
-
En un meta-análisis sobre el uso de antieméticos (ondansetron VO o EV) en niños con DAI, se encontró un efecto beneficioso en la reducción del vómito (RR 0,45; IC 95% 0,33 a 0,62; NNT 5) disminución en el uso de rehidratación EV (RR 0,41; IC 95% 0,28 a 0,62; NNT 5) y disminución en la necesidad de hospitalización (RR 0,52; IC 95% 0,27 a 0,95; NNT 14). (53)
-
Dos ensayos clínicos (54,55) mostraron que el grupo que recibió Ondansetron presentó incremento del flujo de diarrea. La diferencia fue estadísticamente signifi cativa. (11)
SOPORTE NUTRICIONAL
-
EN LOS PACIENTES CON DAI NO SE DEBE RESTRINGIR LA ALIMENTACIÓN (LACTANCIA MATERNA, LECHE CON LACTOSA, ALIMENTOS SÓLIDOS) NI ALTERAR LA CALIDAD DE LOS ALIMENTOS. (B)
-
Se debe continuar con la lactancia durante la DAI. (56) [2++]
-
Los niños que requieren rehidratación deben continuar siendo alimentados. Los alimentos no deben ser retirados por más de 4-6 horas luego del inicio de la rehidratación. [1+]
-
La gran mayoría de niños con DAI puede continuar recibiendo leche con lactosa en forma segura porque el número de fallas en el tratamiento no es significativo, versus los niños con diarrea aguda que reciben dieta sin lactosa. (13) [1++]
-
La dilución de las fórmulas o el reinicio gradual de la alimentación no son necesarios. (13) [1++] Las bebidas con alto contenido de azúcar no deben ser usadas. (13) [2-]
CRITERIOS DE TRANSFERENCIA
-
EL NIVEL DE RESOLUCIÓN DEL ESTABLECIMIENTO DE SALUD ES IMPORTANTE PARA DECIDIR LA TRANSFERENCIA DE UN PACIENTE CON DAI. (D) La transferencia de un paciente con DAI a un nivel superior está indicada:
-
– Cuando hay signos o síntomas sugerentes de shock.
-
– Cuando hay signos y/o síntomas que incrementan el riesgo de progresión hacia el shock.
-
– Cuando las circunstancias sociales requieran supervisión de los profesionales de salud.(13) [4]
CRITERIOS DE ALTA
-
EL ALTA DEL PACIENTE CON DAI, SE INDICA PRINCIPALMENTE POR CRITERIOS CLÍNICOS. (D) El alta hospitalaria se puede considerar cuando:
-
– Se haya logrado la hidratación del paciente, lo cual se evidencia por la ganancia ponderal y la condición clínica.
-
– No se requieran fluidos endovenosos para hidratar al paciente.
-
– La ingesta oral de fluidos sea adecuada para compensar las pérdidas.
-
– Este asegurado un adecuado manejo por parte de los padres.
-
– El seguimiento médico sea factible.(13) [4]
PREVENCIÓN
-
EL LAVADO DE MANOS, LA MEJORA EN LA CALIDAD DEL AGUA Y OTRAS MEDIDAS HIGIÉNICAS, DEBEN SER ACONSEJADAS A LOS PADRES Y CUIDADORES PARA EVITAR LA DAI (A).
-
Las mejoras en el acceso a agua segura y adecuado saneamiento, junto con la promoción de buenas prácticas de higiene (particularmente el lavado de manos con jabón), pueden ayudar a prevenir la diarrea. El lavado sistemático de manos puede reducir en un 50% la prevalencia de diarrea y evitar aproximadamente 1 millón de muertes anuales (57)[4]
-
Aconsejar a los padres y cuidadores de niños que:
-
Deben lavarse las manos con jabón (líquido si es posible), chorro de agua continúa (tibia si es posible) y un secado cuidadoso (factores importantes para prevenir la diseminación de la DAI). Se deben lavar las manos luego de ir al baño (niños) o luego de cambiar pañales (cuidadores, padres) y antes de preparar, servir o comer los alimentos. Una revisión sistemática concluye que las intervenciones que promueven el lavado de manos pueden reducir los episodios de diarrea en aproximadamente un tercio. (58,59,60) [1+]
-
Las intervenciones destinadas a mejorar la calidad microbiológica del agua potable son efectivas para la prevención de la diarrea en las poblaciones de todas las edades. (61) [1+]
-
Las toallas usadas por niños infectados no deben ser compartidas.
-
Los niños no deben asistir al nido o guardería mientras tengan diarrea o vómitos o hasta por lo menos 48 horas luego de del último episodio de diarrea o vómito.
-
Los niños no deben nadar en piscinas por dos semanas luego del último episodio de diarrea. (11) [4]
b. LA VACUNACIÓN CONTRA EL ROTAVIRUS ESTÁ ACONSEJADA EN LOS LACTANTES. (A)
Las vacunas Rotarix© y RotaTeq© son efectivas en la prevención de la diarrea por rotavirus. El balance entre el beneficio y el riesgo favorece al beneficio. [1+]
La vacuna Rotarix© redujo el número de casos de diarrea por rotavirus hasta un 72% durante el primer año de seguimiento (RR 0.28, IC 95% 0.17 a 0.48; 11121 participantes, 6 ensayos) y 67% durante el segundo año de seguimiento (RR 0.33, IC 95% 0.21 a 0.50; 7293 participantes, 5 ensayos). Sin embargo, la heterogeneidad entre los estudios fue significativa.
Asimismo, Rotarix© redujo en un 80% el número de episodios severos luego de un año (RR 0.20, IC 95% 0.11 a 0.35; 35004 participantes, 7 ensayos) y 84% luego de dos años (RR 0.16, IC95% 0.12 a 0.22; 32106 participantes, 7 ensayos). Nuevamente la heterogeneidad entre los estudios fue significativa.La vacuna RotaTeq© redujo el número de casos de diarrea por rotavirus hasta un 73% durante el primer año de seguimiento (RR 0.27, IC 95% 0.22 a 0.33; 7614 participantes, 4 ensayos) y 62% durante el segundo año de seguimiento (RR 0.38, IC 95% 0.26 a 0.55; 1569 participantes, 1 ensayo). Asimismo, RotaTeq© redujo en un 93% el número de episodios severos luego de un año (RR 0.07, IC 95% 0.01 a 0.5; 1485 participantes, 2 ensayos) y 89% luego de dos años (RR 0.11, IC95% 0.03 a 0.47; 1569 participantes, 1 ensayo). (62)
c. SE DEBE RECOMENDAR: ALIMENTAR CON LACTANCIA MATERNA EXCLUSIVA LOS PRIMEROS SEIS MESES DE VIDA, EVITAR EL USO DE BIBERONES, MEJORAR LAS PRÁCTICAS DE MANIPULACIÓN DE LOS ALIMENTOS Y DESECHAR LAS EXCRETAS DE MANERA APROPIADA. (63,64,65,66,67,68,69) (A)
7. REFERENCIAS
1. WORLD HEALTH ORGANIZATION. Ten statistical highlights in global public health. 2007. Disponible en: http://www.who.int/whosis/whostat2007_10highlights.pdf. [Consulta: Enero 2011].
2. BOSCHI-PINTO C, VELEBIT L & KENJI SHIBUYA. Estimating child mortality due to diarrhoea in developing countries. Bulletin of the World Health Organization. 2008; 86:710–717.
3. WORLD HEALTH ORGANIZATION. PNEUMONIA. The forgotten killer of Children. 2006. Geneva: The United Nations Childrens Fund (UNICEF)/World Health Organization (WHO).
4. UNICEF/WHO. Diarrhoea: Why children are still dying and what can be done, 2009. Disponible en: http://www.unicef.org/media/files/Final_Diarrhoea_Report_October_2009_final.pdf. [Consulta: Abril 2011].
5. OFICINA GENERAL DE ESTADÍSTICA E INFORMÁTICA – MINISTERIO DE SALUD (MINSA). 2008. Disponible en: http://www.minsa.gob.pe/ogei/disponibilidad/default.asp, [Consulta: Enero 2011].
6. GRAHAM ID, HARRISON MB. Evaluation and adaptation of clinical practice guidelines. Evid. Based Nurs. 2005; 8(3); 68-72.
7. The ADAPTE Collaboration. The ADAPTE Process: Resource Toolkit for Guideline Adaptation. Version 2.0. 2009. Disponible en: http://www.g-i-n.net. [Consulta: Agosto 2010].
8. RYCROFT-MALONE J. Formal consensus: the development of a national clinical guideline. Qual Health Care 2001; 10(4): 238–44.
9. FIELD MJ, LOHR KN. Guidelines for clinical practice: from development to use. Committee on Clinical Practice Guidelines. Division of Health Care Services. Institute of Medicine (IOM). 1992. Washington DC: National Academy Press.
10. ARMON K, STEPHENSON T, MACFAUL R, et al. An evidence and consensus based guideline for acute diarrhoea management. Archives of Disease in Childhood. 2001; 85:132–42. Actualización del 2005 en el siguiente enlace: http://www.nottingham.ac.uk/paediatric-guideline/diarrhoeaguideline.pdf 11. GUIDELINE DEVELOPMENT GROUP AND THE TECHNICAL TEAM. Diarrhoea and vomiting caused by gastroenteritis in children under 5 years: summary of NICE guidance. BMJ. 2009. Apr 22;338:b1350. doi: 10.1136/bmj.b1350 [Consulta: Setiembre 2010]. 12. WORLD HEALTH ORGANIZATION. Childrens environmental health. Disponible en: http://www.who.int/ceh/en/ [Consulta: Enero 2011]. 13. EUROPEAN SOCIETY FOR PAEDIATRIC GASTROENTEROLOGY, HEPATOLOGY, AND NUTRITION/EUROPEAN SOCIETY FOR PAEDIATRIC INFECTIOUS Diseases evidence-based guidelines for the management of acute gastroenteritis in children in Europe. 2008 May. J Pediatr Gastroenterol Nutr. 2008. May;46 Suppl 2:S81-122. 14. STREIT JM, JONES RN, TOLEMAN MA, STRATCHOUNSKI LS, FRITSCHE TR. Prevalence and antimicrobial susceptibility patterns among gastroenteritis-causing pathogens recovered in Europe and Latin America and Salmonella isolates recovered from bloodstream infections in North America and Latin America: report from the SENTRY Antimicrobial Surveillance Program (2003). Int J Antimicrob Agents. 2006. May;27(5):367-75. 15. FERNÁNDEZ M, FERNÁNDEZ C, MARTÍNEZ G, PÉREZ E, CUZA, ACOSTA J. Etiología de la diarrea con sangre en menores de 5 años. Rev Cubana Pediatr. 2004. v.76 n.4. Oct.-dic. 16. OCHOA TJ, ECKER L, BARLETTA F, MISPIRETA ML, GIL AI, CONTRERAS C, MOLINA M, AMEMIYA I, VERASTEGUI H, HALL ER, CLEARY TG, LANATA CF. Age-related susceptibility to infection with diarrheagenic Escherichia coli among infants from Periurban areas in Lima, Peru. Clin Infect Dis. 2009. Dec 1;49(11):1694-702. 17. INSTITUTO NACIONAL DE ESTADÍSTICA E INFORMÁTICA (INEI). Encuesta Demográfica y de Salud Familiar – ENDES Continua 2009. Mayo 2010. 18. PERÚ. MINISTERIO DE SALUD. Análisis de situación de salud –ASIS 2005. [monografía en internet]. Lima: Ministerio de Salud; 2005. Disponible en: http://www.dge.gob.pe/publicaciones/pub_asis/asis15.pdf. [Consulta: Enero 2011]. 19. PERÚ. MINISTERIO DE SALUD. Dirección General de Epidemiología – Sistema Nacional de Vigilancia Epidemiológica – Sala Situacional 2010. Disponible en: http://www.dge.gob.pe/salasit.php. [Consulta: Enero 2011]. 20. PERALES MT, CAMIÑA M, QUIÑONES C. Infección por Campylobacter y Shigella como causa de diarrea aguda acuosa en niños menores de dos años en el distrito de la victoria, Lima – Perú. Rev Peru Med Exp Salud Publica 2002; 19 (4): 186 – 192. 21. MINSA – Dirección General de Salud de las Personas. Proyecto Vigia. Estudio de etiología de la diarrea en las Direcciones de Salud Cajamarca, Lambayeque, Loreto y Lima Este. 2001. Disponible en: http://www.ins.gob.pe/repositorioaps/0/4/jer/cnsp_resanti_documentos_tecnicos/Estudio_etiologico_diarrea_4_DISAS.pdf [Consulta: Abril 2011]. 22. HUICHO L, CAMPOS M, RIVERA J, GUERRANT RL. Fecal screening tests in the approach to acute infectious diarrhea: a scientific overview. Pediatr Infect Dis J. 1996 Jun;15(6):486-94. 23. GILL CJ, LAU J, GORBACH SL, HAMER DH. Diagnostic accuracy of stool assays for infl ammatory bacterial gastroenteritis in developed and resource-poor countries. Clin Infect Dis. 2003 Aug 1;37(3):365-75. 24. RUIZ, PELAEZ, et al. Accuracy of fecal lactoferrin and other stool tests for diagnosis of invasive diarrhea at a Colombian pediatric hospital. The Pediatric Infectious Disease Journal. 1999. Vol. 18(4),April. pp 342-346. 25. CUARTAS M, et al. Sensibilidad y especifi cidad del recuento de leucocitos en las materias fecales para predecir la presencia de Salmonella o Shigella en pacientes con enfermedad diarreica aguda. Iatreia. 2008. Vol. 21/No. 1. Marzo. 26. RIVERA M, et al. Evaluación de cuatro métodos para la detección de rotavirus en deposiciones en niños chilenos. Rev. Chil. Pediatr. 1995. 66 (3); 150-155. 27. M. ALTINDIS et al. Rotavirus Infection in Children with Acute Diarrhea as Detected by Latex agglutination, Elisa and Polyacrylamide Gel Electrophoresis. Indian Pediatrics. 2004. Vol. 41 June 17 pag 590-94. 28. MACKENZIE A, BARNES G, SHANN F. Clinical signs of dehydration in children. Lancet 1989. 2605–607. 29. ELLIOTT EJ, BACKHOUSE JA, LEACH JW. Pre-admission management of acute gastroenteritis. J Paediatr Child Health. 1996. 32:18-21. 30. OLOUGHLIN EV, NOTARAS E, MCCULLOUGH C, HALLIDAY J, HENRY RL. Home-based management of children hospitalized with acute gastroenteritis. J Paediatr Child Health. 1995. 31:189-91. 31. MACKENZIE A. AND G. BARNES. Randomised controlled trial comparing oral and intravenous rehydration therapy in children with diarrhea. BMJ. 1991. 303 (6799): p. 393 – 396. 32. FONSECA BK, HOLDGATE A, CRAIG JC. Enteral vs intravenous rehydration therapy for children with gas troenteritis: a meta-analysis of randomized controlled trials. Arch Pediatr Adolesc Med. 2004. 158:483–90. 33. CHOICE Study Group. Multicenter, randomized, double-blind clinical trial to evaluate the effi cacy and safety of a reduced osmolarity oral rehydration salts solution in children with acute watery diarrhea. Pediatrics. 2001. 107:613–18. 34. BOLUYT N; BOLLEN CW; BOS AP; KOK JH; OFFRINGA M. Fluid resuscitation in neonatal and pediatric hypovolemic shock: a Dutch Pediatric Society evidence-based clinical practice guideline.. Intensive Care Med. 2006. Jul;32(7):995-1003. 35. CARCILLO JA; DAVIS AL; ZARITSKY. A Role of early fluid resuscitation in pediatric septic shock. JAMA 1991 Sep 4;266(9):1242-5. 36. ROBERT M. et al. Oral and intravenous rehydration of children. Canadian Family Physician. 1993. Vol 39: October. 37. YVONNE C. et al. A Randomized Trial of Oral vs Intravenous Rehydration in a Pediatric Emergency Department. Arch Pediatr Adolesc Med. 2002. Vol 156, Dec. 38. ISSENMAN RM, L,EUNG AK. Oral and intravenous rehydration of children. Canadian Family Physician.1993; 39: 2129-2136. 39. CONCEICAO A. et al. Comparison between normal saline and a polyelectrolyte solution for fl uid resuscitation in severely dehydrated infants with acute diarrhoea. Annals of Tropical Paediatrics. 2005. 25, 253–260. 40. LEIBOVITZ E, JANCO J, PIGLANSKY L, PRESS J, YAGUPSKY P, REINHART H, YANIV I, DAGAN R. Oral ciprofl oxacin vs. intramuscular ceftriaxone as empiric treatment of acute invasive diarrhea in children. The Pediatric Infectious Disease Journal. 2000. Issue: Volume 19(11). November, pp 1060-1067. 41. TERNHAG A, ASIKAINEN T, GIESECKE J, EKDAHL K. A Meta-Analysis on the Effects of Antibiotic Treatment on Duration of Symptoms Caused by Infection with Campylobacter Species. Clinical Infectious Diseases 2007; 44: 696–700. 42. YAMAMOTO T, NAIR GB, ALBERT MJ, PARODI CC, TAKEDA Y. Survey of in vitro susceptibilities of Vibrio cholerae O1 and O139 to antimicrobial agents. Antimicrob Agents Chemother. 1995; 39 (1): 241-4. 43. KHAN WA, SAHA D, RAHMAN A, SALAM MA, BOGAERTS J, BENNISH ML. Comparison of singledose azithromycin and 12-dose, 3-day erythromycin for childhood cholera: a randomised, double-blind trial. Lancet. 2002; 360 (9347): 1722-7. 44. SIRINAVIN S, GARNER P. Antibióticos para el tratamiento de infecciones intestinales por salmonelas (Revisión Cochrane traducida). En: La biblioteca Cochrane Plus, 2008 Número 4. Oxford: Update Software Ltd. Disponible en: http://www.update-software. com. (Traducida de The Cochrane Library, 2008 Issue 3. Chichester, UK: John Wiley & Sons, Ltd.) [Consulta: Enero 2011]. 45. SAFDAR N, SAID A, GANGNON RE, MAKI DG. Risk of Hemolytic Uremic Syndrome After Antibiotic Treatment of Escherichia coli O157:H7 Enteritis. A Metaanalysis. JAMA. 2002;288:996-1001. 46. SZAJEWSKA H, MRUKOWICZ JZ. Probiotics in the treatment and prevention of acute infectious diarrhea in infants and children: a systematic review of published randomized, double-blind, placebocontrolled trials. J Pediatr Gastroenterol Nutr 2001;33 (Suppl 2): S17–S25. 47. ALLEN SJ, MARTINEZ EG, GREGORIO GV, DANS LF. Probiotics for treating acute infectious diarrhoea. Cochrane Database of Systematic Reviews 2010, Issue 11. 48. EMPARANZA J, OZCOIDI, MARTINEZ M, CALLÉN M, ALÚSTIZA E, ASEGUINOLAZA I. Revisión sistemática sobre la eficacia de racecadotrilo en el tratamiento de la diarrea aguda. An Pediatr (Barc). 2008; 69(5):432-8. 49. SANTOS M, MARAÑÓN R, MIGUEZ C, VÁZQUEZ P, SÁNCHEZ C. Use of racecadotril as outpatient treatment for acute gastroenetritis: a prospective, randomized, parallel study. The Journal of Pediatrics. 2009. 155(1): 62-7. 50. LAZZERINI M, RONFANI L. Oral zinc for treating diarrhoea in children. Cochrane Database of Systematic Reviews. 2008: (3): CD005436. 51. WHO/UNICEF Joint Statement: Clinical Management of Acute Diarrhoea. New York, NY, and Geneva, Switzerland: The United Nations Childrens Fund/WHO; 2004. 52. AL-SONBOLI N, GURGEL RQ, SHENKIN A, et al. Zinc supplementation in Brazilian children with acute diarrhoea. Annals of Tropical Paediatrics. 2003. 23:3–8. 53. DE CAMP LR, BYERLEY JS, DOSHI N, STEINER MJ. Use of antiemetic agents in acute gastroenteritis: a systematic review and meta-analysis. Arch Pediatr Adolesc Med. 2008; 162:858–65. 54. RAMSOOK C, SAHAGUN-CARREON I, KOZINETZ CA, MORO-SUTHERLAND D. A randomized clinical trial comparing oral Ondansetron with placebo in children with vomiting from acute gastroenteritis. Annals of Emergency Medicine. 2002;39(4):397-403. 55. ROSLUND G, HEPPS T, MCQUILLEN K. The role of ondasentron in children with vomiting as a result of acute gastritis/gastroenteritis who have failed oral rehydration therapy: a randomized controlled trial. Annals of Emergency Medicine. 2008;52:22–9. 56. AMERICAN ACADEMY OF PEDIATRICS, Provisional Committee on Quality Improvement, Subcommittee on Acute Gastroenteritis. Practice parameter: the management of acute gastroenteritis in young children. Pediatrics. 1996; 97:424–35. 57. BLACK RE, MORRIS SS. Where and why are 10 million children dying every year? Lancet. 2003. Volume 361, Issue 9376, 28 June, Pages 2226-2234. 58. CURTIS V, CAIRNCROSS S. Effect of washing hands with soap on diarrhea risk in the community: a systematic review. Lancet Infect Dis. 2003; 3: 275–81. 59. LUBY SP, AGBOATWALLA M, PAINTER J, ALTAF A, BILLHIMER WL, HOEKSTRA RH. Effect of Intensive Handwashing Promotion on Childhood Diarrhea in High-Risk Communities in Pakistan. A Randomized Controlled Trial. JAMA. 2004; 291:2547-2554. 60. EJEMOT RI, EHIRI JE,MEREMIKWUMM, CRITCHLEY JA. Hand washing for preventing diarrhoea. Cochrane Database of Systematic Reviews. 2008, Issue 1. Art. No.: CD004265. DOI: 10.1002/14651858. CD004265.pub2. 61. LUBY SP, AGBOATWALLA M, PAINTER J, ALTAF A, BILLHIMER W, KESWICK B, HOEKSTRA RM. Combining drinking water treatment and hand washing for diarrhoea prevention, a cluster randomised controlled trial. Tropical Medicine and International Health. 2006. volume 11 no 4 pp 479–489 april. 62. SOARES-WEISER KARLA, MACLEHOSE HARRIET, BEN-AHARON IRIT, GOLDBERG ELAD, PITAN FEMI, CUNLIFFE NIGEL. Vaccines for preventing rotavirus diarrhoea: vaccines in use. Cochrane Database of Systematic Reviews. In: The Cochrane Library. 2011, Issue 04, Art. No. CD008521. DOI: 10.1002/14651858. CD008521.pub5. 63. KRAMER M, KAKUMA R. Optimal duration of exclusive breastfeeding. Cochrane Database of Systematic Reviews. 2009, Issue 1. Art. No.: CD003517. DOI: 10.1002/14651858.CD003517. 64. LÓPEZ Y, SÁNCHEZ F, PERSIA S. Impacto de Programas de Lactancia Exclusiva y Control de Enfermedades Diarreicas en el dispensario médico del INTEC y sus comunidades, Santo Domingo, abrilmayo2000. Rev Med Dom. 2000; 61 (2): 108-114. 65. FEWTRELL M, WILSON D, BOOTH I, LUCAS A. Six months of exclusive breast feeding: how good is the evidence?. BMJ. 2011;342:c5955. 66. WHO Media Centre Statement. 15 January 2011. Exclusive breastfeeding for six months best for babies everywhere. Disponible en: http://www.who.int/mediacentre/news/statements/2011/breastfeeding_20110115/en/index.html#. [Consulta: Abril 2011]. 67. CÁCERES D, ESTRADA E, DEANTONIO R, PELÁEZ D. La enfermedad diarreica aguda: un reto para la salud pública en Colombia. Rev Panam Salud Pública. 2005;17(1):6–14. 68. WHO. Water, sanitation and hygiene: quantifying the health impact at national and local levels in countries with incomplete water supply and sanitation coverage. World Health Organization, Geneva, 2007. (WHO Environmental Burden of Disease Series No. 15). Disponible en: http://whqlibdoc.who.int/publications/2007/9789241595759_eng.pdf. [Consulta: Abril 2011]. 69. CLASEN T, ROBERTS I, RABIE T, SCHMIDT P, Cairncross S. Interventions to improve water quality for preventing diarrhoea. Cochrane Database of Systematic Reviews 2006, Issue 3. Art. No.: CD004794. DOI: 10.1002/14651858.CD004794.pub2. 70. Acute Gastroenteritis Guideline Team, Cincinnati Childrens Hospital Medical Center: Evidence-based clinical care guideline for medical management of acute gastroenteritis in children aged 2 months through 5 years. Guideline 5, pages 1-15, October 31, 2005. Disponible en: http://www.cincinnatichildrens.org/svc/alpha/h/health-policy/ev-based/gastro.htm. [Consulta: Agosto 2010]... CONTINUARÁ: Anexos y Tablas adicionales en la edición No 31-4.