INTRODUCCIÓN
Las fístulas y dehiscencias anastomóticas postoperatorias gastrointestinales son complicaciones que pueden comprometer cualquier nivel del tracto gastrointestinal, presentándose un 41% en recto, 29% en colon, 3% en intestino delgado, 9% en estómago y 16% en esófago 1). Aunque muchas de estas lesiones pueden tratarse quirúrgicamente, las intervenciones endoscópicas han mostrado ser una buena opción, para mejorar los desenlaces de curación y reducir estancia hospitalaria 2,3).
Entre las técnicas endoscópicas, contamos con la terapia de cierre asistida por vacío (E-VAC), que involucra la colocación endoscópica de un apósito de poliuretano conectado a un dispositivo de succión, a nivel de la fístula, que proporciona un drenaje continuo y efectivo de las colecciones perianasotomóticas, promueve la microcirculación y favorece el desarrollo de tejido de granulación para una correcta cicatrización, considerándose una técnica mínimamente invasiva, segura y eficaz 3). En el presente artículo se describe la experiencia de la terapia de cierre asistida por vacío (E-VAC), en pacientes que presentaron complicaciones tipo fístulas y dehiscencias anastomóticas postoperatorias, en un centro de referencia en Colombia.
MATERIALES Y MÉTODOS
Se realizó un estudio serie de casos de pacientes con evidencia dehiscencia de anastomosis y fístula a diferentes niveles del tracto digestivo, posterior a intervenciones quirúrgicas, tratados mediante E-VAC, en el servicio de gastroenterología y endoscopia digestiva de la Clínica Universitaria Colombia, durante un periodo comprendido entre febrero 2019 y noviembre 2021.
Se analizaron variables como edad, sexo, indicación quirúrgica, ubicación anatómica, tamaño del defecto, intervalo de recambio y numero de recambios, así como información nutricional y tiempo de hospitalización. Se intervinieron 6 pacientes con terapia E-VAC para manejo de fístulas y dehiscencias anastomóticas en cirugía gastrointestinal teniendo en cuenta la condición clínica y los hallazgos endoscópicos.
La fuente primaria de información fue la historia clínica de cada paciente y se recolectó la información en base de datos Excel. Se realizó un análisis descriptivo con frecuencias y proporciones para las variables cualitativas y medidas de tendencia central y de dispersión para las cuantitativas. Los datos se analizaron con el paquete estadístico STATA, v 15.0 (StataCorp. 2017. College Station, TX: StataCorp LLC).
RESULTADOS
Se describen 6 casos, 4 de lesiones a nivel del tracto digestivo inferior y 2 de tracto digestivo superior. El 83% fueron hombres, la edad media fue de 51,8 años (+/-17.5). La indicación de E-VAC fue fístula anastomótica colorrectal en el 66%, la ubicación anatómica más frecuente fue anastomosis colorrectal (66%), con menor frecuencia a nivel del cardias (16%) y esófago (16%) (Tabla 1). El compromiso del defecto en la anastomosis colorrectal se describió entre el 20 y el 80% en los 4 pacientes sometidos a terapia E-VAC. El número de recambios promedio fue de 7 recambios por paciente (Tabla 2).
Presentamos el caso de un paciente de 53 años que en el día 4 de postoperatorio de esofagodiverticulostomía endoscópica (Z-POEM) por un divertículo de Zenker, presentó una colección de 10 cm. x 3 cm. Entre la pared posterior de esófago y los cuerpos vertebrales, en quien se evidenció la dehiscencia en el cierre de la mucosotomía con una colección purulenta en mediastino superior y posterior. Se consideró drenaje de la colección mediastinal por vía endoscópica y posteriormente la colocación de un dren de Jackson Pratt por vía endoscópica en el mediastino, el cual se extrajo vía transnasal, y fue reemplazado a las 72 horas por un dispositivo Endosponge, el cual se alojó en el lecho de la colección mediastinal. El apósito fue cambiado a las 72 horas, y al retirar el segundo dispositivo, se evidenció el lecho quirúrgico limpio sin material purulento, con presencia de tejido de granulación, por lo que se decidió aplicación de sellante de fibrina + trombina humana (TISSEEL).
En este caso se logró la resolución de la colección mediastinal mediante intervenciones endoscópicas, requiriendo un total de 6 procedimientos endoscópicos, 3 de los cuales se realizaron de forma ambulatoria (Figura 1).
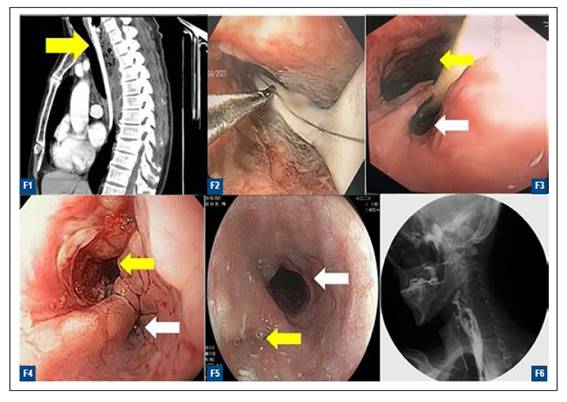
Figura 1 Colección localizada sobre la pared posterior del esófago y la cortical prevertebral que se extiende desde C7 hasta T5 a nivel de la carina de dimensiones 104x16x31 mm; F2: Posicionamiento endoscópico de sonda de drenaje con extremo distal en fondo de la cavidad del absceso mediastinal; F3: Visión endoscópica de la luz esofágica verdadera (Flecha blanca) y espacio prevertebral entre la pared posterior del esófago y la cortical de la columna vertebral a nivel de C5 (Flecha amarilla); F4: Espacio fistuloso prevertebral residual, 3 semanas posteriores al retiro del VAC. (Luz esofágica fecha blanca, Luz de trayecto fistuloso fecha amarilla); F5: Control endoscópico 6 semanas posteriores al retiro del VAC, Se observa la luz esofágica de calibre normal y la cicatriz del cierre del defecto de la pared posterior del esófago (Flecha amarilla); F6: Esofagograma post tratamiento.
El segundo caso se trata de un paciente de 42 años en día 15 de postoperatorio de manga gástrica extrainstitucional, que presentó una colección dependiente de la pared gástrica asociada a la dehiscencia parcial de la sutura mecánica, con un trayecto fistuloso hacia la pared abdominal. En este caso se programaron los recambios y revisiones endoscópicas cada 72 horas, requiriendo un total de 4 procedimientos endoscópicos, lográndose el drenaje total de la colección, sin embargo, con persistencia de dos defectos de solución de continuidad subcardiales de aproximadamente 10 a 15 mm, para lo que se consideró la colocación de un stent metálico completamente cubierto para cirugía bariátrica, alojando la copa distal en el bulbo duodenal y la copa proximal en el esófago inferior.
En el tracto digestivo inferior, presentamos el caso de una paciente de 54 años con adenocarcinoma de la unión rectosigmoidea, quien en el día 4 postoperatorio de resección anterior baja de recto presento una fistula anastomótica a 8 cm del margen anal con una dehiscencia de aproximadamente 30% de la circunferencia. El segundo caso es un paciente masculino de 59 años con adenocarcinoma de recto medio, llevado a resección anterior baja de recto con ileostomía de protección, que en el día 4 postoperatorio presentó una dehiscencia de la anastomosis colorrectal de aproximadamente el 20% de la circunferencia.
El tercer caso es un paciente masculino de 76 años con adenocarcinoma de recto medio, llevado a una resección anterior ultra baja de recto con ileostomía de protección, quien al día 5 del postoperatorio presentó una solución de continuidad de aproximadamente el 80% de la circunferencia; y por último el cuarto caso se trata de un paciente masculino de 24 años con antecedente de adenocarcinoma bajo de recto, llevado a resección anterior ultra baja con anastomosis coloanal manual, en quien se documentó una fístula a nivel de la anastomosis de aproximadamente 50% de la circunferencia (Figura 2).
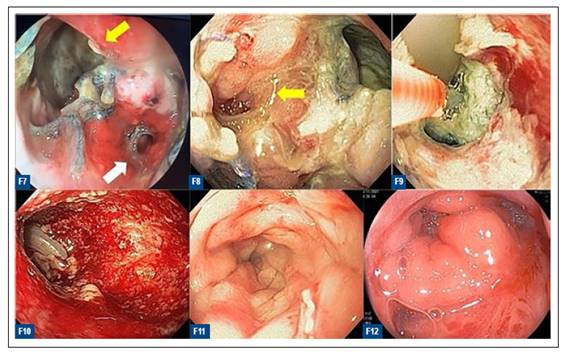
Figura 2 Dehiscencia de anastomosis coloanal asociado a la presencia de un absceso pélvico (fecha amarilla); F8-9: primera inserción de dispositivo VAC; F10: Tercera sesión de terapia VAC con evidencia de tejido de granulación a nivel de dehiscencia de anastomosis coloanal; F11-12: Evaluación final de respuesta a terapia VAC con evidencia de cierre total de la fístula.
DISCUSIÓN
Las fugas y fístulas anastomóticas son complicaciones complejas en cirugía del tracto gastrointestinal, especialmente en pacientes con patologías neoplásicas. En el caso de tumores de recto la escisión mesorrectal total crea una cavidad presacra cercana a la anastomosis donde puede haber acumulación de líquido y detritos que favorecen la presencia de colecciones sobreinfectadas 4,5). Se han identificado varios factores de riesgo para el desarrollo de estas lesiones, como los son el nivel de la anastomosis rectal, se sabe que las anastomosis inferiores (por debajo de 5 cm. Desde el margen anal) conllevan un riesgo 6 veces mayor de fugas, así lo describen Sharp et al. y tal como en 2 de nuestros casos; igualmente la radioterapia neoadyuvante, el estado nutricional del paciente al momento de la cirugía y el tabaquismo son factores de riesgo importantes. Aquellos pacientes que presentan fugas anastomóticas postoperatorias tienen mayor probabilidad de requerir una estoma permanente 6,7).
El manejo endoscópico surgió como una alternativa mínimamente invasiva para el manejo de estas lesiones, con altos índices de éxito y mejor perfil de seguridad en comparación al manejo quirúrgico 3,4). Weidenhagen et al. introdujeron la técnica de cierre endoscópico asistido por vacío en el 2008, inicialmente para el manejo de fugas anastomóticas colorrectales en pacientes con patologías neoplásicas que fueron llevados a resección anterior baja de recto 8) y desde entonces se ha posicionado como una de las intervenciones de elección para el manejo de estos pacientes 4,9).
Entre los años 2019 a 2021, se intervinieron 4 pacientes, con antecedente de adenocarcinoma de recto, todos recibieron neoadyuvancia, en postoperatorio de resección de recto según la localización del tumor, quienes durante el postoperatorio presentaron dehiscencias anastomóticas. En la tabla 3 se muestra información sobre el diagnóstico nutricional, tipo de intervención y días de estancia hospitalaria de estos casos, entre lo que destacamos el estado de desnutrición moderado/severo de estos pacientes y la reducción de la estancia hospitalaria. En tres de los cuatro casos se documentó la presencia de una colección asociada a la dehiscencia anastomótica, y en todos los casos se logró el drenaje completo de las colecciones. Se logró un cierre total de las fístulas anastomóticas en tres de los casos, en los cuales el compromiso de la anastomosis se encontraba entre el 20 al 50%; sin embargo, en el caso en el cual el compromiso anastomótico alcanzaba el 80% de la circunferencia, no fue posible el cierre total de defecto a pesar de lograrse el drenaje completo de la colección y la resolución total del proceso inflamatorio, requiriendo manejo con colostomía derivativa. En todos los casos, a excepción del paciente mencionado previamente, la mayoría de los procedimientos se realizaron de forma ambulatoria. Se realizaron cambios del dispositivo cada 72-96 horas y en promedio se necesitaron 7 procedimientos para lograr el cierre total del defecto, hallazgos similares a lo expuesto en otras series de casos y en revisiones sistemáticas (4, 14).
Los mecanismos mediante los cuales el E-VAC estimula el cierre de defecto transmural son: la microdeformación que conlleva a la reducción de tamaño del defecto durante la aplicación de presión negativa, al promover el cierre de la cavidad; la macrodeformación que está asociada a la generación de factores de crecimiento sobre los bordes de la lesión al ser sometida a presión negativa, cambios en la perfusión tisular inducidos por la presión negativa sobre el tejido que causa hipoxia, estimulando al factor hipoxia inducible 1α estimulando la angiogénesis y mejorando la perfusión tisular, además de la disminución de la carga bacteriana sobre el área comprometida lo cual acelera el proceso de cicatrización. Estos beneficios se han visto cuando la presión de vacío es de al menos -125 mmHg, el dispositivo puede ser colocado de forma intracavitaria si el defecto es mayor de 10 mm o endoluminal en caso de tener un tamaño menor 3). Adicionalmente, esta técnica permite el uso concomitante de otras intervenciones tales como sellantes de fibrina o implante de stents, acelerando el cierre de la filtración 5).
Posteriormente esta técnica se extendió a pacientes con lesiones esofágicas, que siguen siendo una condición potencialmente letal, con tasas de mortalidad que van desde el 25% si se intervienen en las primeras 24 horas de su instauración, alcanzando hasta el 60% cuando la intervención es retrasada 5); mortalidad asociada a complicaciones como fugas entéricas a la cavidad torácica o abdominal y sepsis 10).
Existen varias intervenciones endoscópicas que han sido utilizadas para estas lesiones, como clips, suturas endoscópicas y la colocación de stents, estos últimos asociados a complicaciones importantes como migración u obstrucción de los stents, o estenosis 10). Múltiples revisiones han mostrado que la tasa global de cierre de fugas con E-VAC respecto a otras intervenciones endoscópicas es de aproximadamente 84% versus 54%, como lo documentaron Brangewitz et al. 11), en una revisión retrospectiva en la cual se comparó el uso de E-VAC versus stents intra esofágicos en 71 pacientes con fugas esofágicas, demostrando una menor asociación con estenosis en el grupo E-VAC (9%) en comparación con el uso de stents esofágicos (28%).
Son estos hallazgos prometedores los que han llevado al uso de esta técnica en todo el tracto gastrointestinal 11,12), y aunque la evidencia disponible sobre el uso de E-VAC en fugas y fístulas anastomóticas en pacientes bariátricos es limitada, existen series de casos que evidencian la efectividad y seguridad de esta intervención en esta población, como la reportada por Morell et al.(13), quienes usaron la técnica E-VAC en 6 pacientes con fugas anastomóticas de cirugía bariátrica, logrando un cierre total del defecto en el 100% de los casos con mínimas complicaciones. El éxito de esta intervención en este escenario deriva de resultados favorables observados en el manejo de fugas y fístulas de otras etiologías, como la falla anastomótica secundaria a esofagectomía, síndrome de Boerhaave o perforaciones iatrogénicas, donde la tasa de cierre de fugas es hasta del 94% y se caracteriza por una rápida disminución del proceso inflamatorio y desarrollo de tejido de granulación desde el primer cambio de sistema E-VAC 13,14).
De forma importante vemos como en los dos casos de fístulas anastomóticas de tracto gastrointestinal superior, aparte de lograr un cierre total del defecto, esta técnica fue útil para lograr el adecuado drenaje y control de las colecciones asociadas, llevando a una resolución temprana del proceso infeccioso, favoreciendo el egreso hospitalario temprano en ambos casos y adicionalmente en uno de los dos casos, la fístula anastomótica esofágica, se logró la realización de la mitad de los procedimientos de forma ambulatoria, con mínimas complicaciones en ambos casos.
CONCLUSIONES
Las fugas y fístulas anastomóticas son complicaciones frecuentes y potencialmente mortales en pacientes llevados a intervenciones quirúrgicas gastrointestinales, siendo las intervenciones mínimamente invasivas una opción en el manejo en estos pacientes, y específicamente la terapia E-VAC ha mostrado ser eficaz y segura, promoviendo el cierre del defecto al favorecer la formación de tejido de granulación, y permitir el drenaje de colecciones presentes. Aunque faltan estudios prospectivos controlados para validar su uso en diferentes escenarios, los reportes de casos muestran resultados favorables con E-VAC como terapia de preferencia para estos pacientes.