Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Anales de la Facultad de Medicina
versión impresa ISSN 1025-5583
An. Fac. med. vol.80 no.2 Lima abr./jun. 2019
http://dx.doi.org/10.15381/anales.802.16418
ARTÍCULO DE REVISIÓN
Tumores del estroma gastrointestinal
Gastrointestinal stromal tumors
Jorge Soriano-Lorenzo1,a, Mayte Lima-Pérez2,b, Jorge Soriano-García2,c, Karla Zaldívar-Blanco1,d, Vilma Fleites-Calvo2,e
1 Facultad de Medicina "Manuel Fajardo", Universidad de Ciencias Médicas de La Habana. La Habana, Cuba.
2 Servicio de Oncología Clínica, Hospital Clínico-Quirúrgico "Hermanos Ameijeiras". La Habana, Cuba.
a Estudiante de medicina. ORCID: https://orcid.org/0000-0003-2211-5696.
b Especialista en oncología médica. ORCID: https://orcid.org/0000-0001-6607-3913.
c Especialista en oncología y Doctor en ciencias médicas. ORCID: https://orcid.org/0000-0002-7713-5750.
d Estudiante de medicina. ORCID: https://orcid.org/0000-0002-9606-4839.
e Especialista en oncología médica. ORCID: https://orcid.org/0000-0001-7218-4118.
RESUMEN
Los tumores del estroma gastrointestinal (GIST) son neoplasias mesenquimales originadas en el tracto gastrointestinal. Su localización más frecuente es en estómago e intestino delgado. Pueden originarse a cualquier edad, pero más del 80% de los casos son mayores de 50 años sin predilección de sexo, aunque puede observarse en pacientes más jóvenes asociados a síndromes que predisponen el desarrollo de estos tumores. Presentan sintomatología inespecífica. La tomografía axial computarizada está recomendada para realizar el estudio de extensión y seguimiento de estos pacientes. Los marcadores inmunohistoquímicos más sensibles y específicos son el KIT y DOG1. El tratamiento en caso de lesiones primarias localizadas es la resección quirúrgica, con o sin terapia adyuvante con imatinib durante 3 años en dependencia del riesgo de recidiva. En los casos avanzados o metastásicos se recomienda terapia neoadyuvante con imatinib por tiempo indefinido; el tratamiento en casos de progresión o intolerancia a imatinib es el sunitinib.
Palabras clave: Tumores del Estroma Gastrointestinal; Tracto Gastrointestinal; Mesilato de Imatinib (fuente: DeCS BIREME).
ABSTRACT
Gastrointestinal stromal tumors (GIST) are mesenchymal neoplasms that arise in the gastrointestinal tract, usually in the stomach or the small intestine. GISTs can arise at any age, but more than 80% are reported in individuals older than 50 years men and women are affected at a roughly similar frequency. The few patients are who younger frequently have GIST associated with a syndrome. The clinical manifestations are non-specifics. The computer-tomography is recommended for staging and follow-up. The KIT and DOG1 are the most sensitive and specific immunohistochemistry markers. The standard treatment of localized GIST is complete surgical excision of the lesion, with or without adjuvant imatinib in dependence with the relapse risk. Neoadjuvant imatinib is the standard treatment for locally advanced and metastatic disease. In locally advanced and metastatic disease the imatinib treatment should be continued indefinitely. Following confirmed progression, or intolerance, to imatinib the standard second-line treatment is sunitinib.
Keywords: Gastrointestinal Stromal Tumors; Gastrointestinal Tract; Imatinib Mesylate (source: MeSH NLM).
INTRODUCCIÓN
Los tumores del estroma gastrointestinal (GIST: Gastrointestinal Stromal Tumors) son neoplasias originadas a partir de tejido mesenquimal del tracto gastrointestinal, más raramente se originan en otros tejidos mesenquimales intraabdominales. Su origen celular más probable es de las células intersticiales de Cajal localizadas en el plexo mientérico del tracto gastrointestinal1,2.
Pueden originarse en cualquier sitio a lo largo del tracto digestivo, pero sus localizaciones más frecuentes son el estómago (50-60%), intestino delgado (30-35%), y son menos frecuentes en colon y recto (5%) y en esófago (<1%). Los casos encontrados en otras localizaciones de la cavidad abdominal corresponden al omento, mesenterio y retroperitoneo (<5%), que en ocasiones son resultado de metástasis de un GIST primario no detectado2.
Un 10 a 20% de los pacientes presentan metástasis al momento del diagnóstico, y un 40% de los pacientes con diagnóstico de GIST localizados lo desarrollarán evolutivamente. Los sitios más comunes son el hígado, el omento, y el peritoneo, mientras que las localizaciones extra-abdominales son infrecuentes1.
Se estima que la prevalencia es de aproximadamente 130 casos por millón de habitantes. La edad media de aparición es de 60-65 años sin predilección de sexo, aunque puede observarse en pacientes jóvenes sobre todo asociado a síndromes que predisponen el desarrollo de estos tumores3,4.
METODOLOGÍA DE LA BÚSQUEDA Y SELECCIÓN DE RESULTADOS
En el presente artículo presentamos una revisión de los aspectos clínico-patológicos y terapéuticos más importantes de este tipo de tumores, para ello se realizó una búsqueda en la base de datos PubMed. Los términos de búsqueda fueron "tumor de estroma gastrointestinal e imatinib", "tumor de estroma gastrointestinal y cirugía", "tumor de estroma gastrointestinal y sunitinib" y "tumor de estroma gastrointestinal y regorafenib". El resultado fue un total de 3010 artículos; se analizaron aquellos artículos publicados a partir del año 2000 hasta la fecha. Se incluyeron solamente artículos originales y artículos de revisión. Los resultados de la búsqueda fueron obtenidos en idioma inglés. Los artículos fueron evaluados inicialmente por su título y resumen. Los artículos de interés fueron revisados a texto completo por los autores (358). Se excluyeron aquellos artículos publicados antes de año 2000, publicaciones de reportes de casos, artículos no disponibles a texto completo y artículos cuyo título y resumen no respondían a los objetivos de nuestro estudio.
DESARROLLO DEL TEMA
Factores de riesgo
Se reporta en la mayoría de los casos como una enfermedad esporádica en la cual no puede establecerse relación con un factor de riesgo causal. Sin embargo, algunos GIST surgen en relación con síndromes específicos1,5.
Las mutaciones hereditarias en el gen KIT exones 8, 11, 13 o 17 confieren un alto riesgo de desarrollar GIST de estómago o intestino delgado en edades tan tempranas como 18 años. Las mutaciones hereditarias de PDGFRA se asocian a un elevado riesgo de presentar GIST y frecuentemente desarrollan pólipos inflamatorios de localización gástrica y en intestino delgado. La asociación de GIST gástrico, paraganglioma y condroma pulmonar conocida como triada de Carney es una condición rara no hereditaria que se presenta mayormente en niñas y mujeres jóvenes. Estos casos no presentan expresión de KIT ni de PDGFRA en la inmunohistoquímica, pero muestran baja expresión de la subunidad B de la succinato deshidrogenasa. De forma similar ocurre con el síndrome de Carney-Stratakis, donde se presentan mutaciones en la línea germinal que afecta a subunidades de la enzima succinato deshidrogenasa (SDHA, SDHB, SDHC, SDHD). Los pacientes con neurofibromatosis tipo 1 también presentan un elevado riesgo de desarrollar uno o más tumores de localización principalmente en estómago o intestino delgado1,6,7.
Manifestaciones clínicas y diagnóstico
Aunque la mayoría de pacientes presentan síntomas o masa palpable, en un número considerable se detecta de forma accidental. Los síntomas frecuentes en este tipo de tumor son el sangrado intra-intestinal y en cavidad abdominal, la anemia, dolor abdominal, dispepsia, constipación, náuseas y vómitos. Puede desencadenarse también un cuadro de hemorragia por ruptura tumoral y perforación intestinal, la cual requiere tratamiento quirúrgico de emergencia 8.
El estudio imagenológico mediante tomografía axial computarizada (TAC) multicorte de abdomen y pelvis es el método más apropiado para la realización del estudio de extensión y seguimiento de los GIST. La resonancia magnética (RM) se utiliza como complemento en GIST de recto para visualizar relación con otras estructuras, también se indica para evaluación de lesiones hepáticas indeterminadas en la TAC y en casos donde la TAC está contraindicada. En la imagen por TAC el tumor puede apreciarse como una masa exoluminal bien determinada, que luego de la administración de contraste muestra un realce heterogéneo sobre todo en los tumores de gran tamaño, los cuales pueden tener áreas de necrosis. La tomografía por emisión de positrones puede emplearse para seguimiento y evaluación de respuesta al tratamiento9.
En caso de lesión resecable y altamente sospechosa, no es necesaria la realización de biopsia pre-quirúrgica, debido al riesgo de sangrado y contaminación tumoral de la cavidad abdominal. En caso de que se presente una masa abdominal ≥ 2cm no apta para valoración mediante endoscopia, el abordaje estándar es la extirpación mediante laparotomía o laparoscopía para una posterior confirmación histológica. En casos de metástasis hepática, la toma de muestra de dicha lesión metastásica puede establecer el diagnóstico9,10.
Anatomía patológica
Se distinguen tres patrones morfológicos: fusocelulares, epitelioides y mixtos. Las técnicas de inmunohistoquímica (IHQ) son de gran utilidad en el diagnóstico anatomopatológico, los marcadores más sensibles y específicos son el KIT (CD117) y el DOG111. En diversos estudios el marcador DOG1 ha mostrado una gran sensibilidad y especificidad para el diagnóstico de GIST, sobre todo en casos KIT negativo12,13. Los GIST que no muestran inmunorreatividad para la proteína KIT, presentan la mayoría mutaciones activa-doras del PDGFRA. Otros marcadores de IHQ son el CD34 el cual es expresado en alrededor del 70%, un 20-30% de los casos son positivos para la actina, un 8-10% muestran positividad para la proteína S100 y un 2-4% para la desmina14. También se ha identificado el marcador PKCθ, que puede ser de utilidad en la identificación de GIST con negatividad a los marcadores habituales15. Los receptores KIT y PDGFRA son miembros de la familia de receptores tirosin-quinasa tipo III, son activados mediante la unión con sus respectivos ligandos (figura 1). Las mutaciones en KIT y PDGFRA son mutuamente excluyentes16.
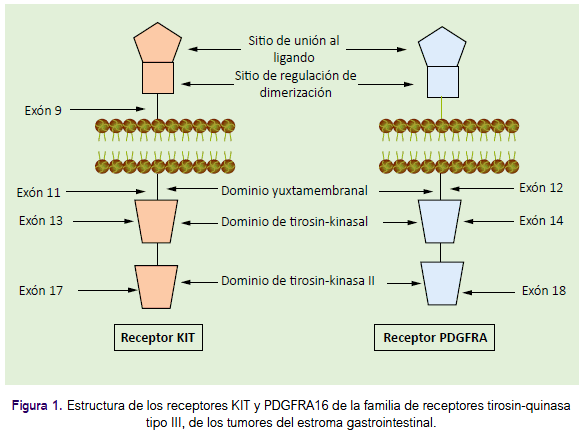
El 75-80% de los GIST presenta mutación del gen KIT, en el 75% de los casos esta mutación ocurre en el exón 11, que afecta la región yuxtamembranal1,17. Entre un 7-10% de los GIST posee mutaciones en el exón 9 que afecta el dominio extracelular; esta mutación provoca un cambio conformacional en el receptor que imita al que sucede cuando se une con su ligando, lo cual mantiene una activación permanente. Esta mutación ocurre fundamentalmente en GIST de intestino delgado y grueso, y raramente ocurre en GIST de localización gástrica18. Las mutaciones en el circuito de activación de la tirosin-kinasa (exón 17) son infrecuentes, al igual que las de la región de unión del ATP (exón 13)19,20,21.
Cerca de un 20-25% de los GIST no poseen mutaciones del receptor KIT; en estos casos, cerca del 10% presenta mutación en el receptor PDGFRA, el cual es un receptor con función similar. Las mutaciones en PDGFRA poseen una importancia similar a las de KIT. Este receptor está formado igualmente por un dominio yuxtamembranal el cual es codificado por el exón 12, un dominio de unión a ATP codificado por el exón 14 y un circuito de activación de la tirosin-quinasa codificado por el exón 1822. La mutación de este receptor provoca una activación constante del mismo en ausencia de su ligando especifico. Las vías por que resultan de la activación de este receptor son idénticas a las activadas por el receptor KIT23. A pesar de la semejanza molecular, los GIST con mutaciones en el receptor PDGFRA muestran algunas diferencias en la presentación patológica con respecto a los GIST con mutaciones en el receptor KIT, que incluye diferencias en el perfil de expresión genética, una sorprendente predilección por el estómago, una expresión variable de la mutación KIT y generalmente un bajo potencial de malignidad24.
De un 10-15% de los GIST no presentan mutaciones en KIT ni en PDGFRA, los cuales son llamados tipo salvaje (en inglés: Wild-Type) 1. Los GIST tipo salvaje pueden clasificarse en dos grupos: SDH-deficiente o no SDH-deficiente. Dentro del grupo SDH-deficiente se encuentran los casos de GIST que ocurren en los pacientes con triada de Carney y en el síndrome de Carney-Strataky; en el grupo de los no SDH-deficiente están los casos de los GIST en pacientes con neurofibromatosis tipo 125,26.
Pronóstico y estadificación
Los factores pronósticos más importantes en el paciente con GIST son el tamaño, el sitio del tumor y el índice mitótico. Miettinen et al.27, en un estudio realizado con 1765 pacientes con diagnóstico de GIST gástrico, reportaron que el índice de metástasis fue de un 86% para los tumores >10 cm con un índice mitótico de >5 mitosis/50HPF; mientras que en los tumores de igual tamaño, pero con un índice mitótico <5 mitosis/50HPF era de un 11%, lo cual demuestra que para establecer el pronóstico de riesgo basado solamente en el tamaño tumoral y el índice mitótico es muy difícil. Por otra parte, en un estudio posterior que incluyó 906 pacientes con diagnóstico de GIST de intestino delgado, un tamaño tumoral >10 cm con un índice mitótico de <5 mitosis/50HPF tuvo un índice de metástasis de un 50%, lo cual establecía que la diferencia en el sitio anatómico donde el tumor se desarrolla es un factor a considerar al momento de establecer un pronóstico28. DeMatteo et al.29, en un estudio que incluyó 127 pacientes con GIST localizados de los cuales 74 pacientes tenían localización gástrica, 35 en intestino delgado, 14 en colon/recto y 4 en otras localizaciones, encontró mayor supervivencia en pacientes con GIST de localización gástrica respecto a los de localización intestinal y de colon/recto, así como mayor supervivencia en aquellos que presentaban un tamaño tumoral <5 cm y un índice mitótico <5 mitosis/50HPF.
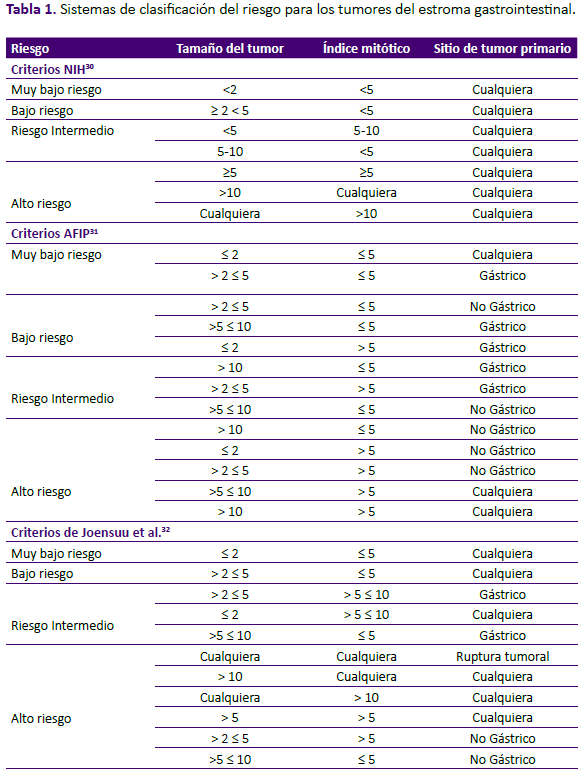
Se han propuesto varios sistemas de clasificación para el pronóstico de los GIST, dos de los más aceptados son los desarrollados por el Instituto Nacional de Salud de los Estados Unidos (NIH) y el Instituto de Patología de las Fuerzas Armadas (AFIP)30,31. Más recientemente, Joensuu et al.32, propuso una clasificación modificada de estos criterios (tabla 1). Estos sistemas de clasificación han sido sometidos a comparación y validación en diferentes estudios, así como muchos de estos trabajos han propuesto la modificación de estos sistemas incluyendo factores adicionales como la invasión de la mucosa, la ulceración del tumor y la ruptura tumoral33,34,35.
En el año 2009, el Memorial Sloan-Kattering Cancer Center desarrolló un nomograma para la predicción del riesgo de recurrencia a 2 y 5 años luego de la resección quirúrgica de los GIST localizados36. Este nomograma ha sido comparado con los tres sistemas de clasificación anteriormente citados y mostró mayor sensibilidad en la predicción de recurrencias37.
Tratamiento
Enfermedad local
La resección quirúrgica completa sin disección de los ganglios linfáticos clínicamente negativos es el tratamiento de elección en caso de GIST localizado. El objetivo es conseguir una resección con márgenes libres de células tumorales (R0). En aquellos casos en los que no se puede conseguir una resección con márgenes libres y los tratamientos pre-operatorios sean inefectivos, se recomienda la cirugía con resección de márgenes microscópicamente positivos (R1)9. Los principales factores que condicionan una R1 son el tamaño tumoral ≥ 10 cm, la localización y el riesgo de ruptura tumoral. McCarter et al.,38 en un estudio que incluyó 819 pacientes procedentes de los estudios ACOSOG Z9000 y ACOSOG Z9001, registró un total de 72 pacientes con confirmación anatomopatológica de R1. Para los pacientes incluidos en el grupo placebo del estudio Z9001, la diferencia en la supervivencia libre de recurrencia (SLR) entre los R1 y R0 no fue significativa (60% vs 76% a 3 años, HR=1,51, 95% IC: 0,76-2,99, p=0,24). De forma similar, en aquellos pacientes de ambos estudios que recibieron tratamiento por 1 año con imatinib, la diferencia de SLR entre pacientes R1 y R0 no fue significativa (82% vs 79% a 3 años, HR=1,095, 95% IC: 0,66-1,82, p=0,73). Sin embargo, el riesgo global de recurrencia fue de 36% en R1 y 27% para R0. Se observó mayor riesgo de recurrencia entre los pacientes R1 que habían sufrido ruptura tumoral con respecto a aquellos que no la habían sufrido con una SLR de 60% en los casos de ruptura y un 80% en los que no (HR=3,58, 95% IC:1,65-7,79, p=0,001). Zhi et al.39, en un meta-análisis realizado con el objetivo de estimar el valor pronóstico de los márgenes quirúrgicos para la supervivencia libre de enfermedad (SLE) y la supervivencia global (SG) en los pacientes con GIST, obtuvo que el índice de recurrencia global de para los grupos R1 y R0 eran de 0,364 (95% IC: 0,299– 0,429) y 0,296 (95% IC: 0,161–0,430), respectivamente. Este meta-análisis confirmó que los márgenes microscópicos influyen en la SLE (HR=1,596, 95% IC: 1,128–2,258; I2=37,5%, p=0,091), pero no en la SG (HR=1,43, 95% IC: 0,608–3,363; I 2 = 60,8%, p=0,013). También concluyó que el tratamiento con imatinib puede atenuar el riesgo de recurrencia de GIST primarios con márgenes R1.
El abordaje quirúrgico mediante laparoscopia puede considerarse en aquellos casos con una localización anatómica favorable. Chen et al.40, en un meta-análisis que incluyó 19 estudios reveló que no existen diferencias en cuanto al resultado a largo plazo en la utilización de laparotomía o laparoscopia, aunque el empleo de la laparoscopia está asociado a un menor índice de complicaciones y corta estadía hospitalaria. Sin embargo, el abordaje laparoscópico no se aconseja en tumores de gran tamaño debido al riesgo de ruptura tumoral41.
En los pacientes de alto riesgo de recaída, el imatinib en terapia adyuvante es el tratamiento estándar. En los estudios ACOSOG Z9000 y ACOSOG Z9001, se demostró que el uso del imatinib en pacientes con alto riesgo de recurrencias prolongaba la SG, aunque la duración óptima de la terapia permanecía indefinida42-44. Posteriormente, el estudio SSGXVIII/AIO45,46, demostró que la terapia extendida a tres años con imatinib posee mejores resultados de supervivencia respecto al tratamiento por un año.
En el estudio SSGXVIII/AIO47, se investigó el efecto de las mutaciones de los genes KIT y PDGFRA sobre la SLR en pacientes tratados con cirugía e imatinib adyuvante, este estudio concluyó que los pacientes con delecciones del exón 11 del gen KIT se beneficiaron con una terapia adyuvante de imatinib más prolongada (3 años) que aquellos que la recibieron durante menos tiempo (1 año). También se obtuvo que los pacientes con mutaciones de los genes PDGFRA y las inserciones o duplicaciones del exón 11 del gen KIT estaban asociadas a una mejor SLR, no así en las mutaciones del exón 9 del gen KIT. Según las recomendaciones, para el diagnóstico y tratamiento de los GIST de la Sociedad Europea de Oncología Médica, los GIST modificados con PDGFRA D842V no deben tratarse con ninguna terapia adyuvante, dada la falta de sensibilidad de este genotipo tanto in vitro como in vivo. Igualmente, los GIST-WT, no poseen indicación de tratamiento adyuvante con imatinib debido a la falta de sensibilidad a este y a otros inhibidores de la tirosinkinasa9.
Se reconocen 5 factores de riesgo para la recurrencia luego de la terapia con imatinib (alto índice mitótico, localización no gástrica, gran tamaño tumoral, ruptura tumoral, terapia adyuvante de 12 meses), los cuales están relacionados de forma independiente con una menor SLR48.
• Enfermedad localmente avanzada y metastásica
La terapia estándar en casos de GIST localmente avanzado, inoperable y metastásico, es el imatinib. En estos pacientes el tratamiento con imatinib es recomendable que se continúe indefinidamente, dado que su interrupción esta seguida de rápida progresión tumoral. En los estudios S0033/CALGB 15010549,50 y EORTC 6200551,52, se evaluó la eficacia de la administración de imatinib a dos dosis iniciales (400mg/día vs 800mg/día en dos dosis de 400mg) en pacientes con enfermedad metastásica o irresecable, ambos estudios mostraron respuestas equivalentes en cuanto a SG para ambas dosis, pero dosis más elevadas estaban asociadas a mayor presencia de efectos adversos. Actualmente la dosis recomendada de imatinib es 400mg/día, lo cual resulta seguro y eficaz; la elevación de la dosis a 800mg/día puede valorarse en casos de progresión con el uso de la dosis estándar.
Hay datos de que en pacientes con tumores portadores de la mutación KIT en el exón 9 tienen mejor Supervivencia Libre de Progresión (SLP) con dosis elevadas, por lo que en este grupo de pacientes se recomienda la administración de 800mg/día. En los pacientes con WTGIST SDH-deficientes hay dudas sobre el beneficio de los inhibidores de la tirosinkinasa, aunque existen reportes de beneficio con el uso del sunitinib53,54.
El uso de la terapia neoadyuvante con imatinib es otra opción que ha resultado beneficiosa. Los estudios originados de análisis retrospectivos con el uso de terapia neoadyuvante han promovido el desarrollo de ensayos clínicos utilizando este esquema. El estudio fase II RTOG 0132/ACRIN 666555 evaluó la seguridad y eficacia del uso del imatinib neoadyuvante en pacientes con GIST primario potencialmente resecable, (Grupo A: 30 pacientes) y con enfermedad metastásica o recurrente potencialmente resecable, (Grupo B: 22 pacientes). La SLP a 2 años fue de 83% para el grupo A y 77% para el grupo B, y la SG fue de 93% para el grupo A y 91% para el grupo B. En el estudio fase III BFR-1456, que incluyó a 25 pacientes con GIST avanzado no metastásico, el 60% tuvo una respuesta parcial a la terapia neoadyuvante con imatinib. A todos los pacientes incluidos en este estudio se le siguió administrando el imatinib, con una mediana de seguimiento de 53,5 meses y se observó una mejoría en la SLP y SG en los pacientes que habían sido sometidos a cirugía luego de la terapia con imatinib con respecto a aquellos que no habían sido operados. En el grupo de los pacientes sometidos a cirugía la SLP a 3 años y la SG fue de 67% y 89% respectivamente. El uso de la terapia neoadyuvante facilita la exéresis quirúrgica y reduce las complicaciones quirúrgicas.
En los casos de progresión de la enfermedad o aquellos pacientes que no toleren la terapia con imatinib, el tratamiento de segunda línea es el sunitinib. Demetri et al.57, en un estudio fase III evaluaron el beneficio del uso de sunitinib en pacientes con resistencia o intolerancia a imatinib. Este estudio demostró un significativo beneficio clínico en cuanto a control de la enfermedad y aumento de la supervivencia en los pacientes tratados con sunitinib luego de la terapia fallida con imatinib. Resultados de un estudio internacional58 que incluyó 1124 pacientes, diseñado con el objetivo de evaluar los beneficios de la terapia con sunitinib, mostró una SLP de 8,3 meses y una SG de 16,6 meses. La dosis recomendada de sunitinib es de 50mg/día durante 4 semanas con 2 semanas de descanso. Otra alternativa que ha resultado ser muy eficaz es la administración de 37,5mg/día de forma ininterrumpida. Los eventos adversos más frecuentes con el uso de este fármaco son la astenia, toxicidad en piel, diarrea, hipertensión e hipotiroidismo. Por lo general son eventos ligeros, lo cual hace que la terapia sea bien tolerada en la mayoría de los casos57 .
La presencia de mutaciones KIT han sido identificadas como predictor de la respuesta terapéutica al tratamiento con imatinib. Las mutaciones del KIT exón 11 están asociadas con una mejor respuesta SLP y SG con respecto a las mutaciones de KIT exón 9 o los WT-GIST. El estudio EORTC-6200559 identificó la presencia de mutaciones en KIT exón 9 como un factor pronostico adverso. En este estudio, el tratamiento con dosis elevadas de imatinib a 800mg/día obtuvo mejores resultados de SLP en los pacientes con GIST portadores de esta mutación. El estudio fase III SWOG S0033/CALGB 15010560, obtuvo igualmente mejores resultados terapéuticos con el uso de 800mg/día para el tratamiento de los pacientes con mutaciones KIT exón 9, pero los resultados obtenidos en la SLP no fueron confirmados, además en este estudio se observó que aquellos pacientes con CD117 positivo obtenían mejores resultados de SG en comparación con los CD 117 negativo, lo cual refleja un beneficio de la terapia con imatinib en estos pacientes. Heinrich et al.61, en un estudio realizado con 97 pacientes con GIST metastásico resistentes al imatinib, obtuvo con la terapia con sunitinib mejores respuestas en pacientes con mutaciones KIT exón 9 o WT-GIST que en aquellos con mutaciones KIT exón 11, lo que se evidencia por mayores índices de SLP y SG.
En aquellos pacientes con GIST localmente avanzado, no resecable o metastásico resistentes a la terapia con imatinib y sunitinib, está indicado el tratamiento con regorafenib. El estudio fase III GRID62, 199 pacientes con GIST metastásico tratados previamente con imatinib y sunitinib fueron distribuidos de forma aleatoria a recibir regorafenib (n=133) o placebo (n=66), la SLP fue mayor en los pacientes que recibieron regorafenib (4,8 meses vs 0,9 meses; p< 0,0001).
Otros fármacos como el nilotinib, sorafenib, papazonib y dasatinib han sido empleados en pacientes con GIST resistentes a imatinib y sunitinib. Los resultados terapéuticos con estos fármacos provienen de estudios en su mayoría fase I-II. El nilotinib ha sido evaluado en diversos ensayos clínicos, en donde sus beneficios terapéuticos no han demostrado gran eficacia. En un estudio fase III, no mostró superioridad a la terapia de apoyo (109 días vs 111 días; p=0,65)63, aunque se sugiere que puede haber un beneficio en pacientes con mutación KIT exón 17 que han sido previamente tratados con imatinib y sunitinib64. El dasatinib ha mostrado eficacia en los GIST con mutación PDGFRA D842V la cual confiere resistencia al tratamiento con imatinib, por lo que puede ser de utilidad en este grupo de pacientes65. Es necesario el desarrollo de posteriores investigaciones para determinar el beneficio terapéutico de estos nuevos fármacos en los pacientes con GIST.
CONCLUSIONES
Los GIST son neoplasias originadas a partir del tejido mesenquimal del tracto gastrointestinal. Su localización más frecuente es en estómago. Las manifestaciones clínicas son inespecíficas. El método para la realización del estudio de extensión en estos pacientes es la TAC. La realización de biopsia pre-quirúrgica no es necesaria en los casos de lesiones con alto índice de sospecha. Los marcadores más sensibles y específicos son KIT (CD117) y el DOG1, en los casos de negatividad a KIT la mayoría presenta mutación de PDGFRA. Aquellos GIST con negatividad a las mutaciones KIT y PDGFRA son denominados GIST salvajes. Los factores pronósticos más importantes son el tamaño, el índice mitótico, y el sitio del tumor. El nomograma desarrollado por el Memorial Sloan-Kattering Cancer Center, resulta adecuado para la predicción de recurrencias. En los GIST localizados el tratamiento estándar es la resección quirúrgica sin disección de ganglios clínicamente negativos, tratando siempre que sea posible conseguir una resección con bordes libre. El uso de terapia adyuvante con imatinib por 3 años se recomienda en aquellos casos de GIST primarios con alto riesgo de recurrencia. En los GIST localmente avanzados y metastásicos se recomienda el tratamiento con imatinib como tratamiento de primera línea, el cual debe ser administrado de forma indefinida, en los casos de intolerancia o progresión tumoral con este, el tratamiento de segunda línea es sunitinib.
REFERENCIAS BIBLIOGRÁFICAS
1. Joensuu H, Hohenberger P, Corless C. Gastrointestinal stromal tumour. Lancet. 2013; 382(9896):973- 83. DOI: 10.1016/S0140-6736(13)60106-3. [ Links ]
2. Corless C. Gastrointestinal stromal tumors: what do we know now?. Modern Pathology. 2014; 27:S1- S16. DOI: 10.1038/modpathol.2013.173. [ Links ]
3. Muccariani C, Rossi G, Bertolini F, Valli R, Cirilli C, Rashid I, et al. Incidence and clinicopathologic features of gastrointestinal stromal tumors. A population-based study. BMC Cancer. 2007; 7:230-36. DOI: 10.1186/1471-2407-7-230. [ Links ]
4. Chan KH, Chan CW, Chow WH, Kwan WK, Kong CK, Mak KF, et al. Gastrointestinal stromal tumors in a cohort of Chinese patients in Hong Kong. World J Gastroenterol. 2006; 12(14): 2223–28. DOI: 10.3748/wjg.v12.i14.2223. [ Links ]
5. Lynch HT, Lynch JF, Shaw TG. Hereditary gastrointestinal cancer syndromes. Gastrointest Cancer Res. 2011;4(suppl 1):S9-S17. [ Links ]
6. Gaal J, Stratakis CA, Carney JA, Ball ER, Kor pershoek E, Lodish MB, et al. SDHB immune-histochemistry: a useful tool in the diagnosis of Carney-Stratakis and Carney triad gastrointestinal stromal tumors. Mod Pathol. 2011; 24(1): 147–51. DOI: 10.1038/modpathol.2010.185. [ Links ]
7. Zhang L, Smyrk TC, Young WF, Stratakis CA, Carney JA. Gastric stromal tumors in Carney triad are different clinically, pathologically, and behaviorally from sporadic gastric gastrointestinal stromal tumors: findings in 104 cases. Am J Surg Pathol. 2010; 34(1): 53–64. DOI: 10.1097/PAS.0b013e3181c20f4f. [ Links ]
8. Caterino S, Lorenzon L, Petrucciani N, Iannicelli E, Pilozzi E, Romatini A, et al. Gastrointestinal stromal tumor: correlation between symptoms at presentation, tumor location and prognosis factor in 47 consecutive patients. World J Surg Oncol. 2011; 9:13. DOI: 10.1186/1477-7819-9-13. [ Links ]
9. Casali PG, Abecassis N, Bauer S, Bielack S, Bonvalot S, Boukovinas I, et al. Gastrointestinal stromal tumours: ESMO-EURACAN clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2018; 0(suppl 0):iv1-iv11. DOI: 10.1093/annonc/mdy095. [ Links ]
10. Sepe PS, Moparty B, Pitman MB, Saltzman JR, Brugge WR. EUS-guide FNA for the diagnosis of GI stromal cell tumors: sensitivity and cytologic yield. Gastrointest Endosc. 2009; 70(2):254-61. DOI: 10.1016/j.gie.2008.11.038. [ Links ]
11. Novelli M, Rossi S, Rodriguez-Justo M, Taniere P, Seddon B, Toffolatti L, et al. DOG1 and CD117 are the antibodies of choice in the diagnosis of gastrointestinal stromal tumors. Histopathology. 2010; 57(2): 259–70. DOI: 10.1111/j.1365-2559.2010.03624.x. [ Links ]
12. Güler B, Özyılmaz F, Tokuç B, Can N, Taştekin E. Histopathological features of gastrointestinal stromal tumor and the contribution of DOG1 expression to the diagnosis. Balkan Med J. 2015; 32(4):388-96. DOI: 10.5152/balkanmedj.2015.15912.
13. Sahin S, Ekinci Ö, Seçkin S, Dursun A. The diagnosis and prognostic utility of DOG1 expression on gastrointestinal stromal tumors. Turk Patoloji Derg. 2017; 33(1):1-8. DOI: 10.5146/tjpath.2016.01376. [ Links ]
14. Kiśluk J, Zińczuk J, Kemona A, GuzińskaUstymowicz K, Żurawska J, Kędra B. Expression of CD117, DOG1 and IGF-1R in gastrointestinal stromal tumors- an analysis of 70 cases from 2004 to 2010. Gastroenterology Rev. 2016; 11(2):115–22. DOI: 10.5114/pg.2015.52587.
15. Kövecsi A, Jung I, Szentirmay Z, Bara T, Bara (Jr) T, Popa D, Gurzu S. PKCθ utility in diagnosing c-KIT/ DOG-1 double negative gastrointestinal stromal tumors. Oncotarget. 2017; 8(34): 55950-57. DOI: 10.18632/oncotarget.19116. [ Links ]
16. Corless CL, Barnett CM, Heinrich MC. Gastrointestinal stromal tumors: origin and molecular oncology. Nat Rev Cancer. 2011; 11(12):865-78. DOI: 10.1038/nrc3143. [ Links ]
17. Fletcher JA, Rubin B. KIT mutation in GIST. Current Opinion in Genetic & Development. 2007; 17(1):3- 7. DOI: 10.1016/j.gde.2006.12.010. [ Links ]
18. Yuzawa S, Opatowsky Y, Zhang Z, Mandiyan V, Lax I, Schlessinger J. Structural basis for activation of the receptor tyrosine kinase KIT by stem cell factor. Cell. 2007; 130(2):323–34. DOI: 10.1016/j.cell.2007.05.055. [ Links ]
19. Lasota J, Corless, Heinrich MC, Debiec-Rychter M, Sciot R, Wardelmann E, et al. Clinicopathologic profile of gastrointestinal stromal tumors (GISTs) with primary KIT exon 13 or exon 17 mutations: a multicenter study on 54 cases. Mod. Pathol. 2008; 21(4):476–84. DOI: 10.1038/modpathol.2008.2. [ Links ]
20. Duensing A, Medeiros F, McConarty B, Joseph NE, Panigrahy D, Singer S, et al. Mechanisms of oncogenic KIT signal transduction in primary gastrointestinal stromal tumors (GISTs). Oncogene. 2004; 23(22):3999–4006. DOI: 10.1038/sj.onc.1207525. [ Links ]
21. Bauer S, Duensing A, Demetri GD, Fletcher JA. KIT oncogenic signaling mechanisms in imatinibresistant gastrointestinal stromal tumor: PI3kinase/ AKT is a crucial survival pathway. Oncogene. 2007; 26(54):7560–68. DOI: 10.1038/sj.onc.1210558. [ Links ]
22. Heinrich MC, Corless CL, Duensing A, McGreevey L, Chen CJ, Joseph N, et al. PDGFRA activating mutations in gastrointestinal stromal tumors. Science. 2003; 299(5607):708–10. DOI: 10.1126/science.1079666. [ Links ]
23. Kang HJ, Nam SW, Kim H, Rhee H, Kim NG, Kim H, et al. Correlation of KIT and platelet-derived growth factor receptor alpha mutations with gene activation and expression profiles in gastrointestinal stromal tumors. Oncogene. 2008; 24(6):1066–74. DOI: 10.1038/sj.onc.1208358. [ Links ]
24. Subramanian S, West RB, Corless CL, Ou W, Rubin BP, Chu KM, et al. Gastrointestinal stromal tumors (GISTs) with KIT and PDGFRA mutations have distinct gene expression profiles. Oncogene. 2004; 23(47):7780–90. DOI: 10.1038/sj.onc.1208056. [ Links ]
25. Wada R, Arai H, Kure S, Pen WX, Naito Z. Wild type GIST: Clinicopathological features and clinical practice. Pathology International. 2016; 66(8):431- 37. DOI: 10.1111/pin.12431. [ Links ]
26. Debiec-Rychter M, Lasota J, Sarlomo-Rikala M, Kordek R, Miettinen M. Chromosomal aberrations in malignant gastrointestinal stromal tumors: correlation with c-KIT gene mutation. Cancer Genet Cytogenet. 2001; 128(1): 24–30. [ Links ]
27. Miettinen M, Sobin LH, Lasota J. Gastrointestinal stromal tumors of the stomach: a clinicopathologic, inmunohistochemical and molecular genetic study of 1765 cases with long-term follow-up. Am J Surg Pathol. 2005; 29(1):52-68. [ Links ]
28. Miettinen M, Makhlouf H, Sobin LH, Lasota J. Gastrointestinal stromal tumors of the jejunum and ileum: a clinicopathologic, inmunohistochemical, and molecular genetic study of 906 cases before imatinib with long-term follow-up. Am J Surg Pathol. 2006; 30(4):477-89. [ Links ]
29. DeMatteo R, Gold JS, Saran L, Gönen M, Liau KH, Maki RG, et al. Tumor mitotic rate, size and location independently predict recurrence after resection of primary gastrointestinal stromal tumor (GIST). Cancer. 2008; 112(3):608-15. DOI: 10.1002/cncr.23199. [ Links ]
30. Miettinen M, Lasota J. Gastrointestinal stromal tumors: pathology and prognosis at different sites. Sem Diagn Pathol. 2006; 23(2):70-83. [ Links ]
31. Fletcher CD, Berman JJ, Corless C, Gorstein F, Lasota J, Longley BJ, et al. Diagnosis of gastrointestinal stromal tumors: A consensus approach. Hum Pathol. 2002; 33(5):459–65. [ Links ]
32. Joensuu H. Risk stratification of patients diagnosed with gastrointestinal stromal tumor. Hum Pathol. 2008; 39(10):1411–19. DOI: 10.1016/j.humpath.2008.06.025. [ Links ]
33. Rutkowski P, Nowecki ZI, Michej W, DebiecRychter M, Woźniak A, Limon J, et al. Risk criteria and prognostic factors for predicting recurrences after resection of primary gastrointestinal stromal tumor. Ann Surg Oncol. 2007; 14(7):2018-27. DOI: 10.1245/s10434-007-9377-9.
34. Ahmed I, Welch NT, Pearsons SL. Gastrointestinal stromal tumors (GIST)- 17 years experience from Mid Trent Region (United Kingdom). Eur J Surg Oncol. 2008; 34(4):445-9. DOI: 10.1016/j.ejso.2007.01.006. [ Links ]
35. Hassan I, You YN, Shyyan R, Dozois EJ, Smyrk TC, Okuno SH, et al. Surgically managed gastrointestinal stromal tumors: a comparative and prognostic analysis. Ann Surg Oncol. 2008; 15(1):52-9. DOI: 10.1245/s10434-007-9633-z. [ Links ]
36. Gold JS, Gönen M, Gutiérrez A, Broto JM, García del Muro X, Smyrk TC, et al. Development and validation of a prognostic nomogram for recurrence-free survival after complete surgical resection of localized primary gastrointestinal stromal tumour: a retrospective analysis. Lancet Oncol. 2009; 10(11):1045–52. DOI: 10.1016/S1470-2045(09)70242-6. [ Links ]
37. Chok AY, Goh B, Koh YX, Lye WK, Allen JC, Quek R, et al. Validation of the MSKCC gastrointestinal stromal tumor nomogram and the comparison with other prognostication systems: single-institution experience with 289 patients. Ann Surg Oncol. 2015; 22(11):3597-605. DOI: 10.1245/s10434-015-4400-z. [ Links ]
38. McCarter MD, Antonescu CR, Ballman KV, Maki RG, Pister PWT, Demetri GD, et al. Microscopically positive margins for primary gastrointestinal stromal tumors: analysis of risk factors and tumor recurrence. J Am Coll Surg. 2012; 215(1): 53–59. DOI: 10.1016/j.jamcollsurg.2012.05.008. [ Links ]
39. Zhi, X, Jiang B, Yu J, Dimitri O, Quin J, Ni Q, et al. Prognostic role of microscopically positive margins for primary gastrointestinal stromal tumors: a systematic review and meta-analysis. Sci Rep. 2016; 6:21541. DOI: 10.1038/srep21541. [ Links ]
40. Chen K, Zhou YC, Mou YP, Xu XW, Jin WW, Ajoodhea H. Systematic review and meta-analysis of safety and efficacy of laparoscopic resection for gastrointestinal stromal tumors of the stomach. Surg Endosc. 2015; 29(2):355-67. DOI: 10.1007/s00464-014-3676-6. [ Links ]
41. Thacoor A. Gastrointestinal stromal tumours: advances in surgical and pharmacological management options. J Gastrointest Oncol. 2018; 9(3):573-78. DOI: 10.21037/jgo.2018.01.10. [ Links ]
42. DeMatteo RP, Ballman KV, Antonescu CR, Corless C, Kolesnikova V, von Mehren M. Long-term result of adjuvant imatinib mesylate in localized, high-risk, primary gastrointestinal stromal tumors (GIST) ACOSOG Z9000 (Alliance) intergroup phase 2 trial. Ann Surg. 2013; 258(3):422–29. DOI: 10.1097/SLA.0b013e3182a15eb7. [ Links ]
43. DeMatteo RP, Ballman KV, Antonescu CR, Maki RG, Pisters PW, Demetri GD. Placebo-controlled randomized trial of adjuvant imatinib mesylate following the resection of localized, primary gastrointestinal stromal tumor (GIST). Lancet. 2009; 373(9669):1097-104. DOI: 10.1016/S0140-6736(09)60500-6. [ Links ]
44. Corless CL, Ballman KV, Antonescu CR, Kolesnikova V, Maki RG, Pisters PW, et al. Pathologic and molecular features correlate with long-term outcome after adjuvant therapy of resected primary GI stromal tumor: the ACOSOG Z9001 trial. J Clin Oncol. 2014; 32(15):1563–70. DOI: 10.1200/JCO.2013.51.2046. [ Links ]
45. Joensuu H, Eriksson M, Sundby Hall K, Hartmann JT, Pink D, Schutte J, et al. One vs three years of adjuvant imatinib for operable gastrointestinal stromal tumor: a randomized trial. JAMA. 2012; 307(12):1265–72. DOI: 10.1001/jama.2012.347. [ Links ]
46. Joensuu H, Erikson M, Sundby Hall KS, Reichardt A, Hartmann JT, Pink D. Adjuvant imatinib for high risk GI stromal tumor: analysis of randomized trial. J Clin Oncol. 2016; 34(3): 244-50. DOI: 10.1200/JCO.2015.62.9170. [ Links ]
47. Joensuu H, Wardelmann E, Sihto H, Eriksson M, Sundby Hall K, Reichardt A. Effect of KIT and PDGFRA mutations on survival in patients with gastrointestinal stromal tumors treated with adjuvant imatinib: an exploratory analysis of a randomized clinical trial. JAMA Oncol. 2017; 3(5):602-9. DOI: 10.1001/jamaoncol.2016.5751. [ Links ]
48. Joensuu H, Eriksson M, Hall KS, Hartmann JT, Pink D, Schütte J. Risk factors for gastrointestinal stromal tumor recurrence in patients treated with adjuvant imatinib. Cancer. 2014; 120(15):2325-33. DOI: 10.1002/cncr.28669. [ Links ]
49. Blanke CD, Demetri GD, von Mehren M, Heinrich MC, Eisenberg B, Fletcher JA, et al. Long-term results from a randomized phase II trial of standardversus higher-dose imatinib mesylate for patients with unresectable or metastatic gastrointestinal stromal tumors expressing KIT. J Clin Oncol. 2008; 26(4):620–25. DOI: 10.1200/JCO.2007.13.4403. [ Links ]
50. Blanke CD, Rankin C, Demetri GD, Ryan CW, von Mehren M, Benjamin RS, et al. Phase III randomized, intergroup trial assessing imatinib mesylate at two dose levels in patients with unresectable or metastatic gastrointestinal stromal tumors expressing the kit receptor tyrosine kinase: S0033. J Clin Oncol. 2008; 26(4):626-32. DOI: 10.1200/JCO.2007.13.4452. [ Links ]
51. Verweij J, Casali PG, Zalcberg J, LeCesne A, Reichardt P, Blay JY, et al. Progression-free survival in gastrointestinal stromal tumours with high-dose imatinib: randomized trial. Lancet. 2004;364(9440):1127-34. DOI: 10.1016/S0140-6736(04)17098-0. [ Links ]
52. Casali PG, Zalcberg J, Le Cesene A, Richardt P, Blay JY, Linder LH, et al. Ten-year progression-free and overall survival in patients with unresectable or metastatic GI stromal tumors: long term analysis of the European Organization for Research and Treatment of Cancer, Italian Sarcoma Group and Australasian Gastrointestinal Trials Groups Inter-group phase III randomized trial on imatininib at two dose levels. J Clin Oncol. 2017; 35(15):1713-20. DOI: 10.1200/JCO.2016.71.0228. [ Links ]
53. Gastrointestinal Stromal Tumor Meta-Analysis Group (MetaGIST). Comparison of two dose of imatinib for the treatment of unresectable or metastatic gastrointestinal stromal tumors: a meta-analysis of 1,640 patients. J Clin Oncol. 2010; 28(7):1247-53. DOI: 10.1200/JCO.2009.24.2099. [ Links ]
54. Farag S, Somaiah N, Choi H, Heeres B, Wang WL, van Boven H et al. Clinical characteristic and treatment outcome in a large multicenter observational cohort of PDGFRA exon 18 mutated gastrointestinal stromal tumor patients. Eur J Cancer. 2017; 76:76-83. DOI: 10.1016/j.ejca.2017.02.007. [ Links ]
Conflictos de interés: Los autores declaran no tener conflictos de interés
Fuente de financiamiento: Autofinanciado
Correspondencia:
Jorge Soriano Lorenzo
sorianolorenzo@infomed.sld.cu
Recibido: 16 de abril 2019
Aprobado: 24 de mayo 2019
Publicación en línea: 28 de junio 2019














