INTRODUCCIÓN
El Ministerio de Salud en la sala situacional de Covid-19 el 15 de enero del 2021 ha reportado 1 056 023 casos confirmados y 38 654 fallecidos1, los pacientes con enfermedad moderada (neumonía), grave o crítica con Síndrome de Dificultad Respiratoria Aguda (SDRA), sepsis o complicaciones2) requieren hospitalización y en ocasiones manejo ventilatorio o en Unidad de Cuidados Intensivos (UCI)(3).
El virus SARS-COV-2 ingresa por vía respiratoria, en su fase inicial prolifera en la nasofaringe, sigue su fase pulmonar con neumonía, y en su fase de hiperinflamación causa SDRA4,5, el virus puede invadir los tejidos cuyas células tienen receptores ACE-26, lesiona el endotelio, activa la inflamación y la coagulación7, la tormenta de citoquinas acelera el proceso inmunotrombótico8 genera microtrombosis pulmonar, trombosis y coagulopatías que empeoran el cuadro clínico y el pronóstico9.
Las coagulopatías son la mayor complicación (62%), seguido de falla renal (49%) y falla cardiaca (43%) según reportes de pacientes hospitalizados en Wuhan10 , donde fueron reportadas las primeras complicaciones tromboembólicas en el 25% de 81 pacientes con neumonía Covid-19 grave, quienes tenían mayor edad (68,4 frente a 57,1 años) y dímero D (5,2 ± 3,0 frente a 0,8 ± 1,2 μg/ml) ambos asociados a alto riesgo de TEV en neumonía Covid-1911.
En 3 hospitales holandeses se ha reportado una incidencia de 31% del compuesto de complicaciones trombóticas (TEV sintomático, accidente cerebrovascular isquémico, infarto de miocardio o embolismo arterial)12, en 3 hospitales de Indianápolis se ha reportado una incidencia de TEV de 28 %, en ellos su dímero D fue mayor de 6,26 ng/ml y precedió al TEV, la hipercoagulabilidad y la muerte13. En una revisión sistemática de 66 estudios (28 173 pacientes) se estimó una prevalencia general de TEV de 14,1% del cual el 7,9% correspondió a hospitalización y el 22,7% a UCI. La prevalencia de TEP en hospitalización fue 3,5% y en UCI 13,7%14.
El dímero D elevado como expresión de la coagulación activada15 fue frecuente16, en cuyo fundamento muchas Instituciones médicas17 han propuesto la tromboprofilaxis con dosis incrementadas o terapéuticas de anticoagulantes18, aunque con poco respaldo científico19.
Iniciando el segundo año de la pandemia, se publica esté articulo con el objetivo de orientar al médico en una tromboprofilaxis racional para prevenir la trombosis y disminuir la mortalidad tanto por la complicación tromboembólica como hemorrágica asociada a la anticoagulación o a la enfermedad en el paciente Covid-19 hospitalizado.
BÚSQUEDA BIBLIOGRAFICA
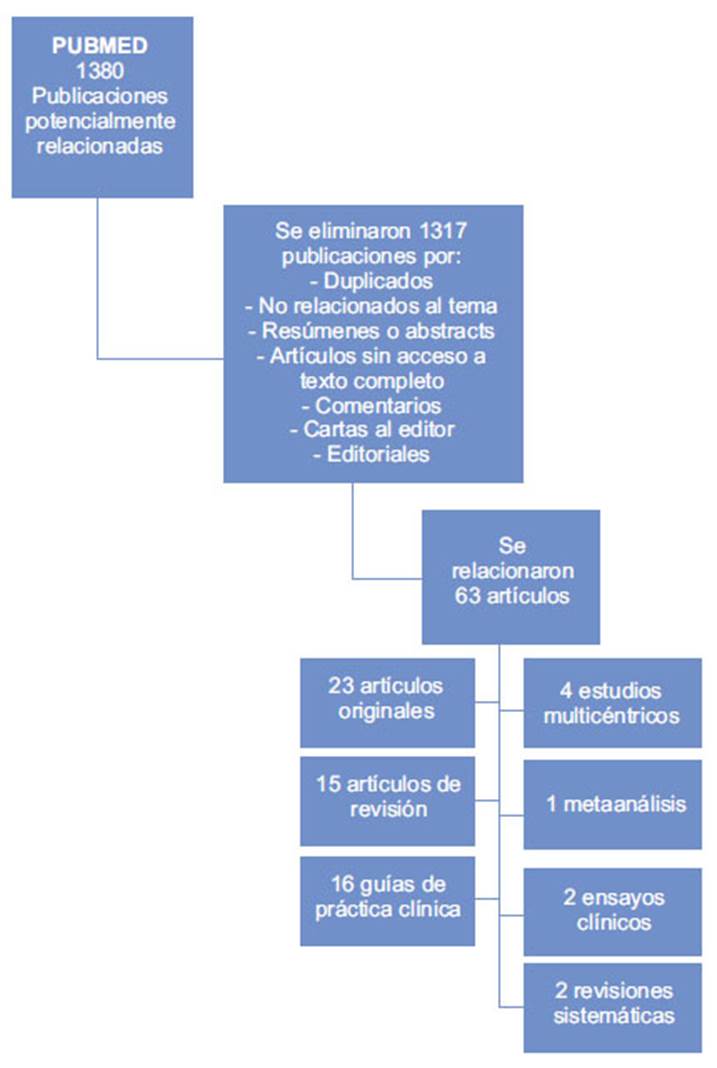
Se realizó la búsqueda en la base de datos PUBMED usando las palabras clave en inglés "anticoagulants and COVID-19", obteniéndose 1,380 resultados durante el 2020.
No se incluyeron los artículos que trataban sobre antiplaquetarios, anticoagulantes orales o anticoagulación exclusivamente terapéutica.
Se eliminaron también duplicados, cartas al editor, comentarios, editoriales, resúmenes o abstracts, aquellos sin acceso al texto completo.
Se efectuó una selección de 63 publicaciones relacionadas con tromboprofilaxis en COVID-19: 23 artículos originales (estudios observacionales, de cohorte retrospectiva y prospectiva, estudios comparativos); y, además, 4 estudios multicéntricos, un metaanálisis, 2 ensayos clínicos controlados, 16 guías, 15 artículos de revisión y 2 revisiones sistemáticas (Figura 1).
CONTENIDO
EVIDENCIA DE TROMBOSIS EN INFECCION COVID-19
HALLAZGOS HISTOPATOLOGICOS EN NECROPSIAS
La primera serie de 11 necropsias en Estados Unidos (New Orleans), reporta trombosis de arterias pulmonares pequeñas y medianas20, daño alveolar difuso con inflamación severa, trombosis y microangiopatía trombótica de los vasos pequeños y capilares del pulmón21 . La principal manifestación fue el daño alveolar difuso, daño de la estructura alveolar, la proliferación de las células tipo II, fibrosis alveolar y trombosis microvascular.
En órganos extrapulmonares se evidenció lesión endotelial y t r o m b o s i s m i c r o v a s c u l a r d i f u s a , sugestivas de microangiopatía trombótica que explicaría el inicio de la insuficiencia multiorgánica22.
En las primeras 12 necropsias en Alemania (Hamburgo) se reportó en 7 Trombosis Venosa Profunda (TVP) en 4 TEP, y en 8 daño alveolar difuso23, el equipo completó 76 necropsias y en 8 de ellas se encontró TEP con neumonía, en 9 embolias pulmonares periféricas y en el 40% del total se halló TVP24.
El SARS-COV-2 afecta principalmente los pulmones, causa daño alveolar difuso llevando a insuficiencia respiratoria severa de riesgo mortal, trombosis de las arterias pulmonares s e g m e n t a r i a s y s u b s e g m e n t a r i a s a p e s a r d e l a tromboprofilaxis20.
HIPERCOAGULABILIDAD ADQUIRIDA
La hipercoagulabilidad es una condición que aumenta el riesgo de formación de coágulos25. El SARS-COV-2, activa la respuesta inflamatoria por varios mecanismos26, libera citocinas, activa neutrófilos y plaquetas, daña el endotelio y activa la coagulación, promoviendo respuestas inmunes innatas y adaptativas27.
La superficie alveolar severamente inflamada en riesgo de sangrado activa la coagulación28, la protrombina activa la trombina, a su vez convierte el fibrinógeno en fibrina que al ser lisada genera el dímero D y productos de degradación del fibrinógeno29 , expresiones de la activación de la coagulación, fibrinólisis30 y hipercoagulabilidad atribuible a la sepsis viral o a la infección bacteriana agregada31.
El incremento del dímero D se empezó a evidenciar en los pacientes más severos32, así en Wuhan se reportó 54 fallecidos (28%) de 191 pacientes, el riesgo de muerte fue 18 veces mayor en pacientes con dímero D mayor a 1 μg/ml frente a los que tenían menor a 0,5 μg/ml. En 172 pacientes el dímero D fue más alto en los fallecidos (5,2 μg/ml) que en los supervivientes (0,6 μg/ml), el 81% de los fallecidos tenía dímero D mayor a 1 μg/ml, que ha sido asociado a mayor probabilidad de muerte hospitalaria33.
En un hospital de Tongui, de 183 pacientes con neumonía Covid-19, 21 murieron, en ellos, el dímero D, los productos de degradación de fibrinógeno, la prolongación del Tiempo de Protrombina (TP), y el tiempo parcial de tromboplastina activada (TPTa) fueron más elevados que en los que sobrevivieron 9. El aumento significativo de dímero D fue un indicador de mal pronóstico y riesgo de mortalidad hasta 18 veces mayor34.
El análisis de 400 historias electrónicas en 5 hospitales de los Estados Unidos reveló que la trombocitopenia y el dímero D elevado fueron predictores de hemorragias. El dímero D elevado junto a otras pruebas de coagulación, inflamación y sepsis fueron predictivas de trombosis, enfermedad crítica y muerte en pacientes hospitalizados con Covid-1935.
En un Hospital General de Wuhan, se estudiaron 343 pacientes hospitalizados por SARS COV2 para evaluar el valor predictivo de mortalidad del dímero D al ingreso. El valor de 2,0 μg/ml tuvo sensibilidad de 92,3% y especificidad del 83,3%. Los pacientes con dímero D ≥ 2,0 μg/ml tuvieron mayor mortalidad que aquellos con dímero D < 2,0 μg/ml, un dímero D > 2,0 μg/ml al ingreso podría ser un marcador temprano y predecir la mortalidad hospitalaria36.
En un metaanálisis de 23 artículos publicado con 1 845 pacientes, el Dímero D estuvo aumentado en el 29% (534 pacientes). En los casos severos estuvo elevado 2,74 veces con relación a los no severos (1,29 vs 0,47 mg/L)37. Otro estudio con 328 pacientes con neumonía Covid-19, reportó TEP en 72 pacientes y el Dímero D > 6 ng/ml asociado a un OR 4.838.
En una revisión sistemática y metaanálisis de más de 30 estudios, que incluyó 53 000 pacientes, se encontró que el incremento del dímero D y la linfopenia, incrementan alrededor de tres veces el riesgo de enfermedad grave39. El dímero D elevado se ha asociado a peor pronóstico40, un incremento mayor al doble es considerado predictor de trombosis y un incremento mayor de 6 veces el valor normal (≥ 3 µg/ml) es considerado fuerte predictor de trombosis y severidad de enfermedad, con indicación de tromboprofilaxis más intensa, necesidad de manejo en UCI y peligro de muerte 14,41.
RIESGO DE TROMBOSIS EN PACIENTE COVID-19 HOSPITALIZADO
Los pacientes Covid-19 hospitalizados, tienen movilidad restringida, inflamación endotelial, activación de las plaquetas y de la coagulación13, confluyen la tríada de Virchow para el desarrollo de TVP42 cuya mayor relevancia en Covid-19 severo es la unificación de la vía inflamatoria y de coagulación en la génesis de la trombosis43.
Los pacientes infectados por SARS-COV-2 son hospitalizados por neumonía, insuficiencia respiratoria, o falla sistémica44, todas corresponden a condiciones médicas agudas45, en quienes las guías internacionales46,47 recomiendan tromboprofilaxis, previa evaluación del riesgo de trombosis y sangrado, siendo las escalas de predicción más utilizadas la de PADUA, IMPROVE VTE e IMPROVE BLEED, (International Medical Prevention Registry on Venous thromboembolism) o una modificación que incorpora el dímero D48.
La escala de PADUA permite mayor predicción de eventos a 90 días49, un paciente adulto hospitalizado por infección o neumonía Covid-19, se calificaría por inmovilización 3 puntos, por infección 1 punto, por falla respiratoria o cardiaca 1 o 2 puntos, adulto mayor 1 punto, alcanzando fácilmente un puntaje mayor a 3 que califica de alto riesgo de TEV, el cual es incrementado por las comorbilidades y la edad mayor de 60 años50.
La escala IMPROVE BLEED asigna puntajes por criterio: ulcera gastroduodenal activa 4,5, recuento plaquetario menor a 150 000 / ml, o sangrado en los 3 meses previos4, edad mayor de 84 años 3,5 y de 40 a 80 años 1,5, estancia en UCI, falla hepática o renal 2,5, cáncer o catéter2, depuración de creatinina de 30 a 59 ml/min/m2 o sexo masculino1. El puntaje mayor a 6 califica de alto riesgo de sangrado51.
También es necesario considerar las contraindicaciones absolutas para el uso de anticoagulantes: hemorragia activa, hipertensión arterial severa descompensada, trastornos de la coagulación o falla hepática con marcada alteración del perfil de coagulación48,52.
La Sociedad Internacional de Trombosis y Hemostasia ha sugerido realizar a todos los pacientes hospitalizados dímero D, TP, recuento de plaquetas y fibrinógeno para estratificar el riesgo y manejo del paciente17, pruebas que tienen amplia variabilidad, pero junto a los criterios clínicos podrían mejorar la estratificación del riesgo trombótico y la intensidad de la tromboprofilaxis53.
Susen y colaboradores han propuesto una estratificación del riesgo tromboembólico en COVID-19, en base a la gravedad de la hipoxemia, el índice de masa corporal y otros factores agregados54:
Muy alto riesgo: Índice de Masa Corporal (IMC) > 30/k/m2, con SDRA y factores de TEV adicionales u oxigenoterapia nasal de alto flujo o Ventilación Mecánica (VM), ECMO, trombosis del catéter o del filtro de diálisis, Síndrome inflamatorio marcado y / o hipercoagulabilidad (fibrinógeno > 8 g / l y / o dímero D > 3 μg / ml o 3000 ng / ml).
Alto riesgo: IMC < 30/k/m2, oxigenoterapia nasal de alto flujo o VM, con o sin factores de riesgo de TEV o IMC> 30 kg / m2 sin oxigenoterapia nasal de flujo alto o VM, pero con factores de riesgo agregados de TEV o IMC> 30 kg / m2 con oxigenoterapia nasal de alto flujo o VM, y sin factores de riesgo agregados de TEV.
Riesgo Intermedio: IMC < 30/k/m2, sin necesidad de oxigenoterapia nasal de alto flujo o VM, con o sin factores de riesgo agregados de TEV y,
Bajo riesgo: paciente no hospitalizado con IMC < 30 kg / m2 y sin factores de riesgo agregados de TEV.
El dímero D mayor de 3 µg/ml, es un biomarcador de trombosis asociado a mal pronóstico, y muerte55. Mediante la revisión de 11 estudios que reportan el riesgo de TEV concluyen que en pacientes hospitalizados COVID-19 el riesgo oscila de 4,4% a 8,2% y hasta 53,8% en UCI56.
Es urgente estratificar el alto riesgo de trombosis, especialmente en pacientes ancianos, con comorbilidades, puntuaciones altas de Tomografía de tórax, dímero D elevado y otras pruebas analíticas, así utilizar una estratificación individualizada del riesgo trombótico y hemorrágico para una tromboprofilaxis racional52.
ESQUEMAS DE TROMBOPROFILAXIS
Usualmente las recomendaciones se basan en el estado del arte de las infecciones agudas o en sepsis previas a la pandemia, sin embargo, las manifestaciones inflamatorias e hipercoagulabilidad de la infección severa del SARS-COV-2, incorpora diferencias que requieren nuevos estudios clínicos aleatorizados con anticoagulantes y otras alternativas.
La mayoría de las series se limitan a pacientes de UCI, el 29,2 por 100.000 habitantes infectados por SARS-COV-2 requieren hospitalización; cerca del 60% no ingresa a UCI57. La mayoría de los consensos internacionales se han concentrado en el riesgo de TEV y la prevención, más que en la confirmación del diagnóstico3,17,52,58,59,60,61,62,63,64,65.
En el paciente COVID-19, moderado a crítico, el proceso inflamatorio severo y coagulación disfuncional se inicia en la matriz alveolar, con incremento de dimero D y microtrombosis en la vasculatura pulmonar, seguido, por un estado hipercoagulable generalizado que lleva a trombosis macro y microvascular55, en ellos se basa la clasificación que caracteriza las Anomalías Hemostáticas Asociadas a Covid-19 (AHAC)66.
El dímero D elevado es un factor de riesgo independiente de mal pronóstico, y muerte15,41, un incremento mayor de 6 veces el valor normal fue el fundamento para incrementar el anticoagulante profiláctico a dosis intermedias o terapéuticas, actualmente el severo incremento de dímero D no justifica el ajuste de dosis anticoagulante sin parámetros clínicos55.
Tang y colaboradores, para pacientes COVID-19 de alto riesgo con dímero D superior a 3,0 μg / ml, sugieren profilaxis con enoxaparina, 30 mg cada 12 horas si el peso corporal es menor de 120 kg o IMC ≤ 40 y 40 mg cada 12 horas para pacientes con un peso mayor9.
Se ha encontrado que la trombosis ocurre a pesar del uso profiláctico y terapéutico de heparina43, la anticoagulación puede ser insuficiente para prevenir el TEV en la enfermedad grave por SARS-COV-225) lo que destaca la necesidad de terapias alternativas o adicionales55.
No existe suficiente evidencia que soporte tromboprofilaxis efectiva a dosis incrementada o terapéutica de anticoagulantes, ni garantice la seguridad a esas dosis, en cambio hay consenso en la aplicación de tromboprofilaxis a dosis estándar en todos los pacientes internados en el hospital o en UCI, que están avalados por la fisiopatología de la enfermedad y por la evaluación del riesgo tromboembólico en pacientes con condiciones médicas agudas en hospitalización.
Las directrices del CHEST considera factores de riesgo y estimaciones de la incidencia de TEV en pacientes no críticos COVID-19 mayores al 1% aún con tromboprofilaxis, consideran a todos estos pacientes de alto riesgo de TEV y sugieren tromboprofilaxis en ausencia de contraindicaciones. Recomiendan HBPM, fondaparinux o HNF, con la ventaja que la HBPM reduce la exposición del personal y el riesgo de trombocitopenia inducida por heparina19.
El panel de expertos del CHEST, recomienda la profilaxis anticoagulante a dosis estándar y no la dosis intermedia (HBPM cada 12 horas o dosis aumentada según el peso) ni terapéutica para pacientes hospitalizados y críticos, falta evidencia suficiente para asegurar el beneficio de dosis mayores. Recomiendan evaluar la tromboprofilaxis prolongada, cuando el riesgo de TEV supera el riesgo de sangrado con un beneficio neto de la profilaxis. No recomiendan el uso de antiplaquetarios19.
Las guías de la Sociedad Italiana de Trombosis y Hemostasia sugieren la profilaxis con enoxaparina 40 mg por vía subcutánea (SC) cada 24 horas para todos los pacientes hospitalizados, salvo contraindicación13,14, para pacientes con IMC mayor a 40 kg/m2 o peso mayor a 120 kg, aplicar enoxaparina 40 mg SC cada 12 horas y en los pacientes con insuficiencia renal (depuración de creatinina <30 ml/min), recomiendan HNF 5000 UI, SC dos o tres veces al día67.
La guía de Trombosis y hemostasia de Brasil recomienda para todos los pacientes COVID-19 hospitalizados tromboprofilaxis a dosis profiláctica, y reservar la dosis terapéutica para trombosis confirmada, sugieren HBPM a dosis estándar ajustada por peso corporal y función renal en espera de mejor evidencia tanto para mayor dosis como para continuar la tromboprofilaxis después del alta en los pacientes con alto riesgo de TEV inmovilizados, salvo contraindicaciones68.
La ISTH recomienda la profilaxis durante la hospitalización y por 7 a 10 días después del alta14, también recomiendan compresión neumática intermitente, a diferencia de los expertos del CHEST69.
Aproximadamente el 9% de los pacientes que recibieron dosis terapéutica experimentaron sangrado frente al 3% de los que recibieron dosis profiláctica70.
CONCLUSIONES
El virus SARS-CoV-2 genera hiperinflación e hipercoagulabilidad, con microtrombosis pulmonar, macrotrombosis y severo incremento del dímero D en la enfermedad crítica con mal pronóstico, pero éste es un criterio insuficiente para incrementar la dosis profiláctica anticoagulante.
Todos los pacientes con COVID-19 hospitalizados o en UCI requieren tromboprofilaxis convencional con HBPM o HNF salvo contraindicación.
En aquellos con anticoagulación oral permanente reemplazar por HBPM o HNF durante la hospitalización.
La profilaxis post alta solo indicarla a casos individuales con múltiples factores de riesgo de TEV y bajo riesgo de sangrado por 7 a 14 días.
Em caso de contraindicación absoluta al uso de anticoagulantes, usar dispositivos de comprensión neumática intermitente y medias antiembólicas.
Con los resultados de los ensayos clínicos controlados aleatorizados se podrán proponer nuevos esquemas seguros y efectivos para prevenir la micro y macro trombosis y la mortalidad en el paciente Covid-19 hospitalizado