INTRODUCCIÓN
Los adultos mayores (AM) se definen generalmente como las personas mayores de 60 o 65 años, son el segmento de la población de más rápido crecimiento y la aparición de epilepsia es mayor en este grupo de edad que en cualquier otro grupo 1. Varios estudios en Europa y Estados Unidos han demostrado sistemáticamente que la incidencia de crisis epilépticas agudas provocadas y no provocadas, epilepsia y el estado epiléptico es mayor en los AM en comparación con la población más joven. Se ha estimado que la incidencia anual de epilepsia es de 85 por cada 100000 personas de 65 a 69 años, de 159 por cada 100000 personas mayores de 80 años y de 81 por cada 100000 personas en todos los grupos de edad 2. La tasa de prevalencia de epilepsia en los AM es de aproximadamente 1,5%. La mortalidad aumenta progresivamente con la edad, la etiología y el estado epiléptico. En general, la mortalidad en los AM es del 38%, pero aumenta a casi el 50% en los mayores de 80 años 3,4,5.
En los AM la etiología de epilepsia difiere de la de otros grupos de edad y el diagnóstico de epilepsia es un reto a causa de la alta prevalencia de trastornos que simulan crisis epilépticas, como síncope, amnesia global transitoria, ataque isquémico transitorio y vértigo 1,4,6. La selección de los fármacos anticrisis epiléptica (FAE) adecuados para el tratamiento de epilepsia en los AM es un tema importante, ya que esta población presenta alteraciones en los parámetros farmacocinéticos y farmacodinámicos. Asimismo, los AM son propensos a las interacciones farmacológicas, ya que habitualmente toman varios fármacos para los trastornos comórbidos 1. A pesar de la magnitud y complejidad del problema, sorprendentemente se ha realizado poca investigación clínica y básica en esta población. Por ello, el objetivo del presente artículo es proporcionar una revisión narrativa de la literatura científica sobre los FAE empleados en el tratamiento de epilepsia en los AM, de acuerdo con las características de su tipo de epilepsia y las modificaciones en la capacidad metabólica de los FAE que surgen con la edad.
MATERIAL Y MÉTODOS
Criterios de búsqueda
Se efectuó una búsqueda bibliográfica en febrero de 2021. Con el fin de identificar estudios relevantes sobre epilepsia en los AM, se utilizó la base de datos electrónica Pubmed y se aplicó una combinación de términos y títulos de temas médicos (MeSH): “epilepsy”, “seizures”, “anticonvulsants”, “elderly”, “new-onset”, “newly diagnosed”, “causes”, entre múltiples combinaciones con los conectores AND y OR. Se seleccionaron los estudios en los que los términos “epilepsy”, “seizures”, “anticonvulsants”, “elderly” se encontraban en el título o en el resumen, y los estudios en los que “new-onset”, “newly diagnosed”, “causes” se encontraban en cualquier campo. Con el fin de identificar estudios basados en la población de los AM y estudios pertinentes adicionales, se realizó búsquedas bibliográficas adicionales en las siguientes revistas Epilepsia y Neurology utilizando los términos “epilepsy”, “seizures”, “anticonvulsants”, “elderly”.
Criterios de inclusión
Para cumplir con los criterios de inclusión en esta revisión narrativa, un estudio tenía que:1) revisar o informar sobre el tratamiento de epilepsia en los AM independientemente del tipo de epilepsia estudiada, 2) ser estudio tipo metaanálisis, estudios controlados aleatorizados, estudios clínico originales y revisión 3) estar escrito en inglés. Se excluyeron los estudios de tratamiento de epilepsia tratados con métodos distintos de la intervención farmacológica, por ejemplo, intervención quirúrgica y se excluyó estudios de tratamiento de estado epiléptico.
Selección de estudios
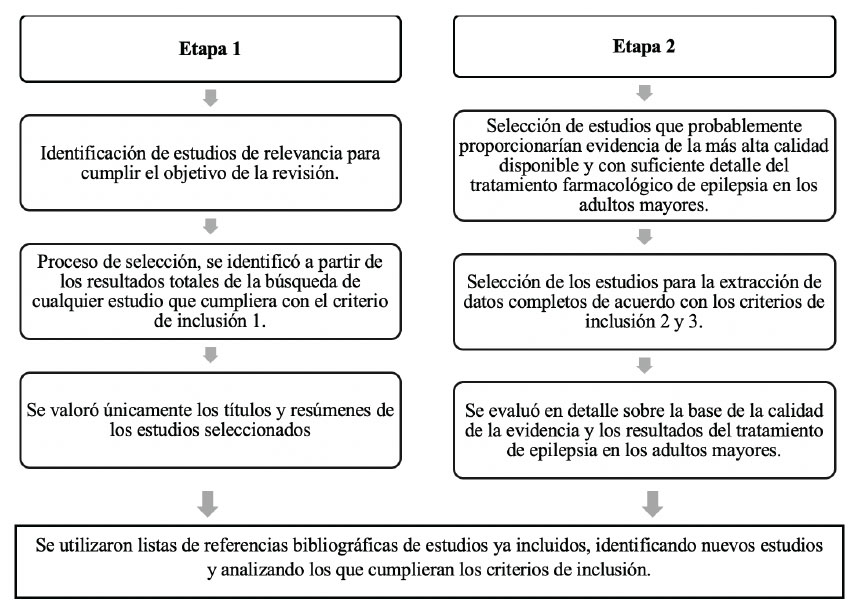
No se impusieron restricciones basadas en la fecha de publicación. Se eliminaron los estudios duplicados. El proceso de selección de estudios se realizó en dos etapas (Figura 1).
RESULTADOS
A continuación, se sintetiza el contenido de los estudios publicados incluidos en esta revisión narrativa.
Características diferenciales de la Epilepsia en los Adultos Mayores
Diferente Etiología
Las crisis epilépticas agudas ocurren como resultado de un insulto agudo al sistema nervioso central (SNC). La mayoría de estas crisis son secundarias a disturbios metabólicos, traumas, abstinencia alcohólica, toxicidad e infecciones del SNC. La epilepsia es decir la afección crónica que se caracteriza por la presencia de crisis epilépticas recurrentes, dentro de las principales causas, aparecen las siguientes: evento vascular cerebral (EVC), demencia, neoplasias, trauma, entre otras. Muchas veces no es posible identificar la causa 7.
La etiología más frecuente de epilepsia en los AM es el EVC relacionada con casi el 50% 1,2,4,8. Además, la epilepsia puede ser el primer signo de un EVC que aún no ha aparecido y las crisis epilépticas pueden ocurrir en presencia de un EVC isquémico, hemorragia subaracnoidea y hemorragia intracerebral, siendo más probable una asociación con el EVC hemorrágico 1,2,6,9. En el Veterans Affairs Coopertive Study, reveló que los factores etiológicos más comunes de epilepsia en los AM estaban relacionados con el EVC. La media de edad de los pacientes inscritos en el estudio fue de 72 años, la etiología relacionada al EVC incluyó, infarto cerebral en el 30%, arteriosclerosis cerebrovascular en el 16% y hemorragia cerebral en el 2%. Asimismo, se encontró que la lesión cerebral traumática fue la etiología en el 7% y las malformaciones arteriovenosas y tumores benignos contribuyeron en el 2%. El 18% restante de los pacientes del estudio las crisis epilépticas se presentaron por otras causas conocidas diferentes 10. Casi el 24% de los pacientes del estudio tuvieron una etiología desconocida de sus crisis epilépticas 11. En otro estudio poblacional retrospectivo de crisis epilépticas en los AM después de un EVC demostró, que el EVC aumenta el riesgo de crisis epilépticas hasta 23 veces en comparación con la población general durante el primer año después del infarto 12.
Existe un conocimiento limitado de los mecanismos fisiopatológicos en las crisis epilépticas posteriores al EVC. La presencia de múltiples comorbilidades como hipertensión, hiperlipidemia y diabetes puede alterar los mecanismos homeostáticos dentro de la penumbra isquémica 11. La mayoría de los estudios experimentales han abordado las crisis epilépticas tempranas en lugar de las crisis epilépticas tardías. Las crisis epilépticas tempranas pueden estar relacionadas con cambios agudos como alteraciones metabólicas (aumento de sodio y calcio intracelular), glutamato excesivo, hipoxia, hipoperfusión e irritación por hemoderivados. Las crisis epilépticas tardías probablemente se deben a anomalías crónicas como cicatrización, cambios en la excitabilidad neuronal y depósito de hemosiderina 13.
Otra causa de epilepsia relacionada con frecuencia en los AM es el trastorno neurocognitivo mayor que representa el 10 - 20% y los AM que padecen está patología tienen un riesgo de dos a diez veces mayor de desarrollar epilepsia 1,2,14,15. De todos los trastornos neurocognitivos la enfermedad de Alzheimer (EA) y la enfermedad de Creutzfeldt-Jakob tienen un mayor riesgo de presentar epilepsia, su incidencia llega hasta el 20%. Sin embargo, la demencia mixta, la demencia vascular y la demencia con cuerpos de Lewy pueden representar un porcentaje muy pequeño de epilepsia 2. Un estudio demostró que el 22% de los pacientes con EA, la mayoría de los cuales se encontraban en estadios severos, experimentaron al menos una crisis epiléptica no provocada 16. En un estudio prospectivo de EA que posteriormente fueron EA comprobados por autopsia, se notificó crisis epilépticas en el 10 - 17% 17.
El mecanismo epileptogénico específico aún es incierto en pacientes con neurodegeneración; hay varias razones que pueden estar asociadas con epilepsia secundaria en la demencia, incluido el depósito de β-amiloide, la pérdida neuronal y la gliosis, los cambios químicos, los fármacos antidemenciales y las comorbilidades 18,19. El depósito de β-amiloide es un cambio patológico fundamental en la EA, y también es considerado como un mecanismo epileptogénico importante para los pacientes con EA. El β-amiloide está relacionado con la actividad sináptica y actúa como un potente regulador de la transmisión sináptica, provocando facilitación presináptica en concentraciones relativamente bajas y depresión postsináptica en niveles más altos, lo que produce actividad epileptiforme 20. La posible pérdida selectiva de las neuronas inhibidoras podría ser otro mecanismo de desarrollo de epilepsia en los pacientes con EA 21. También, los cambios químicos en los pacientes con EA pueden inducir crisis epilépticas; estos factores químicos incluyen alteraciones en acetilcolina, dopamina, ácido gamma-aminobutírico y otros neurotransmisores, o cambios en la excitotoxicidad celular y las funciones de los canales de sodio y calcio 14. Además, el consumo de medicamentos asociados a la demencia es un factor de riesgo importante para desarrollar epilepsia. Los estudios han demostrado que un historial de uso de antipsicóticos es un factor de riesgo para epilepsia en la EA 22.
Los tumores cerebrales explican la etiología en el 5 - 12% de los casos de epilepsia en los AM y el 20 - 45% de los pacientes con tumores cerebrales desarrollan crisis epilépticas como síntoma temprano. La epilepsia se presenta en el 65 - 95% de los pacientes con astrocitoma, oligodendroglioma y meningioma 1,2,23,24. La localización de los tumores también es un factor para el desarrollo de epilepsia, generalmente los tumores ubicados en los lóbulos temporales, los lóbulos frontales y los lóbulos parietales tienen más probabilidades de causar epilepsia en comparación con los tumores ubicados en la médula 2.
Finalmente, el traumatismo craneoencefálico explica la etiología hasta en el 10 - 20% de los casos de epilepsia en los AM 1,2,25. Los factores de riesgo asociados con epilepsia postraumática incluyen, lesiones penetrantes, gravedad de la lesión, contusiones biparietales o múltiples, hemorragia intracraneal, ubicación frontal o temporal de la lesión, fractura de cráneo, hematoma subdural, desplazamiento de la línea media del cerebro mayor de 5 mm, amnesia y pérdida del conocimiento durante más de 1 día, múltiples procedimientos intracraneales y aparición de crisis epilépticas postraumáticas tempranas 2.
Diferentes manifestaciones clínicas
Existen diferencias en las manifestaciones clínicas de la epilepsia entre los AM y otros adultos más jóvenes. Las crisis epilépticas focales es el tipo de crisis más común de la epilepsia en pacientes AM, mientras que las crisis epilépticas generalizadas son más comunes en pacientes adultos jóvenes. De los dos subtipos de crisis epilépticas focales, con alteración de la conciencia, es más común en los AM. Aunque la epilepsia en los AM puede manifestarse como una crisis epiléptica tónico-clónica generalizada, es más probable que las crisis en la mayoría de los casos sea una crisis tónico-clónica focal o bilateral no reconocida previamente 1.
Según Spitz y cols., alrededor del 50% de las crisis epilépticas tónico clónicas generalizadas en los AM fueron diagnosticadas inmediatamente de epilepsia, pero sólo el 21% de los pacientes AM que presentaron crisis epilépticas focales complejas fueron diagnosticadas de epilepsia 26. Adicionalmente, se encontró que más del 60% de todas las crisis epilépticas en los AM fueron crisis epilépticas focales simples o complejas. Las crisis epilépticas tónico-clónicas generalizadas se observaron en el 27% de los pacientes evaluados, y el 13% de los pacientes presentaron crisis epilépticas tónico-clónicas focales y secundariamente generalizadas. En otro estudio, se encontró que las crisis epilépticas tónico-clónicas generalizadas secundarias ocurrían en solo el 26% de los pacientes AM, en comparación con el 65% de los adultos más jóvenes 27.
En la Tabla 1, se resumen las manifestaciones clínicas de las crisis epilépticas focales en los AM, las cuales son diferentes de las que se observan en los adultos más jóvenes. Las auras típicas, que incluyen el miedo, la sensación epigástrica y los fenómenos de deja vu, ocurren a un ritmo menor. Los automatismos generalmente no están presentes y las crisis epilépticas pueden manifestarse solo como una mirada en blanco con alteración transitoria de la conciencia 4,6. Otra diferencia significativa es la confusión postictal, que puede durar varias horas o hasta varios días en comparación con minutos en los adultos jóvenes. Está confusión postictal prolongada también podría contribuir a un diagnóstico tardío de epilepsia en los AM 4,28,29. Las diferencias clínicas pueden estar relacionadas con el origen anatómico de las crisis epilépticas, que es más probable que sea mesial temporal en pacientes más jóvenes y extratemporal, especialmente frontal, en los AM 6. La localización del lóbulo extratemporal es común debido a que la etiología más frecuente es el EVC en los AM 4.
Tabla 1 Diferencias en la sintomatología de las crisis epilépticas entre adultos mayores y adultos jóvenes

Fuente: Adaptado de “Epilepsy in the elderly: Special considerations and challenges”, de JN Acharya et al, 2014, Annals of Indian Acdemy of Neurology, 17, p.S19 (https://doi.org/10.4103/0972-2327.128645).CCBY4
Tratamiento farmacológico de la Epilepsia en los Adultos Mayores
Consideraciones Generales
El objetivo del tratamiento farmacológico de epilepsia en los AM, debe ser el control completo de la epilepsia sin o con mínimos efectos secundarios, de modo que la capacidad funcional de los AM se restaure a su máximo potencial. El apoyo de la familia y los cuidadores es fundamental para un resultado exitoso 13. Al iniciar el tratamiento de epilepsia en los AM, es necesario considerar el tipo de crisis, el síndrome epiléptico, los trastornos comórbidos, los tratamientos médicos concomitantes y los parámetros farmacocinéticos y farmacodinámicos de los FAE. La evidencia clínica indica que los FAE más nuevos para el manejo de epilepsia en los AM son mejores que los FAE más antiguos debido a sus menores riesgos de efectos adversos e interacciones farmacológicas 1,30.
La epilepsia en los AM generalmente responde bien al tratamiento, se puede esperar que hasta el 80% de los pacientes permanezcan libres de crisis epilépticas con los FAE 2,28,31. Mattson y cols., observaron que el 62% de los pacientes AM de 65 años y el 30% de los de 40 años o menos estaban libres de crisis epilépticas después de dos años. Por otro lado, en el mismo estudio, se observó que el 64% de los pacientes AM tuvieron que dejar de tomar los FAE, en comparación con el 33% de los adultos más jóvenes. Por lo tanto, la tolerabilidad es un factor importante a la hora de elegir los FAE 32.
Los AM con crisis epilépticas provocadas deben recibir tratamiento para el precipitante agudo identificable y, por lo general, no necesitan de los FAE. En las crisis epilépticas no provocadas, la decisión de tratar depende de si el paciente tuvo una única crisis epiléptica o recurrentes (epilepsia). A diferencia de la situación en los adultos más jóvenes, el tratamiento con los FAE puede ser apropiado después de una única crisis epiléptica en los AM. Esto se debe a que tienen un alto riesgo de recurrencia 4,29,33,34, ya que generalmente son crisis epilépticas focales y reflejan una patología estructural. Los AM con crisis epilépticas recurrentes claramente necesitan tratamiento. Es importante determinar la etiología de epilepsia, ya que las crisis epilépticas pueden ser la primera manifestación de una afección previamente no reconocida, que puede requerir un tratamiento específico además de los FAE. El médico debe prescribir los FAE utilizando un régimen de empezar con poco e ir despacio, para minimizar el riesgo de efectos adversos 1. Por lo general, se recomienda comenzar con una dosis baja y ajustar lentamente la dosis para evitar la toxicidad, alcanzar una dosis de mantenimiento modesta y valorar los efectos adversos. Si el primer fármaco falla como resultado de una reacción idiosincrásica, mala tolerabilidad a dosis bajas a moderadas o falta de eficacia, se debe probar una alternativa. Si el paciente tolera el segundo fármaco con una respuesta útil pero subóptima, se puede considerar el tratamiento combinado con dosis bajas de los FAE. Las instrucciones escritas, la explicación detallada del tratamiento y la provisión de dosificación pueden ayudar a la adherencia 28.
Modificaciones del metabolismo en los adultos mayores
El envejecimiento fisiológico altera los parámetros farmacocinéticos y farmacodinámicos de los FAE. Existe una atrofia de la mucosa gástrica y una reducción de la motilidad intestinal, que puede modificar la absorción de los FAE haciéndolos irregular. Por otro lado, se produce una reducción del agua corporal total, lo que provoca una modificación del volumen de distribución de los FAE y de su vida media, lo que en ocasiones puede tener consecuencias importantes 35.
Adicionalmente se reduce la unión de los FAE a las proteínas plasmáticas y la capacidad para eliminar los fármacos también es menor en los AM que en otros grupos de edad, el metabolismo hepático es mucho más lento, lo que puede conducir a la acumulación de los FAE 1,33,36,37. Cuando el médico opta por los FAE para los AM, es importante considerar la posibilidad de interacciones farmacológicas, ya que muchos de estos pacientes toman otros fármacos para enfermedades comórbidas. En este sentido, cuanto menor sea la unión a proteínas y menor sea el metabolismo hepático de los FAE, más fácil será su uso y menor será el riesgo de interacción con otros posibles fármacos concomitantes 27,32.
El aclaramiento renal también se reduce con el envejecimiento. Además, la tasa de filtración glomerular disminuye en > 50% entre la tercera y la octava década de la vida 38.
Efectos secundarios de especial relevancia en los adultos mayores
El potencial de interacciones farmacológicas es extremadamente importante al elegir los FAE en los AM, ya que muchos de ellos toman otros medicamentos para las comorbilidades. En un estudio, aproximadamente el 25% de los pacientes AM informaron haber tomado quince o más medicamentos recetados. Los FAE más antiguos, como los inductores o inhibidores enzimáticos, aumentan la probabilidad de interacciones con otros fármacos. La carbamazepina (CBZ), la fenitoína (PHT) y el fenobarbital (PB) son inductores de enzimas que pueden disminuir los niveles de fármacos administrados concomitantemente. Las concentraciones de anticoagulantes orales, antidepresivos, antimicrobianos, psicotrópicos y fármacos cardiovasculares pueden reducirse con estos FAE inductores de enzimas. A diferencia de los inductores enzimáticos, el ácido valproico (VPA) es un inhibidor enzimático que aumentará la concentración de fármacos concomitantes. Los FAE más nuevos con relativamente pocas interacciones farmacológicas, como, la lamotrigina (LTG) y el levetiracetam (LEV), podrían ser más adecuados para los AM con regímenes de polifarmacia 1,33,39.
Debido a la acción inhibidora del SNC, muchos FAE pueden causar trastornos cognitivos. Los AM suelen presentar una reducción de su capacidad de reserva cerebral, lo que los hace especialmente sensibles a este efecto secundario. La posibilidad de inducir trastornos cognitivos es alta con los FAE como la PHT, el PB, el topiramato (TPM) y las benzodiazepinas (BZD). Los FAE que causan trastornos cognitivos con menor frecuencia y que, por tanto, son más seguros en los AM son la LTG, el LEV, la oxcarbazepina (OXC) y la gabapentina (GBP) 1,33.
La osteoporosis es un trastorno común en los AM, particularmente entre las mujeres, y puede ser la causa de una discapacidad significativa por la presencia de dolor crónico y la predisposición a las fracturas. Varios FAE pueden inducir osteoporosis, enfatizando un riesgo que ya es alto simplemente como resultado del envejecimiento. Algunos FAE, como la PHT, el PB o la CBZ, lo hacen interfiriendo con el metabolismo de la vitamina D. El VPA puede inducir osteoporosis activando los osteoblastos que destruyen el tejido óseo (14,34,40, 41).
Se debe considerar la posibilidad de un aumento de peso en los AM, y este efecto adverso aumenta el riesgo de diabetes tipo II, mortalidad cardiovascular y problemas osteoarticulares en una población donde el riesgo es mayor 42. Entre ellos, el VPA la CBZ, la pregabalina (PGB), la GBP y la vigabatrina (VGB) se han asociado con el aumento de peso 43. El TPM puede inducir la pérdida de peso, lo que puede ser útil para los AM con sobrepeso, pero en otros casos este efecto también puede ser perjudicial y provocar desnutrición 44. Por tanto, los FAE más recomendados son aquellos que no tienden a modificar el peso, entre ellos la LTG, el LEV y la OXC 45.
La conducción auriculoventricular puede afectarse con el empleo de la PHT, la CBZ, la LTG y la lacosamida (LCM); por lo tanto, el médico debe tener cuidado al utilizar estos FAE para tratar pacientes con arritmias cardíacas. Los FAE pueden afectar los perfiles de lípidos, la CBZ posiblemente aumenta los niveles de lipoproteínas de baja y alta densidad, y la OXC, el LEV y el TPM posiblemente aumentan el nivel de lipoproteínas de baja densidad 1. La hiponatremia debida a la CBZ, particularmente cuando se coadministra con diuréticos, ocurre con mayor frecuencia en los AM, aunque a menudo es asintomática 28.
La PHT, el PB, la CBZ, OXC y la LTG pueden producir reacciones idiosincrásicas, en particular erupciones cutáneas, e interacciones farmacológicas complejas, ya que todos son sustratos e inductores de las enzimas monooxigenasa hepática 1,28.
Eficacia y evidencia clínica
Las pautas y recomendaciones de los FAE pueden variar entre países 1. Varios estudios controlados doble ciego han demostrado que los nuevos FAE son equivalentes a los antiepilépticos antiguos para controlar las crisis epilépticas, pero con menos efectos secundarios y mejor tolerabilidad 46. La epilepsia farmacorresistente es poco común y su incidencia exacta en esta población no está clara 37,47.
La Liga Intenacional contra la epilepsia (ILAE) recomendó para epilepsia de tipo focal emplear la GBP y la LTG (Nivel A), la CBZ (Nivel C), el TPM y el VPA (Nivel D). La Sociedad Estadounidense de Epilepsia y la Academia Estadounidense de Neurología (AES/AAN) recomendaron como monoterapia eficaz para epilepsia focal recién diagnosticada y no tratada la LTG (Nivel B) y la GBP (Nivel C). Las pautas del Instituto Nacional de Salud y Excelencia Clínica del Reino Unido (NICE) no recomendó preferencia entre los FAE antiguos y nuevos en el tratamiento de epilepsia focal. Además, no existen pautas para los AM con otro tipo de epilepsia (1, 48,49).
Aunque el uso clínico de los FAE nuevos se está volviendo más atractivo por varias razones, los FAE antiguos siguen ocupando una proporción sustancial de las opciones de tratamiento en la práctica clínica, incluso en los AM. Aunque la PHT y, en menor medida, el VPA y el PB todavía se prescriben ampliamente para el tratamiento de epilepsia en los AM, muchos neurólogos consideran la CBZ como un fármaco preferible 50.
Los FAE recomendados por un perfil más favorable en los AM son el LEVque no tiene metabolismo hepático y con escasa posibilidad de interacciones (Nivel de evidencia I). A continuación, se recomienda la LTGl, cuyo metabolismo hepático y su unión a proteínas aumenta ligeramente el riesgo de interacciones medicamentosas y de reacciones alérgicas graves, pero evitables con una titulación lenta (Nivel de evidencia I). Entre los FAE nuevos, la LTG es el más investigado en los AM. Se realizó un ensayo aleatorizado doble ciego Lamotrigine Elderly Study Group, comparando la LTG y la CBZ en 150 pacientes AM recién diagnosticados de epilepsia, y demostró que el tiempo hasta la primera crisis epiléptica no difirió entre los tratamientos LTG y CBZ 1,51. En el estudio Veterans Affairs Coopertive Study que comparó la CBZ, la LTG y la GBP en 593 pacientes AM con epilepsia, encontró que la tasa de libertad de crisis epilépticas no difirió significativamente entre los FAE antes mencionados 1,52.
Un ensayo aleatorizado, doble ciego, mostró que la tasa de ausencia de crisis epilépticas no difirió significativamente entre los tratamientos CBZ, la LTG y el LEV 1,53. En el estudio Keppra vs. Older Monotherapy in Epilepsy Trial (KOMET), el tiempo hasta la primera crisis epiléptica fue similar para los tratamientos con el LEV y la CBZ o el VPA 1,54. Un metaanálisis encontró que la probabilidad de ausencia de crisis epilépticas fue mayor para el LEV que para la LTG y no difirió significativamente entre el LEV y la CBZ 1,55.
El tratamiento en monoterapia de algunos FAE como la LTG, el LEV, la GBP y la LCM se han evaluado en un ensayo clínico aleatorizado con un diseño de no inferioridad y utilizando la CBZ de liberación inmediata o de liberación controlada como comparador. En general, estos FAE mostraron un control similar de las crisis epilépticas pero una mejor tolerabilidad en comparación con la CBZ. Un reciente metaanálisis en monoterapia realizado en epilepsia en los AM de1425 pacientes, no mostró diferencias estadísticamente significativas entre los tratamientos en los resultados de eficacia, aunque la LTG, el LEV y la LCM tuvieron la mayor probabilidad de clasificarse como los mejores para la ausencia de crisis epilépticas 56. También, se han realizado estudios aleatorizados en poblaciones que incluyen trastorno neurocognitivo mayor como la EA, pacientes con crisis epilépticas posteriores a un EVC y pacientes con tumores cerebrales. En pacientes con EA, se han estudiado la LTG, el LEV y el PB; y los efectos cognitivos más adversos fueron para el PB. En un ensayo aleatorizado con el LEV en pacientes con crisis epilépticas después de un EVC, reportó que el LEV fue tan eficaz como la CBZ y mejor tolerado con menos efectos negativos sobre la función ejecutiva, la atención y la funcionalidad 38.
Otro aspecto clave incluye abordar los desencadenantes de crisis epilépticas, a medida que los pacientes envejecen, su sensibilidad al alcohol aumenta, lo que puede ponerlos en riesgo de sufrir más crisis epilépticas. Tanto el neurólogo como el médico de atención primaria deben evaluar el abuso de alcohol y permanecer atentos a los trastornos de laboratorio, como pruebas de función hepática elevadas o volumen corpuscular medio elevado que pueden presentarse. Se debe evaluar la higiene del sueño en los AM, ya que la falta de sueño es un desencadenante común de las crisis epilépticas 57. Los AM con epilepsia pueden tener enfermedades psiquiátricas comórbidas que necesitan un enfoque de tratamiento multidisciplinario. Inmediatamente después del diagnóstico, los pacientes son vulnerables y tienen un mayor riesgo de depresión. Eventos adversos psiquiátricos han sido reportados con el uso de algunos FAE, particularmente PB, TPM, LEV, VGB, Tiagabina y Zonisamida 58. El neurólogo debe brindar orientación al médico de atención primaria y al psiquiatra, y se puede sugerir que emplee FAE con un perfil psiquiátrico más favorable. El psiquiatra deberá tener en cuenta que muchos fármacos psiquiátricos, incluidos los antipsicóticos, el bupropión, la clozapina y el litio, reducen el umbral convulsivo 59.
CONCLUSIONES
De lo anterior, podemos concluir que nos encontramos ante una población que presentará frecuentemente epilepsia focal sintomática, por lo que se puede esperar una buena respuesta al tratamiento médico, incluso a dosis más bajas. La mayoría de los FAE disponibles han demostrado una eficacia similar para tratar este tipo de crisis. Por tanto, la elección del fármaco dependerá fundamentalmente de su perfil farmacocinético y de la probabilidad de efectos secundarios que, como hemos visto, repercuten especialmente en los AM. Los FAE con perfil farmacocinético más favorable son LTG y LEV, cuyo metabolismo hepático y unión a proteínas aumenta ligeramente el riesgo de aparición de interacciones farmacológicos. Además, estos FAE tienen pocos efectos cognitivos, no provocan osteoporosis y no afectan al peso corporal, lo que los hace especialmente atractivos para el tratamiento de la epilepsia en los AM. Debería hacerse un mayor esfuerzo para incluir a los pacientes AM en los ensayos clínicos y para comprender mejor los efectos adversos crónicos de los FAE en esta población. Se deben abordar los factores psicosociales y la adherencia a los medicamentos. Un modelo de atención más integral para la atención hospitalaria y ambulatoria que incluya médicos de atención primaria, geriatras, neurólogos, epileptólogos y personal de enfermería sería útil para brindar una atención óptima a los pacientes AM.