Introducción
La “kañiwa” (Chenopodium pallidicaule Aellen, Chenopodiaceae) es una planta herbácea anual cuyo grano se considera muy nutritivo por su alto contenido de proteínas y buen perfil de aminoácidos. Crece principalmente en los altiplanos de Perú y Bolivia entre los 3600 a 4400 m.s.n.m. en ambientes extremos donde la temperatura promedio anual es menor a 10 °C. Debido a su resistencia al frío extremo, alto contenido proteico y a la facilidad con que es cultivada, la kañiwa es considerada un componente importante para la seguridad alimentaria1. La kañiwa, al igual que su pariente cercano la quinua (Chenopodium quinoa), no contiene gluten, por lo que ambos granos andinos son de gran interés para personas con enfermedad celiaca. A diferencia de la quinua, la kañiwa tiene la ventaja de tener bajo contenido de saponinas, por lo que no es necesario hacer lavados con abundante agua para retirar del grano estos compuestos de sabor amargo2.
Las variedades de kañiwa se diferencian en base a la forma de crecimiento de la planta, que puede ser erguida o muy ramificada; así como en los diferentes colores que presentan el tallo, follaje, vesículas y semillas3.
La Estación Experimental Zonal “Illpa” (Puno) del Instituto Nacional de Innovación Agraria (INIA) conserva alrededor de 430 accesiones de kañiwa. Entre las variedades más conocidas están por ejemplo la Ramis, Chilliwa, Cupi, Akallpi, entre otras. Debido a su gran diversidad morfológica, la discriminación de las accesiones de kañiwa por taxonomía clásica es complicada, por lo que se ha empezado a usar herramientas moleculares como el AFLP (Amplified Fragment Length Polymorphism)4.
La discriminación de especies puede llevarse a cabo mediante estudios genómicos, y complementariamente por estudios proteómicos y metabolómicos. La metabolómica es el estudio integral del metaboloma, el cual se define como el conjunto completo de las moléculas de bajo peso molecular (metabolitos) que son químicamente transformadas por el metabolismo de un sistema biológico. La metabolómica de tipo “non-targeted” realiza un análisis exhaustivo de todos los analitos medibles en una muestra5. Los perfiles químicos detallados pueden ser adquiridos por diferentes técnicas analíticas, siendo una de las más utilizadas la cromatografía líquida de ultra-alta performance acoplada a la espectrometría de masas de alta resolución (UHPLC-HRMS). Los datos obtenidos son sometidos a análisis estadísticos multivariados como el PCA (Análisis de componentes principales) con el objetivo de hallar similitudes y diferencias químicas entre las muestras (variedades, especies, accesiones) y el OPLS-DA (Análisis discriminante de proyecciones ortogonales de estructuras latentes) para postular biomarcadores que permitan su diferenciación. Utilizando esta estrategia Wang et al.6 encontraron los biomarcadores que permiten discriminar la especie Hedyotis diffusa de Hedyotis corymbosa. Otro ejemplo es el trabajo de Luo et al.7 quienes utilizaron la metabolómica non-targeted para detectar los metabolitos que diferencian dos variedades de Citrus reticulata.
El objetivo del presente estudio fue utilizar el enfoque metabolómico non-targeted para encontrar potenciales biomarcadores que permitan discriminar dos variedades de kañiwa (Chenopodium pallidicaule Aellen), plomo claro (“Chilliwa”) y roja (“Ramis”) provenientes del departamento de Puno.
Parte experimental
Material vegetal y tratamiento de muestras
Las variedades de kañiwa estudiadas fueron la kañiwa plomo claro (“Chilliwa”) y la kañiwa roja (“Ramis”). Las muestras procedieron del distrito de Ayaviri, provincia de Melgar, departamento de Puno y fueron identificadas por el Dr. Mario Tapia Núñez, de la Universidad Global del Cusco. Las semillas de kañiwa fueron molidas hasta la obtención de un polvo fino. Para cada variedad de kañiwa se procedió con la extracción de los metabolitos a partir de 100 mg de muestra que fueron colocados en 3 microviales de 1,7 mL. La extracción fue llevada a cabo a temperatura ambiente con 800 µL de metanol al 80% (Metanol LCMS y agua tipo 1, 18 MΩ.cm) bajo condiciones de agitación con vortex por 1 minuto y ultrasonido por 10 minutos. Luego, los microviales fueron sometidos a centrifugación por 10 minutos (10000 rpm, 4 °C); a partir de cada sobrenadante se tomó 600 µL que fueron trasladados a tres nuevos microviales. Se repitió el mismo procedimiento de extracción por segunda vez con el marco inicial para obtener 3 microviales con 1200 µL de extracto de cada variedad de kañiwa. Asimismo, se preparó un microvial de control de calidad (QC) mezclando 100 µL de cada microvial de los seis extractos (3 extractos por cada variedad de kañiwa) hasta obtener un volumen final de 600 µL. El QC proporciona una medida de la repetibilidad y robustez, a su vez permite monitorear el sistema y la estabilidad de las muestras en el transcurso del análisis. Finalmente, se preparó una muestra de Blanco que consistió de un volumen de 600µL del solvente de extracción (metanol 80%) bajo las mismas condiciones de extracción de las muestras, pero en ausencia de muestra.
Perfil químico de extractos por UHPLC-HRMS
Para la separación de los metabolitos se utilizó un cromatógrafo líquido UHPLC Dionex Ultimate 3000 Thermo Scientific equipado con un detector de arreglo de diodos y columna cromatográfica Phenomenex Luna® Omega C18 100 Å (150 mm x 2,1 mm x 1,6 µm). La fase móvil consistió de ácido fórmico al 0,1% en agua tipo I (Solvente A) y ácido fórmico LCMS al 0,1% en acetonitrilo LCMS (Solvente B). Los compuestos fueron eluídos de la columna utilizando el siguiente sistema de gradiente: 5% B de 0-5 min, 5-95% B 5-12 min. La velocidad de flujo fue 0,3 µL/min, el volumen de inyección fue 5 µL y la temperatura del horno de la columna fue 30 oC.
El Espectrómetro de masas fue un equipo de Thermo ScientificTM Q ExactiveTM híbrido Cuadrupolo-Orbitrap. La detección de masa fue llevada a cabo utilizando una fuente de electrospray HESI en modos de ionización positiva y negativa a 70000 de poder de resolución utilizando el modo Full MS/ddMS2 (Top N) sin fragmentación HCD. Para la ionización MS2 se utilizó el modo dd-MS2/dd-SIM FT con resolución 17500. El tipo de data de espectro fue profile. El rango de masa fue de 140-2000 Da y la temperatura del capilar fue 300 °C con voltaje de ionización spray a 4.0 kV (modo positivo) y 4,2 kV (modo negativo). El tiempo de adquisición fue de 15 min.
Análisis de datos
Luego de la adquisición de cromatogramas por UHPLC-HRMS, la data fue convertida de formato *.RAW (Thermo) a formato *.ABF utilizando el software ABF convert descargable online8. Posteriormente, la data fue importada al software MS-DIAL9 para su alineación, deconvolución, identificación y normalización. Para la identificación automatizada de las características o entidades con MS DIAL, se utilizaron las bases de datos públicas (MS/MS Public (+, -)), bases de datos de MS-FINDER y la base de datos del Diccionario de Productos Naturales (DNP) 26.2. Los análisis multivariados, tales como el Análisis de Componentes Principales (PCA), Proyecciones ortogonales a estructuras latentes-Análisis discriminante (OPLS-DA), así como el S-plot para la identificación de las variables que influyen en el modelo OPLS-DA (biomarcadores), fueron realizados con el software estadístico SIMCA P 15.
RESULTADOS Y DISCUSIÓN
Luego del análisis cromatográfico por UHPLC-HRMS de los extractos metanólicos de las muestras de semillas de kañiwa, se obtuvieron los perfiles metabolómicos de cada variedad. Mediante el software MS-DIAL se encontraron 2189 señales cromatográficas (“características”) en el modo ESI positivo y 2779 en el modo ESI negativo. Estas señales corresponden a los metabolitos extraídos de las variedades de kañiwa, pero también incluyen las señales cromatográficas del solvente de extracción, compuestos aductos, dímeros, entre otros. La data del proceso MSDIAL fue exportada en formato *.CSV para su tratamiento con el software Excel. Se realizó un primer filtrado de características, para ello se omitieron los datos cuya relación del promedio de áreas relativas del blanco y del QC sea mayor a 1,5; cuyo valor p sea mayor a 0,05 en la prueba t de Student y cuya desviación estándar relativa (RSD) de las áreas del QC sea mayor a 30 %. Posteriormente, se utilizó el Package MScombine del software estadístico R10. MSCombine permite el análisis estadístico de un único conjunto de datos, por lo que evita la necesidad del análisis en paralelo (uno por cada polaridad). También posibilita filtrar características o entidades, tales como los compuestos aductos más comunes encontrados en los dos modos de ionización. De esta forma, se aseguró que el análisis por PCA no contenga información irrelevante. El PCA es un análisis multivariado no supervisado que permite reducir la dimensionalidad de la data, por lo cual es considerado un método que permite observar visualmente la estructura interna de la data tal cual, sin asignación de variables categóricas.
La figura 1 muestra el PCA de la tabla resultante del análisis por MScombine. La varianza explicada es 80 % (PC1 y el PC2 explican el 53 % y el 27 % de la varianza, respectivamente), mientras que el valor de ajuste y predicción R2X y Q2 fueron 0,793 y 0,616, respectivamente. El R2X proporciona la calidad de ajuste del modelo. El parámetro R2X describe la fracción de los datos originales explicados por el modelo (si R2 = 1,0 significa que el modelo explica el 100 % de los datos). Mientras que Q2 describe la capacidad predictiva del modelo y es la fracción de los datos originales explicada por el modelo de validación cruzada que mide la capacidad del modelo para predecir un nuevo conjunto de datos11. Para un modelo biológico se considera un valor de R2X y Q2 >0,7. Del PCA se observa un buen agrupamiento de las muestras (clusters) por cada variedad y una buena separación de clases (variedades) de kañiwa. Se observa que las muestras QC están cerca del centro del diagrama y juntas, lo que certifica la robustez del análisis. También se muestra la elipse de confianza, o Hotelling T2, que es una versión t-Student para análisis multivariado y permite observar valores atípicos (valores fuera de la elipse se consideran valores atípicos) bajo un nivel de significancia de p = 0,05.
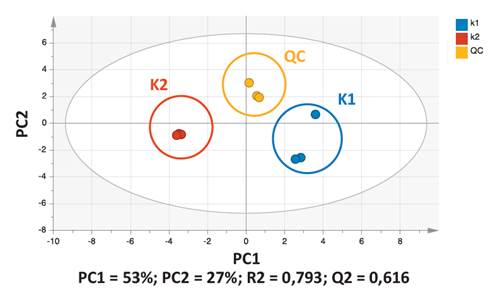
Figura 1 PCA de las dos variedades de kañiwa (K1: variedad “Chilliwa”; K2: variedad “Ramis”); QC (muestra de control de calidad, utilizada para monitorear el sistema y la estabilidad de las muestras en el transcurso del análisis).
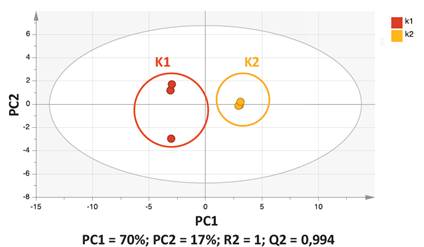
Del PCA se pueden excluir las muestras QC para realizar un análisis OPLS-DA. La figura 2 muestra el análisis supervisado OPLS-DA que, a diferencia del PCA, permite asignar categorías para el análisis discriminante (ceros y unos, 0 y 1). El OPLS-DA, realizado con escalado Pareto, permite forzar la separación de las clases categóricas al proyectarlas sobre el eje Y del diagrama. El software SIMCA P analiza los datos con la correspondiente clasificación de las variables. Se observa una clara separación de las variedades que son estadísticamente significativas con valores de R2Y y Q2 igual a 1 y 0,994, respectivamente. El modelo OPLS-DA fue validado internamente por CV-ANOVA (p <0,05).
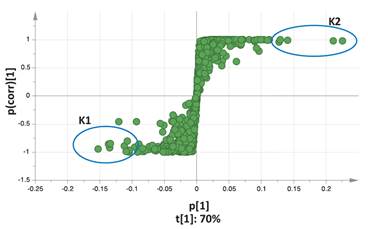
Del OPLS-DA para dos categorías se puede realizar un análisis S-Plot. En la figura 3 se muestra el diagrama S-Plot realizado en base al análisis OPLS-DA. En el diagrama S-plot, los puntos agrupados en el centro representan las variables correlacionadas (metabolitos o señales cercanas a la línea base del cromatograma, p), mientras que los puntos extremos representan las variables con máxima covarianza (loadings, p) que influyen en el modelo discriminante OPLS-DA (al extremo derecho los posibles biomarcadores de la kañiwa roja “Ramis”; mientras que al extremo izquierdo los posibles biomarcadores de la kañiwa plomo claro “Chilliwa”). El S-Plot permitió entonces encontrar biomarcadores potenciales para la diferenciación de las dos variedades de kañiwa en estudio.
Del diagrama S-plot, se puede exportar la tabla de resultados de todos los puntos (tabla 1). La tabla 1 muestra algunos de los potenciales biomarcadores encontrados para ambas variedades de kañiwa. El rango de pesos de dichos biomarcadores varía de 153 hasta 885 uma. Cinco de estos metabolitos tienen un tiempo de retención alrededor del minuto 1, mientras que los demás se encuentran posteriores al minuto 10.
Tabla 1 Biomarcadores potenciales para la diferenciación entre las variedades “Chilliwa” (K1) y “Ramis” (K2)
| Biomarcador químico | Modo de Ionización | Peso molecular | tR (min) | K1 | K2 |
| N-acetil triptófano | Negativo | 245,091 | 11,14 | ✔ | |
| Delfinidina-O-(6''-O-α-ramnopiranosil-β-glucopiranósido) | Negativo | 609,144 | 10,80 | ✔ | |
| 2',5'-Dihidroxiflavona 5'-acetato | Negativo | 295,059 | 12,83 | ✔ | |
| N-trans-sinapoiltiramina | Negativo | 342,133 | 11,94 | ✔ | |
| Isoramnetina-3-O-Glucósido | Negativo | 755,201 | 10,45 | ✔ | |
| Ácido glucónico | Negativo | 195,049 | 1,15 | ✔ | |
| Ácido 3-indolacetil aspártico | Positivo | 291,096 | 11,14 | ✔ | |
| Annularin H | Positivo | 413,143 | 10,97 | ✔ | |
| Kaempferol 4'-metil éter 3-(2Glc-glucosilrutinósido) | Negativo | 769,216 | 10,68 | ✔ | |
| Isoramnetina-3-O-rutinósido | Negativo | 623,159 | 11,00 | ✔ | |
| Crustecdisona | Negativo | 525,304 | 10,81 | ✔ | |
| Ácido vernólico | Negativo | 295,226 | 14,15 | ✔ | |
| Makisterona B | Negativo | 539,320 | 11,02 | ✔ | |
| Ácido pinélico | Negativo | 329,232 | 12,23 | ✔ | |
| 2',6,7-Trihidroxiisoflavona | Negativo | 283,066 | 1,62 | ✔ | |
| Ácido floionólico | Negativo | 331,247 | 12,19 | ✔ | |
| Xantosina | Negativo | 283,066 | 1,22 | ✔ | |
| Genkwadaphnin-20-palmitato | Negativo | 885,444 | 11,43 | ✔ |
Dentro de los biomarcadores identificados solo en la variedad Chilliwa está el compuesto crustecdisona, una fitoecdisona aislada previamente de las semillas de kaladana (Convolvulaceae)12. Otros compuestos presentes solo en la variedad Chilliwa y que están ausentes en la variedad Ramis son: ácido vernólico, makisterona B, ácido pinélico, 2',6,7-trihidroxiisoflavona, ácido floionólico, xantosina y genkwadaphnin-20-palmitato (tabla 1). Ninguno de estos compuestos ha sido encontrado previamente en Kañiwa. Por ejemplo, el ácido vernólico es un ácido graso epoxigenado que se ha reportado en semillas de Vernonia galamensis13. El ácido pinélico, un metabolito derivado del ácido linoleico, ha sido aislado de la especie Salsola tetrandra, un arbusto de la familia Chenopodiaceae14. Genkwadaphnin-20-palmitato es un diterpeno obtenido de extractos de Daphne oleoides15.
Para la variedad Ramis se pudieron identificar 10 biomarcadores: N-acetil triptófano, delfinidina-O-(6''-O-α-ramnopiranosil-β-glucopiranósido), 2',5'-dihidroxiflavona 5'-acetato, N-trans-sinapoiltiramina, isoramnetina-3-O-Glucósido, ácido glucónico, ácido 3-indolacetil aspártico, annularin H, kaempferol 4'-metil éter 3-(2Glc-glucosilrutinósido) e isoramnetina- 3-O-rutinósido (tabla 1). Ninguno de estos compuestos ha sido reportado previamente para la kañiwa. Por ejemplo, N-trans-sinapoiltiramina ha sido aislada de las especies Piper boechmeriaefolium16. Annularin H es un policétido presente en el hongo Annulatascus triseptatus17. La antocianina delfinidina-O-(6''-O-α-ramnopiranosil-β-glucopiranósido) puede encontrarse en las flores de los tulipanes18. Esta antocianina explicaría el color rojo de la kañiwa roja Ramis, metabolito no presente en la kañiwa plomo claro Chilliwa, por lo que se puede considerar como un importante biomarcador para diferenciar las dos variedades de kañiwa estudiadas. Los metabolitos N-Acetiltriptófano (presente solamente en la variedad Ramis) y la Crustecdisona (presente solamente en la variedad Chilliwa) son los que se encuentran más separados entre sí en el gráfico S-Plot, lo cual significa que son los metabolitos que mejor discriminan a ambas variedades.
Cabe resaltar que los resultados obtenidos se limitan a las muestras de las variedades de kañiwa utilizadas en el presente estudio. Para corroborar la reproducibilidad de los biomarcadores propuestos, es necesario realizar estudios metabolómicos non-targeted en las mismas variedades de kañiwa, pero de diferentes zonas de cultivo, colectados en diferentes épocas del año para ver si estas variables influyen en la expresión de los biomarcadores. En el presente estudio, la identificación de los biomarcadores fue solo de tipo putativa, no absoluta. Para la identificación certera de los biomarcadores siempre es necesario contar con los estándares analíticos, los cuales mayormente no se encuentran disponibles de manera comercial. En aquellos casos en los que no se pueda acceder a los estándares analíticos, se hace necesario aislar los compuestos de su fuente natural para luego realizar su identificación por medio de estudios de resonancia magnética nuclear y espectrometría de masas de alta resolución.
CONCLUSIONES
Se obtuvieron los perfiles metabolómicos de las variedades de kañiwa plomo claro “Chilliwa” y kañiwa roja “Ramis” mediante el análisis UHPLC-HRMS. Existe diferencia entre los metabolomas de la kañiwa plomo clara “Chilliwa” y kañiwa roja “Ramis”, lo cual ha sido comprobado por el PCAy el OPLS-DA. Mediante el S-plot se logró encontrar 18 biomarcadores: Crustecdisona, ácido vernólico, makisterona B, ácido pinélico, 2',6,7-trihidroxiisoflavona, ácido floionólico, xantosina y Genkwadaphnin-20-palmitato correspondientes a la kañiwa plomo clara “Chilliwa”; N-acetiltriptofano, delfinidina-O-(6''-O-α-ramnopiranosil-β- glucopiranósido), 2',5'-dihidroxiflavona 5'-acetato, N-trans-sinapoiltiramina, isoramnetina- 3-O-Glucósido, ácido glucónico, ácido 3-indolacetil aspártico, annularin H, kaempferol 4'-metil éter 3-(2Glc-glucosilrutinósido) e isoramnetina-3-O-rutinósido correspondientes a la kañiwa roja “Ramis”. Los metabolitos fueron identificados en base a su similaridad de espectros de Masa MS/MS o MS2 con valores de scores o puntajes >0,7, por lo que son identificaciones putativas o hipótesis de identificación. En ese sentido, se necesitarían de compuestos estándares para elevar el nivel de certidumbre de estas identificaciones, los cuales frecuentemente son difíciles de tener a disposición.