INTRODUCCIÓN
El síndrome neuroléptico maligno (SNM) es una rara y potencialmente fatal reacción adversa medicamentosa, comúnmente asociada a medicamentos antipsicóticos (neurolépticos), pero no limitados a estos 1. Se caracteriza por la presencia de fiebre, rigidez muscular, estado mental alterado y disfunción autonómica. El estudio riguroso del SNM mediante el método científico se enfrenta a desafíos intrínsecos. El SNM se caracteriza por su impredecibilidad y su baja frecuencia de presentación, lo que dificulta la identificación de marcadores clínicos. Además, este trastorno suele manifestarse como una emergencia médica que pone en peligro la vida del paciente, lo que dificulta la obtención de un consentimiento informado para la participación en protocolos de investigación. Estas particularidades explican la escasez de estudios clínicos centrados en esta entidad 2.
El objetivo de esta revisión es proporcionar una visión general actualizada del SNM, con énfasis en la epidemiología, los factores de riesgo, la presentación clínica, los posibles mecanismos subyacentes y el tratamiento. Se espera que la presente revisión pueda ser útil para mejorar el reconocimiento temprano, el diagnóstico y el tratamiento del SNM, lo que a su vez puede contribuir a reducir la morbimortalidad asociada a esta condición.
DESARROLLO DEL TEMA
Búsqueda de la literatura
Para llevar a cabo la búsqueda de la literatura relacionada se utilizaron los siguientes términos y conectores: (“Neuroleptic Malignant Syndrome/classification”[Mesh] OR “Neuroleptic Malignant Syndrome/complications”[Mesh] OR “Neuroleptic Malignant Syndrome/diagnosis”[Mesh] OR “Neuroleptic Malignant Syndrome/epidemiology”[Mesh] OR “Neuroleptic Malignant Syndrome/etiology”[Mesh] OR “Neuroleptic Malignant Syndrome/genetics”[Mesh] OR “Neuroleptic Malignant Syndrome/mortality”[Mesh] OR “Neuroleptic Malignant Syndrome/pathology”[Mesh] OR “Neuroleptic Malignant Syndrome/physiopathology”[Mesh] OR “Neuroleptic Malignant Syndrome/prevention and control”[Mesh] OR “Neuroleptic Malignant Syndrome/therapy”[Mesh]).
La búsqueda electrónica fue realizada mediante el motor de búsqueda PubMed. Se priorizaron los ensayos clínicos aleatorizados, revisiones sistemáticas, estudios retrospectivos, series de casos y algunos reportes de caso. Además, se revisaron los artículos obtenidos a través de las referencias bibliográficas de las revisiones recientes sobre el SNM.
Epidemiología
La incidencia reportada del SNM ha variado durante las últimas décadas, no obstante, siempre se ha caracterizado por su baja frecuencia. En 1993 se describió una incidencia del 0,2 al 3% 3, pero en los últimos años se ha observado una disminución hasta el 0,01 al 0,02% 4, posiblemente debido a un mayor cuidado en la prescripción y titulación de la medicación.
En un reciente metaanálisis se encontró que el SNM se diagnostica con más frecuencia en la adultez temprana, y la frecuencia del diagnóstico disminuye gradualmente a lo largo del resto de la vida. Los varones tienen aproximadamente un 50% mayor probabilidad de ser diagnosticados a cualquier edad 5. Esto podría atribuirse al mayor uso de antipsicóticos en los varones, diferencias farmacocinéticas y farmacodinámicas 6.
Factores de riesgo
A pesar de que en la literatura se menciona que el SNM es una reacción idiosincrática e impredecible relacionada principalmente (pero no solamente) con el uso de antipsicóticos de primera generación, se han descrito algunos factores de riesgo asociados a su aparición 7. Los factores de riesgo más establecidos están relacionados con algunas características del tratamiento: uso de antipsicóticos de alta potencia 8,9; uso de altas dosis de antipsicóticos 10-13; incremento rápido de las dosis de antipsicóticos 11,12,14,15; uso de antipsicóticos inyectables de depósito 11,12,15,16; específicamente, de primera generación 17.
Respecto al uso de antipsicóticos de segunda generación, en una revisión sistemática se encontró una menor incidencia de SNM, además de menor gravedad clínica y resultados letales poco frecuentes comparado con el uso de antipsicóticos de primera generación. No obstante, se sabe que los antipsicóticos de segunda generación no están exentos de inducir un SNM, pudiendo presentar características atípicas del mismo, es decir, mostrar una menor intensidad en los síntomas extrapiramidales o fiebre intensa 18. En un estudio de cohorte de 172 casos de SNM y 1441 controles emparejados se encontró que la incidencia de SNM fue de 1,99 por cada 10 000 personas-años, y que la formulación y clase de antipsicóticos no afectaron significativamente el riesgo de desarrollar SNM 13. En algunos estudios se reportaron que el SNM se encontraba asociado con la polifarmacia, en lugar de la dosis total de antipsicótico 8,19.
Medio ambiente
Los siguientes factores ambientales han sido reportados como de riesgo para la aparición del SNM. En una serie de 24 casos se reportó que un 92% de los pacientes presentó deshidratación al momento de la aparición del SNM 10. No es claro si esto es un factor desencadenante o consecuencia de la reducción de la ingesta de líquidos por la rigidez o de la diaforesis por la fiebre. Sea como fuese, la deshidratación podría complicar el SNM debido al incremento de la concentración efectiva del neuroléptico en el fluido extracelular 10. Otros factores descritos son la sujeción o restricción mecánica 7 y las temperaturas extremas 7.
Características psicopatológicas
En algunas series de casos se reportaron los siguientes posibles factores de riesgo asociados con las características psicopatológicas de cada paciente: agitación psicomotriz 11,12,15, confusión 11, conducta desorganizada 11 y catatonia 11,20.
Factores hereditarios
Los recientes hallazgos en farmacogenética indican que los polimorfismos genéticos para las enzimas metabolizadoras de fármacos, los transportadores de fármacos, y posiblemente, las moléculas dirigidas a fármacos, están asociados con las diferencias interindividuales en las respuestas farmacológicas relacionadas tanto con la eficacia como las reacciones adversas 21.
Los estudios de asociación genética han buscado identificar polimorfismos que influyan en la susceptibilidad al SNM, especialmente relacionados a los receptores D2, receptores de serotonina, y el citocromo P450 2D6. Si bien se han asociado algunos polimorfismos candidatos con el SNM, aún se necesita de mayor evidencia. Además, el SNM podría incluir condiciones heterogéneas con síntomas característicos comunes, pero con diferentes mecanismos causales 21.
Etiología
Los síntomas asociados al SNM fueron descritos por primera vez en 1956 por Ayd, y fue definido como tal por Delay y Deniker en 1968 al reportar una respuesta inusual al haloperidol 22. En un inicio, la etiología del SNM se relacionó con los neurolépticos (antipsicóticos de primera generación), es decir, aquellos psicofármacos que ayudaban a controlar los síntomas psicóticos y producían como efecto secundario síntomas extrapiramidales 23. Sin embargo, se ha visto que se puede presentar también debido al uso de antipsicóticos de segunda generación (atípicos), estabilizadores del humor, como el litio, y hasta medicación distinta a los psicofármacos que tengan alguna actividad anti dopaminérgica como metoclopramida, prometazina, tetrabenazina, entre otros 24-27.
Fisiopatología
El mecanismo subyacente a los síntomas del SNM, probablemente esté relacionado con un bloqueo excesivo de los receptores dopaminérgicos, principalmente el D2. El antagonismo de este receptor en las vías nigroestriatal, hipotalámica y mesolímbica/cortical probablemente explicaría respectivamente la rigidez, la hipertermia y la alteración del estado mental 1.
No obstante, la idea de que el SNM se deba únicamente al bloqueo excesivo del receptor D2 puede resultar demasiado simplista, ya que no tiene en cuenta la rara aparición del síndrome y su inicio impredecible, incluso en pacientes con episodios previos 28. Otros cofactores pueden incluir el desequilibrio de los sistemas de norepinefrina, GABA, y serotonina 28. La hiperactividad central simpático-suprarrenal también se ha postulado como una probable explicación de la etiología del SNM. El estado hipermetabólico es posiblemente el resultado de un exceso de noradrenalina en relación con la dopamina. Además, estudios recientes en farmacogenética indican un posible papel para la predisposición genética del SNM, por lo que es necesario obtener una adecuada historia familiar 29.
Cuadro clínico
Signos y síntomas
Los cambios en el estado mental y rigidez son los síntomas iniciales en el 82,3% de los pacientes, presentándose antes que la hipertermia y la disfunción autonómica 30. Estos cambios en el estado mental han sido reportados en el 97% de los casos e incluyen manifestaciones de confusión mental que varían desde la somnolencia al coma 31.
La rigidez generalizada, descrita como tubería de plomo, ha sido reportada en el 97% de los casos de SNM. El signo de rueda dentada podría no estar presente. También han sido reportados temblores y mioclonías. Otros signos extrapiramidales y bulbares, incluidas distonías focales, sialorrea, disfagia, disartria, opistótonos, crisis oculogíricas y discinesias, son menos frecuentes 31.
La hipertermia y sudoración profusa ocurre en el 98% de los pacientes con SNM, excediendo los 38°C en el 87% y 40°C en el 40%. La hipertermia prolongada podría predisponer a complicaciones del sistema nervioso, incluidos daños irreversibles cerebelares o cerebrales 31.
Pueden presentarse síntomas catatónicos, tales como: autismo, negativismo, manierismos, flexibilidad cérea, verbigeración o ecofenómenos. Se ha documentado una fuerte correlación entre la severidad del SNM y la presencia de síntomas catatónicos 32,33. Para algunos investigadores, la forma letal de la catatonía es clínicamente indiferenciable del SNM 34. Para otros, la catatonía sería un síndrome psicomotor cortical, mientras que el SNM sería un síndrome motor subcortical 35.
El SNM atípico se caracteriza por la ausencia de rigidez severa o hipertermia de aparición tardía en presencia de otros síntomas de SNM 36,37. Se ha encontrado que el SNM atípico es similar al SNM clásico en términos de predilección por los hombres. En contraste, es más común a partir de los 50 años. Los antipsicóticos de segunda generación están más comúnmente asociados con el NMS atípico que los antipsicóticos de primera generación 36. La clozapina, aripiprazol y amisulprida estarían asociadas particularmente con presentaciones atípicas del SNM, con infrecuentes elevaciones de la CPK 18,38,39. La risperidona produce un cuadro clínico similar al SNM asociado a los antipsicóticos de segunda generación. Algunos antipsicóticos de primera generación han sido asociados con características graves como la mioglobinuria o falla renal aguda 39.
La valoración de la severidad se da con los síntomas observables, desarrollándose así una clasificación basada en niveles. En el nivel I, se observa parkinsonismo inducido por medicamentos, con rigidez y/o temblor. El nivel II se caracteriza por catatonía inducida por medicamentos, con rigidez leve a moderada en rueda dentada, alteración del estado mental y mutismo. El nivel III representa el SNM leve, con rigidez leve a moderada en rueda dentada, catatonía o confusión, temperatura ≤ 38°C y frecuencia cardíaca ≤ 100 latidos/min. Con un aumento de la gravedad, el nivel IV muestra el SNM moderado, con rigidez moderada a severa en «tubería de plomo», catatonía o confusión, temperatura entre 38°C y 40°C, y frecuencia cardíaca entre 100 y 120 latidos/min. Finalmente, el nivel V presenta el SNM severo, con rigidez severa en «tubería de plomo», catatonía o coma, temperatura ≥ 40°C y frecuencia cardíaca ≥ 120 latidos/min. Esta clasificación proporciona un enfoque claro para identificar y comprender la gravedad de la presentación clínica del SNM inducido por medicamentos, lo que puede facilitar su diagnóstico temprano y la toma de decisiones clínicas adecuadas para mejorar los resultados en estos pacientes 1,40,41.
Diagnóstico y diagnóstico diferencial
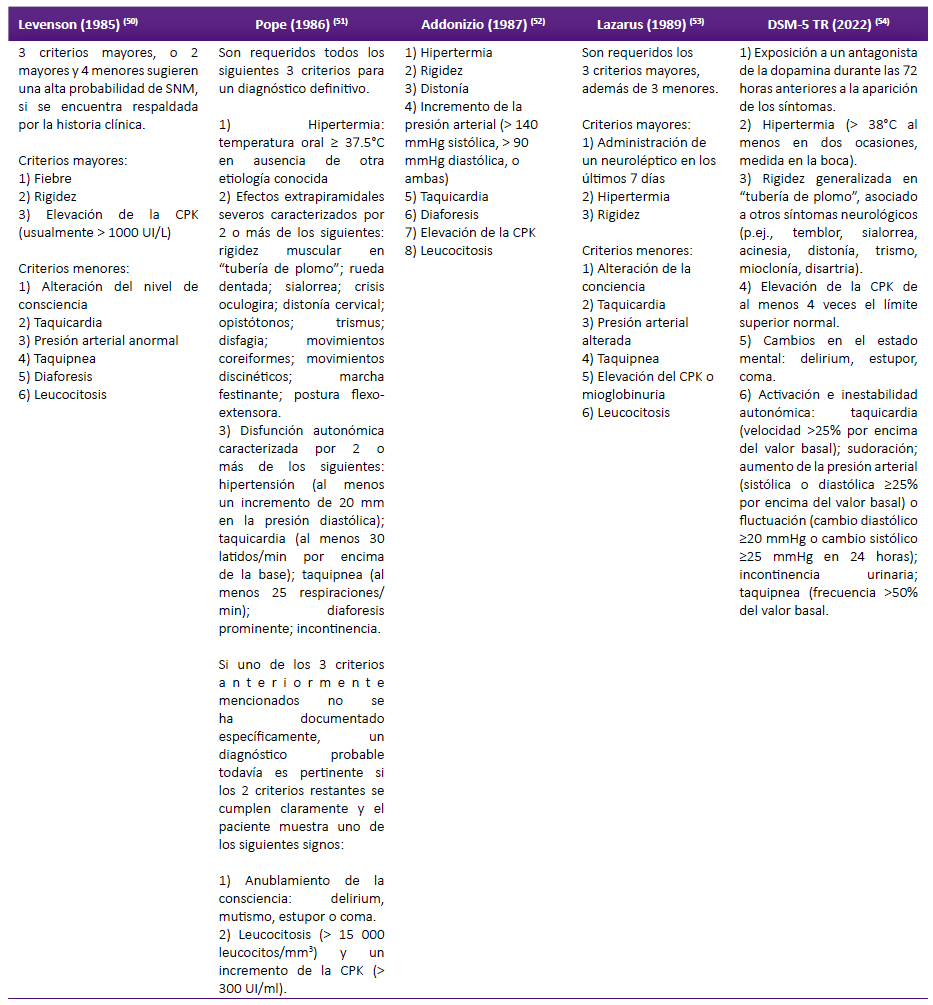
El diagnóstico del SNM puede plantear un desafío debido a la diversidad de sus manifestaciones clínicas y la necesidad de excluir otras condiciones médicas de síntomas similares. En la tabla 1 presentamos los criterios diagnósticos del SNM según diversos autores.
Existen muchas enfermedades y condiciones médicas que imitan la presentación de un SNM, tales como golpes de calor, infecciones del sistema nervioso central (SNC), encefalopatías tóxicas, entre otras. Entre los diagnósticos diferenciales infecciosos, se incluyen la meningitis o encefalitis, el absceso cerebral, la sepsis y la rabia, cuyas características distintivas abarcan desde la presencia de una enfermedad viral prodrómica, cefalea o signos meníngeos, hasta alteraciones en estudios de neuroimagen y líquido cefalorraquídeo. Los diagnósticos diferenciales metabólicos, como la falla renal aguda, la rabdomiólisis, la tirotoxicosis y el feocromocitoma, se basan en pruebas de función renal o tiroidea anormales y la ausencia de tratamiento neuroléptico, así como la presencia de hipertensión severa y catecolaminas o metanefrinas elevadas. Los diagnósticos diferenciales ambientales, como el golpe de calor y el envenenamiento por arañas, están vinculados a historias de esfuerzos físicos intensos o exposición a altas temperaturas, así como la presencia de piel seca y caliente y lesiones cutáneas sugerentes de mordedura de araña.
El diagnóstico diferencial más relevante es el inducido por drogas, que comprende subtipos como la hipertermia maligna, los síndromes inducidos por antipsicóticos (parkinsonismo, distonía aguda, acatisia aguda, discinesia tardía, tremor postural), y los síndromes no inducidos por antipsicóticos (síndrome serotoninérgico, delirium anticolinérgico, toxicidad por inhibidor de monoamina oxidasa, toxicidad por litio, envenenamiento por salicilato, envenenamiento por estricnina, drogas de abuso como cocaína, anfetaminas, metanfetaminas, fenciclidina, etc.), cada uno con características clínicas específicas, incluyendo antecedentes familiares de hipertermia maligna, presencia de hipercinesias y toxicología positiva. Además, se destacan las características del síndrome de abstinencia de alcohol, benzodiacepinas, baclofeno, sedativos e hipnóticos, así como los trastornos neuropsiquiátricos, como el parkinsonismo, el estado epiléptico no convulsivo y la catatonia letal, que ayudan a diferenciar el SNM de estos diagnósticos. Por último, el diagnóstico diferencial autoinmune, en este caso la polimiositis, se caracteriza por debilidad proximal, alteraciones en electromiografía o biopsia muscular, y la presencia de cáncer o enfermedad pulmonar intersticial 4.
Uno de los diferenciales para tener en cuenta, sobre todo en pacientes con polifarmacia de antipsicóticos y antidepresivos, es el síndrome serotoninérgico. Ambos síndromes comparten características clínicas como fiebre, hipertonía, inestabilidad autonómica y cambios en el estado mental, lo que dificulta su diferenciación 42. Esto se vuelve más complejo considerando que muchos antipsicóticos atípicos tienen importantes propiedades serotoninérgicas. No obstante, la diferencia clínica entre ambos síndromes es crucial, ya que el tratamiento farmacológico depende del agente causante, como antipsicóticos o antidepresivos. En la tabla 2 se encuentran las principales diferencias entre el SNM y el síndrome serotoninérgico.
Tabla 2. Diferencias entre el síndrome neuroléptico maligno y el síndrome serotoninérgico.
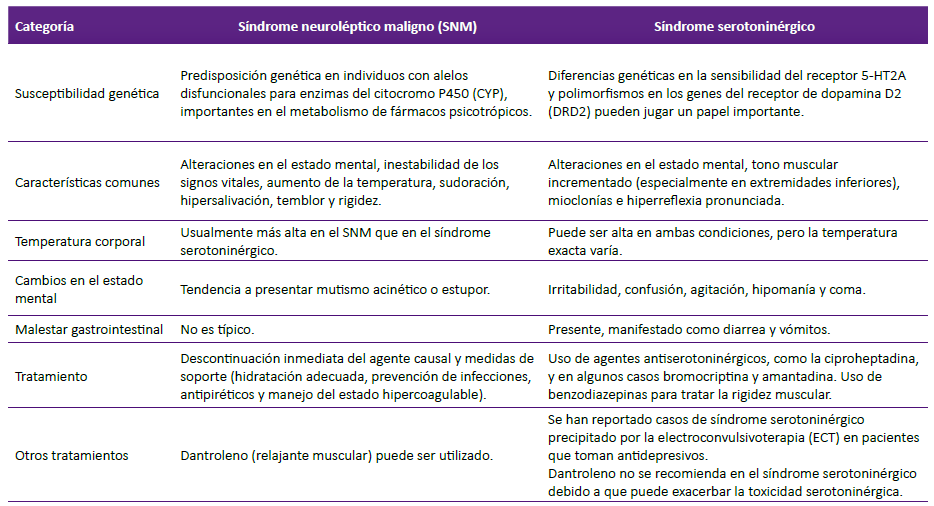
Elaborado a partir de Debeljak & Kores (55.
Exámenes complementarios
Los análisis de laboratorio desempeñan un papel crucial en el diagnóstico del SNM. Se deben obtener muestras de sangre para medir los niveles de creatina fosfoquinasa (CPK), un marcador de daño muscular, y evaluar la función renal y hepática. Además, se pueden realizar pruebas adicionales para descartar infecciones, alteraciones electrolíticas y otras anomalías metabólicas.
Se recomienda el hemograma completo para identificar leucocitosis, además de hemólisis, así como sus consecuencias. Los cultivos sanguíneos permiten descartar la posibilidad de un choque séptico. El perfil de función hepática para descartar la posibilidad de una falla hepática aguda o crónica, la urea y creatinina para descartar una falla renal, los niveles de calcio, fosfato, potasio y sodio para descartar algún desequilibrio electrolítico, los niveles de CPK para descartar la presencia de rabdomiólisis u otros tipos de necrosis de los miocitos, los niveles de hierro sérico debido a la rabdomiólisis u otras patologías hemolíticas, el análisis de gases arteriales para descartar fallas respiratorias o acidosis metabólica, los niveles de mioglobina en orina para descartar mioglobinuria, el perfil de coagulación para descartar fallas hepáticas o coagulopatía intravascular diseminada, y el perfil toxicológico sérico y urinario para descartar intoxicación por cocaína, anfetaminas, entre otros.
En un caso típico de SNM, se observan una serie de cambios en diferentes parámetros, lo que contribuye a su diagnóstico y seguimiento. En el plasma, se evidencian aumentos en las enzimas y proteínas, como LDH, CPK, TGO y TGP. La mioglobina, por otro lado, disminuye en concentración. Los electrolitos séricos y remanentes de proteólisis también se ven afectados, mostrando aumentos en los niveles de fosfato, potasio, ácido úrico y urea, y disminuciones en los niveles de calcio y magnesio. Los leucocitos y las plaquetas en la sangre periférica están elevados, los leucocitos predominantemente son neutrófilos. En la orina, se observa la presencia de proteínas, lo que indica proteinuria, y se detecta mioglobina, resultando en mioglobinuria. Además, el pH de la orina muestra una tendencia hacia acidosis metabólica. Estos resultados de laboratorio brindan información crucial para el diagnóstico y manejo adecuado del SNM, permitiendo un abordaje más específico y efectivo en esta grave condición clínica 6.
Tratamiento
Medidas generales y complementarias
Entre las medidas generales se recomienda retirar inmediatamente el agente causante sospechado del SNM. Además, valorar la posibilidad de retirar otros psicofármacos que podrían contribuir a la presencia del SNM (litio, terapia anticolinérgica, agentes serotoninérgicos). Debido a la mortalidad reportada en estos pacientes, debe pasar a una unidad de cuidados intermedios o intensivos para un monitoreo cercano de las funciones biológicas. Se debe asegurar la estabilidad cardiorrespiratoria, asegurar un estado euvolémico mediante el uso de fluidos intravenosos, disminuir la temperatura mediante métodos farmacológicos o físicos, y valorar el uso de heparina o enoxaparina para evitar la aparición de trombosis venosa profunda.
Tratamiento farmacológico
La evidencia científica que apoya el uso de los agentes que mencionaremos es limitada por diversos motivos: 1) se utilizan de forma anecdótica, aún no se cuenta con evidencia científica respecto a su eficacia; 2) ausencia de un tratamiento farmacológico óptimo basado en la evidencia, y 3) alta morbilidad y mortalidad en el SNM 6. En la tabla 3 presentamos un resumen del tratamiento psicofarmacológico.
Tabla 3. Tratamiento farmacológico del síndrome neuroléptico maligno.
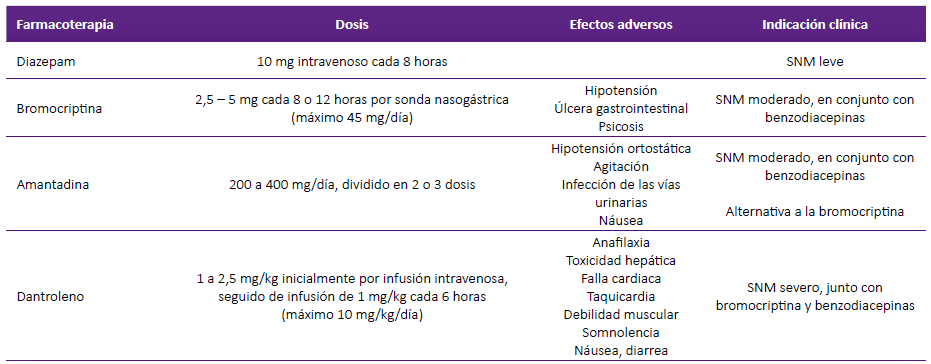
Elaborado a partir de van Rensburg & Decloedt 43.
Las benzodiacepinas pueden ser útiles para el alivio de la agitación o síntomas catatónicos 6. En nuestro medio contamos con diazepam, el cual debe ser administrado a 10 mg intravenoso cada 8 horas.
Entre los agentes dopaminérgicos, la bromocriptina estimula los receptores dopaminérgicos tipo 1 y antagoniza los receptores tipo 2 en el hipotálamo y la vía nigroestriada del sistema nervioso central. Puede utilizarse 2,5 a 5 mg de forma oral o por sonda nasogástrica cada 8 horas. Puede incrementarse hasta 30 - 45 mg/día de ser necesario. Se debe tener en cuenta que este medicamento puede empeorar los síntomas psicóticos y la hipotensión, además de generar problemas gastrointestinales, como náuseas o vómitos 43. La suspensión prematura de la bromocriptina ha dado lugar a síntomas de rebote en algunos casos 41. La amantadina. 100 mg de forma oral o por sonda nasogástrica cada 8 horas, hasta llegar a una dosis total de 200 - 400 mg/día.
El dantroleno es un relajante muscular utilizado en el tratamiento de la hipertermia maligna. Se puede administrar de 1 a 2,5 mg/kg inicialmente por infusión intravenosa, seguido de infusión de 1 mg/kg cada 6 horas (máximo 10 mg/kg/día). En una revisión sistemática de reportes de casos se encontró que la monoterapia con dantroleno ha sido reportada como efectiva hasta en el 76,7% dentro de las primeras 24 horas, sin embargo, también ha sido reportado una mayor mortalidad respecto a otros tratamientos (16,2%) 44.
Terapia electroconvulsiva (ECT)
Se ha utilizado la ECT para tratar el SNM grave, o aquellos casos en los que el diagnóstico psiquiátrico subyacente es la depresión psicótica o la catatonía, y en los casos en los cuales no se pueda descartar una catatonía letal 45,46. Puede ser considerada como un tratamiento de segunda línea, administrándose si las medidas de soporte y tratamiento farmacológico fallan durante los primeros siete días. En un estudio realizado a 48 pacientes con SNM se encontró que la ECT se asoció con una disminución no significativa de la mortalidad en comparación con aquellos que recibieron un tratamiento psicofarmacológico 47. En una revisión de 55 reportes de casos se encontró que el tratamiento con 10 sesiones de ECT produjo una recuperación completa o parcial en el 90% de los pacientes 45.
Evolución, pronóstico y complicaciones
La mayoría de los episodios de SNM se resuelven dentro de las dos primeras semanas, aunque se han reportado tiempos de recuperación de 7 a 11 días 10,31. Respecto a la reinstauración de la medicación neuroléptica se debe considerar que el riesgo de recurrencia del SNM puede ser del 37%, por lo que se deben tener en cuenta las siguientes consideraciones 1: a. Se debe seleccionar el agente con menor afinidad por los receptores D2, b. Se puede intentar la reinstauración de los antipsicóticos luego de las dos semanas de recuperación del SNM, c. Iniciar con dosis bajas, d. Monitorizar cercanamente a los pacientes por signos tempranos del SNM, e. Evitar la administración de antipsicóticos parenterales, y f. Evitar la combinación de litio con antipsicóticos.
En un estudio recientemente publicado se evaluaron las complicaciones médicas de 1346 pacientes estadounidenses con SNM, en el cual se identificaron predictores de mortalidad independientes que pueden guiar a los médicos en el manejo y el pronóstico de este síndrome 48. Se encontró que la rabdomiólisis fue la complicación más común, con una prevalencia del 30,1%, pero su asociación con la mortalidad no fue significativa (OR = 1,0, IC95%: 0,6 - 1,7, p = 0,910). De manera similar, las convulsiones mostraron una prevalencia del 12,9%, pero no se asociaron de manera significativa con la mortalidad (OR = 1,12, IC95%: 0,6 - 2,3, p = 0,644). Por otro lado, las complicaciones más graves, como la falla respiratoria aguda (prevalencia del 16,1%) y la insuficiencia renal aguda (prevalencia del 17,7%) mostraron asociaciones significativas con la mortalidad (OR = 8,5, IC95%: 5,2 - 13,8, p < 0,001 y OR = 3,6, IC95%: 2,2 - 5,9, p < 0,001, respectivamente). La sepsis también demostró asociación significativa con la mortalidad (prevalencia del 6,2%, OR = 8,2, IC95%: 4,7 - 14,4, p < 0,001), al igual que el infarto agudo de miocardio (prevalencia del 1,7%, OR = 8,1, IC95%: 3,2 - 20,3, p < 0,001) y la falla hepática aguda (prevalencia del 1,5%, OR = 12,5, IC95%: 5,0 - 31,7, p < 0,001). Finalmente, el embolismo pulmonar tuvo una prevalencia del 1% y no mostró asociación significativa con la mortalidad (OR = 2,9, IC95%: 0,6 - 13,1, p = 0,172) 48.
En consonancia con estos resultados, en una reciente revisión sistemática se analizaron 683 casos de SNM, los predictores independientes de mortalidad por SNM fueron la falta de discontinuación de antipsicóticos (OR = 4,39), problemas respiratorios (OR = 3,54), gravedad de la hipertermia (OR = 1,30) y edad avanzada (OR = 1,05). Tanto el uso de antipsicóticos orales como el de inyectables de acción prolongada no mostraron una diferencia significativa en cuanto a la incidencia de muerte (7 % frente a 10,1 %, respectivamente; p = 0,241). Asimismo, no se encontró una asociación significativa entre la clase de antipsicóticos (primera generación frente a segunda generación) y la mortalidad por SNM (8,8 % frente a 4,4 %, respectivamente; p = 0,064) 49.
Estos hallazgos resaltan la importancia de considerar otros factores clínicos, como la discontinuación de antipsicóticos, los problemas respiratorios, la gravedad de la hipertermia y la edad avanzada, para evaluar el riesgo de mortalidad en pacientes con SNM. Además, sugieren que la elección de la formulación o la clase de antipsicóticos puede no ser un factor determinante en la mortalidad asociada con el SNM.
LIMITACIONES DE LA REVISIÓN
Este artículo de revisión narrativa proporciona una visión integral y actualizada del SNM, aunque es necesario tener en cuenta sus limitaciones para interpretar adecuadamente los hallazgos presentados. Una limitación es la utilización de una fuente única de información. La búsqueda de literatura se restringió exclusivamente al buscador PubMed, lo que pudo dejar fuera estudios relevantes publicados en otras bases de datos o revistas especializadas no recuperadas mediante PubMed. Otra limitación potencial es el sesgo de publicación. Dado que los estudios con resultados positivos o significativos tienen más probabilidades de ser publicados, existe la posibilidad de que el artículo esté sesgado hacia resultados más favorables o llamativos, lo que podría influir en la interpretación de los hallazgos.
CONCLUSIONES
El SNM es una reacción adversa rara pero potencialmente fatal relacionada principalmente con el uso de antipsicóticos. Es crucial un reconocimiento temprano, diagnóstico preciso y tratamiento adecuado. Los factores de riesgo incluyen medicamentos de alta potencia, dosis altas y desequilibrios ambientales. El SNM se presenta con cambios mentales, rigidez muscular e hipertermia. El diagnóstico es desafiante, pero la identificación de factores de riesgo y un manejo clínico adecuado son fundamentales para reducir la morbimortalidad asociada.