Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO  uBio
uBio
Compartilhar
Revista de Investigaciones Veterinarias del Perú
versão impressa ISSN 1609-9117
Rev. investig. vet. Perú vol.25 no.2 Lima abr. 2014
ARTÍCULO DE REVISIÓN
Características de canal, calidad de carne y composición química de carne de llama: una revisión
Carcass characteristics, quality of meat and chemical composition of meat llama: a review
Lindon W. Mamani-Linares1,3, Faustina Cayo2, Carmen Gallo1
1 Instituto de Ciencia Animal, Facultad Ciencias Veterinarias, Universidad Austral de Chile, Valdivia, Chile
2 Universidad Pública de El Alto, La Paz, Bolivia
3 E-mail: willymlmvzupea_2@hotmail.com
RESUMEN
La carne de llama presenta un alto nivel proteico, perfil de aminoácidos similar a otros rumiantes, bajo nivel de colesterol y lípidos. El perfil de ácidos grasos se caracteriza por moderados niveles de ácidos grasos saturados y altos niveles de ácidos grasos monoinsaturados, pero bajos niveles de ácidos grasos poliinsaturados. La canal de animales de 36 a 44 meses es la más indicada para obtener cortes especiales, mientras que la carne de los animales de más edad, basado en sus características tecnológicas, es más adecuada para la fabricación de productos elaborados. Las canales de llamas jóvenes se caracterizan por tener bajo peso, pobre conformación y poca cobertura grasa. La suplementación alimenticiadeanimalesjóvenespermitemejorar lacalidaddela canalyel rendimiento de los cortes nobles, así como también la calidad de carne.
Palabras clave: características de canal, calidad de carne, composición química, llamas
ABSTRACT
Llama meat has a high protein level and low cholesterol and lipid levels. The amino acidsprofileissimilar toother ruminants.Thefattyacidprofileischaracterizedbymoderate levels of saturated fatty acids and high levels of monounsaturated fatty acids and low levelsof polyunsaturated fattyacids. Thecarcassofanimalsfrom 36 to44 months ofage is the most suitable for commercial cuts, while meat from older animals, based on their technological characteristics, is more suitable for the manufacture of meat products. Carcasses of young llamas are characterized by low weight, poor conformation and little fat cover. Feed supplementation in young animals helps improve carcass quality and performance of commercial cuts, as well as meat quality.
Key words: carcasscharacteristics,qualityofmeat,chemicalcomposition, llamas
Introducción
La llama (Lama glama), una de las cuatro especies de camélidos sudamericanos (CSA), se encuentra localizada en la zona andina de Bolivia, Perú, Chile, Argentina y Ecuador, en altitudes entre 2800 y 5000 msnm (Campero, 2005). La llama está adaptada a zonas de forraje fibroso cuyos carbohidratos estructurales hacen difícil su digestión (Sumar, 2010). La hembra alcanza la madurez a los 75 kg mientras que el macho llega a los 115 kg, variando de acuerdo al genotipo (Wurzinger et al., 2005; Cardozo, 2007). La llama tiene un gran potencial como fuente de carne en el altiplano, produciendo carcasas más grandes que las de alpacas (Lama pacos). Asimismo, el cuarto posterior presenta los cortes de más valor y una mayor proporción de músculo que la alpaca (Cristofanelli et al., 2005).
La carne de CAM es adecuada para el consumo humano, tanto por su composición química como desde el punto de vista de la calidad. La llama y la alpaca representan la más importante fuente de proteína para la población andina (Pérez et al., 2000). Contiene alta biodisponibilidad de hierro y zinc (3.3 y 4.4 mg/100 g), siendo casi el doble que otras carnes rojas (Polidori et al., 2007a). Ambas especies producen carne con bajos niveles de grasa (0.49-2.05%) y colesterol (39.0-56.3 mg/100 g) comparada con otras carnes rojas (Cristofanelli et al., 2004; Mamani-Linares y Gallo, 2013a).
Información científica sobre producción, calidad de carne y contenido nutricional es requerida por los ganaderos para promocionar la carne de llama en mercados locales e internacionales. Sin embargo, esta información se encuentra dispersa y escasa. Esta revisión recopila la información disponible para facilitar el acceso e identifica aspectos donde se requiere una mayor investigación.
Factores Productivos y de Manejo que Afectan la Producción de los Camélidos
En la región andina existen aproximadamente 3 899 350 llamas y 4 000 408 alpacas. Perú es el país con mayor población de CSA en el mundo, teniendo el 89.9% de las alpacas y el 32.0% de las llamas, en tanto que Bolivia posee el 63.8% de las llamas y el 8.9% de las alpacas (UNEPCA, 1999; FAO, 2005; INE, 2008). La población de camélidos en Bolivia, según el censo agropecuario de 2008, es de 2 486 169 llamas y 355 964 alpacas, siendo Oruro el departamento con mayor población de llamas, seguido de Potosí, La Paz y Cochabamba (INE, 2008), con una característica común de baja extracción y reposición en los rebaños (Cuadro 1).
El consumo de carne de llama es tradicional en la región altiplánica, especialmente en Bolivia. El desarrollo futuro de la carne de llama es prometedor y se ha exportado como carne exótica (Campero, 2005). Se estima una producción anual de 14 973 TM de carne de CSA. De este volumen, 59 a 75% se destina a la venta (animales en pie + animales faenados) y de 25 a 41% se destina al consumo familiar de los productores. Asimismo, el 60.3% se destina al consumo de carne fresca (consumo familiar + venta al mercado) y el resto al procesamiento de charqui y embutidos (salchicha). Por otro lado, el 40% de la carne proviene de animales menores de tres años y el restante 60% a animales mayores a tres años, donde la incidencia de sarcocystosis es mayor al 70% (PRORECA, 2004; FAO, 2005; INE, 2008).
En la llama se presentan dos fenotipos característicos (Cuadro 1). El tipo Khara (animal tipo carne) sin fibra en las extremidades, cabeza, ni orejas y con crecimiento reducido de fibra en el cuello, y el tipo Thampulli (animal tipo fibra) con abundante cobertura de fibra en extremidades, cuello y cabeza (Wurzinger et al., 2005; Cardozo, 2007).
Factores como edad, raza, fenotipo y alimentación influyen en forma significativa en la ganancia de peso, peso al final del periodo de engorda y el rendimiento de canal (Bustinza, 2001).
Efecto de la alimentación
Se han llevado a cabo diversos estudios para mejorar la producción de carne en la Khara y la fibra en el Thampulli. En las estaciones experimentales de Condoriri, Patacamaya, Choquenaira y otras granjas bolivianas, así como en centros de investigación de Perú (La Raya, Chuquibambilla, y otros), se han reportado buenos resultados en ganancia de peso y peso al final del periodo de engorda con diferentes esquemas de finalización (Sequeiros, 2007).
En el Perú, García et al. (2002) observaron mayores ganancias de peso en llamas de dos años (183 g/d) que en las de un año de edad (146 g/d) en un periodo de 90 d, así como mayores ganancias de peso en la estación de lluvia (171 g/d) que en la estación seca (136 g/d). Asimismo, se observó una mayor ganancia de peso en pastos cultivados como ryegrass + trébol (199 g/d) y phalaris + trébol (182 g/d) que en las praderas nativas (78 g/ d). Por otro lado, animales alimentados a base de concentrado presentaron mejores respuestas en ganancia de peso y conversión alimenticia con respecto a los que consumieron ryegrass o phalaris, y estos últimos, mejores respuestas que aquellos que consumieron praderas nativas (García y San Martín, 1999).
En el caso de Bolivia, las llamas presentaron ganancias de peso de 122 a 238 g/día en pasturas nativas durante la época de lluvia (Choque y Tapia, 2003), en tanto que en el Centro Experimental de Altura en Salta, Argentina, se lograron ganancias diarias de peso de 216 g/día en llamas alimentadas en pasturas cultivadas, mientras que con pastura nativa lograban 115 g/día (Rebuffi y Aguirre, 1996). Por otro lado, la suplementación con concentrado en periodo seco permitió mayores ganancias de peso (203 vs. 106 g/d) y, consecuentemente, mayor peso a la faena (Mamani-Linares y Gallo, 2013b).
Efecto de la edad
La alpaca tiene un menor peso corporal que la llama desde el nacimiento, haciéndose esta diferencia más marcada desde el sexto mes de edad (Cuadro 2), llegando las llamas machos a alcanzar pesos vivos de 63.2 kg y las alpacas 46.1 kg a los 25 meses de edad (Cristofanelli et al., 2004). Por otro lado, trabajos realizados en Bolivia (Condori et al., 2003b; Wurzinger et al., 2005; Choque y Tapia 2003) señalan pesos vivos de 73 a 79 kg en llamas machos a los 24 meses de edad. Asimismo, en condiciones ambientales altoandinas, las llamas alcanzan la madurez a los 5 años, donde las hembras Thampulli y Khara obtienen pesos de 93 y 96 kg, respectivamente (Wurzinger et al., 2005).
Según datos del INE (2008), las llamas son usualmente faenadas entre los 41 a 45 meses con pesos de 62 a 81 kg, según la región de crianza (Cuadro 1).
Efecto del sexo y fenotipo sobre las características biométricas
Existe un evidente dimorfismo sexual y fenotípico en la llama que se puede observar en las características biométricas.
Las llamas Kharas alcanzan 99 cm de altura a la cruz en tanto que las Thampullis llegan a medir 95 cm. Con relación al perímetro torácico, Wurzinger et al. (2005) y Vera (2008) encontraron valores en adultos de 98 cm para los machos Thampulli y 99 cm para las hembras Thampulli, mientras que de 101 a 110 cm en machos Khara y de 99 a 113 cm en hembras Khara. Asimismo, Cardozo y Choque (1987) encontraron que los machos miden 101 cm de perímetro torácico en comparación a los 112 cm de las hembras.
Con referencia al largo del cuerpo, Vera (2008) reporta para los machos Khara adultos medidas entre 80 y 85 cm y para las hembras de 86.6 a 88 cm, en tanto que Cardozo y Choque (1987) reportaron valores más altos (95 a 101 cm), aunque estas diferencias pueden deberse a la definición de la característica.
En el Cuadro 3 se presenta el coeficiente de correlación de Pearson de peso vivo y las medidas biométricas. Este coeficiente de correlación indica una fuerte relación entre las mediciones biométricas de altura a la cruz, largo del cuerpo y perímetro del tórax y el peso vivo de los animales (Mamani-Linares y Gallo, 2013b), lo cual demuestra la utilidad de las mediciones biométricas, especialmente del perímetro torácico como predictores del peso corporal.
Características de la Canal y Rendimiento de los Cortes
El comportamiento productivo de los animales de abasto incide directamente en la calidad de las canales, específicamente en el valor comercial o calidad composicional. Dentro de estos parámetros se encuentra el peso de canal, composición física en términos de músculo, hueso y grasa, y rendimiento de los cortes nobles y de grasa en distintos depósitos.
Peso y rendimiento de la canal
El Cuadro 4 presenta datos relacionados con peso vivo y rendimiento de la canal de llamas, los cuales son resultados de trabajos realizados en Chile, Perú y Bolivia (García, 1995; Pérez et al., 2000; Choque y Tapia, 2003; Cristofanelli et al., 2004;Arzabe et al., 2006; Mamani-Linares y Gallo, 2013a,b; Laura, 2012). En todos los casos, los animales fueron criados y alimentados en pastoreo en un sistema extensivo.
En el trabajo de Pérez et al. (2000), realizado en Chile con animales mayores de 3 años, los machos presentaron un peso vivo de 100.6 kg con peso y rendimiento de la canal de 56.2 kg y 55.8%, respectivamente, en tanto que los valores para las hembras fueron de 104.6 kg, 56.7 kg y 54.2%, respectivamente. Asimismo, García (1995) reportó pesos de canal de 30 a 46 kg en llamas faenadas en el matadero de Arica, y Bustinza (2001), por su parte, menciona que el rendimiento de canal es menor en animales de 2 y 6 años (56.2%) y mayor en animales de 3 y 4 años (59.5%).
Las diferencias entre los trabajos se podrían explicar por las diferencias en edades y tipos de animales, así como por la condición corporal y época del año, debido a la disponibilidad de alimentos en las diferentes ecorregiones.
Calidad de la canal
La determinación de la calidad de la canal es uno de los factores más importantes desde el punto de vista económico, tanto para el productor como para la industria, puesto que está condicionada por las exigencias del mercado y tiene un efecto directo en el precio (Franco, 2009); no obstante, son escasos los estudios realizados sobre calidad de canales en CSA.
La canal de la llama se caracteriza por ser magra y con baja cobertura grasa, debido a que la mayor concentración de grasa se encuentra alrededor de los órganos internos (Cuadro 5). Sin embargo, debe tenerse en cuenta que la grasa es un componente importante de la canal de los animales criados para la producción de carne, ya que tiene funciones importantes, tales como el aislamiento térmico de la canal, reduciendo la caída brusca de temperatura durante el enfriamiento post-mortem (acortamiento por frío) y por estar asociada con el sabor, textura y jugosidad de la carne (Gallo, 2010).
Otra consecuencia de la pobre cobertura de grasa subcutánea y conformación de las canales de llama es que las hace susceptibles a pérdidas elevadas de humedad durante la refrigeración. Estas pérdidas tienden a ser más altas en las canales pequeñas que en las grandes; por ejemplo, canales con menos de 33 kg pierden el 3% de peso, mientras que canales más pesadas pierden el 2.3% (Fig. 1) (Mamani-Linares y Gallo 2013b).
Turín et al. (1999) estudiaron el efecto de la alimentación sobre la conformación y el grado de engrasamiento de canales de alpaca utilizando escalas de 1 (muy deficiente) a 5 (muy bueno) para la evaluación de las formas de la canal y de la extensión y grosor de la grasa subcutánea. Animales de 21 meses bajo pastoreo tradicional sobre pasturas naturales altoandinas presentaron valores de conformación promedio entre regular y bueno (3 a 4) y un grado de engrasamiento regular (3), en tanto que alpacas criadas en pastos cultivados en terrenos favorables presentaron canales con conformación y grado de engrasamiento muy buenos (5).
Características morfométricas o medidas objetivas de canal
Las características morfométricas o medidas objetivas de la canal se presentan en el Cuadro 6. Estas medidas tienen una estrecha relación con el buen rendimiento cárnico y la conformación.
Algunas medidas objetivas de la canal son influenciadas por la edad y otras por el sistema de alimentación o finalización. Según Yáñez et al. (2004), el perímetro torácico es una medida afectada por su base ósea, músculo y deposición de grasa. La deposición de tejido adiposo, principalmente en la región esternal, está relacionada con el grado de acabado. Asimismo, el largo del cuerpo en animales de la misma edad usualmente no difiere cuando son sometidos o finalizados con diferentes dietas, dado que esta medida morfométrica está relacionada a la estructura ósea, la cual no está directamente afectada por la alimentación animal a esas edades. Por otro lado, el perímetro de grupa es la variable que muestra mayor diferencia en animales finalizados con diferentes dietas, debido a que es una medida basada en la cantidad de masa muscular. Esta medida, según Araújo Filho et al. (2007), es indicador de la deposición de carne de primera calidad.
En concordancia con esta información, Mamani-Linares y Gallo (2013b) reportaron que las canales de animales suplementados con concentrado presentaron valores más altos en perímetro del tórax, perímetro de pierna y perímetro de grupa.
El Cuadro 7 presenta los coeficientes de correlación de Pearson entre las medidas morfométricas y variables relacionadas a la canal. Algunas de las variables indicadas en el cuadro tienen al menos un valor de correlación por encima de 0.70 con alguna otra variable, indicando la existencia de colinealidad entre esas variables. Las características de peso vivo y peso de la canal caliente fueron las que presentaron correlaciones altas y positivas con las principales medidas morfométricas (largo de cuerpo, perímetro torácico, profundidad de tórax).
Rendimiento de los cortes mayores de la canal En los Cuadro 8 se observa el peso y el porcentaje de rendimiento de los cortes de la canal en llamas criadas y engordadas a base de pastura nativa. 
El rendimiento de los cortes de la canal entre las especies de CSA es diferente. Cristofanelli et al. (2005) hicieron una evaluación en 20 llamas y 40 alpacas machos en Arequipa, Perú, criados extensivamente y sacrificadas a los 25 meses de edad. Se encontró que el porcentaje de la pierna con respecto al peso de la canal fue significativamente menor para las alpacas que para las llamas, concluyendo que la llama tiene mayor potencial intrínseco como fuente de carne en la zona altoandina. Las grandes diferencias entre cortes que se emplean en cada país o región dificulta la comparación entre canales sobre la base de los cortes; sin embargo, el corte pierna es uno de los más valiosos (corte de primera).
Composición tisular de cortes de canal
La composición tisular junto con el rendimiento de la canal han sido los criterios más utilizados para evaluar la calidad de la canal. La composición tisular abarca todos los tejidos del animal desde el punto de vista histológico; nervioso, óseo, muscular, adiposo, conjuntivo y epitelial.
La proporción de músculo de los cortes pierna y chuleta de la llama es significativamente mayor que en otros cortes, mientras la proporción de grasa y hueso en el corte paleta es el más elevado (Cuadro 9). Por otro lado, de acuerdo a Cristofanelli et al. (2005), la proporción de músculo en el corte paleta y pierna de la llama es significativamente más alto que en el de la alpaca.
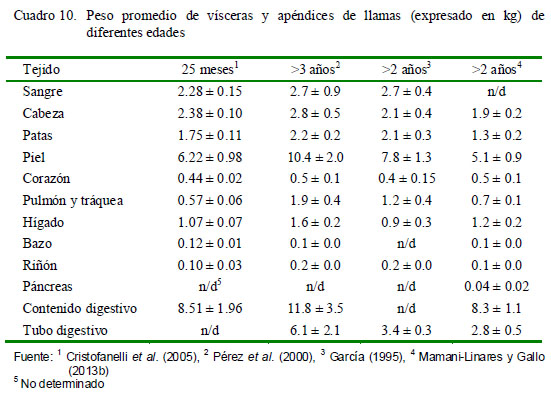
El peso promedio de vísceras y apéndices de llamas de diferentes edades se muestran en Cuadro 10. Con excepción del peso de bazo, corazón y patas, el peso de las demás vísceras se incrementa proporcionalmente con la edad de los animales.
Composición Química de la Carne
El conocimiento de la composición química de la carne de llamas es importante para el entendimiento de su valor nutricional, así como también para interpretar su calidad sensorial y aptitud para el tratamiento industrial.
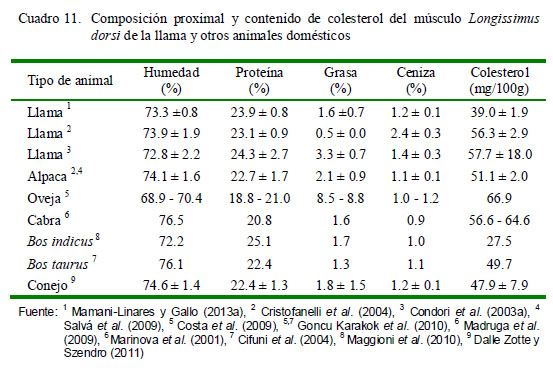
En la literatura científica internacional se encuentra amplia información sobre los componentes de la carne de alpaca, especialmente del músculo Longissimus dorsi. Así por ejemplo, se dispone de los trabajos de Cristofanelli et al. (2004), Polidori et al. (2007b) y Salvá et al. (2009) con animalescriados de forma tradicional en el Perú. En el caso de la llama, solo se encuentra información relacionada a los componentes químicos mayoritarios de la carne (Cuadro 11). En general, la carne de alpaca y llama es baja en grasa.
La composición química del músculo L. dorsi de la alpaca entre 18 a 24 meses de edad tiene un contenido promedio de humedad, proteína, grasa intramuscular y minerales de 74.17, 22.7, 2.1 y 1.1%, respectivamente (Salvá et al., 2009) (Cuadro 11). El contenido de humedad y proteína es bastante similar a los valores reportados por Cristofanelli et al. (2004); sin embargo, conun mayor contenido de grasa intramuscular, aunque inferior al hallado por Polidori et al. (2007b) para L. dorsi de llamas del Perú. Asimismo, hubo discrepancia en el contenido de cenizas encontrado por Salvá et al. (2009) y Cristofanelli et al. (2004). Por otra parte, la composición proximal del L. dorsi de alpaca ha sido muy similar a la descrita para el camello de Arabia (Kadim et al., 2006; Hoffman, 2008).
En la carne de llamas criadas en Chile se encontró 21.8 y 19.9% de proteína en machos y hembras, respectivamente (Pérez et al., 2000), en tanto que en animales de Bolivia se hallaron niveles ligeramente más elevados (23.5 a 24.3 %) (Condori et al., 2003a). Asimismo, la concentración de lípidos en la carne de llamas criadas en Chile (Pérez et al., 2000), tanto en machos como hembras, fue mayor en comparación con los resultados obtenidos por Cristofanelli et al. (2004, 2005), posiblemente debido a los diferentes métodos de extracción de lípidos empleados. La suplementación alimenticia con concentrado tiende a incrementar el contenido de grasa intramuscular del músculo L. dorsi; sin embargo, estos valores son bajos en comparación a otras carnes (Mamani- Linares y Gallo, 2013b).
Cristofanelli et al. (2004) determinaron valores de 51 y 56 mg/100 g de colesterol en carne (L. dorsi) de alpacas y llamas, respectivamente (Cuadro 11). El contenido de colesterol es más alto en carne de llama que alpaca; sin embargo, ambas carnes presentan valores más altos que en la carne de conejos y bovinos (Cuadro 11), pero muy parecido al contenido de colesterol en carne de camellos (42-47 mg/100 g) (RIRDC, 2007; Duckett et al., 2009). Por otro lado, los ovinos presentan valores más altos (65.9 a 67.9 mg/100 g) (Costa et al., 2009).
Coates y Ayerza (2004) estudiaron en llamas argentinas el contenido de colesterol en el músculo L. dorsi (52 mg/100 g) y en grasa renal (93 mg/100 g), estableciendo así la diferencia en el contenido de colesterol entre ambos tejidos.
Perfil de aminoácidos del músculo L. dorsi
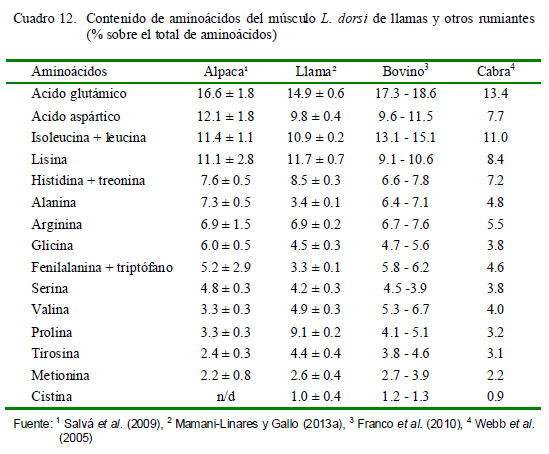
El contenido de aminoácidos en L. dorsi de llamas y otros rumiantes se muestran en el Cuadro 12. Hay pocos reportes sobre la composición de aminoácidos de la carne de CSA, aunque hay más sobre de carne de camello (Dawood y Alkanhal, 1995). En general, la composición de aminoácidos de la carne de alpaca y llamas es comparable a la carne de otras especies (Kadim et al., 2008; USDA, 2008).
Salvá et al. (2009) reportan en la carne de alpaca niveles más altos de ácido aspártico y lisina y niveles más bajos de valina y prolina en comparación con la carne de camello y bovino. Por otro lado, la carne de llama (Cuadro 12) muestra altos niveles de prolina, similares niveles de lisina, metionina, ácido aspártico y ácido glutámico y niveles menores de isoleucina y alanina en comparación con la carne de alpaca y bovino.
Contenido de minerales del músculo L. dorsi
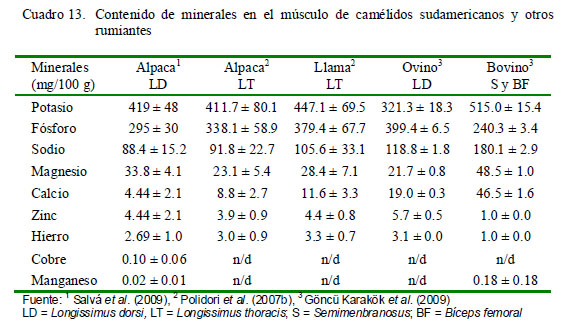
El contenido de minerales de la carne de llama y alpaca se muestra en el Cuadro 13. La carne de estas dos especies presenta niveles de potasio más elevados que otros minerales, lo cual también es observado en camellos (Dawood y Alkanhal 1995; Kadim et al., 2006). El contenido de potasio, fósforo y calcio en carne de llamas es significativamente mayor que en la carne de alpaca. Asimismo, los bovinos presentan niveles mayores de potasio, magnesio, calcio y sodio en comparación con alpacas y llamas, pero niveles más bajos de zinc (Göncü Karakök et al., 2010). También se puede observar que el contenido de hierro en carne de llamas es mayor que en la carne de bovino (Duckett et al., 2009), pero similar a la carne de ovino.
Contenido de vitaminas del músculo L. dorsi
El contenido de a-tocoferol de la carne es un parámetro relevante, ya que mayores niveles mejoran la calidad general de la carne, principalmente por la inhibición de la oxidación de pigmentos y ácidos grasos; además, evita la pérdida de color, característica deseable durante el almacenamiento (Wood et al., 2008). Salvá et al. (2009) reportan promedios de concentración de 0.31 ± 0.21 μg/g de a-tocoferol y 0.17 ± 0.16 μg/g de retinol en carne de alpaca. No se encontraron valores de tocoferoles en carne de llamas en la literatura.
Los niveles en la carne de alpaca se encuentran por debajo del nivel crítico (3.0- 3.5 μg/g de músculo) sugerido para la estabilidad óptima de lípidos de la carne (Arnold et al., 1993; Realini et al., 2004), que suele ser alcanzado en carne de bovinos alimentados a pasto (Descalzo y Sancho, 2008). La concentración de a-tocoferol en forrajes frescos puede teóricamente resultar en una saturación del músculo con a-tocoferol, ya que el forraje verde puede ser una buena fuente dietética de a-tocoferol (Faustman et al., 1998). Sin embargo, los valores de tocoferol encontrados en la carne de ovino son generalmente más bajos que el nivel crítico (Demirel et al., 2006).
De acuerdo a Realini et al. (2004), la suplementación con 1000 I.U. de a-tocoferol/ animal/día por 100 días en ganado engordado con concentrado es suficiente para alcanzar similares niveles de a-tocoferol en ganado alimentado con pasto (3.74 vs. 3.91 μg/g), superando los niveles propuestos como concentración crítica para mejorar la vida útil de la carne en el anaquel.
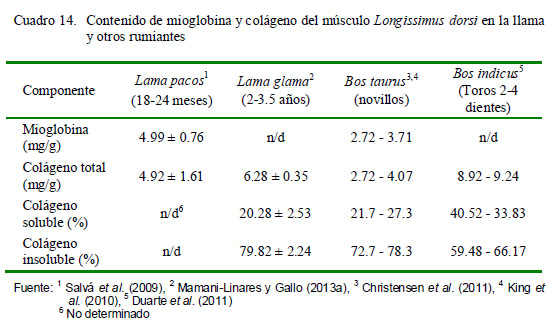
Contenido de mioglobina y colágeno del músculo L. dorsi
La mioglobina es la principal proteína responsable del color de la carne, aunque otras hemoproteínas como la hemoglobina y el citocromo C también pueden desempeñar un rol en el color de la carne de res, cordero, cerdo y pollo (Mancini y Hunt, 2005). La concentración de mioglobina en el músculo L. dorsi de alpaca es de 4.99 ± 0.76 mg/g (Cuadro 14). No se encontraron datos sobre el contenido de pigmentos de la carne de otros camélidos en la literatura. Sin embargo, los valores en la carne de alpaca son ligeramente superiores a los reportados por King et al. (2010) y Christensen et al. (2011) en carne de vacuno (2.72 a 3.71 mg/g). En el bovino, la genética influye en la variación del contenido de mioglobina, toda vez que hay variaciones importantes entre razas de carne (King et al., 2010).
El colágeno es el tejido conectivo que más contribuye a la reducción de terneza de la carne. Aunque el colágeno constituye menos del 2% del músculo esquelético, está asociado con la dureza y puede ser muy resistente a la degradación física durante la cocción (Weston et al., 2002). Se reporta 4.92 mg/g de colágeno en carne de alpaca (18-24 meses) y de 6.28 mg/g en la llama (Cuadro 14). Contenidos inferiores se han detectado en el músculo Longissimus de toros jóvenes (1-2 años) (Torrescano et al., 2003; Rhee et al., 2004; Serra et al., 2008) y corderos de 8- 10 meses (Tschirhart-Hoelscher et al., 2006). Asimismo, contenidos de colágeno total más elevados fueron observados en bovinos cebuínos de 3 años finalizados a pasto (Duckett et al., 2007), pero con menor porcentaje de colágenos insolubles comparado con llamas.
Perfil de ácidos grasos del músculo L. dorsi
Se dispone de amplia información del contenido de ácidos grasos de músculos y grasa perirrenal en carne de alpaca y llama (Salvá et al., 2009; Mamani-Linares y Gallo, 2013a).
Según Salvá et al. (2009), el principal ácido graso en el perfil de ácidos grasos de la grasa intramuscular (IMF) y grasa perirrenal (PRF) de alpacas es C18:1 n-9 (con 24.2% del total de ácidos grasos), seguido por C16:0 (22.0%) y C18:0 (19.8%). No obstante, se observan diferencias para casi todos los ácidos grasos individuales entre IMF y PRF. Los ácidos grasos saturados (SFA) representan entre 51.2 y 63.9%, los ácidos grasos monoinsaturados (MUFA) entre 37.1 y 30.3%, y los poliinsaturados (PUFA) entre 11.7 y 5.8% del total de ácidos grasos en la IMF y PRF, respectivamente, encontrándose diferencias entre ambos depósitos de grasa.
La grasa intramuscular de alpaca tiene una relación de 0.26:1 para PUFA:SFA, que es intermedia entre la reportada para la carne de otros rumiantes, mientras tanto la relación de n-6:n-3 en grasa intramuscular de alpaca es 3.74:1, que es mayor en comparación con las proporciones de 2:1 y 3:1 reportadas para carne de bovinos y ovinos (USDA, 2008). La relación de PUFA:SFA y n-6:n-3 en grasa intramuscular de alpaca fue próxima al mínimo (0.4) y máximo (4) de la relación recomendada (BDH, 1994). Además, el contenido de ácido linolénico conjugado (CLA) fue 1.2 y 1.0% de los ácidos grasos totales para IMF y el PRF, respectivamente. Estos valores oscilaron dentro de los rangos reportados en la carne de vacuno (0.12-1.0%) y cordero (0.43-1.9%) (Schmid et al., 2006).
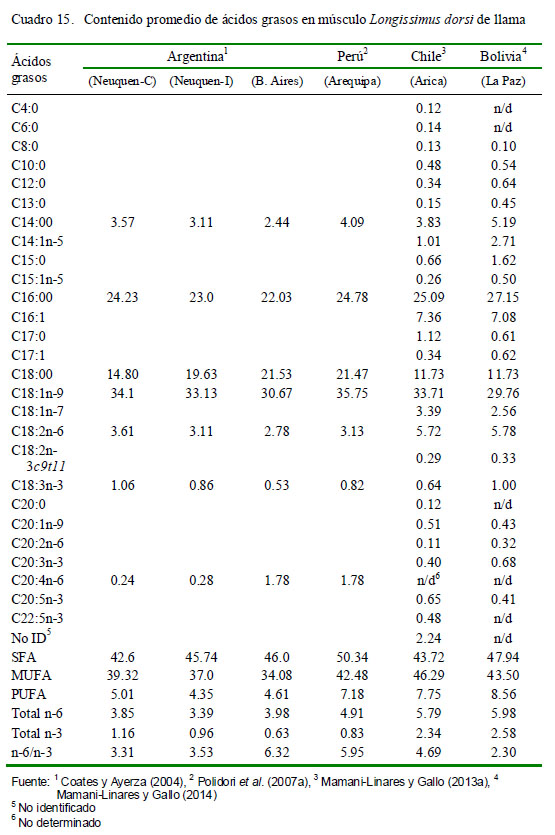
Los trabajos realizados por Coates y Ayerza (2004) y Polidori et al. (2007a) sobre el perfil de ácidos grasos en carne de llama determinaron solo siete ácidos grasos mayoritarios, faltando determinar la mayoría de los n-3 y CLA. En estos trabajos se determinó el perfil de ácidos grasos en el músculo L. thoracis y lumborum de llamas argentinas (5-8 años de edad) y peruanas (2 años), encontrando entre 46 a 50% de SFA y de 34 a 42% para MUFA en relación a los ácidos grasos totales (Cuadro 15).
En general, la proporción de ácidos grasos del músculo L. dorsi de las llamas guarda relación con la proporción de ácidos grasos de bovinos criados en sistemas extensivos y finalizados a pasto (Realini et al., 2004), quienes presentan 49.1, 41.0 y 10.0% para SFA, MUFA y PUFA, respectivamente.
La proporción de ácidos grasos saturados en llamas (Coates yAyerza, 2004; Polidori et al., 2007a) puede considerarse como una de las más elevadas después del guanaco (Gonzalez et al., 2004). En comparación, la concentración de ácidos grasos saturados se encuentra entre 47.7 y 59.7% en el camello (RIRDC, 2007) y entre 35.2 y 44.8% en bovinos finalizados a pastura (Dierking et al., 2010).
Las concentraciones de MUFA en carne de llama son de las más altas en los animales, y puede compensar el efecto negativo de los ácidos grasos saturados en los problemas de salud humana (Simopoulos, 1999; German y Dillard, 2004). La concentración de PUFA registrada en la carne de llama (Cuadro 15) es baja en comparación con otras carnes como del bovino, que presenta 9.96% (Realini et al., 2004).Aunque el total de PUFA es bajo, la relación entre los ácidos grasos n-6/n-3 se ajusta a la recomendada para el consumo humano (Simopoulos, 1999). En el camello, las concentraciones de ácidos grasos poliinsaturados en la carne van entre 6.1 y 14.7% (RIRDC, 2007), en función del músculo analizado.
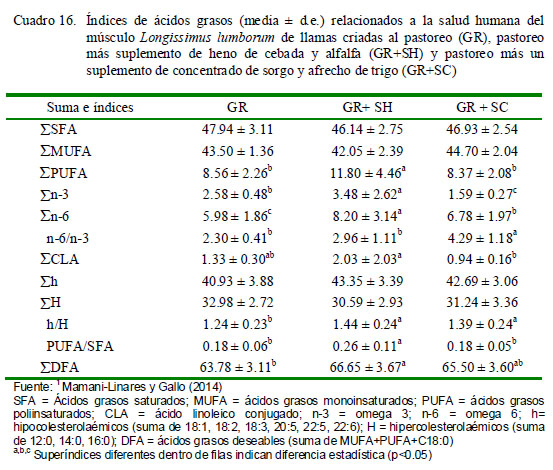
Desde el punto de vista nutricional, la grasa de llamas criadas en pastoreo (en periodo seco) con suplementación con heno de alfalfa y cebada parece ser más adecuada que cuando es criada solo al pastoreo o con suplemento concentrado de sorgo-afrecho de trigo (Cuadro 16), debido a una mayor proporción de n-3 y CLA y tasas inferiores de n-6: n-3 (Mamani-Linares y Gallo, 2014).
Se ha demostrado que dietas basadas en pasto pueden mejorar significativamente la composición de los ácidos grasos (FA). Las
dietas basadas en pasto verde mejoran los isómeros totales de CLA (C18:2), del ácido trans-vaccénico (TVA) (C18: 1 t11), un precursor de CLA, y de ácidos grasos como omega-3 (n-3) en un g/g grasa base (Realini et al., 2004). Asimismo, se ha demostrado que el perfil de ácidos grasos de la carne de llama faenada en la estación lluviosa tiene mayores niveles de grasas poliinsaturadas y CLA en relación a animales faenados en la estación seca (Cuadro 17). Las grasas de llamas faenadas en la estación de lluvias tienen niveles más bajos de ácidos grasos perjudiciales para la salud, lo cual puede ser influenciado por la presencia de leguminosas como Trifolium amabile en los campos de pastoreo.
Características Tecnológicas de la Carne
En los últimos años se ha puesto énfasis en la búsqueda de métodos de evaluación de canales que permitan no solo predecir rendimientos (rendimiento de cortes nobles, proporción de músculo y grasa, etc.), sino también las características organolépticas y tecnológicas de la carne, a fin de poder estimar la calidad final del producto a nivel de consumidor (Gallo, 2010). Propiedades tecnológicas de la carne como el pH, la capacidad de retención de agua, la textura, el color y su estabilidad permiten evaluar su aptitud y comportamiento en las etapas de conservación, comercialización, industrialización y preparación para el consumo.
El pH es un parámetro importante relacionado con la susceptibilidad de la carne a su deterioro y se usa para decidir sobre el tipo de procesamiento al que se va a destinar la carne. El pH depende de factores tales como el estrés ante-mortem al que ha sido expuesto el animal, factores genéticos predisponentes a dicho estrés, condiciones post-mortem, sexo, clase o categoría de animal, tipo de alimentación recibida en la finalización, y región anatómica en que se mide, entre otros (Tarrant y Grandin, 1993; Apaoblaza et al., 2008).
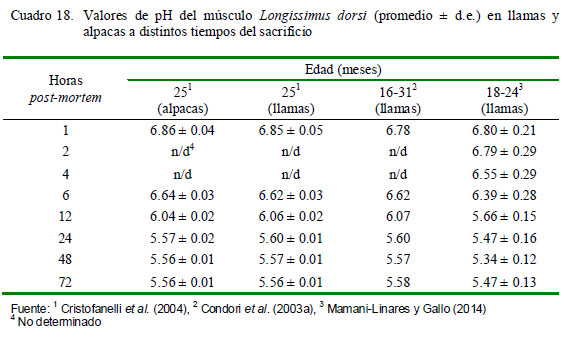
En los casos que el animal se somete a un estrés prolongado antes del sacrificio, consume prácticamente sus reservas de glucógeno, de allí que no hay glicólisis anaerobia post-mortem, por lo que las carnes presentan la condición conocida como «corte oscuro» (Hood y Tarrant, 1980). No obstante, la alpaca parece ser poco susceptible a la pérdida de calidad de la carne debida al estrés y no suele presentar estos defectos. Cristofanelli et al. (2004) midieron el pH en las canales de 20 llamas y 40 alpacas machos después de 1, 6, 12, 24, 48 y 72 h postmortem, observando en todos los casos un proceso glicolítico normal (Cuadro 18), alcanzándose finalmente valores de pH en torno a 5.5 a los 72 h en llamas, concordante con los resultados de Salvá et al. (2009), quienes reportan pH de 5.63 a los 48 h postmortem en alpacas, mientras que en llamas se ha observado un pH de 5.47 a las 24 h post-mortem (Mamani-Linares y Gallo, 2014).
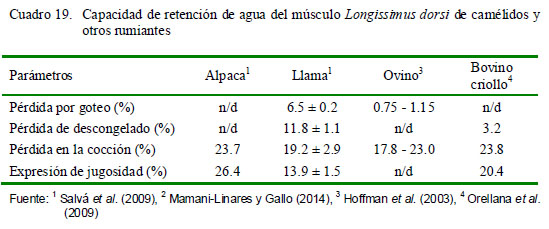
La capacidad de retención de agua (CRA) se define como la capacidad de la carne para retener el agua durante la aplicación de fuerzas externas, tales como corte, calentamiento, trituración o prensado (Zhang et al., 2005). La CRA es una propiedad tecnológica importante que determina las pérdidas de peso, principalmente por liberación de jugos, que se producen en toda la cadena de distribución y transformación de la carne. Los valores de CRA pueden ocasionar pérdidas económicas, al afectar la calidad de la carne y de sus productos (jugosidad, palatabilidad, etc.). Los factores que influyen sobre la CRA de la carne son el espacio entre las miofibrillas (espacio libre donde se retiene el agua) y la presencia de moléculas que aportan cargas y se enlazan con la molécula del agua (Price y Schweigert, 1994). La CRA de los camélidos ha demostrado ser ligeramente menor a la de otras especies (Cristofanelli et al., 2004).
Salvá et al. (2009) reportaron valores de CRA para carne de alpaca (Cuadro 19) de 26.4% como expresión de jugosidad y 23.7% como la pérdida de cocción, siendo este último valor similar a los reportados para la carne de camellos de 2 años edad (Kadim et al., 2006) y toros jóvenes (Rhee et al., 2004; Serra et al., 2008). En llamas se observan altos valores de pérdidas por descongelamiento, posiblemente debido al extremadamente bajo contenido de grasa intramuscular (Mamani-Linares y Gallo, 2014).
La terneza puede ser definida como la facilidad con que la carne se deja masticar, que puede descomponerse en tres sensaciones por el consumidor: una inicial o facilidad a penetración y corte, otra más prolongada que sería la resistencia que ofrece a la rotura a lo largo de la masticación, y una final que daría sensación de residuo más o menos importante (Osorio et al., 2009). La fuente de variación de la terneza se puede atribuir a la edad, sexo, peso y raza del animal, músculo, marmoleo, tasa y extensión de glicólisis, y estrés ante mortem (Muchenje et al., 2009). Según Muir et al. (2000) y Monsón et al. (2005), la terneza de la carne es función del contenido de colágeno (totales y solubles), estabilidad térmica y estructura de las miofibrillas del músculo (degradación de las proteínas miofibrilares). Asimismo, el contenido de colágeno parece estar altamente correlacionado con la fuerza de corte de la carne, aunque frecuentemente se observa una baja correlación en carne cocida (Lepetit, 2007).
La maduración de la carne a temperatura de refrigeración y envasado al vacío es un método eficaz para mejorar su terneza (Franco, 2009). En el vacuno, el 80% de la mejora en la terneza se alcanza transcurridas las dos semanas (Koohmaraie et al., 2002), siendo en la primera semana donde los resultados son más evidentes (Hadlich et al., 2006). Sin embargo, esta mejora en la terneza conforme avanza la maduración, dependerá de la raza, del sistema de producción-alimentación, del músculo y de la temperatura de almacenamiento (Realini et al., 2004; Franco, 2009).
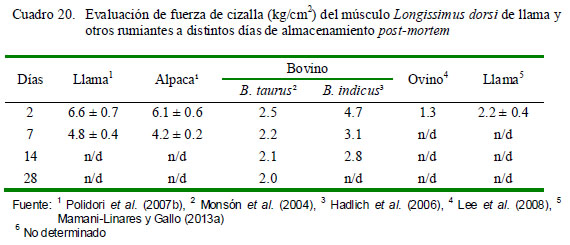
Los valores de fuerza de corte (WBFS), reportados por Salvá et al. (2009) para alpaca, en ambos sexos, fueron de 4.67 kg/cm2; esto es 20% menor que los reportados por Polidori et al. (2007b) para el Longissimus dorsi de alpacas macho de 25 meses de edad, después de dos días de almacenamiento postmortem. Asimismo, Mamani-Linares y Gallo (2013a) reportan valores de WBFS aún más bajos (2.16 kg/cm2) para llamas Khara. Esta variación puede atribuirse en parte a diferencias metodológicas, es decir, al tamaño de la muestra y proceso de calentamiento o cocción (bolsas en agua u horno), así como al sexo del animal.
Los valores de WBFS (fuerza de cizalla) de la carne de llamas Khara (2.2 kg/ cm2) son superiores a aquellos de la carne de ovino, ligeramente inferior a los obtenidos para el músculo Longissimus dorsi de Bos taurus (Monsón et al., 2004), y muy inferiores a los de Bos indicus reportados por Hadlich et al. (2006) (Cuadro 20).
El color de la carne es un factor importante que influye en la aceptación del consumidor, en las decisiones de compra y en la satisfacción proporcionada por los productos cárnicos (Lawrie y Ledward, 2006). El color está relacionado con la concentración de mioglobina y pigmentos proteicos presentes en el músculo. Entre los factores que pueden influir en el color de la carne se encuentran las enzimas, la dieta, la edad del animal e incluso la actividad realizada por el animal (Muchenje et al., 2009).
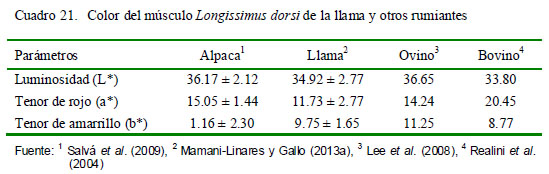
Las características del color del Longissimus dorsi de los CSA y otros rumiantes se muestra en el Cuadro 21. Aunque existe escasa disponibilidad de información en la literatura para la carne de alpaca, se encontró que tanto L* y a* se encuentran dentro de los valores reportados para carne de camello (32.7 a 37.7 para L* y de 13.4 a 17.1 para a*) por Babiker y Yousif (1990) y Kadim et al. (2006), e intermedios para la carne de cordero (Tschirhart-Hoelscher et al., 2006) y de vacuno (Muchenje et al., 2009). Por otro lado, Salvá et al. (2009) encontraron un valor de b* (tenor verde - amarillo) considerablemente más bajo para la alpaca con respecto a los encontrados en bovinos y ovinos. No se tiene explicación para estas diferencias, lo que podría dar lugar a que la carne de alpaca tiene un color característico. Por otro lado en llamas Khara se encontraron valores con tenor de rojez bajos comparado con alpacas y ovinos (Mamani-Linares y Gallo, 2013a).
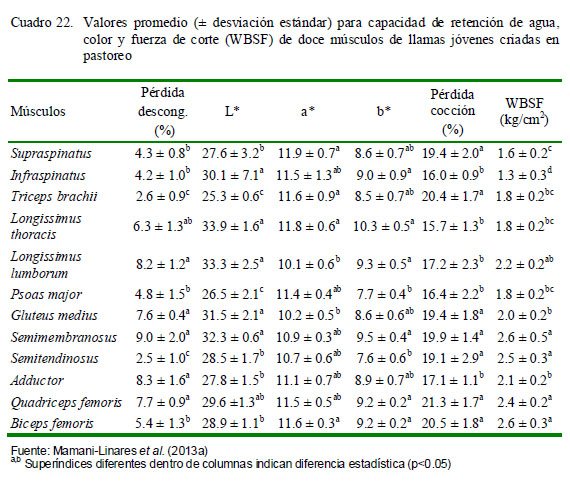
El Cuadro 22 muestra la capacidad de retención de agua, color y WBSF de los principales músculos de la llama. Según Lawrie y Ledward (2006), los parámetros más importantes considerados en la evaluación de la calidad de la carne son apariencia, jugosidad, terneza y sabor. En el cuadro se muestra que los músculos de apoyo (Longissimus thoracis y Psoas major) son más tiernos que los músculos locomotores (Semitendinosus, Quadriceps femoris, Biceps femoris). Asimismo, los músculos que tienen mejores características de color son Longissimus thoracis, Longissimus lumborum, Gluteus medius y Semimembranosus; además, los músculos con mayor capacidad de retención de agua son Semitendinosus e Infraspinatus.
CONCLUSIONES
La carne de llama presenta un alto nivel proteico, perfil de aminoácidos similar a otros rumiantes, y bajo nivel de colesterol y lípidos. El perfil de ácido grasos se caracteriza por moderados niveles de ácidos grasos saturados y altos niveles de ácidos grasos monoinsaturados, pero bajos niveles de ácidos grasos poliinsaturados; sin embargo, muestra una relación beneficiosa entre los diferentes ácidos grasos.
La canal de animales de 36 a 44 meses es la más indicada para obtener cortes especiales, mientras que la carne de los animales de más edad, basado en sus características tecnológicas, es más adecuada para la fabricación de productos elaborados.
Las canales de llamas jóvenes se caracterizan por tener bajo peso, pobre conformación y poca cobertura grasa, por lo que deben ser refrigerados para evitar el acortamiento por frío o ser estimulados eléctricamente antes de la refrigeración, para mantener o mejorar la textura de la carne.
La suplementación alimenticia de animales jóvenes permiten mejorar la calidad de la canal y el rendimiento de los cortes nobles.
LITERATURA CITADA
1. Aguilar CJC. 1999. Suplementación de heno y ensilaje de alfalfa para el incremento de peso vivo en llamas ancutas machos. Tesis de grado. Oruro, Bolivia: Universidad Técnica de Oruro. 167 p. [ Links ]
2. Apaza E, Quispe J. 1996. Correlación fenotípica: peso vivo al nacimiento y peso vivo al destete en llamas. ALLPAKA 5: 53-63. [ Links ]
3. Apaza N, Málaga J. 1996. Engorde de llamas y alpacas en pastos cultivados (Alfalfa – Dactylis). ALLPAKA 5: 14-20. [ Links ]
4. Apaza ZE, Pinedas MS. 2001. Crecimiento en llamas del CIP La Raya. ALLPAKA 9: 39-50. [ Links ]
5. Apaoblaza A, Pulido R, Gallo C. 2008. Efecto de una suplementación en base a maíz roleado, sobre la prevención de corte oscuro (CO) y algunas variables de calidad de la carne en novillos. En: Libro de Resúmenes XXXIII Congreso Anual de la Sociedad Chilena de Producción Animal. Valdivia, Chile. p 251-252. [ Links ]
6. Araújo Filho JT, Costa RG, Fraga AB, Sousa WH, Gonzaga Neto S, Batista ASM, Cunha MGG. 2007. Efeito de dieta e genótipo sobre medidas morfométricas e não constituintes da carcaça de cordeiros deslanados terminados em confinamento. Rev Bras Saúde Prod Anim 8: 394-404. [ Links ]
7. Arnold RN, Scheller KK, Arp SC, Williams SN, Schaefer DM. 1993. Dietary a-tocopheryl acetate enhances beef quality in Holstein and beef breed steers. J Food Sci 58: 28-33. [ Links ]
8. Arzabe C, Rodríguez T, Condori G, Claros A, Martínez Z, Cochi N, Quispe JL, et al. 2006. Determinación del rendimiento y la rentabilidad de los cortes menores de la carne de llama (Lama glama). En: Memoria de la XVI Reunión Nacional de ABOPA. Sucre, Bolivia. p 217-232. [ Links ]
9. Babiker SA, Yousif KH. 1990. Chemical composition and quality of camel meat. Meat Sci 27: 283-287. [ Links ]
10. [BDH] British Department of Health. 1994. Nutritional aspects of cardiovascular disease. Report on health and social subjects N.° 46. London: Her Majestys Stationery Office. [ Links ]
11. Bustinza V. 2001. La alpaca. Puno, Perú: Universidad Nacional del Altiplano. 495 p. [ Links ]
12. Campero JR . 2005. Lama (Lama glama) and guanaco (Lama guanicoe): general perspective. En: Proc ICAR/ FAO Seminar ICAR. Technical Series N.° 11. Sousse, Tunisia. p 11-18. [ Links ]
13. Cardozo A. 2007. Camélidos. Cochabamba, Bolivia: Poligraf. 467 p. [ Links ]
14. Cardozo A, Choque F. 1987. Comparación de 5 caracteres zoométricos en llamas Kcaras y Thampullis. En: X Reunión Nacional de ABOPA. La Paz, Bolivia. p 3-6. [ Links ]
15. Choque S, Tapia M. 2003. Aptitud productiva de ankuta qara, phulla, suxalli en iral y tolar del altiplano boliviano. En: Memoria III Congreso Mundial sobre Camélidos. Potosí, Bolivia. p 479-483. [ Links ]
16. CifuniGF,Napolitano F,RiviezziAM, Braghieri A, Girolami A. 2004. Fatty acid profile, cholesterol content and tenderness of meat from Podolian young Bulls. Meat Sci 67: 289-297. [ Links ]
17. Coates W, Ayerza R. 2004. Fatty acid composition of llama muscle and internal fat in twoArgentinian herds. Small Rum Res 52: 231-238. [ Links ]
18. Condori G, Ayala C, Renieri C, Rodríguez T, Martínez Z. 2003a. Evaluación química de la carne de llama en diferentes periodos del crecimiento. En: Memoria III Congreso Mundial sobre Camélidos. Potosí, Bolivia. p 597-603. [ Links ]
19. Condori G, Ayala C, Renieri C, Rodríguez T, Martínez Z. 2003b. Evaluación biométrica de llama macho en crecimiento. En: Memoria III Congreso Mundial sobre Camélidos. Potosí, Bolivia. p 611-617. [ Links ]
20. Costa RG, Malveira AS, de Azevedo PS, Ramos do Egypto RC, Madruga MS, de Araújo JT. 2009. Lipid profile of lamb meat from different genotypes submitted to diets with different energy levels. R Bras Zootec 38: 532-538. [ Links ]
21. Cristofanelli S, Antonini A, Torres D, Polidori P, Renieri C. 2004. Meat and carcass quality from Peruvian llama (Lama glama) and alpaca (Lama pacos). Meat Sci 66: 589-593. [ Links ]
22. Cristofanelli S, Antonini A, Torres D, Polidori P, Renieri C. 2005. Carcass characteristics of Peruvian llama (Lama glama) and alpaca (Lama pacos) reared intheAndeanhighlands. SmallRumRes 58: 219-222. [ Links ]
23. Dalle Zotte A, Szendro Z. 2011. The role of rabbit meat as functional food. Livestock Sci 127: 176-182. [ Links ]
24. Dawood A, Alkanhal MA. 1995. Nutrient composition of Najdi-camel meat. Meat Sci 39: 71-78. [ Links ]
25. Demirel G, Ozpinar H, Nazli B, Keser O. 2006. Fatty acids of lamb meat from two breeds fed different forage: concentrate ratio. Meat Sci 72: 229-235. [ Links ]
26. Descalzo AM, Sancho AM. 2008. A review of natural antioxidants and their effects on oxidative status, odor and quality of fresh beef produced in Argentina. Meat Sci 79: 423-436. [ Links ]
27. Dierking RM, Kallenbach RL, Grün IU. 2010. Effect of forage species on fatty acid content and performance of pasture finished steers. Meat Sci 85: 597-605. [ Links ]
28. Duckett SK, Neel JPS, Sonon RN, Fontenot Jr JP, Clapham WM, Scaglia G. 2007. Effects of winter stocker growth rate and finishing system on: II. Ninth-tenth-eleventh-rib composition, muscle color and palatability. J Anim Sci 85: 2691-2698. [ Links ]
29. Duckett SK, Neel JPS, Fontenot JP, Clapham WM. 2009. Effects of winter stocker growth rate and finishing system on: III. Tissue proximate, fatty acid, vitamin, and cholesterol content. J Anim Sci 87: 2961-2970. [ Links ]
30. FAO. 2005. Situación actual de los camélidos sudamericanos en Bolivia. TCP/RLA/2914. Roma, Italia. 56 p. [ Links ]
31. Faustman C, Chan WKM, Schaefer DM, Havens A. 1998. Beef color update: the role of vitamin E. J Anim Sci 76: 1019-1026. [ Links ]
32. Franco J. 2009. Importancia de los factores productivos, tecnológicos y de manejo en la calidad de la canal y de la carne vacuna. En: Bianchi G, Feed O (ed). Franco D, González L, Bispo E, Rodríguez P, Garabal JI, Moreno T. 2010. Study of hydrolyzed protein composition, free amino acid, and taurine content in different muscles of Galician blonde beef. J Muscle Foods 21: 769-784. [ Links ]
33. Franco D, González L, Bispo E, Rodríguez P, Garabal JI, Moreno T. 2010. Study of hydrolyzed protein composition, free amino acid, and taurine content in different muscles of Galician blonde beef. J Muscle Foods 21: 769-784. [ Links ]
34. Gallo C. 2010. La calidad de las canales y su carne. Informativo sobre carne y productos cárneos. Facultad de CienciasVeterinarias, UniversidadAustralde Chile. N.° 39. 74 p. [ Links ]
35. García CA. 1995. Contribución al conocimiento del consumo de carne de camélidos sudamericanos (CSA) en Chile. Memoria de título. Valdivia, Chile: Escuela de Medicina Veterinaria, Universidad Austral de Chile. 72 p. [ Links ]
36. García W, San Martín F. 1999. Efecto de cuatro tipos de alimentación sobre la ganancia de peso en llamas de uno y dos años de edad durante el periodo de seca. En: Resúmenes II Congreso Mundial sobre Camélidos. Cuzco, Perú. [ Links ]
37. García WV, San Martín FH, Novoa CM, Franco ELL. 2002. Engorde de llamas bajo diferentes regímenes alimenticios. Rev Inv Vet Perú 13: 1-9. [ Links ]
38. German JB, Dillard CJ. 2004. Saturated fats: What dietary intake? Am J Clin Nutr 80: 550-559. [ Links ]
39. Göncü Karakök S, Ozogul Y, Saler M, Ozogul F. 2010. Proximate analysis. Fatty acid profiles and mineral contents of meats: a comparative study. J Muscle Foods 21: 210-223. [ Links ]
40. Gonzalez F, Smulders FJM, Paulsen P, Skewes O, Konig HE. 2004. Anatomical investigations on meat cuts of guanacos (Lama guanicoe, Muller, 1776) and chemical composition of selected muscles. Wien Tierärztl Monat 91: 77-84. [ Links ]
41. Gutiérrez RLQ. 2003. Engorde de maltones con ensilaje de cebada, triticale y heno de alfalfa. Tesis de grado. Oruro, Bolivia: Facultad de Ciencias Agrícolas y Pecuarias, Universidad Técnica de Oruro. 87 p. [ Links ]
42. HadlichJC,MoralesDC,Silveira AC, Oliveira HNd, Chardulo LAL. 2006. Efeito do colágeno na maciez da carne de bovinos de distintos grupos genéticos. Acta Sci Anim Sci 28: 57-62. [ Links ]
43. Hoffman L. 2008. The yield and nutritional value of meat from African ungulates, camelidae, rodents, ratites and reptiles. Meat Sci 80: 94-100. [ Links ]
44. Hoffman LC, Muller M, Cloete SWP, Schmidt D. 2003. Comparison of six crossbred lamb types: sensory, physical and nutritional meat quality characteristics. Meat Sci 65: 1265-1274. [ Links ]
45. Hood DE, Tarrant PV. 1980. The problem of dark-cutting in beef. The Hague: Martinus Nijhoff. 501 p. [ Links ]
46. [INE] Instituto Nacional de Estadística. 2008. Encuesta Nacional Agropecuaria. Bolivia: INE. p 265-380. [ Links ]
47. Kadim IT, Mahgoub O, Al-Marzooqi W, Al-Zadjali S, Annamalai K, Mansour MH. 2006. Effects of age on composition and quality of muscle Longissimus thoracis of the Omani Arabian camel (Camelus dromedaries). Meat Sci 73: 619-625. [ Links ]
48. Kadim IT, Mahgoub O, Purchas RW. 2008. A review of the growth, and of the carcass and meat quality characteristics of the one-humped camel (Camelus dromedaries). Meat Sci 80: 555-69. [ Links ]
49. King DA, Shackelford SD, Kuehn LA, Kemp CM, Rodriguez AB, Thallman RM, Wheeler TL. 2010. Contribution of genetic influences to animal-to-animal variation in myoglobin content and beef lean color stability. J Anim Sci 88: 11601167. [ Links ]
50. Koohmaraie M, Kent PM, Shackelford SD, Veiseth E, Wheeler TL. 2002. Meat tenderness and muscle growth: is thereany relationship? Meat Sci 62: 345-352. [ Links ]
51. Laura L. 2012. Alternativas de agregación de valor con la transformación de productos derivados de carne de llama (Lama glama) en la localidad de Curahuara de Carangas, Oruro. Tesis de grado. La Paz, Bolivia: Facultad de Ingeniería Agronómica, Universidad Mayor de San Andrés. 157 p. [ Links ]
52. Lawrie RA, Ledward DA. 2006. Lawries meat science. 7th ed. Cambridge, England:Woodhead Publishing. 464 p. [ Links ]
53. Lee JH, Kannan G, Eega KR, Kouakou B, Getz WR. 2008. Nutritional and quality characteristics of meat from goats and lambs finished under identical dietary regime. Small Rum Res 74: 255-259. [ Links ]
54. Lepetit J. 2007. A theoretical approach of the relationships between collagen content, collagen cross-links and meat tenderness. Meat Sci 76: 147-159. [ Links ]
55. Madruga MS, Lacerda de Medeiros EJ, Hauss de Sousa W, Gomes MG, Pereira JM, Ramos do Egypto Queiroga RC. 2009. Chemical composition and fat profile of meat from crossbred goats reared under feedlot systems. R Bras Zootec 38: 547-552. [ Links ]
56. Maggioni D, Marques JA, Rotta PP, Perotto D, Ducatti T, Visentainer JV, do Prado IN. 2010. Animal performance and meat quality of crossbred young bulls. Livest Sci 127: 176-182. [ Links ]
57. Mamani-Linares LW, Gallo CB. 2013a. Meat quality attributes of the Longissimus lumborum muscle of the Khara genotype of llama (Lama glama) reared extensively in northern Chile. Meat Sci 94: 89-94. [ Links ]
58. Mamani-Linares LW, Gallo CB. 2013b. Effects of supplementary feeding on carcass and meat quality traits of young llamas (Lama glama). Small Rumin Res 114: 233-239. [ Links ]
59. Mamani-Linares LW, Gallo CB. 2014. Meat quality, proximate composition and muscle fatty acid profile of young llamas (Lama glama) supplemented with hay or concentrate during the dry season. Meat Sci 96: 394-399. [ Links ]
60. Mamani-Linares LW, Cayo F, Gallo CB. 2013a. Calidad tecnológica de doce músculos de llama jóvenes (Lama glama) bajo un sistema de crianza extensiva. Rev Inv Vet Perú 24: 168-175. [ Links ]
61. Mamani-Linares LW, Cayo F, Gallo C. 2013b. Efecto de estación del año sobre la composición proximal y perfil de ácidos grasos de carne de llamas en crianza extensiva. Rev Inv Vet Perú 24: 417-424. [ Links ]
62. Mancini RA, Hunt MC. 2005. Current research in meat color. Meat Sci 71: 100-121. [ Links ]
63. Marinova P, Banskalieva V, Alexandrov S, Tzvetkova V, Stanchev H. 2001. Carcass composition and meat quality of kids fed sunflower oil supplemented diet. Small Rum Res 42: 219-227. [ Links ]
64. Monsón F, Sañudo C, Sierra I. 2005. Influence of breed and ageing time on the sensory meat quality and consumer acceptability in intensively reared beef. Meat Sci 71: 471-479. [ Links ]
65. Muchenje V, Dzama K, Chimonyo M, Strydom P, Hugo A, Raats J. 2009. Some biochemical aspects pertaining to beef eating quality and consumer health: a review. Food Chem 112: 279-289. [ Links ]
66. Muir PD, Wallace GJ, Dobbie PM, Bown MD. 2000. A comparison of animal performance and carcass and meat quality characteristics in Hereford, Hereford x Friesian, and Friesian steers grazed together at pasture. New Zeal J Agric Res 43: 193-205. [ Links ]
67. Orellana C, Peña F, García A, Perez J, Martos J, Domenech V, Acero R. 2009. Carcass characteristics, fatty acid composition, and meat quality of Criollo Argentino and Braford steers raised on forage in a semi-tropical region of Argentina. Meat Sci 81: 57-64. [ Links ]
68. Osorio MT, Zumalacárregui JM, Alaiz-Rodríguez R, Guzman-Martínez R, Engelsen SB, Mateo J. 2009. Differentiation of perirenal and omental fat quality of suckling lambs according to the rearing system from Fourier transforms mid-infrared spectra using partial least squares and artificial neural networks análisis. Meat Sci 83: 140-147. [ Links ]
69. Pérez P, Maino M, Guzman R, Vaquero C, Kobrich C, Pokniak J. 2000. Carcass characteristics of llamas (Lama glama) reared in central Chile. Small Rum Res 37: 93-97. [ Links ]
70. Polidori P, Antonini M, Torres D, Beghelli D, Renieri C. 2007b. Tenderness evaluation and minerals levels of llama (Lama glama) and alpaca (Lama pacos) meat. Meat Sci 77: 599-601. [ Links ]
71. Polidori P, Renieri C, Antonini M, Passamonti P, Pucciarelli F. 2007a. Meat fatty acid composition of llama (Lama glama) reared in the Andean highlands. Meat Sci 75: 356-358. [ Links ]
72. Price J, Schweigert B. 1994. Ciencia de la carne y de los productos cárnicos. 2ª ed. Zaragoza, España: Acribia. 592 p. [ Links ]
73. [PRORECA] Proyecto Regional de Camélidos. 2004. Mapeo y análisis competitivo de la cadena productiva de camélidos. La Paz, Bolivia: PRORECA. 56 p. [ Links ]
74. Realini CE, Duckett SK, Brito GW, Dalla Rizza M, De Mattos D. 2004. Effect of pasture vs. concentrate feeding with or without antioxidants on carcass characteristics, fatty acid composition, and quality of Uruguayan beef. Meat Sci 66: 567-577. [ Links ]
75. Rebuffi G, Aguirre D. 1996. Efecto del plano nutricional sobre la ganancia de peso post-destete de llama (Lama glama) en pastoreo. ALLPAKA 5: 21-24. [ Links ]
76. Rhee MS, Wheeler TL, Shackelford SD, Koohmaraie M. 2004. Variation in palatability and biochemical traits within and among eleven beef muscles. J Anim Sci 82: 534-550. [ Links ]
77. [RIRDC] Rural Industries Research and Development Corporation. 2007. Composition of new meats, analyses and nutrient composition of innovative meat industries. Australia: RIRDC Publication N.° 07/036. 51 p. [ Links ]
78. Salvá BK, Zumalacárregui JM, Figueira AC, Osorio MT, Mateo J. 2009. Nutrient composition and technological quality of meat from alpacas reared in Peru. Meat Sci 82: 450- 455. [ Links ]
79. Sequeiros LM. 2007. Alimentación y nutrición de camélidos. En: Cardozo GA (ed). Camélidos. Cochabamba, Bolivia: Poligraf. p 309-322. 80. Serra X, Guerrero L, Guardia M, Gil M, Sañudo C, Panea B. 2008. Eating quality of young bulls from three Spanish beef breed-production systems and its relationships with chemical and instrumental meat quality. Meat Sci 79: 98-104. [ Links ]
81. Schmid A, Collomb M, Sieber R, Bee G. 2006. Conjugated linoleic acid in meat and meat products: a review. Meat Sci 73: 29-41. [ Links ]
82. Simopoulos A. 1999. Essential fatty acids in health and chronic disease. Am J Clin Nutr 70: 560-569. [ Links ]
83. Sumar J. 2010. Nutrition in camelids. En: Wittwer F, et al. (eds). Updates on ruminant production and medicine. XXVI World Buiatric Congress. Santiago, Chile. p 343-357. [ Links ]
84. Tarrant PV, Grandin T. 1993. Cattle transport. En: Livestock handling and transport. UK: CAB Internat. p 109-126. [ Links ]
85. Torrescano G, Sánchez-Escalante A, Giménez B, Roncalés P, Beltrán J. 2003. Shear values of raw samples of 14 bovine muscles and their relation to muscle collagen characteristics. Meat Sci 64: 85-91. [ Links ]
86. Tschirhart-Hoelscher TE, Baird BE, King DA, McKenna DR, Savell JW. 2006. Physical, chemical, and histological characteristics of 18 lamb muscles. Meat Sci 73: 48-54. [ Links ]
87. Turín C. 1999. Influencia de la alimentación con pastos naturales y cultivados en alpacas tuis Huacaya de 6 y 18 meses de edad. Tesis de Ingeniero Zootecnista. Lima: Facultad de Zootecnia, Universidad Nacional Agraria La Molina. 110 p. [ Links ]
88. [UNEPCA] Unidad Ejecutora del Proyecto de Desarrollo de Criadores de Camélidos en el Altiplano Andino. 1999. Censo nacional de llamas y alpacas. Bolivia: FIDA, CAF, FDC, UNEPCA. 174 p. [ Links ]
89. [USDA] United States Department of Agriculture. 2008. National nutrient database for standard reference. Release 21. [Internet]. Disponible en: http://www.ars.usda.gov/ba/bhnrc/ndl [ Links ]
90. [VALE] Valorización de la Economía Campesina. 2013. Informe de admisión de la VI feria nacional de camélidos. Potosí, Bolivia: VALE. 48 p. [ Links ]
91. Vera R. 2008. Medidas biométricas in vivo de llamas Khara según: tipo de pradera en la cual fueron criados, sexo y categoría de edad en el municipio de Santiago de Machaca, La Paz-Bolivia. Tesis de grado. La Paz, Bolivia: Universidad Católica Boliviana. 172 p. [ Links ]
92. Webb EC, Casey NH, Simela L. 2005. Goat meat quality. Small Rum Res 60: 153-166. [ Links ]
93. Weston AR, Rogers RW, Althen TG. 2002. Review: The role of collagen in meat tenderness. Prof Anim Scientist 18: 107-111. [ Links ]
94. Wood JD, Enser M, Fisher AV, Nute GR, Sheard PR, Richardson RI. 2008. Fat deposition, fatty acid composition and meat quality: a review. Meat Sci 78: 343- 358. [ Links ]
95. Wurzinger MT, Delgado J, Nqrnberg M, Valle Zárate A, Stemmer A, Ugarte G, Sflkner J. 2005. Growth curves and genetic parameters for growth traits in Bolivian llamas. Livest Prod Sci 95: 73-81. [ Links ]
96. Yáñez EA, Resende KT, Ferreira ACD. 2004. Utilização de medidas biométricas para predizer características cabritos Saanen. Rev Bras Zoot 33: 1564-1572. [ Links ]
97. Zhang SX, Farouk MM, Young OA, Wieliczko KJ, Podmore C. 2005. Functional stability of frozen normal and high pH beef. Meat Sci 69: 765-772. [ Links ]
98. Zenteno LlM. 2003. Complemento al pastoreo con henos de cebada (Hordeum vulgare), alfalfa (Medicago sativa) en ancutas. Tesis de grado Oruro, Bolivia: Facultad de Ciencias Agrícolas y Pecuarias, Universidad Técnica de Oruro. 182 p. [ Links ]
Recibido: 1 de octubre de 2013
Aceptado para publicación: 22 de diciembre de 2013