Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Anales de la Facultad de Medicina
versão impressa ISSN 1025-5583
An. Fac. med. v.69 n.3 Lima set. 2008
Efectos de inhibidores de colinesterasa en pacientes con enfermedad asociada a cuerpos de Lewy
Cholinesterase inhibitors effects in patients with Lewy's bodies associated disease
Nilton Custodio1,4, Rosa Montesinos1,3, Liliana Bendezú1,2, Patricia Cortijo1,2, Hernando Torres1,4, Juan Escobar1,5
1 Unidad de Diagnóstico de Deterioro Cognitivo y Prevención de Demencia, Clínica Internacional. Lima, Perú.
2 Departamento de Neurología, Hospital Militar Central. Lima, Perú
3 Departamento de Medicina Física y Rehabilitación, Clínica Internacional. Lima, Perú.
4 Unidad de Investigación. Clínica Internacional. Lima, Perú.
5 Facultad de Medicina Humana, Universidad Nacional Mayor de San Marcos. Lima, Perú.
Resumen
Objetivos: Analizar los efectos de los inhibidores de colinesterasas (ICE) donepezilo, rivastigmina y galantamina en el tratamiento de demencia con cuerpos de Lewy (DCL) y demencia de la enfermedad de Parkinson (DEP). Diseño: Estudio tipo ensayo abierto. Lugar: Servicio de Neurología, Hospital Militar Central (HMC), y Unidad de Diagnóstico de Deterioro Cognitivo y Prevención de Demencia, Clínica Internacional. Participantes: Pacientes con demencia asociada a cuerpos de Lewy y demencia de la enfermedad de Parkinson. Intervenciones: Las mediciones de eficacia en 33 pacientes con diagnóstico de DCL y DEP se realizó con el Mini-Mental State Examination (MMSE), Alzheimer Disease Assessment Scale cognitive subscale (ADAS-cog), Alzheimers Disease Cooperative Study-Clinical Global Impression of Change (ADCS-CGIC), Alzheimers Disease Cooperative Study-Activities of Daily Living Inventory (ADCS-ADL), Neuro-Psychiatry Inventory (NPI), Prueba de dibujo de Reloj de Manos (PDR-M) y la Unified Parkinson´s Disease Rating Scale-motor subscale (UPDRS-part III). Principales medidas de resultados: Síntomas cognitivos, funcionamiento global y actividades de vida diaria de los pacientes. Resultados: Diecisiete pacientes fueron tratados con rivastigmina, 9 con galantamina y 7 con donepezilo. Luego de 6 meses de tratamiento, los pacientes en tratamiento con rivastigmina mejoraron en 1,39 puntos en ADAS-cog respecto de su medición basal, mientras que los pacientes tratados con donepezilo y galantamina no mostraron cambios (cambios <0,2 puntos). Respecto al ADCS-ADL, los pacientes tratados con rivastigmina, donepezilo y galantamina demostraron disminución de 0,42, 0,58 y 0,75 puntos, respectivamente. En el MMSE, los pacientes tratados con rivastigmina y donepezilo no mostraron cambios y los pacientes tratados con galantamina tuvieron una disminución promedio de 1,19 puntos. No hubo diferencias significativas en la incidencia de síntomas parkinsonianos en los tres grupos de tratamiento. Los eventos adversos fueron similares en los tres grupos de tratamiento. Conclusiones: Los inhibidores de colinesterasa pueden ser benéficos en el manejo de síntomas cognitivos, el funcionamiento global y actividades de vida diaria en pacientes con demencia con cuerpos de Lewy y demencia de la enfermedad de Parkinson.
Palabras clave: Enfermedad de Parkinson; demencia con cuerpos de Lewy; inhibidores de colinesterasa; demencia; terapia.
Abstract
Objectives: To analyze the effects of cholinesterase inhibitors (CHEIs) prescribed for treatment of dementia with Lewy bodies (DLB) and dementia associated with Parkinsons disease (PDD). Design: Open essay study. Setting: Neurology Service, Hospital Militar Central, and Cognitive Deterioration Diagnosis Unit and Dementia Prevention, Clinica Internacional. Participants: Patients with dementia associated to Lewy bodies and dementia associated with Parkinsons disease. Interventions: Outcome measures included the Mini-Mental State Examination (MMSE), the Alzheimer Disease Assessment Scale cognitive subscale (ADAS-cog), Alzheimers Disease Cooperative Study-Clinical Global Impression of Change (ADCS-CGIC), Alzheimers Disease Cooperative Study-Activities of Daily Living Inventory (ADCS-ADL), Neuro-Psychiatry Inventory (NPI), Ten Point Clock-Drawing Test (CDT) and Unified Parkinson´s Disease Rating Scale-motor subscale (UPDRS-part III). Main outcome measures: Patients cognitive symptoms, global function and daily life activities. Results: Seventeen patients were treated with rivastigmine, nine with galantamine and seven with donepezil. At six months, rivastigmine-treated patients improved by 1,39 points from baseline on the ADAS-cog, while donepezil and galantamine treated patients showed no change (changes of <0,2 points). On the ADCS-ADL, patients treated with rivastigmine, donepezil and galantamine showed decreases of 0,41, 0,68 and 0,86 points, respectively. On the MMSE, donepezil and rivastigmine-treated patients showed no change and galantamine-treated patients showed a mean decrease of 1,19 points. The difference with regard to the incidence of parkinsonian symptoms as adverse events was not reflected in significant differences in UPDRS motor scores between the three groups. Side effects were similar in the three treatment groups. Conclusions: Cholinesterase inhibitors may be of benefit for cognitive impairments with impact on global function and activities of daily living in patients with dementia with Lewy bodies and dementia associated with Parkinsons disease.
Key words: Parkinson disease; Lewy body disease; cholinesterase inhibitors; dementia; therapy.
INTRODUCCIÓN
La demencia con cuerpos de Lewy (DCL) representa la segunda causa de demencia degenerativa después de la enfermedad de Alzheimer (EA) (1,2). De hecho, estudios realizados en comunidad en personas mayores de 85 años han encontrado que el 5% reunió los criterios del Consorcio para DCL, representando 22% de todos los casos de demencia (3). Por otro lado, los pacientes con enfermedad de Parkinson (EP) tienen un riesgo incrementado de desarrollar demencia, la cual se denomina demencia de la enfermedad de Parkinson (DEP), según lo demuestran grandes estudios europeos basados en comunidad (4). En una revisión sistemática de estudios de prevalencia de DEP, 24 a 31% de pacientes tienen demencia y 3 a 4% de la carga de demencia en la población es debida a DEP (5); y más del 75% de pacientes con EP desarrolla demencia después de los 10 años de iniciado los síntomas motores (6). Pero, en la práctica clínica diaria resulta difícil diferenciar DEP de DCL, pues, no existen criterios de consenso para DEP. Los criterios del consorcio para DCL, en 1996 (7), distinguieron DEP de DCL, no sobre la base de alguna característica clínica o patológica en particular, sino sobre la base de la regla arbitraria del año; es decir, los pacientes con menos de un año de parkinsonismo previo a la demencia son catalogados como DCL, mientras que los pacientes con duración del parkinsonismo mayor a un año antes del desarrollo de la demencia son diagnosticados como DEP; este criterio aún es recomendado por el tercer reporte del Consorcio (8). En el balance, la evidencia concerniente a síntomas motores y síntomas cognitivos asociados a DEP y DCL respalda el consenso creciente que estos desórdenes son más similares que diferentes, y que la distinción entre ellas es artificial (9). Los investigadores más críticos dicen que no se las puede separar como dos entidades distintas, y plantean que ambas (DEP y DCL) reflejarían un espectro único de dos enfermedades que se presentan con fenotipos diferentes (se ha planteado, que el continuum sería EP-DEP-DCL), pero que tienen la misma explicación molecular: los cuerpos de Lewy y la alfa-sinucleina. Por lo tanto, es válido, para evitarse problemas, denominarlas como Enfermedad por cuerpos de Lewy (9,10).
La marcada deficiencia colinérgica en pacientes con DEP y DCL sugieren la eficacia de los inhibidores de colinesterasas (ICE) en estas dos entidades nosológicas y es posible que el efecto benéfico sea mayor que lo observado en los pacientes con EA, para quienes ellos fueron originalmente desarrollados (11). Los ICE pueden ser beneficiosos para el compromiso cognitivo fluctuante, sobre todo en el impacto sobre el funcionamiento global y actividades de vida diaria (8,11-13). El tamaño del efecto es comunicado como mayor en pacientes con DCL, que el observado cuando se los emplea para pacientes con EA (14). Las guías de la Academia Americana de Neurología (12) concluyen, luego de una revisión sistemática de la literatura publicada hasta diciembre de 2004, que donepezilo o rivastigmina deben ser considerados en el manejo de pacientes con DEP (Recomendación nivel B) y rivastigmina, en el tratamiento de pacientes con DCL (Recomendación nivel B). Por otro lado, una revisión Cochrane acerca de la eficacia, seguridad, tolerabilidad y aspectos fármaco-económicos de los ICE en la DEP, concluye que rivastigmina mejora la cognición y actividades de vida diaria, resultando en beneficio clínicamente significativo en cerca de 15% de los casos (15).
Con la finalidad de evaluar los beneficios comparativos de rivastigmina, donepezilo y galantamina, se realizó un estudio abierto para verificar su eficacia y seguridad tras 6 meses de tratamiento, en un grupo de pacientes con DCL y DEP reclutados del servicio de neurología del Hospital Militar Central y de la Unidad de Diagnóstico de Deterioro Cognitivo y Prevención de Demencia de la Clínica Internacional, en Lima, Perú.
MÉTODOS
El presente estudio fue diseñado como un ensayo abierto para ser llevado a cabo en el Servicio de Neurología del Hospital Militar Central (HMC) y en la Unidad de Diagnóstico de Deterioro Cognitivo y Prevención de Demencia de la Clínica Internacional (CI), en pacientes con demencia asociada a cuerpos de Lewy: DCL y DEP. Se inició en el año 2003, en el Hospital Militar Central, y en el año 2005, en la Clínica Internacional. Previo al inicio del estudio, se obtuvo la aprobación de los comités de ética de cada institución, para conducir investigaciones clínicas en sujetos humanos.
Los pacientes que aceptaron ingresar al estudio y cumplieron los criterios de inclusión fueron registrados después de la evaluación basal y recibieron, según la disponibilidad del centro de investigación, rivastigmina, donepezilo o galantamina. La seguridad y eficacia fueron evaluadas a las semanas 16, 24, 30, 36, 42 y 48. En esta publicación se comunica los resultados del tratamiento hasta los 6 meses.
Los criterios de inclusión para pacientes con DEP fueron: individuos con reciente diagnóstico, de sexo masculino o femenino, mayores de 50 años de edad, quienes habían sido diagnosticados con enfermedad de Parkinson, de acuerdo a los criterios clínicos de la United Kingdom Parkinsons Disease Society Brain Bank (16), y un diagnóstico de demencia basado en los criterios de la cuarta edición del Diagnostic and Statistical Manual of Mental Disorders (código 294.1) (17), con un inicio de los síntomas cognitivos dos años después del diagnóstico de EP. Los criterios de inclusión para pacientes con DCL incluyeron, además, las guías de consenso para DCL probable (7). Los pacientes tenían demencia leve a moderadamente severa, según los puntajes alcanzados en el Mini-Mental State Examination (MMSE) (18), entre 10 y 24. Además, los pacientes requerían de la presencia de un cuidador, con permanencia en la vivienda del paciente de por lo menos 3 días por semana. Los criterios de exclusión fueron la presencia de algún otro desorden neurodegenerativo primario diferente a la EP, otras causas de demencia (metabólica, traumática, medicamentosa o infecciosa), presencia de una enfermedad cardiaca, pulmonar, renal o hepática de grado severo e inestable, hipersensibilidad conocida a medicamentos similares a los ICE, el uso previo de algún ICE o Memantina. El tratamiento de los síntomas motores y conductuales fueron iniciados o ajustados según la evaluación clínica de los neurólogos del estudio.
Los pacientes diagnosticados del Hospital Militar Central fueron asignados solo al grupo de rivastigmina, debido a que, desde mediados de 1999, en el Hospital Militar Central se dispone de rivastigmina y, hasta la finalización del estudio, era el único ICE aceptado por el petitorio farmacológico institucional del ejército peruano.
La elección del tratamiento de los pacientes de la Unidad de Diagnóstico de Deterioro Cognitivo y Prevención de Demencia de la Clínica Internacional fue pseudo-aleatorizada basados en el orden de ingreso a la Unidad, en la siguiente secuencia: rivastigmina, donepezilo y galantamina. El protocolo farmacológico para la administración de los ICE fue el siguiente:
1. Un periodo de titulación, que se inició con una cápsula de rivastigmina de 1,5 mg, BID, por 4 semanas, seguido de 1 cápsula de rivastigmina de 3 mg, BID, por otras 4 semanas. Según el nivel de tolerancia, a partir del tercer mes los pacientes del HMC recibieron 1 cápsula de rivastigmina de 3 mg, TID, por 4 semanas, mientras que los pacientes de la CI recibieron 1 cápsula de 4,5 mg, BID, por el mismo tiempo; luego, todos los pacientes recibieron 1 cápsula de 6 mg, BID, como tratamiento de mantenimiento.
2. Una cápsula de galantamina de 4 mg, BID, por 4 semanas, seguida de una cápsula de 8 mg, BID, como tratamiento de mantenimiento. A partir del año 2007, con la introducción al mercado peruano de galantamina ER, los pacientes de la CI, recibieron 1 cápsula de galantamina ER de 8 mg, QD, por 4 semanas, y luego 1 cápsula de galantamina ER de 16 mg, QD, como terapia de mantenimiento.
3. Una tableta de donepezilo de 5 mg, QD, por 4 semanas, seguido por una tableta de donepezilo de 10 mg, QD, como terapia de mantenimiento.
Las evaluaciones de eficacia fueron realizadas en el basal y luego en las semanas 16 y 24. Para evaluar los cambios cognitivos, se llevaron a cabo MMSE (18), el Alzheimer Disease Assessment Scale cognitive subscale (ADAS-cog) (19) y, para las funciones de atención, planeamiento, programación motora y ejecución, la prueba del dibujo del reloj- versión Manos (20). Para evaluar los cambios globales, realizamos el Alzheimers Disease Cooperative Study-Clinical Global Impression of Change (ADCS-CGIC) (21). Para evaluar la funcionalidad realizamos el Alzheimers Disease Cooperative Study-Activities of Daily Living Inventory (ADCS-ADL) (22) y para los cambios conductuales realizamos el Neuro-Psychiatry Inventory (NPI) (23). El MMSE es una evaluación aproximada de la función cognitiva, con puntajes de 0 a 30 puntos, siendo los menores puntajes correspondientes a peor compromiso cognitivo. La porción cognitiva del ADAS (ADAS-cog) (19) evalúa orientación, memoria, lenguaje, funciones viso-espaciales y praxis. Los puntajes van del 0 al 70, siendo los puntajes más elevados para el compromiso más severo. La PDR-M evalúa la capacidad del individuo para poner sobre un círculo dibujado los números del 1 al 12, tal como van en un reloj, y luego evalúa la dirección y proporcionalidad de las manecillas del reloj al intentar plasmar las 11:10 horas. El puntaje máximo es 10, siendo los puntajes más bajos para los pacientes con compromiso más severo. El ADCS-CGIC (21) es una escala categórica de 7 puntos que nos proporciona una evaluación global del cambio comparado desde el basal. Un puntaje de 1 indica mejoría marcada; un puntaje de 2, mejoría moderada; un puntaje de 3, mejoría mínima; un puntaje de 4, sin cambios; un puntaje de 5, empeoramiento mínimo; un puntaje de 6, empeoramiento moderado; y, un puntaje de 7, empeoramiento marcado. Los cambios mínimos están predefinidos como cambios clínicamente detectables que no afectan el estado clínico del paciente; los cambios moderados revelan cambios detectables que tienen un efecto correspondiente con el estado clínico; y cambios marcados indican un efecto dramático sobre el estado clínico del paciente. El ADCS-ADL (22) tiene puntajes de 0 a 78 puntos, siendo los mayores puntajes para un mejor funcionamiento. El NPI (23) evalúa delusiones, alucinaciones, agitación, depresión, ansiedad, euforia, apatía, desinhibición, irritabilidad y conducta motora aberrante; obtiene puntajes de 0 a 144, siendo los puntajes más altos en tanto los síntomas conductuales fueran más severos y frecuentes.
Las evaluaciones de seguridad incluyeron los registros de signos vitales, del peso corporal y de todos los eventos adversos, exámenes de laboratorio para funcionamiento hepático, renal y metabólico. Los cambios en los síntomas motores del parkinsonismo fueron evaluados a nivel basal y en las semanas 16 y 24, a través de la Unified Parkinson's Disease Rating Scale-motor subscale (UPDRS-part III) (24), obteniendo puntajes de 0 a 108 puntos, siendo que los puntajes mayores indican síntomas motores más severos.
Las variables de eficacia fueron analizadas por medio del análisis de covarianza, teniendo a los grupos de tratamiento y las mediciones basales correspondientes usadas como covariables. La frecuencia de eventos adversos fue analizada entre los grupos de tratamiento por medio de la prueba exacta de Fisher. Los valores establecidos como significativos para p fueron menos de 0,05.
RESULTADOS
De los 36 pacientes seleccionados inicialmente, tres fueron excluidos del análisis de eficacia: uno, retirado prematuramente del estudio antes de la primera evaluación, que correspondió al grupo de pacientes que recibieron donepezilo, pues en el inicio de la semana 5, cuando se incrementó la dosis a 10 mg diarios, se exacerbaron los síntomas conductuales; y los otros dos fueron retirados, debido a que la evaluación de las 24 semanas fue realizada con un retraso mayor de 2 semanas (un paciente estaba recibiendo donepezilo y el otro, galantamina).
Dado que la asignación de pacientes en el Hospital Militar Central fue solo para el grupo de rivastigmina, la población final a analizar fue heterogénea. El Hospital Militar Central aportó nueve pacientes a la investigación (todos en el grupo de rivastigmina: 6 con diagnóstico de DEP y 3 con DCL) y la Clínica Internacional contribuyó con 24 pacientes (8 pacientes en el grupo rivastigmina: 5 con diagnóstico de DEP y 3 con DCL; 7 en el grupo donepezilo: 4 con diagnóstico de DEP y 3 con DCL; y 9 en el grupo galantamina: 6 con diagnóstico de DEP y 3 con DCL).
Treinta y tres pacientes cumplieron los requisitos para el análisis de eficacia, de los cuales 22 fueron de sexo masculino y 11 de sexo femenino (edad media ± DS: 73,8 ± 7,8; rango: 67 a 91 años) (Tabla 1). Veintiún pacientes tuvieron el diagnóstico de DEP (14 de sexo masculino y 7 de sexo femenino) y 12 pacientes con diagnóstico de DCL (8 de sexo masculino y 4 de sexo femenino). El promedio de años de educación en esta muestra fue de 8,8 ± 4,1 (media ± DS). La mayoría de pacientes (30 de 33; 90,9%) fueron portadores de enfermedades médicas coexistentes, siendo las más frecuentes hipertensión arterial, diabetes mellitus e hipotensión ortostática. El tiempo promedio de diagnóstico de enfermedad de Parkinson fue 7,1 años en los pacientes con DEP, mientras que el tiempo de diagnóstico de DCL fue 18,3 ± 9,1 meses. El UPDRS motor promedio fue 27,9 ± 3,1.
Basados en la evaluación del MMSE (16,4 ± 3,0) y ADAS-cog (24,3 ± 10,9), la muestra estudiada tuvo un grado de demencia moderada (Tabla 1), teniendo en cuenta que las puntuaciones de MMSE de 20 a 24 consideran demencia leve, de 10-19, demencia moderada, y puntuaciones menores de 10, demencia severa (18); mientras tanto, las puntuaciones en ADAS-cog de 10 a 15 consideran demencia muy leve, de 16 a 20, demencia leve, de 21 a 30, demencia moderada, de 31 a 45, demencia moderadamente severa, y puntuaciones mayores de 45, demencia severa (19).
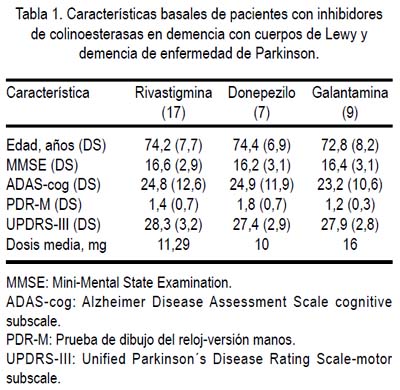
La dosis promedio de rivastigmina por día al final de la fase de titulación fue de 11,29 mg y permaneció estable durante la fase de mantenimiento. Al final de los 6 meses, 14 pacientes (82,4%) estaban recibiendo 12 mg/día, mientras que 2 pacientes (11,8%) recibían 9 mg/día y un paciente (5,8%) recibía 6 mg/día. El 100% de los pacientes del grupo de donepezilo y galantamina recibió la dosis optima recomendada (10 y 16 mg/día, respectivamente).
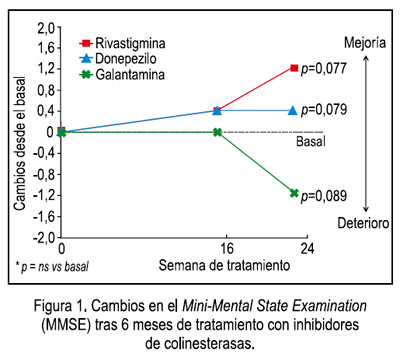
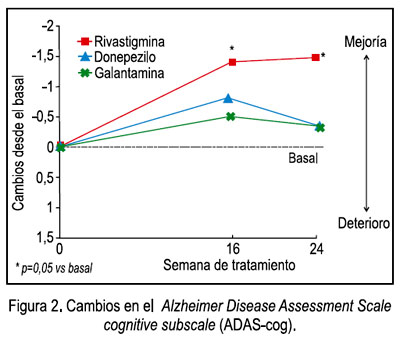
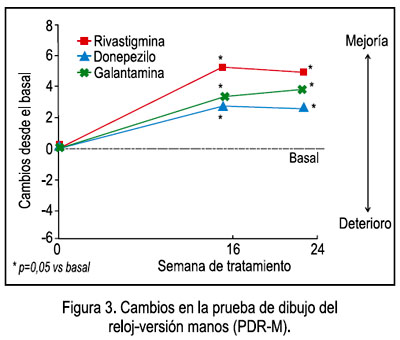
Tras 6 meses de tratamiento, los ICE consiguieron estabilizar las habilidades cognitivas, con una tendencia a mejorar, respecto del basal. La evaluación del MMSE no muestra cambios estadísticos significativos respecto del basal, a pesar de una ligera mejoría en el grupo de pacientes con rivastigmina y donepezilo; sin embargo, con galantamina se observa una disminución de 1,19 puntos, sin alcanzar significancia estadística (p = 0,089) (Figura 1). En cuanto a la evaluación del ADAS-cog, tras 6 meses de tratamiento, los pacientes con rivastigmina mejoraron 1,39 puntos (p < 0,05 vs. basal), mientras que los pacientes con donepezilo y galantamina mostraron mejorías menores a 0,2 puntos, respecto del basal (Figura 2). Se observa también que, a las 16 semanas, solo rivastigmina alcanzó una significancia estadística, al mejorar en 1,35 puntos sobre el basal (p < 0,05), mientras que donepezilo y galantamina alcanzaron una mejoría entre 0,4 y 0,8 puntos (diferencia no significativa respecto del basal). La evaluación de las variaciones de la PDR-M a las 16 y 24 semanas revela mejoría en los 3 grupos de tratamiento (p < 0,05 vs. basal), sin diferencia significativa entre ellos (Figura 3).
El puntaje promedio para el ADCS-CGIC, a la semana 24, fue 3,8 en el grupo rivastigmina, 3,9 en el grupo donepezilo y 3,8 en el grupo galantamina. El análisis comparativo de los resultados en las siete categorías posibles (mejoría marcada, moderada o mínima; sin cambios; o empeoramiento marcado, moderado o mínimo) muestra que significativamente más pacientes tienen resultados favorables en los tres grupos de tratamiento, pero no hay diferencia significativa entre ellos.
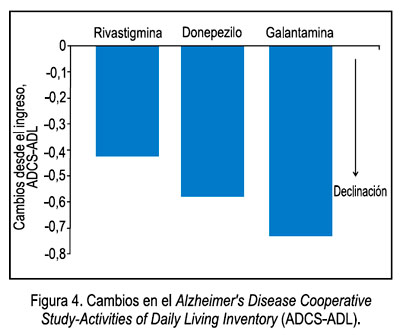
Las variaciones en el ADCS-ADL tras 24 semanas de tratamiento fue de -0,42 ± 0,93 para el grupo bajo tratamiento con rivastigmina, de -0,58 ± 0,80 para el grupo en tratamiento con donepezilo y de -0,75 ± 0,68 para el grupo galantamina (Figura 4), variaciones no significativas entre ellos.
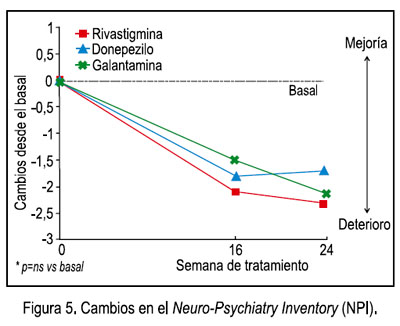
Tras 24 semanas de tratamiento, los puntajes del NPI muestran un deterioro no significativo respecto del basal, de 2,4 ± 0,6 con rivastigmina, de 1,8 ± 0,6 con donepezilo y de 2,1 ± 0,3 con galantamina (Figura 5), sin variaciones significativas entre los tres grupos de tratamiento.
Los eventos adversos predominantes fueron de naturaleza colinérgica, siendo los más frecuentes náuseas, vómitos y baja de peso (Tabla 2), sin encontrar diferencia significativa entre los grupos de tratamiento. La mayoría fueron leves a moderados en intensidad y no significaron el retiro del tratamiento o la rotación hacia otro tipo de ICE. No se registró muertes ni eventos adversos severos, que condicionaran hospitalización.
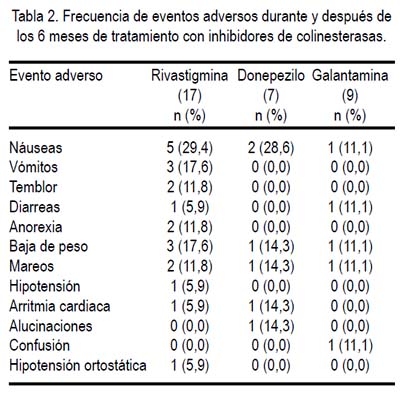
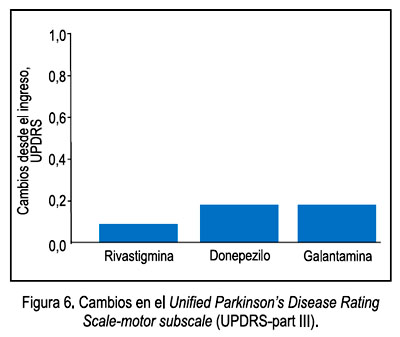
Si bies es cierto se observa que el temblor fue un evento adverso presente en 11,8% de pacientes con rivastigmina, no observado en los otros dos grupos de tratamiento, esto no significó el retiro o disminución de la dosis alcanzada en el momento del inicio del temblor; y además no se observó exacerbación o aparición de otro síntoma parkinsoniano, como bradicinesia o rigidez. En la evaluación del UPDRS, tras las 24 semanas de tratamiento con ICE, las variaciones no son significativas, menores a 0,2, sin encontrar diferencia significativa entre ellos (Figura 6).
El presente estudio no incluye grupo placebo, debido a la probada eficacia de los ICE en la enfermedad de Alzheimer (EA) y demencias relacionadas (25-27). Los ICE alcanzaron una moderada pero significativa mejoría en las tasas cognitivas y globales de demencia, mas no, en las valoraciones conductuales de pacientes con demencia asociada a cuerpos de Lewy. Si bien es cierto no hay diferencia significativa en los grupos de tratamiento, el patrón de los resultados podría indicar una cierta tendencia numérica de mejores resultados con rivastigmina>donepezilo>galantamina, pero se necesita estudios prospectivos y de mayor número de pacientes para confirmar tal sospecha.
La magnitud de los efectos en términos de puntajes para el ADAS-cog, en nuestra población, fueron similares a los habitualmente observados en pacientes con DCL (28) y DEP (29,30), así como en pacientes con EA, que están bajo tratamiento con ICE (31,32), en los cuales se observa que los pacientes que recibieron rivastigmina, más que los pacientes que recibieron donepezilo y galantamina, mostraron mejoría significativa, desde la semana 16 y se mantuvo con una ligera disminución hacia la semana 24, comparado con el placebo (29). No existe algún estudio comparativo directo entre ICE en el tratamiento de pacientes con DCL y DEP en estadio moderado, que respalde nuestros resultados, aunque Touchon y colaboradores (33) han publicado un análisis retrospectivo del estudio EXCEED, que es un estudio aleatorizado que incluye aproximadamente 1 000 pacientes con EA moderada a moderadamente severa, que recibieron tratamiento con donepezilo o rivastigmina por 2 años. Este análisis retrospectivo investigó si los pacientes con EA moderada a moderadamente severa, con y sin síntomas sugestivos de DCL, mostraban diferentes patrones de respuesta al tratamiento. Las mediciones de eficacia fueron la batería de compromiso severo (SIB), MMSE, escala de deterioro global (GDS), NPI y una escala de actividades de la vida diaria (ADCS-ADL). Cuarenta y nueve pacientes con EA y síntomas sugestivos de DCL recibieron tratamiento (25 rivastigmina y 24 donepezilo). En esta sub-población, los cambios desde el basal, después de 2 años de tratamiento con rivastigmina, fueron significativamente mejores que los observados con el grupo donepezilo, en el análisis de SIB, MMSE y ADCS-ADL. Por otro lado, el puntaje total del ADAS-cog resulta de la suma de varias funciones cognitivas, por lo que es difícil asignarle un significado clínico único a un cambio promedio del puntaje total, dado que esto puede representar cambios de diferentes magnitudes en dominios individuales y que varían de paciente a paciente. Pero, lo que sí está muy claro en pacientes con EA es que la declinación de 3 a 4 puntos representa en promedio una progresión en 6 meses en la evolución de la enfermedad (34). En nuestro estudio, se logró con rivastigmina una mejoría promedio de 1,9 puntos en los puntajes de ADAS-cog, siendo la mejoría menor con donepezilo y galantamina. Si bien es cierto, las variaciones cognitivas en el contexto de la evolución natural de la enfermedad no han sido establecidas en pacientes con enfermedad con cuerpos de Lewy, se supone que estas podrían ser de mayor declinación comparados con los pacientes diagnosticados con EA (35). Podemos decir que en esta serie de pacientes se ha logrado estabilizar la enfermedad; pero, dado el corto tiempo de 6 meses de evaluación, no podemos afirmar si estamos en el periodo inicial de estabilización de la enfermedad, la conocida etapa de luna de miel o primavera de los ICE, que habitualmente dura 6 meses y luego se va a producir el deterioro esperado de esta patología neurodegenerativa. Así, entonces, si la mejoría cognitiva obtenida con los ICE en pacientes con demencia asociada a cuerpos de Lewy va a ser mantenida en el largo plazo, no puede ser sostenida con estos resultados.
Respecto a los puntajes obtenidos en ADCS-CGIC, los tres grupos de tratamiento alcanzaron puntajes compatibles con mínima mejoría o sin cambios, teniendo en cuenta que los cambios mínimos están predefinidos como cambios clínicamente detectables que no afectan el estado clínico del paciente. Estos resultados son ligeramente menores a los obtenidos por rivastigmina en la investigación de Emre (29) y colaboradores, en la cual un elevado porcentaje de pacientes en el grupo rivastigmina comparados al placebo tuvo una mejoría moderada a marcada (19,8 % vs. 14,5 %), mientras que menos porcentaje de pacientes tuvo un empeoramiento moderado o marcado (13,0% vs. 23,1%).
El perfil de eventos adversos fue compatible con mecanismos subyacentes de estimulación colinérgica, siendo los más comunes náuseas y vómitos, datos consistentes con los resultados de Emre (29) y Ravina (30) y colaboradores, en pacientes con DEP, y los de Mc Keith (28) y colaboradores en pacientes con DCL y en los pacientes con EA que fueron sometidos a tratamiento con ICE (31,32). Si bien es cierto se observó un incremento en la frecuencia de temblor en los pacientes bajo tratamiento con rivastigmina, este no significó el retiro de la droga del estudio y además no se vieron reflejados en el puntaje total o los puntajes de los ítems individuales del UPDRS Motor, al final de los 6 meses de tratamiento.
Las limitaciones del presente estudio son la pequeña muestra de la población estudiada, el diseño abierto, con muestra no aleatoria, siendo esta ultima la principal limitación, pues puede afectar los resultados del estudio. Pero, el hecho de no seguir un protocolo rígido especifico en esta patología y ser guiados por la experiencia personal, basados en las recomendaciones de las guías diagnosticas y terapéuticas (31,32) sugeridas por la neurología basada en evidencias, puede convertirse en una ventaja del estudio, pues refleja los resultados del tratamiento de pacientes con demencia asociada a cuerpos de Lewy, con los ICE en la práctica clínica diaria; o, mejor dicho, sus resultados en el mundo real. De hecho, necesitamos estudios a gran escala, conducidos en un largo periodo de tiempo, para confirmar si existen diferencias importantes en la eficacia y seguridad a largo plazo de los ICE en pacientes con demencia asociada a cuerpos de Lewy. Es importante señalar, además, que los resultados de esta investigación son observaciones preliminares y no deben ser aceptadas como conclusiones finales. Por último, otra limitación del estudio es la escasa evaluación de las funciones de atención, ejecución y habilidades viso-espaciales, pues solo empleamos PDR-M. Los pacientes con DCL y DEP reflejan el compromiso cortical y subcortical, pero sobre todo el compromiso subcortical expresado en el desorden de atención y disfunción viso-espacial (36,37), que ayuda a diferenciar este desorden de la EA, pues los pacientes con DCL responden mejor que los pacientes con EA a las tareas de memoria verbal; pero, responden peor a las tareas de habilidades viso-espaciales (38). Empleamos la PDR-M porque es de administración fácil y rápida y puede evaluar las siguientes habilidades cognitivas: comprensión auditiva, planeamiento, memoria visual, reconstrucción de una imagen gráfica, habilidades vísuo-espaciales, programación motora y ejecución, conocimiento numérico y concentración.
En conclusión, los ICE resultan en una discreta, pero significativa, mejoría en los síntomas de demencia asociada a cuerpos de Lewy. Los eventos adversos más frecuentes fueron náuseas, vómitos y temblor. Dado que la demencia es un factor pronóstico para discapacidad progresiva y aumento progresivo de la utilización de los servicios hospitalarios y de casas de reposo, nuestros hallazgos pueden tener implicancias en la práctica clínica diaria.
REFERENCIAS BIBLIOGRÁFICAS
1. OBrien JT, Erkinjuntti T, Reisberg B. Vascular cognitive impairment. Lancet Neurol. 2003;2:89-98. [ Links ]
2. McKeith I, Mintzer J, Aarsland D, Burn D, Chiu H, Cohen-Mansfield J. Dementia with Lewy bodies. Lancet Neurol. 2004;3:19-28. [ Links ]
3. Rahkonen T, Eloniemi-Sulkava U, Rissanen S, Vatanen A, Viramo P, Sulkava R. Dementia with Lewy bodies according to the consensus criteria in a general population aged 75 years or older. J Neurol Neurosurg Psychiatry. 2003;74:720-4. [ Links ]
4. De Lau LML, Schipper CMA, Hofman A, Koudstaal PJ, Breteler MMB. Prognosis of Parkinson disease: risk of dementia and mortality: the Rotterdam study. Arch Neurol. 2005;62:1265-9. [ Links ]
5. Aarsland D, Zaccai J, Brayne C. A systematic review of prevalence studies of dementia in Parkinsons disease. Mov Disord. 2005;10:1255-62. [ Links ]
6. Aarsland D, Tandberg E, Larsen JP, Cummings JL. Frequency of dementia in Parkinsons disease. Arch Neurol. 1996;53:538-42. [ Links ]
7. McKeith IG, Galasko D, Kosaka K, Perry EK, Dickson DW, Hansen LA, et al. Review. Consensus guidelines for the clinical pathologic diagnosis of dementia with Lewy bodies (DLB): report of the consortium on (DLB) international workshop. Neurology. 1996;47:1113-24. [ Links ]
8. McKeith IG, Dickson DW, Lowe J, Emre M, OBrien JT, Feldman H, et al. Diagnosis and management of dementia with Lewy bodies: Third report of the DLB Consortium. Neurology. 2005;65:1863-72. [ Links ]
9. McKeith IG, MosimanN UP. Dementia with Lewy bodies and Parkinsons disease. Parkinsonism Relat Disord. 2004;10:S15-S18. [ Links ]
10. Tsuboi Y, Dickson DW. Dementia with Lewy bodies and Parkinsons disease with dementia: Are they different?. Parkinsonism Relat Disord. 2005;11:S47-S51. [ Links ]
11. Burn D. Cortical Lewy body disease and Parkinsons disease dementia. Curr Opin Neurol. 2006;19:572-9. [ Links ]
12. Miyasaki JM, Shannon K, Voon V, Ravina B, Kleiner-Fisman G, Anderson K, et al. Practice parameter: evaluation and treatment of depression, psychosis, and dementia in Parkinson disease (an evidence-based review). Report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology. 2006;66:996-1002. [ Links ]
13. Aarsland D, Mosimann UP, McKeith IG. Role of cholinesterase inhibitors in Parkinsons disease and dementia with Lewy bodies. J Geriatr Psychiatry Neurol. 2004;17:164-71. [ Links ]
14. Samuel W, Caligiuri M, Galasko D, Lacro J, Marini M, McClure FS, et al. Better cognitive and psychopathologic response to donepezil in patients prospectively diagnosed as dementia with Lewy bodies: a preliminary study. Int J Geriatr Psychiatry. 2000;15:794-802. [ Links ]
15. Maidment I, Fox C, Boustani M. Cholinesterase inhibitors for Parkinsons disease dementia. Cochrane Database Syst Rev. 2006;CD004747. [ Links ]
16. Gibb WR, Lees AJ. The relevance of the Lewy body to the pathogenesis of idiopathic Parkinsons disease. J Neurol Neurosurg Psychiatry. 1988;51:745-52. [ Links ]
17. Diagnostic and statistical manual of mental disorders. 4th ed. DMS-IV. Washington, D.C.: American Psychiatric Association; 1994. [ Links ]
18. Folstein MF, Folstein SE, McHugh PR. Mini-mental state. A practical method for grading the cognitive state of patients for the clinician. J Psychiatr Res. 1975;12:189-98. [ Links ]
19. Rosen WG, Mohs RC, Davis KL. A new rating scale for Alzheimers disease. Am J Psychiatry. 1984;141:1356-64. [ Links ]
20. Manos PJ, Wu R. The ten point clock test: a quick screen and grading method for cognitive impairment in medical and surgical patients. Int J Psychiatry Med. 1994;24:229-44. [ Links ]
21. Ferris SH, Mackell JA, Mohs R, Schneider LS, Galasko D, Whitehouse PJ, et al. Validity and reliability of the Alzheimers Disease Cooperative Study-Clinical Global Impression of Change: the Alzheimers Disease Cooperative Study. Alzheimer Dis Assoc Disord. 1997;11(Suppl 2):S22-S32. [ Links ]
22. Galasko D, Bennett D, Sano M, Ernesto C, Thomas R, Grundman M, et al. An inventory to assess activities of daily living for clinical trials in Alzheimers disease: the Alzheimers Disease Cooperative Study. Alzheimer Dis Assoc Disord. 1997;11(Suppl 2):S33-S39. [ Links ]
23. Cummings JL, Mega M, Gray K, Rosenberg-Thompson S, Carusi DA, Gornbein J. The Neuropsychiatric Inventory; Comprehensive assessment of psychopathology in dementia. Neurology. 1994;44:2308-14. [ Links ]
24. Fahn S, Elton RL, Members of the UPDRS Development Committee. Unified Parkinsons disease rating scale. In: Fahn S, Marsden CD, Calne DB, Goldstein M, eds. Recent developments in Parkinsons disease. Florham Park, N.J.: Macmillan Healthcare Information; 1987. p. 153-64. [ Links ]
25. Farlow M, Anand R, Messina J Jr, Hartman R, Veach J. A 52-week study of the efficacy of rivastigmine in patients with mild to moderately severe Alzheimers disease. Eur Neurol. 2000;44:236-41. [ Links ]
26. Raskind MA, Peskind ER, Wessel T, Yuan W. Galantamine in AD: A 6-month randomized, placebo-controlled trial with a 6-month extension. The Galantamine USA-1 Study Group. Neurology. 2000;54:2261-8. [ Links ]
27. Winblad B, Engedal K, Soininen H, Verhey F, Waldemar G, Wimo A, et al. A 1-year, randomized, placebo-controlled study of donepezil in patients with mild to moderate AD. Neurology. 2001;57:489-95. [ Links ]
28. McKeith I, Del-Ser T, Spano PF, Emre M, Wesnes K, Anand R, et al. Efficacy of rivastigmine in dementia with Lewy bodies: a randomised, double-blind, placebo-controlled international study. Lancet. 2000;356:2031-36. [ Links ]
29. Emre M, Aarsland D, Albanese A, Byrne J, Deuschl J, Deyn PP, et al. Rivastigmine for dementia associated with Parkinsons disease. N Engl J Med. 2004;351:2509-18. [ Links ]
30. Ravina B, Putt M, Siderowf A, Farrar JT, Gillespie M, Crawley A, et al. Donepezil for dementia in Parkinsons disease: a randomized, double blind, placebo controlled, crossover study. J Neurol Neurosurg Psychitry. 2005;76:934-9. [ Links ]
31. Waldemar G, Dubois B, Emre M, Georges J, McKeith IG, Rossor M, et al. Recommendations for the diagnosis and management of Alzheimers disease and other disorders associated with dementia: EFNS guideline. Eur J Neurol. 2007;14:e1-e26. [ Links ]
32. Fillit HM, Doody RS, Binaso K, Crooks GM, Ferris SH, Farlow MR, et al. Recommendations for best practices in the treatment of Alzheimers disease in managed care. Am J Geriatr Pharmacother. 2006;4:S9-S24.
33. Touchon J, Bergman H, Bullock R, Rapatz G, Nagel J, Lane R. Response to rivastigmine or donepezil in Alzheimer`s patients with symptoms suggestive of concomitant Lewy body pathology. Cur Med Res Opin. 2006;22:49-59.
34. Stern RG, Mohs RC, Davidson M, Schmeidler J, Silverman J, Kramer-Ginsberg E, et al. A longitudinal study of Alzheimers disease: measurement, rate, and predictors of cognitive deterioration. Am J Psychiatry. 1994;151:390-6.
35. Aarsland D, Litvan I, Salmon D, Galasko D, Wentzel-Larsen T, Larsen JP. Performance on the dementia rating scale in Parkinsons disease with dementia and dementia with Lewy bodies: comparison with progressive supranuclear palsy and Alzheimers disease. J Neurol Neurosurg Psychiatry. 2003;74:1215-20.
36. Collerton D, Burn D, McKeith I, OBrien J. Systematic review and meta-analysis show that dementia with Lewy bodies is a visualperceptual and attentional-executive. Dement Geriatr Cogn Disord. 2003;16:229-37.
37. Calderon J, Perry RJ, Erzinclioglu SW, Berrios GE, Dening TR, Hodges JR. Perception, attention, and working memory are disproportionately impaired in dementia with Lewy bodies compared with Alzheimers disease. J Neurol Neurosurg Psychiatry. 2001;70:157-64.
38. Walker Z, Allan RL, Shergill S, Katona CLE. Neuropsychological performance in Lewy body dementia and Alzheimers disease. Br J Psychiatry. 1997;170:156-8.
Manuscrito recibido el 10 de julio de 2008 y aceptado para publicación el 15 de agosto de 2008.
Correspondencia:
Dr. Nilton Custodio Capuñay
Unidad de Investigación - Clinica Internacional
Av. Garcilazo de la Vega 1420
Lima 1, Perú
Correo-e: niltoncustodio@neuroconsultas.com














