Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Anales de la Facultad de Medicina
versão impressa ISSN 1025-5583
An. Fac. med. vol.76 no.2 Lima abr./jun. 2015
http://dx.doi.org/dx.doi.org/10.15381/anales.v76i2.11147
CASO CLÍNICO
Tumor neuroendocrino ileal con síndrome carcinoide, patología de difícil diagnóstico y pronóstico variable
Ileal neuroendocrine tumor with carcinoid syndrome, neoplasia of difficult diagnosis and variable prognosis
Gonzalo Miranda1,a, Laura Luna1,b
1 Servicio de Endocrinología, Hospital Guillermo Almenara Irigoyen, EsSalud, Lima, Perú.
a Residente de Endocrinologia; b Médico Asistente.
Resumen
Los tumores neuroendocrinos (TNE) presentan dificultad en el diagnóstico por sus síntomas inespecíficos y el manejo es un reto. Se presenta el caso de un varón de 78 años de edad, con dolor crónico en hemiabdomen superior. Ingresó a emergencia con obstrucción intestinal y síntomas de síndrome carcinoide (SC). En cirugía se resecó tumor ileal con resultado anatomopatológico de tumor neuroendocrino, cromogranina positivo, índice proliferativo ki 67 de 2 a 3%. El paciente continuó con síntomas de SC, altos niveles de 5-HIA, metástasis hepáticas en RMN. Se inició octreotide con adecuada respuesta clínica. La experiencia con el presente caso indica estar alerta con los síntomas de TNE funcionantes, debido al aumento en su incidencia. Es de utilidad solicitar marcadores inmunohistoquimicos. La identificación de un TNE con índice de mitosis y proliferación bajo indica buen pronóstico.
Palabras clave: Tumor neuroendocrino ileal, síndrome carcinoide, tumores neuroendocrinos.
Abstract
The neuroendocrine tumor (NET) is of difficult diagnosis due to nonspecific symptoms; management is also a challenge. We present the case of a 78 year-old male who suffered of chronic upper abdominal pain and was admitted to emergency with intestinal obstruction and symptoms of carcinoid syndrome (CS). At surgery an ileal tumor was resected with pathology report of NET positive for chromogranin A and ki 67 proliferative index of 2-3%. The patient continued with CS symptoms and presented high levels of 5-HIAA and liver metastases by MRI. Octreotide was started with good outcome. Experience with this case indicates to be alert at symptoms of functioning NET, due to an increase in its incidence. It is useful to request immunohistochemical markers. Identification of NET with low grade mitosis and proliferation signal good prognosis.
Keywords: Ileal neuroendocrine tumor, carcinoid syndrome, neuroendocrine tumor.
INTRODUCCIÓN
Los tumores neuroendocrinos (TNE) son relativamente raros y presentan diversas localizaciones, tanto a nivel gastrointestinal, pancreático, epitelio respiratorio o células parafoliculares, como hipofisiario, paratiroideo y adrenomedular (1).
Se ha comunicado aumento de la incidencia de TNE, que se calcula en 2 a 3 x 100 000 por año, con ligero predominio en mujeres. En EE UU ha aumentado su incidencia de 1,09 a 5,25 por 100 000 por año, entre 1973 y 2004 (1). Un reporte del Instituto Nacional del Cáncer de EE UU, en base a 11 427 casos de tumores tratados entre 1973 y 1997 encuentra que la mayoría está localizado en el tracto gastrointestinal (TGI; 55%) y a nivel broncopulmonar (30%). En el TGI, la mayoría se origina en el intestino delgado y especialmente en el íleon (45% del total del TGI), seguido por el recto (20%), apéndice (16%), colon (11%) y estómago (7%). Sin embargo, desde la implantación del tamizaje por colonoscopia (aproximadamente el año 2000), la proporción de pacientes diagnosticados con carcinoides rectales ha sido mayor que la de pequeños carcinoides intestinales (2).
En relación al diagnóstico, se recomienda la clasificación de la OMS 2010 de tumores del sistema digestivo, basada en el concepto de que todo TNE tiene potencial maligno y debe ser clasificado de acuerdo a su grado y estadiaje. La clasificación de la OMS (tabla 1) separa los TNE bien diferenciados en grado bajo (G1) y grado intermedio (G2). Asimismo, los TNE pobremente diferenciados son carcinomas neuroendocrinos de grado alto (G3) (3).
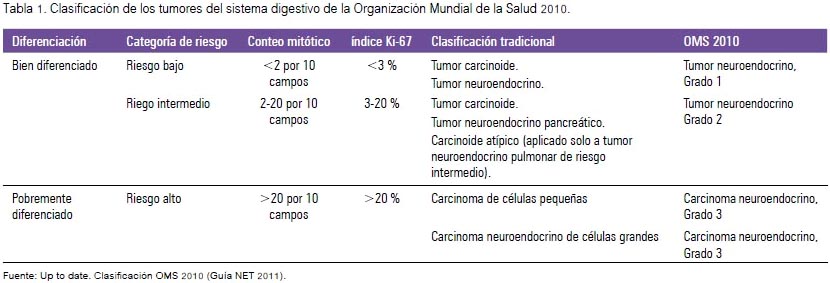
El grado se refiere a la actividad proliferativa de los tumores, comúnmente medido por el índice mitótico (número de mitosis por 10 campos de gran potencia - HPF) o el índice Ki-67. Mientras que la mayoría de los tumores carcinoides son de crecimiento relativamente lento, algunos se comportan agresivamente; el límite para definir el carcinoma neuroendocrino pobremente diferenciado gastroenteropancreático es 20 mitosis por 10 campos de alta potencia (20/10 HPF) (fuente: clasificación OMS 2010) (3). Esta nueva clasificación ayuda en el pronóstico de supervivencia. De forma tal que se ha descrito una tasa de supervivencia a 5 años de 96%, 73% y 28% para los grados 1, 2 y 3, respectivamente (1).
Los TNE gastrointestinales pueden clasificarse como tumores no funcionantes, porque no tienen cuadro clínico relacionado a la secreción de una determinada hormona, y tumores funcionantes que causan síntomas debido a los péptidos y hormonas liberadas (pueden producir el síndrome carcinoide). La mayoría de TNE son no funcionantes y se presentan con efecto de masa del tumor primario por metástasis (generalmente hepática) (1). Sin embargo, pueden presentarse en ausencia de metástasis, en caso de ubicación retroperitoneal con drenaje venoso, evitando el hígado. También puede existir dolor en hipocondrio derecho por crecimiento hepático (similar al infarto pulmonar), debido a hemorragia o necrosis o a un tumor hepático secundario. Incluso un trastorno cardiaco puede ser en 20% de los casos la forma de presentación inicial (1).
Los síntomas clínicos pueden ser generales o correlacionarse con la localización del tumor. Además, se ha descrito náuseas y vómitos y en algunos casos anemia debida al sangrado intestinal. El dolor puede ser por invasión tumoral, obstrucción intestinal o isquemia mesentérica.
La crisis carcinoide está caracterizada por enrojecimiento intenso, bronco-espasmo, taquicardia y presión arterial amplia y fluctuante rápidamente. Estas crisis son generalmente precipitadas por inducción de anestesia para cualquier operación, manipulación intraoperatoria del tumor u otro procedimiento terapéutico invasivo, como embolización y ablación con radiofrecuencia.
De una serie de casos de 35 618 TNE reportados entre 1973 y 2004, Yao y col encontraron una creciente incidencia de las NET y aumento de la duración de supervivencia en el tiempo, lo que sugiere que los tumores neuroendocrinos son más prevalentes que lo divulgado previamente. Por ello, los médicos necesitan estar familiarizados con la historia natural y los patrones de progresión de la enfermedad, que son característicos de estos tumores (4).
El único tratamiento con potencial para lograr la cura de los pacientes con tumores gastroenteropancreaticos es la resección quirúrgica completa. En los pacientes que tienen síntomas de síndrome carcinoide, los análogos de somatostatina, como octreotide, son sumamente eficaces para controlar los síntomas.
Para los pacientes que son sometidos a cirugía por carcinoide metastásico con antecedente de síndrome carcinoide, se recomienda la administración subcutánea de octreotide antes del procedimiento, para reducir la incidencia de crisis carcinoide.
Actualmente existen alternativas a la terapia médica como técnica paliativa para los pacientes sintomáticos con carcinoide no resecable, tales como la embolización de la arteria hepática, la quimioembolización o la radioembolización.
CASO CLÍNICO
Paciente varón de 78 años quien hace 3 años cursó con dolor abdominal en mesogastrio, tipo retortijón, de moderada intensidad, intermitente. Por ecografía se evidenció colelitiasis y se programó para cirugía electiva en julio de 2011. Cuatro meses posterior a la cirugía, presentó nuevamente dolor abdominal difuso de similares características, y concomitantemente estreñimiento y distensión abdominal que remitía con ingesta abundante de líquidos. Se agregó hiporexia y baja de peso de 10 kg. Luego de dos años, tuvo dolor abdominal intenso acompañado por distensión abdominal, diagnosticado como abdomen agudo. Ingresó a emergencia y en la laparotomía exploratoria se halló líquido serohemático 20 mL y asa de intestino delgado necrosado de 1,5 m de longitud a nivel del intestino medio (íleon distal), así como volvulación. Se realizó resección del vólvulo e ileostomía, con diagnóstico postoperatorio de obstrucción intestinal a nivel de íleon distal. Cuatro semanas después se agregaron episodios de enrojecimiento facial de aproximadamente 10 a 15 minutos de duración, generalmente posterior al esfuerzo físico y eventos estresantes, acompañados de sudoración profusa, prurito a nivel de miembros inferiores de moderada intensidad, palpitaciones y tremor.
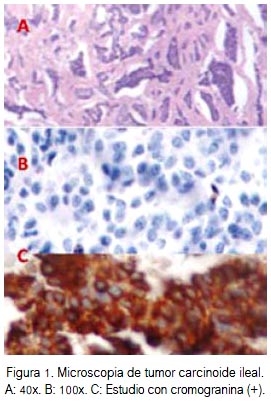
El informe anatomopatológico fue de tumor neuroendocrino ileal carcinoide, con estudio por inmunohistoquimica con cromogranina positivo (figura 1C) e índice de proliferación Ki 67 calculado hasta 3%.
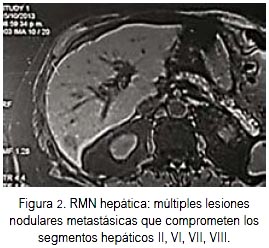
Asimismo al paciente se le realizó dosaje de ácido 5 hidroxiindolacético (5-HIAA) en orina, encontrándose nivel de 28,9 ug/24 h (rango normal: 0 a 10). Ante el cuadro clínico descrito, se realizó búsqueda por imágenes de posibles metástasis hepáticas por tomografía y resonancia magnética, encontrándose hallazgos positivos en la RMN de múltiples nódulos secundarios que comprometían los segmentos hepáticos II, VI, VII y VIII.
Posteriormente, el paciente fue sometido a PET CT de tórax abdomen y pelvis, hallándose igualmente restricción de señal a nivel hepático en los mismos segmentos que en la resonancia magnética (figuras 2 y 3).
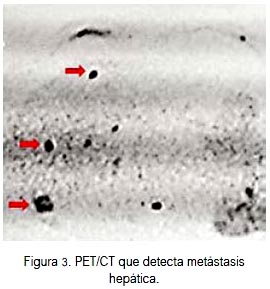
El tratamiento inicial fue con octreotide subcutáneo y luego con octreotide de acción prolongada (LAR), a dosis de 20 mg cada 4 semanas.
Después de seis meses de tratamiento, se encontró disminución en orina del ácido 5-hidroxiindolacético (5-HIAA) de 15,8 mg/24 horas. Luego de 3 meses disminuyó a 1,6 mg/24 horas. Actualmente cursa con mejoría de su estado general. El paciente presentó otras comorbilidades, como insuficiencia renal crónica moderada por hipertrofia renal crónica, actualmente compensada.
Actualmente, luego de 7 meses, cursa con mejoría de su estado general. Se evidencia aumento de 5 kilogramos de peso acompañado de disminución gradual de los niveles de creatinina y de 5-HIAA. En el estudio de RMN de abdomen se evidencia persistencia de imágenes metastásicas.
Los tumores neuroendocrinos son difíciles de diagnosticar, con retraso del diagnóstico por algunos años. Aunque la mayoría de TNE son no funcionantes, sus síntomas pueden ser vagos, intermitentes o incluso pueden permanecer largo tiempo asintomáticos. Entre los pacientes sintomáticos, el dolor abdominal es el síntoma inicial más común, ocurriendo aproximadamente en el 40 por ciento. El dolor suele ser vago, no específico, intermitente y presente por muchos años, inclusive puede ser asumido incorrectamente como un síndrome de intestino irritable durante años antes del diagnóstico. La obstrucción intestinal intermitente ocurre en 25 por ciento.
En el caso publicado, el paciente presentó dolor abdominal crónico intermitente, que en la evaluación médica fue atribuido primero a una litiasis vesicular, llegando incluso a ser intervenido quirúrgicamente.
Posteriormente el paciente cursó con un cuadro de abdomen agudo atribuido a una obstrucción intestinal e ingresó a laparotomía exploratoria, encontrándose una tumoración a nivel ileal, por lo que se le realizó resección de la tumoración y anastomosis ileo-yeyunal. Cuatro semanas tras la intervención quirúrgica el paciente presentó enrojecimiento facial y palpitaciones sin sudoración, con sospecha de síndrome carcinoide. El síndrome carcinoide ocurre en 20% de los casos de tumores bien diferenciados del yeyuno o íleo y consiste generalmente de enrojecimiento sin sudor (70% casos), con o sin palpitaciones, y dolor abdominal intermitente (40% casos), como los presentaba el paciente, aunque también puede acompañarse de diarrea (50%), lagrimeo y rinorrea. Generalmente es debido a metástasis hepáticas con liberación a la circulación de componentes vasoactivos, incluyendo aminas biogénicas (serotonina o taquiquininas).
El diagnóstico final fue posquirúrgico, por resultado de anatomía patológica, que permitió identificar el tumor neuroendocrino. El informe patológico fue de tumor ileal carcinoide, bajo la terminología tradicional, con un índice de Ki 67% de hasta 3%, que en base a la clasificación de la OMS 2010 corresponde a un tumor neuroendocrino grado 2 (riesgo intermedio).
El Ki 67 es una proteína nuclear grande (350 KDa) que está estrechamente relacionada con el nucléolo y heterocromatina, la cual parece estar involucrada en la regulación del ciclo celular y/u organización del nucléolo. Esta clasificación es importante, porque se relaciona estrechamente con el comportamiento clínico, de forma tal que al tratarse de un TNE grado 2 tiene mejor pronóstico, con supervivencia a 5 años de 67%. Se describe que incluso en presencia de metástasis hepáticas (40%), los pacientes pueden sobrevivir varios años (5).
En el momento del diagnóstico inicial se debe hacer un examen clínico completo para excluir neoplasia endocrina multiple tipo 1 y 2, enfermedad de Von Hippel-Lindau y esclerosis tuberosa, neurofibromatosis tipo 1; también, se debe hacer búsqueda de historia familiar (1,4).
Los exámenes basales deben incluir cromogranina A plasmática y ácido 5-hidroxi-indolacético urinario (5-AHIA), con rango de 2 a 8 mg/24 h. La importancia de este biomarcador se asocia a que la mayoría de NET son secretores, por lo que el dosaje de estos metabolitos derivados de la serotinina en orina es útil no solo para el diagnóstico sino también para evaluar la respuesta del tumor al tratamiento y como seguimiento de la progresión. En el caso presentado se evidenció buena respuesta al tratamiento con octreotide de acción prolongada, hasta el momento, al haber disminución de los valores de AHIA urinarios. En todos los pacientes con síndrome carcinoide debe evaluarse enfermedad carcinoide coronaria (2), mediante un ecocardiograma.
Antes de planear el tratamiento, debe determinarse el grado del tumor, metástasis, grado histológico y biomarcadores secretorios. En ausencia de diagnóstico del tumor primario, el enfoque será múltiple, siendo la tomografía, la resonancia magnética y la gammagrafía del receptor de somatostatina (SSRS) buenas alternativas (9). La tomografía computada por emisión de fotón único (SPECT) se recomienda en caso de primarios desconocidos con imágenes iniciales negativas.
En nuestro caso, al haberse determinado el tumor primario a nivel ileal, el siguiente paso fue determinar la presencia de metástasis, sobretodo hepáticas, para lo cual se le solicito TEM hepática, que fue negativa. Sin embargo, las metástasis hepáticas fueron evidenciadas mediante RMN y PET/CT, técnicas que han demostrado ser más sensibles (4).
En relación al tratamiento, el objetivo principal es mantener al paciente libre de enfermedad y sintomatología el mayor tiempo posible y ofrecer una buena calidad de vida (1,3). Como ya se ha mencionado, el único tratamiento curativo existente es la resección quirúrgica completa. En nuestro caso, la resección del tumor primario fue realizada, pero ya existía metástasis hepática.
En 6 de 8 artículos de una revisión sistemática recientemente publicada (14), se recomienda el uso de dosis más altas de octreotide LAR, cuando las dosis más bajas son insuficientes para controlar la enfermedad; aunque, se debe tener cautela, pues los índices de toxicidad a largo plazo, aún con dosis menores a 30 mg, no están establecidos.
El factor pronóstico positivo en nuestro paciente radica en que se trató de un TNE bien diferenciado grado 2. Para casos de TNE con metástasis hepáticas, como el nuestro, existen diversas alternativas de tratamiento. Dentro de las terapias regionales, la resección hepática es a menudo considerada en pacientes con enfermedad hepática, en caso de que al menos el 90% de la masa del tumor puede ser resecado. De lograrse, se obtienen resultados similares a aquellos con resección completa.
Mayo y col informaron de resultados de 339 pacientes de 8 centros principales que fueron tributarios de tratamiento quirúrgico por tumor neuroendocrino con metástasis hepática, en los cuales se encontró que la presencia de enfermedad sincrónica, un estado hormonal de TNE no funcional y la presencia de enfermedad extrahepática fueron predictores independientes de menor supervivencia (6).
Aunque la resección quirúrgica para un tumor neuroendocrino con metástasis hepática neuroendocrina está asociada con una supervivencia prolongada, la mayoría de los pacientes desarrollará enfermedad recurrente. Los pacientes con metástasis hepáticas hormonalmente funcionantes sin enfermedad extrahepática previa o sincrónica son los que principalmente se benefician con mayor supervivencia con el manejo quirúrgico (10).
La distribución de metástasis hepáticas afecta la supervivencia. Las metástasis solitarias, la presencia de un gran depósito metastásico con pequeños depósitos aislados semejante al evidenciado en nuestro paciente (imagen) (11) y la presencia de diseminación metastásica, tienen tasas de supervivencia a 5 años de 100%, 84% y 51%, respectivamente.
Dentro de las opciones complementarias a la cirugía existen técnicas ablativas (RFA/crioablación), terapias no quirúrgicas como la radioembolizacion, y modalidades de tratamiento sistémico (quimioterapia citotóxica, análogos de la somatostatina y tratamientos moleculares). La ablación térmica por radiofrecuencia (ARF) más comúnmente tiene un papel en los tumores de pequeño volumen, enfermedad pausilesional o en combinación con la resección (10,12). La quimioembolizacion está indicada para múltiples metástasis no resecables, bilobares o casos de neoplasias endocrinas no-pancreáticas poco diferenciadas y de alto grado o con curso clínico agresivo, que no presentó nuestro paciente
Los objetivos de estas terapias son dobles: aumentar la supervivencia global al estabilizar el crecimiento del tumor y reducir la morbilidad en pacientes sintomáticos. En caso haya un compromiso hepático mayor de 75%, se considera a la embolización como una contraindicación relativa, puesto que estos pacientes tienden a tener menor respuesta al tratamiento junto con mayores índices de complicaciones. Además, la presencia de trombosis de la vena porta principal es una contraindicación estricta, ya que la embolización arterial hepática se basa en el suministro de sangre venosa portal para rescatar el parénquima hepático no tumoral.
Los tumores neuroendocrinos en 80% expresan una alta densidad de receptores de la somatostatina (SSTR 1 – 5). Este péptido se une con alta afinidad a los receptores de somatostatina de tipos SSTR2 y SSTR5. Por tanto, la terapia sistémica con análogos de somastostatina inhibe la secreción de péptidos y aminas de células neuroendocrinas, cuando no es posible la resección o no sería tolerada por la fisiología del paciente.
En el caso de nuestro paciente aún está en evaluación la posibilidad de tratamiento quirúrgico de metástasis hepáticas, dado que queda pendiente la reevaluación de la ileostomía realizada previamente.
Podemos concluir, luego de describir nuestros hallazgos y al contrastarlos con otras experiencias foráneas, que el tumor neuroendocrino ileal debe ser considerado en el diagnóstico diferencial del síndrome doloroso abdominal, en forma particular en pacientes ancianos. Es necesario el estadiaje mediante el conteo de mitosis y el índice de ki67% como una práctica habitual ante esto tipos de tumores, en el proceso diagnóstico y en función al enfoque terapéutico. Para ello, además de haber localizado el tumor primario, se debe tener en cuenta el número y localización de las metástasis, para considerar la resección de las mismas como terapia única o asociada a otros tipos de tratamientos coadyuvantes. Todo ello debe evaluarse en relación al estado funcional y morbilidades que presente el paciente, así como el pronóstico de la enfermedad de acuerdo al grado de diferenciación.
REFERENCIAS BIBLIOGRÁFICAS
1. Yao JC, Hassan M, Phan A, Dagohoy C, Leary C, Mares JE, Abdalla EK, Fleming JB, Vauthey JN, Rashid A, Evans DB. One hundred years after "carcinoid": epidemiology of and prognostic factors for neuroendocrine tumors in 35,825 cases in the United States. J Clin Oncol. 2008 Jun 20;26(18):3063-72. doi: 10.1200/JCO.2007.15.4377.
2. Ahlman H, Nilsson O, McNicol AM, Ruszniewski P, Niederle B, Ricke J, Jensen R, Kos-Kudła B, Oberg K, O'Connor JM, Pavel ME, Vullierme MP; Frascati Consensus Conference participants. Poorly-differentiated endocrine carcinomas of midgut and hindgut origin. Neuroendocrinology. 2008;87(1):40-6.
3. Zimmermann ME, Bosman FT. Proliferative activity of well differentiated tumors of the gut. Histol histopathol. 2003 Apr;18(2):353-8.
4. Teunissen JJ, Kwekkeboom DJ, Valkema R, Krenning EP. Nuclear medicine technique for the imaging and treatment of NET. Endocr Relat Cancer. 2011 Oct 17;18 Suppl 1:S27-51. doi: 10.1530/ERC-10-0282.
5. Rinke A, Müller HH, Schade-Brittinger C, Klose KJ, Barth P, Wied M, Mayer C, Aminossadati B, Pape UF, Bläker M, Harder J, Arnold C, Gress T, Arnold R; PROMID Study Group. Placebo-controlled, double-blind, prospective, randomized study on the effect of octreotide LAR in the control of tumor growth in patients with metastatic neuroendocrine midgut tumors: a report from the PROMID Study Group. J Clin Oncol. 2009 Oct 1;27(28):4656-63. doi: 10.1200/JCO.2009.22.8510.
6. Glazer ES, Tseng JF, Al-Refaie W, Solorzano CC, Liu P, Willborn KA, Abdalla EK, Vauthey JN, Curley SA. Long-term survival after surgical management of neuroendocrine hepatic metastases, HPB (Oxford), 2010 Aug;12(6):427–33. doi: 10.1111/j.1477-2574.2010.00198.x
7. Taghavi S, Jayarajan SN, Powers BD, Davey A, Willis AI. Examining rectal carcinoids in the era of screening colonoscopy: a surveillance, epidemiology, and end results analysis. Dis Colon Rectum. 2013 Aug;56(8):952-9 doi: 10.1097/DCR.0b013e318291f512
8. Boudreaux JP. Surgery for gastroenteropancreatic neuroendocrine tumors (GEPNETS). Endocrinol Metab Clin North Am. 2011 Mar;40(1):163-71, ix. doi: 10.1016/j.ecl.2010.12.004
9. Ramage JK1, Ahmed A, Ardill J, Bax N, Breen DJ, Caplin ME, Corrie P, Davar J, Davies AH, Lewington V, Meyer T, Newell-Price J, Poston G, Reed N, Rockall A, Steward W, Thakker RV, Toubanakis C, Valle J, Verbeke C, Grossman AB; UK and Ireland Neuroendocrine Tumour Society. Guidelines for the management of gastroenteropancreatic neuroendocrine (including carcinoid) tumours (NETs). Gut. 2012 Jan;61(1):6-32. doi: 10.1136/ gutjnl-2011-300831.
10. Gu P, Wu J, Newman E, Muggia F. Treatment of liver metastases in patients with neuroendocrine tumors of gastroesophageal and pancreatic origin. Int J Hepatol. 2012;2012:131659. doi: 10.1155/2012/131659
11. Søreide JA. Treatment of liver metastases from neuroendocrine tumours in relation to the extent of hepatic disease. Br J Surg. 2009 Jul;96(7):823; author reply 823-4. doi: 10.1002/bjs.6707.
12. Saxena A, Chua TC, Chu F, Al-Zahrani A, Morris DL. Optimizing the surgical effort in patients with advanced neuroendocrine neoplasm hepatic metastases: a critical analysis of 40 patients treated by hepatic resection and cryoablation. Am J Clin Oncol. 2012 Oct;35(5):439-45.
13. Yao KA, Talamonti MS, Nemcek A, Angelos P, Chrisman H, Skarda J, Benson AB, Rao S, Joehl RJ. Indications and results of liver resection and hepatic chemoembolization for metastatic gastro-intestinal neuroendocrine tumors. Surgery. 2001 Oct;130(4):677-82.
14. Broder MS, Beenhouwer D, Strosberg JR, Neary MP, Cherepanov D. Gastrointestinal neuroendocrine tumors treated with high dose octreotide-LAR: A systematic literature review. World J Gastroenterol. 2015 Feb 14;21(6):1945-55. doi: 10.3748/wjg. v21.i6.1945.
Artículo recibido el 28 de diciembre de 2014 y aceptado para publicación el 13 de marzo de2015.
Fuente de financiamiento: De los autores
Conflictos de interés: No existen
Correspondencia
Dra. Laura Luna
Servicio de Endocrinología del Hospital Nacional Guillermo Almenara
Av. Grau 800, Lima
Teléfono: 324 2983 anexo 44123
Correo electrónico: dralelv@yahoo.fr
Dr. Gonzalo Miranda Manrique
Correo electrónico: sith1685@hotmail.com














