INTRODUCCIÓN
La tendencia actual es que la mortalidad del cáncer va disminuyendo gracias a una detección más temprana, así como por los adelantos en su tratamiento. Sin embargo, algunas de las nuevas drogas antineoplásicas pueden afectar, directa o indirectamente, al corazón y ocasionar una entidad clínica relativamente nueva denominada "cardiotoxicidad" 1. En los próximos años, la población de sobrevivientes al cáncer crecerá, se estima que, para la próxima década, en Estados Unidos la cifra será de 18 millones, lo que significa un incremento de 30 % de supervivientes; pero el riesgo por muerte cardiaca y por muerte súbita será 5,9 y 3,9 veces mayor en la población que recibió terapia oncológica 2. El Childhood Cancer Survivor Study reportó que luego de 15 a 25 años de ser diagnosticados de cáncer, los niños que sobrevivieron tuvieron 8,2 veces más frecuencia de muerte cardiaca, 15 veces más de desarrollar insuficiencia cardiaca y 10 veces más de enfermedad coronaria isquémica 3.
En 1967, Charlotte Tan 4) publicó uno de los primeros trabajos acerca de daño miocárdico por uso de daunorrubicina en niños con leucemia, pero es hasta 1996 que la Dra. Daniela Cardinale, del Instituto Europeo de Oncología en Milán, empieza a utilizar el término "cardiotoxicidad" como una nueva disciplina para referirse al efecto tóxico de las terapias antineoplásicas en el corazón 5.
El compromiso cardiaco por el tratamiento del cáncer a la fecha es muy amplio, y se puede manifestar como:
Cardiopatía isquémica
Insuficiencia cardiaca
Arritmias cardiacas y prolongación del QT
Hipertensión arterial
Enfermedad tromboembólica venosa o arterial
Pericarditis
Sin embargo, la cardiotoxicidad se describía clásicamente como la entidad clínica que podía abarcar desde la disfunción ventricular izquierda asintomática transitoria, hasta la muerte por insuficiencia cardiaca, y se relacionaba con mayor frecuencia al uso de los antraciclínicos pero, actualmente, se registran también con otros nuevos fármacos oncológicos. La ecocardiografía y la fracción de eyección del ventrículo izquierdo son los parámetros tradicionales para evaluar el daño. Gracias a la tecnología en imágenes surgen nuevos métodos, como el de valorar el grado de deformación o strain miocárdico para descubrir la disfunción cardiaca en un estadio subclínico. Este estudio es de gran trascendencia clínica, porque permitiría descubrir precozmente el compromiso miocárdico y actuar para evitar un mayor daño.
CARDIOTOXICIDAD
Según la Sociedad Americana de Ecocardiografía y la Asociación Europea de Imagen Cardiovascular se definirá cardiotoxicidad a una disminución de la fracción de eyección de ventriculo izquierdo (FEVI) > 10 % con respecto al basal, o con valores menores del límite inferior de la normalidad (53 %).
Esta disminución debe confirmarse con un estudio repetido después de 2 a 3 semanas del estudio diagnóstico inicial (6.
INSUFICIENCIA CARDIACA Y ANTINEOPLÁSICOS
La disfunción ventricular sintomática o asintomática por efecto del tratamiento oncológico es una reacción secundaria relativamente frecuente, pero con alta mortalidad. La insuficiencia cardiaca inducida por las antraciclinas tiene un mal pronóstico, con una mortalidad a dos años de un 60 % 7. Los medicamentos antineoplásicos se clasifican según el riesgo de desarrollar insuficiencia cardiaca en tres categorías:
Riesgo alto: antraciclinas, ciclofosfamida y trastuzumab. Riesgo moderado: docetaxel, pertuzumab, sunitinib, sorafenib. Riesgo bajo: bevacizumab, dasatinib, imatinib y lapatinib 8.
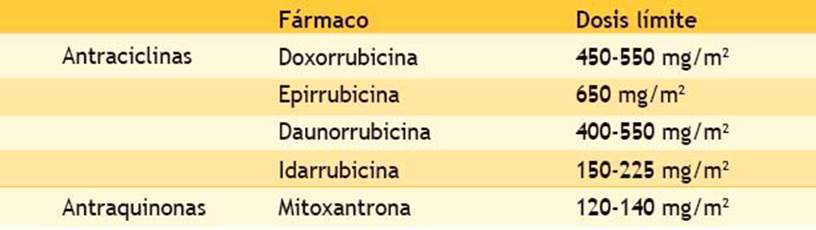
ANTRACICLINAS
Son fármacos muy útiles en el tratamiento del cáncer desde los años 50, pero tienen su mayor limitante en su dosis y el riesgo de daño miocárdico. Químicamente, son antibióticos denominados "citostáticos" por su efecto antitumoral. El primero de su clase es la daunorrubicina obtenida del Streptomyces peucetius. Las antraciclinas actúan como un agente intercalante que se inserta a la doble hélice del ADN, interfiere así con la replicación, la transcripción y la reparación lo que facilita su degradación 9.
La frecuencia de insuficiencia cardiaca por antraciclinas es muy variable, si consideramos diversos factores que influyen en su desarrollo. El clásico reporte de Von Hoff mostró 3 % con una dosis acumulada de doxorrubicina de 400 mg/m2, 7 % a una dosis de 550, y 18 % a 700 mg/m2. Se ha estimado en 5 % de insuficiencia cardiaca con una dosis acumulada de 300 mg/m2, y se hace la referencia de toxicidad subclínica en un rango de 0 % a 57 % 10. Si el paciente desarrolla miocardiopatía dilatada e insuficiencia cardiaca, el pronóstico es malo, con una mortalidad de 50 % a los 7 años de seguimiento.
Mecanismos de cardiotoxicidad por antraciclinas
El mecanismo de la cardiotoxicidad por antraciclinas no se conoce con exactitud. Las hipótesis más difundidas son dos: El primer mecanismo es la generación de especies reactivas de oxígeno (ERO). Al ingresar las antraciclinas a las células sufren una serie de procesos rédox, por lo que el grupo quinona ubicado en el anillo B de las antraciclinas se reduce formando un radical semiquinona, el cual se oxida y produce la formación masiva de radicales libres, ocasionando alteraciones antioxidantes y proinflamatorias que afectan tanto al ADN como a las mitocondrias, lo que conlleva a la muerte celular. La generación de ERO es producto de la vía enzimática a través de la cadena respiratoria mitocondrial, o de una vía no enzimática a través del hierro. La antraciclina también interactúa con el hierro intracelular, formando un complejo con el hierro férrico que produce una exagerada formación de ERO: estos complejos afectan a la cardiolipina (constituyente de la membrana de las organelas) lo que finalmente destruye a las membranas lipídicas mitocondriales, del retículo endoplasmático (RES) y celulares, esto provoca el descenso del calcio intracelular y, por ende, un detrimento de la función miocárdica. Un factor que influye a un mayor daño de las ERO es que el músculo cardiaco tiene una baja capacidad antioxidante, los niveles de catalasa y de superóxido dismutasa son reducidos en comparación con otros tejidos (11,12.
Un segundo mecanismo, propuesto por Sui Zhang, es el efecto de las antraciclinas en las topoisomerasas. Las topoisomerasas tienen un rol importante sobre la estructura del ADN: intervienen en el enrollamiento (para ser almacenado), y también participan en su desenrollamiento, en el momento de la replicación. Existen dos tipos de topoisomerasas: la 1 actúa sobre una de las dos cadenas del ADN y así facilita su transcripción; y la 2, que corta ambas cadenas. A su vez, la topoisomerasa 2 presenta dos isoenzimas Top 2α y Top 2β. La Top 2α se encuentra en las células cancerosas como en las que participan en fase de proliferación, la actividad antitumoral de los antraciclínicos es formar complejo Top2α-adriamicina-ADN lo que ocasiona apoptosis. La Top 2β se encuentra en los cardiomiocitos, los antraciclínicos actúan en estas isoenzimas activando el p53, lo que provoca muerte celular temprana de estas células y la pérdida de las miofibrillas del músculo cardiaco. Además, el complejo Top 2β-adriamicina bloquea a los promotores de los PPAR-gamma alfa y beta, lo que facilita el incremento de ERO y la disfunción mitocondrial. La toxicidad por antraciclinas es dependiente de la dosis e irreversible, que ocasiona primero una disfunción diastólica, que debe considerarse como un predictor de riesgo y, en forma tardía, una disfunción sistólica 12,13.
Tipos de cardiotoxicidad por antraciclinas
Según la Dra. Daniela Cardinale, la cardiotoxicidad es un fenómeno continuo y único, que empieza con la injuria celular y terminaría en la insuficiencia cardiaca 14; clásicamente, se puede clasificar de acuerdo al tiempo de presentación en tres grupos:
Cardiotoxicidad aguda y subaguda: se presenta desde el inicio del esquema farmacológico hasta 2 semanas después de finalizar la terapia. Los tipos más frecuentes son las arritmias cardiacas, cambios en el electrocardiograma (trastornos de la repolarización ventricular), prolongación del intervalo QT, pericarditis o miocarditis. Es poco frecuente, independiente de la dosis y transitoria.
Cardiotoxicidad crónica temprana: aparece durante el primer año de haber terminado la terapia oncológica, y está relacionada con signos y síntomas de insuficiencia cardiaca. Es dosis-dependiente e irreversible.
Cardiotoxicidad crónica tardía: se evidencia después del primer año de haber concluido el régimen terapéutico, incluso luego de décadas. Incluye la disfunción ventricular y la insuficiencia cardiaca 8.
Factores de riesgo de cardiotoxicidad por antraciclinas 6,15
Dosis total acumulada: con >250 mg/m2 de doxorrubicina o equivalente se incrementa el riesgo.
Velocidad de administración: la velocidad lenta es menos cardiotóxica
Radioterapia mediastinal: altas dosis >30 Gy
Otras terapias: trastuzumab, ciclofosfamida en altas dosis, taxanos, cisplatino, mitomicina
Edad >70 años y menores de 15 años (los niños son más sensibles)
Sexo femenino
Raza negra
Factores genéticos: trisomía 21
Desnutrición
Hipertensión arterial
Enfermedad cardiovascular previa: cardiopatía isquémica, insuficiencia cardiaca
Insuficiencia renal
TRASTUZUMAB
El trastuzumab forma parte de la nueva terapia biológica en el cáncer, es un anticuerpo monoclonal humanizado dirigido contra el dominio extracelular del receptor del HER2neu (receptor del factor de crecimiento epidérmico) que es un receptor tirosinquinasa transmembrana, que estaría funcionando como un protoncogén. La familia está constituida por 4 tipos de receptores: HER1, HER2, HER3 y HER4. Trastuzumab tiene alta afinidad y especificidad por el receptor HER2. Este gen se encuentra sobreexpresado y amplificado en un 25 a 30 % de pacientes con cáncer de mama y se asocia a mal pronóstico 17.
La cardiotoxicidad sintomática por trastuzumab es de 3 a 7 %, mientras que la reducción asintomática de la función cardiaca es de un 10 %. En el caso del uso conjunto con antraciclinas, la toxicidad se incrementa hasta un 27 %, por lo que el riesgo disminuye si se administra trastuzumab al menos 90 días después de finalizar las antraciclinas 18.
Mecanismos de cardiotoxicidad por trastuzumab
La neuregulina es una proteína producida por el endotelio microvascular coronario y el endocardio. Esta proteína se une al receptor HER4, el cual se heterodimeriza con el HER2, lo cual favorece la fosforilación del ATP y el acoplamiento mecánico del miocito. El trastuzumab, al bloquear al receptor HER2 en los cardiomicitos, provocaría una depleción de ATP y una alteración de la función contráctil. Generalmente, se observa una reducción de la función ventricular izquierda asintomática. Rara vez evoluciona hacia una franca insuficiencia cardiaca irreversible 1, 8, 19.
Factores de riesgo de cardiotoxicidad por trastuzumab:
TIPOS DE CARDIOTOXICIDAD
Existen dos tipos de cardiotoxicidad inducida por fármacos antineoplásicos según Suter y Ewer (Tabla 2):
Tipo I: Es la cardiotoxicidad característica de las antraciclinas y de agentes alquilantes (por ejemplo, la ciclofosfamida), es irreversible, ocasiona pérdida de células (necrosis/apoptosis), es dosis-dependiente y está causada por la formación de radicales libres, estrés oxidativo y desorden miofibrilar. Tiene el peor pronóstico.
Tipo II: Este tipo es característico de fármacos como el trastuzumab, es reversible, produce disfunción celular (mitocondrial y de proteínas) (Tabla 2).
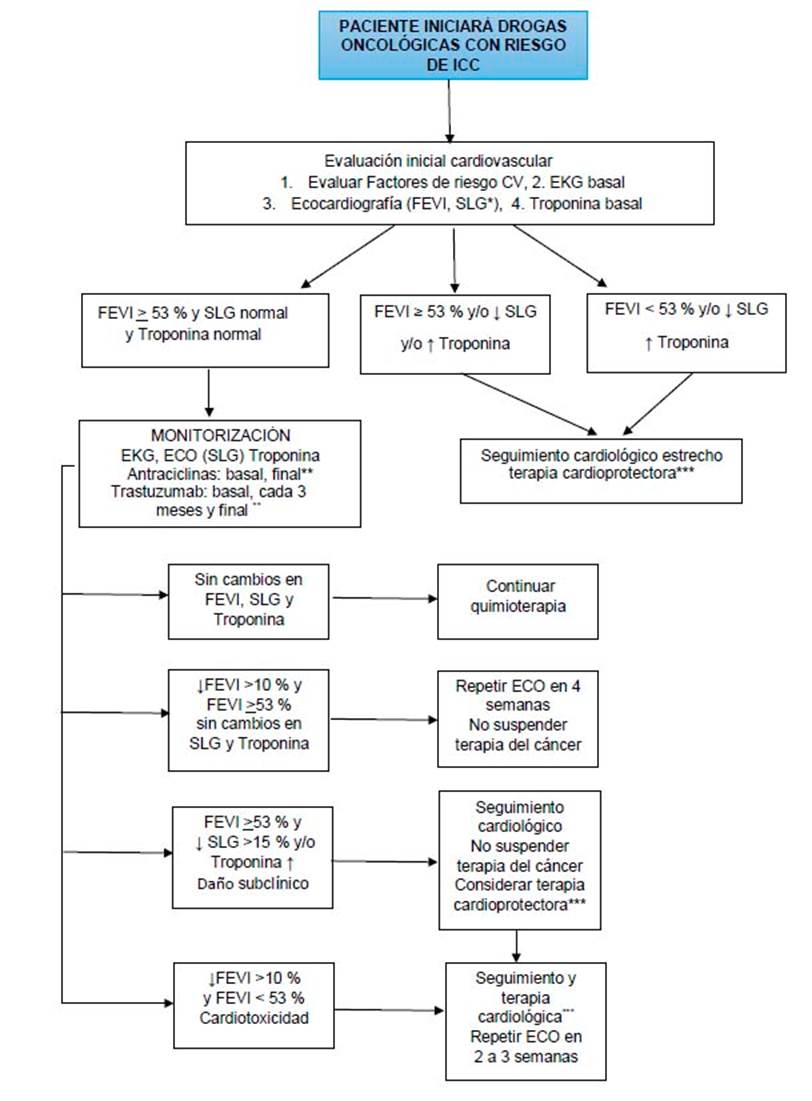
MONITOREO PARA EVITAR LA CARDIOTOXICIDAD 6,15
La Sociedad Estadounidense de Oncología Clínica recomienda la estratificación del riesgo de disfunción cardiaca antes del inicio del tratamiento del cáncer potencialmente cardiotóxico. Los pacientes con función cardiaca limítrofe (FEVI de 50 a 55 %) y con comorbilidades cardiacas tienen un riesgo de 3,6 a 11,8 veces mayor para desarrollar disfunción cardiaca 20.
El monitoreo consta de los siguientes pasos:
Evaluación de los factores de riesgo, recomendar a los pacientes el control de la presión arterial, no fumar, mantener el nivel de lípidos en rangos normales y modificar a estilos de vida favorables
Evaluación clínica basal
Electrocardiograma basal y periódico
Ecocardiograma: si es posible Strain Longitudinal Global (SLG)
Biomarcadores: troponina I y, en casos especiales, ProBNP
Conclusión final conjuntamente con el oncólogo clínico para elección de quimioterapia personalizada
El consenso de expertos para la evaluación de imágenes de múltiples modalidades del paciente adulto durante y después de la terapia oncológica recomienda un ecocardiograma basal (ecocardiografía 3D y SLG, si la tecnología está disponible) que incluya el cálculo de la FEVI 21,22.
Antraciclinas
Recomendaciones con FEVI <45% del basal:
Medirla a los 250 a 300 mg/m2 de dosis acumulada de doxorrubicina.
Medirla a los 450 mg/m2 de dosis acumulada.
Medirla antes de cada dosis después de los 450 mg/m2 de dosis acumulada.
Descontinuar temporalmente la quimioterapia si hay una caída ≥10 % de la FEVI basal o la FEVI es <45 %.
Recomendaciones
Trastuzumab
Tener una FEVI <45% se asocia como factor de riesgo para desarrollar la falla cardiaca. Por ello, al inicio de un régimen con este tipo de medicación siempre se debe:
Tener una FEVI basal con ecografía 3D (idealmente) o ecografía 2D.
Evaluación del Strain Longitudinal Global (SLG) por ecocardiografía de rastreo de moteado (Speckle Tracking).
Medición de troponina I.
Se debe remitir a cardiología si:
FEVI < 53 % (Considerar confirmación con RNM).
SLG menor de límite inferior normal.
Troponina I positiva.
Se realiza seguimiento cada 3 meses durante la terapia si:
Interrumpir 1 mes y revaluar:
Identificación temprana de disfunción cardiaca relacionada con la terapéutica del cáncer (DCRTC)
La vigilancia y detección de DCRTC se realiza mediante el uso de la FEVI derivada de la ecocardiografía y, más recientemente, de imágenes de deformación miocárdica (Strain); estableciendo el estadio B de insuficiencia cardiaca, y se pueda iniciar la terapia respectiva; el cálculo exacto de los volúmenes del VI en la evaluación de la remodelación del VI; y la identificación potencial de situaciones donde los cambios en las condiciones de carga pueden estar jugando un papel en los cambios de la FEVI o de la deformación miocárdica. El cálculo preciso de la FEVI debe hacerse con el mejor método disponible en el laboratorio de ecocardiografía (idealmente, ecocardiografía 3D) 23,24.
Estrategias cardioprotectoras con antraciclinas
Alterar estructura de la antraciclina (epirubicina).
Cambios en la farmacocinética (preparaciones liposomales que eviten el ingreso al endotelio y al miocardio, pero sí puede difundir al tumor).
Modificar la pauta de administración (Infusión continua 24-96 h vs bolos).
Agentes cardioprotectores (dexrazoxano que actúa como quelador del hierro y reduce la mortalidad tanto en niños como adultos, sin disminuir el efecto de la quimioterapia).
Monitorización a largo plazo
No hay acuerdo en cómo realizarlo. Hay que establecer el riesgo de toxicidad y los de alto riesgo (dosis recibida de antraciclinas >250 mg/m2 o ≥35 Gy de radioterapia toráxica o terapias combinadas). Se propone realizar un ecocardiograma a los 2 años de finalizado el tratamiento y después cada 5 años, y en mujeres debe realizare antes y al final de la gestación.
Exámenes auxiliares
Ecocardiografía: Es la técnica de elección para valorar la función cardiaca. A través de la ecocardiografía se pueden obtener la siguiente información:
Evaluación de la función diastólica del ventrículo izquierdo, para lo cual se pueden determinar: la función diastólica del ventrículo izquierdo a través del patrón de llenado mitral (onda E/onda A), el doppler tisular, relación E/e´.
Índice de rendimiento cardiaco o TEI que expresa un valor en relación a la función sisto-diastólica del ventrículo izquierdo.
Fracción de eyección: que es el valor de referencia de la función cardiaca, para lo cual se utiliza el método de Simpson. La FEVI por técnica tridimensional tiene menos variabilidad (5,8 %) 25. Una reducción del 10 % de la FEVI define la cardiotoxicidad. Su mayor limitante entre otros es que tiene baja sensibilidad para detectar cambios menores de la función cardiaca y no sirve como un elemento de pronóstico en el paciente en tratamiento oncológico.
Strain o deformación miocárdica y la velocidad de deformación o strain rate. El más utilizado es el Strain Longitudinal Global (SLG), y una reducción en más del 15 % del valor basal se considera indicador de disfunción subclínica del ventrículo izquierdo (estadio B de la insuficiencia cardiaca) y sugiere como el mejor predictor de cardiotoxicidad 26.
Técnicas imagenológicas adicionales:
Resonancia magnética nuclear: Se puede utilizar en casos en que las imágenes por ecocardiografía no fuesen adecuadas. Permite evaluar con mayor exactitud que la ecocardiografía la función cardiaca.
Medicina nuclear: Permite una mejor evaluación de la fracción de eyección; sin embargo, se somete al paciente a radiación ionizante.
Biomarcadores: las troponinas sirven para detectar precozmente el daño del cardiomicito y es un predictor de morbilidad y mortalidad cardiovascular, por lo que se recomienda tener un control basal y controles posteriores según protocolos. El más utilizado es la troponina I. La evaluación integral de la fracción de eyección, el SLG y troponina I pueden permitir detectar la disfunción ventricular subclínica y establecer una terapia cardioprotectora evitando el mayor daño de la función cardiaca. Los péptidos natriuréticos permiten una evaluación de estados de sobrecarga de volumen en las cavidades cardiacas, presentes en la disfunción de ventrículo izquierdo; su valor puede aumentar cuando la insuficiencia cardiaca está en estadio subclínico 27.
Biopsia endomiocárdica: es el método más seguro para diagnosticar el daño miocárdico; sin embargo, es un procedimiento invasivo que los pacientes no aceptan con facilidad.
CASO CLINICO
Mujer de 17 años de edad, natural y procedente de Lima. Acude a Consultorio Externo del INEN el 17-9-2018 por dolor en pierna izquierda de 2 meses de evolución. Sin antecedentes cardiovasculares de importancia. Asintomática cardiovascular: no angina de pecho, no palpitaciones, tolera el decúbito, no falta de aire.
Fue diagnosticada de osteosarcoma primario tibial proximal izquierda el 25 de setiembre del 2018. TEM de tórax no metástasis. Inició quimioterapia el 22 octubre del 2018 con adriamicina (37,5 mg/m2) y cisplatino (60 mg/m2). Luego MAP: metotrexate, doxorrubicina y platino (mayo a julio 2019). El 19 de agosto del 2019 se realiza evaluación por uso de antraciclinas (450 mg/m2).
Examen físico:
PA: 100/60 mmHg. Frecuencia cardiaca:90 lat/min
Peso 52 kg. Talla: 1,61 m
Ruidos cardiacos rítmicos y regulares
No tercer ruido. No soplos
Miembros inferiores: sin edemas. Pulsos periféricos: normales
Radiografía de tórax: normal
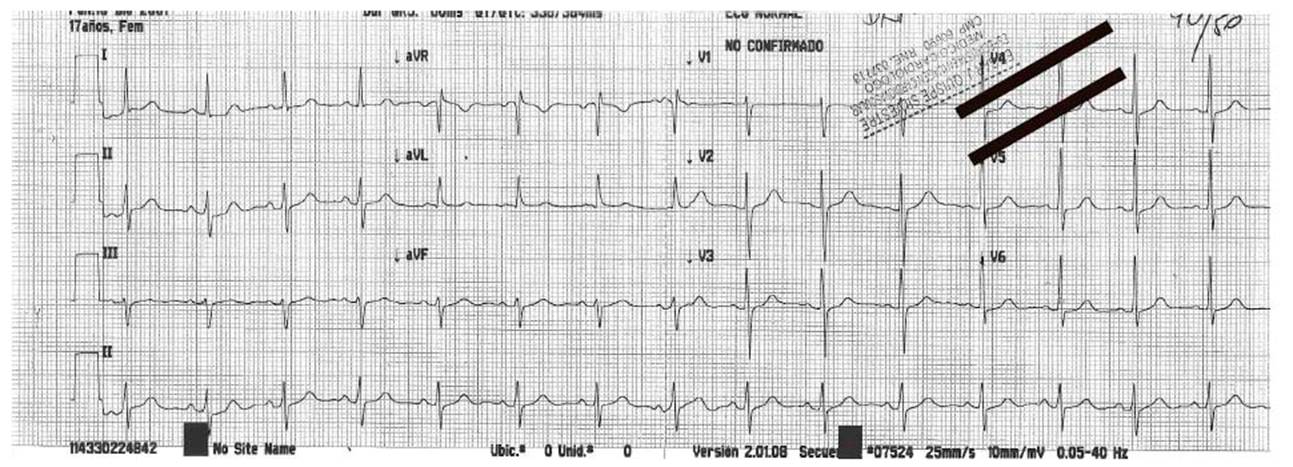
Electrocardiograma: normal
Exámenes auxiliares:
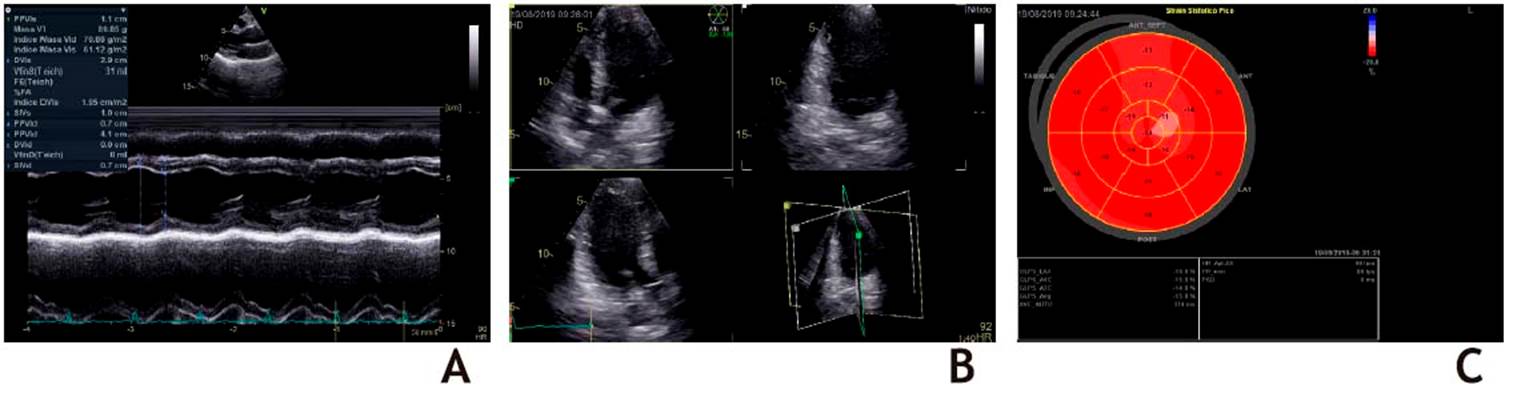
Ecocardiografía: Función sistólica de ventrículo izquierdo normal. Fracción de eyección 60%. Strain Longitudinal Global (SLG) - 15 %
Troponina I: 115 ng/mL (VN: 34 ng/L)
Conclusión: disfunción ventricular izquierda asintomática. Se indica carvedilol 6,25 mg/día por tres meses.
Seguimiento: Control el 26-11-2019 asintomática cardiovascular.
Ecocardiografía: Función sistólica de ventrículo izquierdo normal.
Fracción de eyección 62 %. SLG - 20 %. Troponina I: 19 ng/mL (VN 34 ng/L).
DISCUSIÓN
El caso que se presenta es un ejemplo de la situación actual de un numeroso grupo de pacientes oncológicos. La supervivencia de los pacientes con cáncer crece cada vez más, lo cual es un logro en el campo de la medicina. Una enfermedad que hasta no hace mucho era sinónimo de muerte, en las dos últimas décadas ha tenido un cambio muy importante gracias a la detección cada vez más temprana, a los nuevos tratamientos que incluyen nuevos avances en los procedimientos quirúrgicos, la nueva tecnología en la radioterapia y los nuevos fármacos. Así, en Canadá, entre el 2001 y 2010, la mortalidad en mujeres ha disminuido en 1,2 % por año y en hombres 1,8 % por año 28.
Sin embargo, muchos de los fármacos oncológicos y/o el uso de la radioterapia torácica tienen efectos colaterales sobre el corazón, que, con relativa frecuencia, ocasionan la muerte del paciente, después de recuperarse del cáncer. Esta condición clínica se conoce con el término de "cardiotoxicidad" que, en este momento, se puede prevenir, diagnosticar y tratar; por lo que surge una nueva subespecialidad, la Cardio-Oncología, que estudia las complicaciones cardiovasculares derivadas de los tratamientos oncológicos, las cuales deben tratarse en las unidades de esta especialidad 17.
Las unidades funcionales de Cardio-Oncología son multidisciplinarias, participan oncólogos, cardiólogos, hematólogos, radioterapistas, especialistas afines, y enfermeras. Realizan la evaluación integral del paciente oncológico, establecen el estado de riesgo para desarrollar cardiotoxicidad, plantean un diagnóstico lo más precoz posible, o definen una estrategia de tratamiento y seguimiento en el paciente que ya desarrolló un daño cardiaco hasta la supervivencia posterior 29. Y una tarea final que ha sido la base del desarrollo de la medicina, la investigación y la divulgación del conocimiento que permita a los médicos mantenerse en la vanguardia de los grandes adelantos para la salud de la población (1,18. El éxito de estas unidades interdisciplinarias radica en la colaboración entre sus miembros, que abordan el problema desde diferentes puntos de vista, pero con un solo objetivo, el paciente.
La medicina moderna ya no es la clásica profesión del tratamiento, debe ser de prevención. Precisamente, este caso clínico muestra a una paciente asintomática cardiovascular y con función cardiaca preservada, hasta no hace mucho tiempo no se le hubiera prestado mayor interés, y posteriormente hubiera desarrollado insuficiencia cardiaca, condición que implica una alta mortalidad. Sin embargo, en las unidades de Cardio-Oncología, al utilizar los nuevos protocolos y equipos de alta tecnología, emplea nuevos parámetros como Strain Longitudinal Global y la medición de troponina I que, en este caso, se encontraban alterados, y se estableció el diagnóstico de disfunción ventricular izquierda asintomática. La paciente recibió el tratamiento respectivo y se evitó el avance a una insuficiencia cardiaca, cumpliendo así el objetivo de propugnar la prevención