INTRODUCCIÓN
En diciembre de 2019, en Wuhan (China), se registró un brote de cuadros con síntomas clínicos comunes de neumonía, tras el ingreso masivo de pacientes en los hospitales locales. Poco después, la Organización Mundial de la Salud (OMS) confirmó la aparición de un nuevo coronavirus, llamado SARS-CoV-2, como el agente etiológico de estos síntomas y nombró a esta enfermedad como COVID-19. Desde el año pasado, esta pandemia, sin precedente en las últimas décadas, atrae la atención de muchos médicos, científicos y agencias reguladoras de todo el mundo que buscan conocer la patogenia, técnicas de diagnóstico, posibles terapias y vacunas eficaces contra el agente infeccioso 1,2.
Una gran diversidad de estrategias de inmunoterapia se ha desarrollado e implementado para controlar la infección por SARS-CoV-2 y tratar la enfermedad que ocasiona, la COVID-19 3,4. En poco más de un año, diversas plataformas vacunales para ser incluidas en estrategias masivas de vacunación han sido diseñadas y evaluadas (en preclínica, clínica y escalado productivo) 5,6. Cada país tiene la libertad de masificar la inmunización contra este virus; sin embargo, y de manera general, se ha optado por priorizar a las personas más expuestas o con alto riesgo de desarrollar una enfermedad grave, es decir, los profesionales de la salud y los adultos mayores.
En condiciones normales, la investigación y desarrollo de vacunas para uso humano tomarían muchos años y costarían millones de dólares, sobre todo cuando se utilizan nuevas tecnologías que no han sido examinadas de manera exhaustiva. Pero, ya que en el mercado no existían vacunas contra el coronavirus, muchos países han autorizado planes de vacunación de emergencia contra el SARS-CoV-2. Estas vacunas se desarrollaron y evaluaron durante el último año en distintas naciones y corresponden a diferentes plataformas, como vacunas de virus inactivados, de virus vivos atenuados, de vectores virales recombinantes, de ARN mensajero, entre otras tecnologías. La vacuna aplicada a los profesionales de la salud en el Perú (Sinopharm) está elaborada a partir de un virus inactivado y ha sido desarrollada por empresa china Sinopharm China National Biotec Group (CNBG) 7,8. Este producto muestra algunas ventajas en las condiciones requeridas para el almacenamiento y transporte. Algunos tipos de vacunas, como las de plataforma ARN mensajero, son bastante inestables a temperatura ambiente y pueden requerir congeladores que, por lo general, no se encuentran en centros de salud rurales lejanos o que no cuentan con sistemas que aseguren la cadena de frío, por lo que las vacunas no refrigeradas pueden ser una solución más viable para estos lugares 9.
En el Perú, la mayoría de los trabajadores de la salud han sido vacunados; entre ellos, el 84,42 % de los médicos 10. El Ministerio de Salud ha aplicado a su personal dos dosis de la vacuna china Sinopharm. Esta vacuna, de probada inmunogenicidad y seguridad 11,12, enfrenta al sistema inmune de los vacunados con la totalidad de antígenos virales, pues se basa en la inactivación del virus por efecto de la droga β-propionolactona 13.
La capacidad del sistema inmune de limitar la infección viral a las células depende de diversos factores, como la inducción de anticuerpos neutralizantes 14. En consecuencia, es relevante evaluar la capacidad de una vacuna de inducir la formación de estos anticuerpos y determinar los factores que pueden influir en su presencia en el suero de los individuos vacunados. El presente trabajo describe la información de la base de datos del centro Gamma Médica Servicios Médicos de la ciudad de Lima, donde han asistido profesionales sanitarios vacunados para cuantificar los anticuerpos neutralizantes en el suero. En este trabajo solo se ha incluido a las personas que recibieron la vacuna SINOPHARM, y comparó la presencia de anticuerpos neutralizantes en dos grupos: las personas con diagnóstico de COVID-19 antes de la vacunación y los individuos que no tuvieron este diagnóstico.
MATERIALES Y MÉTODOS
Diseño y población de estudio
Investigación descriptiva y de diseño transversal. Los datos analizados corresponden a 117 profesionales de la salud vacunados con dos dosis de la vacuna Sinopharm, que acudieron al centro Gamma Médica en los meses de marzo y abril del 2021 para detectar anticuerpos neutralizantes contra SARS-CoV-2 mediante la técnica de inmunoensayo de electroquimioluminiscencia (eCLIA) de Shenzhen Lifotronic Technology Co., Ltd. Se excluyeron ocho registros que no consignaban el tipo de vacuna administrada.
Variables y mediciones
Se consideraron las variables edad, sexo, antecedentes de infección con SARS-CoV-2 (diagnosticados con COVID-19) y concentración de anticuerpos neutralizantes.
Análisis estadístico
Los datos se analizaron mediante la estadística descriptiva para las variables en estudio. Para el análisis de anticuerpos neutralizantes se utilizó como punto de corte la detección de 10 UA/mL de anticuerpos, según la recomendación del fabricante de la técnica de detección utilizada (Shenzhen Lifotronic Technology Co., Ltd.). Las diferencias estadísticas entre los valores de lectura de anticuerpos neutralizantes, entre individuos que tuvieron o no COVID-19, se determinó mediante la prueba t de Student para muestras no emparejadas, con un nivel de confianza de 95 %. Los datos se analizaron con el software estadístico IBM SPSS v.27.
RESULTADOS
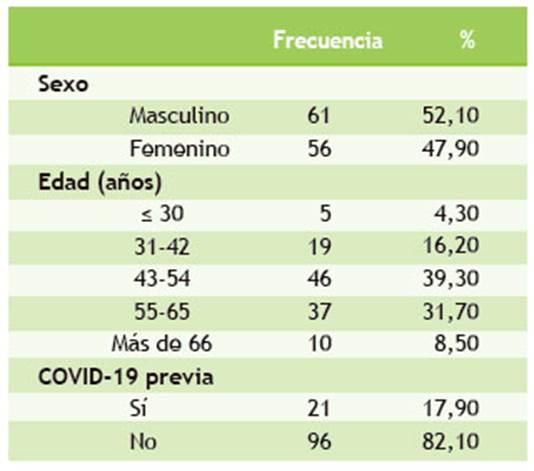
En el estudio, 117 profesionales de la salud recibieron dos dosis de la vacuna anti-SARS-CoV-2 desarrollada por la empresa Sinopharm. De ellos, el 52,10 % son de sexo masculino; el 79,50 % tiene más de 42 años, y el 17,90 % manifestó haber tenido COVID-19 antes de ser vacunados (Tabla 1).
En la Tabla 2 se muestra el análisis de los datos correspondientes a la presencia de anticuerpos neutralizantes contra SARS-CoV-2 en los individuos vacunados. El valor de corte considerado para definir la presencia o no de anticuerpos neutralizantes en el suero es 10 UA/mL, mientras que el valor máximo reportado en la base de datos fue de 600 UA/mL. Se observa que el 47,90 % de los individuos vacunados no desarrollaron anticuerpos neutralizantes contra el nuevo coronavirus.
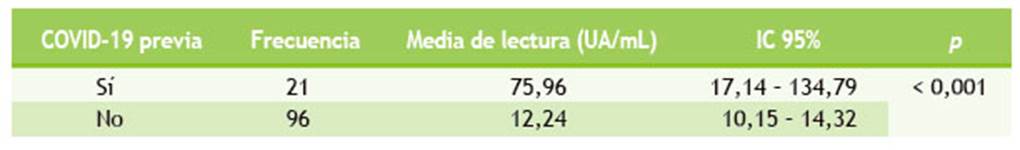
Tabla 2 Presencia de anticuerpos neutralizantes en individuos con o sin diagnóstico de COVID-19 antes de la vacunación
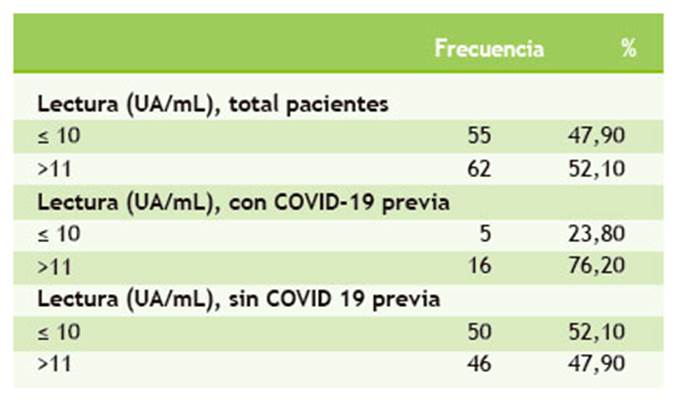
Al comparar la presencia de anticuerpos neutralizantes en el suero de individuos vacunados que habían sido o no diagnosticados con COVID-19, se detectó una mayor frecuencia de individuos con anticuerpos neutralizantes en el grupo con diagnóstico previo de COVID-19 (76,20 % vs. 47,90 %).
Se comparó el valor de los anticuerpos neutralizantes cuantificados en individuos con o sin diagnóstico previo de COVID-19 y, como se observa en la Tabla 3, hay una diferencia estadísticamente significativa a favor de los individuos que tuvieron COVID-19 antes de ser vacunados (p < 0,001).
DISCUSIÓN
El rol crucial de los profesionales de la salud en el manejo de la pandemia por SARS-CoV-2 es innegable, y por ello se denomina a este grupo como personal de primera línea. En consecuencia, es sumamente importante garantizar que su trabajo continúe para cumplir, de manera óptima, la invaluable labor de prevención y atención de los enfermos. Las infecciones del personal sanitario contraídas durante el trabajo se han descrito desde el inicio de la pandemia y han provocado intensas discusiones sobre el equipo de protección personal (EPP) adecuado 15, tal como reportan Wu et al., cuyo trabajo muestra una tasa de infección del 3,80 % entre los profesionales de la salud en Wuhan, China 16.
En todo el mundo, la vacunación masiva para inmunizar a la población contra el virus SARS-CoV-2 es una estrategia muy importante para controlar la pandemia y reducir la morbimortalidad asociada. En este sentido, diversas plataformas vacunales han sido la base para el desarrollo de productos contra este virus, y han empleado material genético (ARN y ADN), antígenos (proteina S) y virus inactivados 3. Instituciones como Pfizer, Moderna, AstraZeneca, Gamaleya, Johnson & Johnson y Sinopharm lideran el escalado productivo de vacunas y su distribución mundial 4.
A la fecha, en el Perú, un poco más de 1,3 millones de personas han recibido al menos dos dosis de alguna de las vacunas contra SARS-CoV-2; y cerca de 3 millones, al menos una dosis 17. En la mayoría de los casos, los profesionales sanitarios han sido inmunizados con el producto de la empresa china Sinopharm 10. La Organización Mundial de la Salud (OMS) reporta que esta vacuna ha demostrado un adecuado perfil de seguridad y una eficacia cercana al 80 %, lo que ha impulsado su uso en todo el mundo 12. No obstante, se ha planteado la necesidad de varias dosis de reforzamiento para incrementar su inmunogenicidad a largo plazo 18.
La vacuna de Sinopharm fue desarrollada a partir de una variante viral inactivada con la droga β-propionolactona 13.
Las vacunas que utilizan esta plataforma vacunal inducen la respuesta inmune contra diferentes antígenos virales, Aunque, por lo regular, son necesarias múltiples dosis para generar una respuesta de memoria de larga duración. Estos productos se caracterizan por su seguridad, fácil manipulación y almacenamiento, y por tener bajos costos de producción 4.
La información de la base de datos del Centro Gamma Médica Servicios Médicos incluye los valores de la concentración de anticuerpos neutralizantes en el suero de 117 profesionales sanitarios que recibieron dos dosis de la vacuna Sinopharm. Encontramos un porcentaje mayor de personas con anticuerpos neutralizantes en el grupo que había sido previamente diagnosticado con COVID-19. Así mismo, al comparar la concentración de estos anticuerpos (expresada como UA/mL) en las personas vacunadas que habían padecido o no COVID-19 antes de la vacunación, el valor resulta significativamente más alto en los que habían tenido la enfermedad.
Las vacunas fabricadas a partir de patógenos completos, como la desarrollada por Sinopharm, pueden enfrentar al sistema inmune a todo el mundo antigénico del microorganismo. Es decir que, a diferencia de otras vacunas 19,20, la respuesta inmune que induce no está focalizada en antígenos directamente ligados a la infección, como la proteína S. Haber padecido COVID-19 antes de ser vacunado estimula la actividad del sistema inmune, lo cual es reforzado luego por la propia vacunación. De alguna manera, en los individuos que han tenido COVID-19, una vacuna que incluya todos los antígenos virales se comportaría como dosis de reforzamiento tras la infección natural. El resultado de este estudio es valioso y apunta a la necesidad de incluir una dosis adicional de esta vacuna, sobre todo en el personal de alto riesgo