Introducción
La disponibilidad y el tipo de alimento juegan un rol importante en las relaciones ecológicas de los animales (Dure 1998, Belver & Avila 2002), condicionando su biología, y por ende su distribución y evolución (Pianka 1982, Pincheira 2008). Los organismos seleccionan su alimento de acuerdo con las características morfológicas, fisiológicas y adaptativas adquiridas a lo largo de su evolución (Pough et al. 2001), encontrándose especies que consumen poca variedad de ítems alimenticios (especialistas) y otras una amplia variedad (generalistas) (Meyers & Herrel 2005). Asimismo, la dieta condiciona el comportamiento de los organismos, por lo que su estudio es una herramienta fundamental en la elaboración de proyectos de conservación y/o manejo de las especies (Reed 2002).
El género Liolaemus es un grupo de lagartijas sudamericanas distribuidos en los territorios de Argentina, Bolivia, Brasil, Chile, Paraguay, Perú y Uruguay (Pincheira et al. 2008). Actualmente se conocen 272 especies, de las cuales 62 constituyen el grupo L. montanus (Pincheira et al. 2008, Lobo et al. 2010, Aguilar et al. 2017c, Aguilar et al. 2018, Aguilar et al. 2019, Uetz 2020). Este grupo se encuentra ampliamente distribuido a lo largo de los Andes del centro y sur del Perú, alcanzando los territorios de Bolivia, Chile y Argentina (Pincheira 2008, Aguilar et al. 2017c).
El grupo Liolaemus montanus posee una fuerte tendencia a consumir componentes vegetales, habiéndose registrado hasta la fecha veintiséis especies omnívoras, siete herbívoras, y once artropófagas (Pincheira 2008, Abdala et al. 2013). Para el Perú se cuenta con información para cinco especies artropófagas: L. insolitus Cei y Péfaur 1982 (50 - 264 m de altitud); L. poconchilensis Valladares 2004 (750 - 1150 m); L. etheridgei Laurent 1998 (2400 - 4269 m), L. evaristoi Gutiérrez et al. 2018 (4395 m) y L. qalaywa Chaparro et al. 2020; y tres omnívoras: L. annectens Boulenger 1901 (3500 - 4688 m); L. signifer (Duméril & Bribon 1837) (3700 - 4800 m) y L. victormoralesii Aguilar et al. 2019 (4175 - 4252 m) (Cei 1993, Pincheira 2008, Aguilar et al. 2017d, Aguilar et al. 2017b, Gutiérrez et al. 2018, Aguilar et al. 2019).
Liolaemus polystictus Laurent 1992 es una lagartija perteneciente al grupo L. montanus, endémica de los Andes peruanos y distribuida desde la puna de la región Huancavelica hasta los límites con la región Ayacucho, entre los 4043 a 4766 m de altitud (Aguilar 2016a). Esta zona de los Andes peruanos se caracteriza por un clima frio y glacial, con una atmósfera seca, donde las temperaturas son sumamente variables entre el día y la noche, siendo la temperatura media anual de 9.2 °C y el promedio de precipitaciones de 750 mm (INEI 2000).
Liolaemus polystictus presenta actividad diurna, ocupando micro-hábitats pedregosos, aunque ha sido observada, en menor frecuencia, bajo plantas de porte almohadillado. Si bien L. polystictus no se encuentra bajo categoría de amenaza en la lista roja de la Unión Internacional para la Conservación de la Naturaleza (UICN), así como tampoco en la lista de protección de especies de fauna amenazada protegidas por la legislación peruana (Decreto Supremo 004-2014-MINAGRI), sus poblaciones se encuentran en constante amenaza por el desarrollo de la agricultura, ganadería y la actual situación de calentamiento global (Aguilar 2016a); sumado a ello su distribución coincide con varias concesiones mineras, por lo cual es preocupante la poca información ecológica con la que se cuenta. Es por ello que el presente trabajo busca obtener información ecológica sobre la especie, específicamente caracterizando la dieta de L. polystictus, para lo cual se trabajó a lo largo de su distribución, alcanzando incluso los 5100 m de altitud.
Material y métodos
El trabajo de campo se realizó en las provincias de Castrovirreyna (Abra Chonta, 13°04’45.8"S, 75°03’03.3"W) y Huancavelica (Abra Huayraccasa, 13°04’52.4"S, 75°01’42.4"W) en la región Huancavelica, Perú, durante agosto del 2017. Los individuos fueron avistados durante la remoción de piedras y/o vegetación de porte almohadillado, siendo capturados manualmente. El horario de muestreo dependió de las condiciones climáticas en la puna durante la temporada húmeda, entre las 09:00 y 14:00 horas, el cual coincidió con la actividad de la especie, ya que durante la tarde las fuertes lluvias y granizadas impedían la evaluación y la actividad de la lagartija. Sin embargo, los reptiles por su condición ectotérmica presentan metabolismo lento (Andrade 2016), por lo cual la digestión tarda varios días en realizarse, permitiendo encontrarse el contenido estomacal, en la mayoría de los casos, completo. Posteriormente, fueron sacrificados con 0.1 mL de Pentobarbital sódico (Halatal), y sus estómagos extraídos. Los especímenes fueron fijados en formalina al 10%, mientras que sus estómagos en etanol al 70%. Todas las muestras fueron depositadas en el Departamento de Herpetología del Museo de Historia Natural de la Universidad Nacional Mayor de San Marcos (MUSM).
Asimismo también, fueron considerados datos de medidas biométricas y de los contenidos estomacales de 41 individuos depositados en el Departamento de Herpetología del MUSM. Estas muestras fueron colectadas en las provincias de Huancavelica, en marzo del 2015 y Huaytara (13°20’6.39"S y 74°56’55.50"W) en noviembre del 2006 y 2015, ambas localidades pertenecientes a la región Huancavelica. La captura de estos individuos dependió del horario de las condiciones climáticas, siendo los periodos de colecta principalmente por las mañanas; sin embargo, como se indicó anteriormente, la digestión en los reptiles es lenta, permitiendo encontrarse contenidos estomacales en buen estado. A los individuos provenientes de la colección de herpetología del MUSM, se procedió a retirar sus estómagos y se volvió a fijarlos con etanol al 70%.
Si bien fueron analizados individuos de diferentes poblaciones, el análisis se basó en la caracterización general de la dieta de la especie; ello debido, a la baja cantidad de individuos colectados por localidad.
Se tomaron medidas biométricas de boca-cloaca (SVL), ancho de la cabeza (AC) y de longitud mandibular (LM), con ayuda de un vernier de 0.1mm de precisión, y se determinó el sexo por la presencia de poros precloacales más desarrollados en los machos que las hembras, y también por un patrón de coloración anaranjado intenso en el vientre de los machos que no se observa en las hembras.
Los estómagos fueron disectados y su contenido analizado en el laboratorio de Zoología de la Facultad de Ciencias Biológicas de la Universidad Nacional Mayor de San Marcos (UNMSM), para ello se empleó un estereos copio Leica EZ4 HD, con el fin de identificar y cuantificar todos los ítems alimentarios observados. En caso de las medidas, largo (L) y ancho (A), se empleó el software LAS EZ 3.4 DVD 272 (Leica Microsystems) y la unidad de medida empleada fueron los milímetros. Los artrópodos fueron identificados hasta el nivel de Orden y sus volúmenes determinados considerando cada ítem como un esferoide (Dunham 1983), donde el volumenfue igual a 4/3π(0.5L)(0.5A)2mm3. Para la determinación del volumen vegetal se procedió a la técnica empleada por Semhan y Halloy (2016), la cual consiste en formar mecánicamente un esferoide compacto con el fin de poder tomar medidas de ancho y largo, y calcular el volumen similar al material animal. No se determinó el contenido vegetal hasta familia o especie por no encontrarse estructuras completas que permitan su identificación, específicamente de aquellas provenientes de individuos de la colección de herpetología del MUSM; locual sesgó el estudio al observar las proporciones entre el contenido animal y vegetal.
La caracterización de los ítems alimentarios se realizó mediante el cálculo del índice de importancia relativa (IRI; Pinkas et al. 1971), a partir de la obtención de los porcentajes N (N%), frecuencias de ocurrencias F(FO%) y porcentajes volumétricos V (V%) de cada ítemalimentario, considerando para el fin únicamente elmaterial animal. El índice IRI fue propuesto por Pinkaset al. (1971) como AL/ ΣAL; dónde AL=(N% + V%) xFO%, el valor resultante de encontrarse incluido entreel 100 y 75% es considerado fundamental, si es entre el75 y 50% se considera secundario, mientras que si seubica entre el 25 y 50% es considerado accesorio, valores menores se consideran ítems accidentales (Montori1991). Adicionalmente, caracterizamos la dieta por elporcentaje de material vegetal consumido, siendo aplicado los valores propuestos por Espinoza et al. (2004)como: 0-10%, artropófago; 11 - 50%, omnívoro; y del51 - 100%, herbívoro.
Para los análisis estadísticos, previamente se realizóla prueba de bondad de ajuste de Kolmogorov; como resultado de esta prueba la distribución de los valores dela variable "número total de presas consumidas" no seajustaron a un modelo normal, tanto para machos (z=0.58; p= 0.0026) y hembras (z= 0.70; p= 0.0001) comopara juveniles (z= 0.74; p<0.0001). Lo mismo ocurriópara el "contenido volumétrico vegetal" entre adultos(machos y hembras; z= 0.50; p<0.0001) y juveniles (z=0.50; p= <0.0004); y entre machos (z=0.55; p=0.0005),hembras (z=0.50; p<0.0001) y juveniles (z= 0.50; p=0.0004). De la misma manera para el "ancho de la cabeza" en machos (z= 1; p= <0.0001) y en hembras (z= 1;p= <0.0001). Por lo cual se optó en todos los casos poremplear la prueba no paramétrica de Wilcoxon, la cuales análoga a la prueba paramétrica T-Student, siendoespecífica para muestras pequeñas (Bellera et al. 2010).
Adicionalmente, se determinó la amplitud de nicho trófico (Nb) mediante el índice de Levins (Dure 1998), donde Nb= (Σ Pi j 2)-1 y Pij es la proporción del número deveces que apareció el ítem presa i en la muestra total j.
Para observar la posible relación entre el tamaño de la cabeza y el cuerpo con las presas consumidas, se empleó la correlación de Sperman, ello debido a que de acuerdo con la prueba de bondad de ajuste de Kolmogorov, las variables empleadas no se ajustaron a una distribución normal. La correlación se realizó entre la longitud, ancho y volumen máximo de los ítems alimentarios, con el ancho de la cabeza, la longitud mandibular y la longitud hocico-cloaca. Esta prueba se realizó para toda la muestra; y entre machos, hembras y juveniles. Todas las pruebas estadísticas fueron evaluadas con el paquete libre Infostaf/L versión 2017 (Universidad Nacional de Córdova 2017) con un nivel de significancia de 0.05.
Adicionalmente, realizamos una compilación bibliográfica respecto a la distribución y dieta de las especies del grupo Liolaemus montanus. La cual fue complementada con información brindada por La Unión Internacional para la Conservación de la Naturaleza (UICN).
Resultados
En total se colectó trece individuos de Liolaemus polystictus, dos de ellos sobre los 5000 m de altitud, adicionalmente, empleamos 41 especímenes de la colección herpetológica del MUSM. En total la muestra estuvo constituida por 14 machos (SVL= 75.24 ± 5.42 mm), 23 hembras (SVL= 62.37 ± 5.66mm) y 17 juveniles (SVL=55.64 ± 6.28mm). Del total de muestras analizadas únicamente dos estómagos se encontraron vacíos.
Se reportaron diez ítems alimentarios del tipo animal en los estómagos de L. polystictus (Tabla 1 y Tabla2), de los cuales los órdenes Coleoptera (N%= 32.05,FO%= 59.26, V%= 41.36), Hymenoptera (N%= 19.23,FO%= 38.89, V%= 13.81) y Diptera (N%= 16.67, FO%=42.59; V%= 10.96) constituyeron los principales alimentos tanto por su frecuencia, número de ítems y porcentaje volumétrico (Tabla 1). Sin embargo, al analizarlos datos en conjunto con el material vegetal (FO%=77.78, V%= 77.03), los valores para el contenido volumétrico animal se redujeron considerablemente (Tabla1 y Tabla 2); donde Coleoptera (N%= 32.05; V%= 9.50),Hymenoptera (N%= 19.23, V%= 3.17) y Diptera (N%=16.67, V%= 2.52) pasaron a ser relegados por el contenido volumétrico vegetal. Estos resultados muestran que L. polystictus (V%= 77.03) es una especie con tendencia a la herbivoría.
Tabla 1 Composición de la dieta de Liolaemus polystictus (n= 54) para machos, hembras y juveniles. %N= número total de presas en porcentaje, %FO= frecuencia de ocurrencia en el total de estómagos en porcentaje, %Vol.= porcentaje volumétrico de las presas.
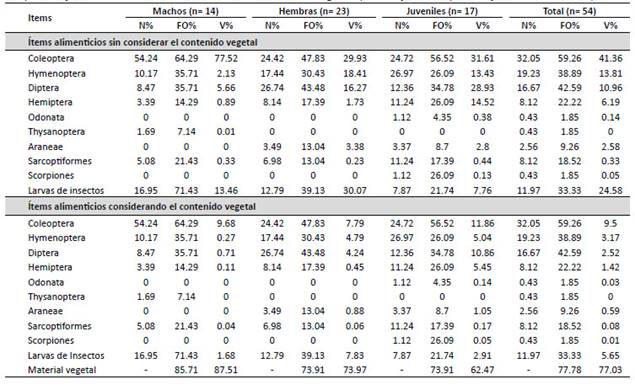
Tabla 2 Composición de Ítems alimentarios animales de Liolaemus polystictus (n= 54), para machos, hembras y juveniles. IRI= Índice de importancia relativa.
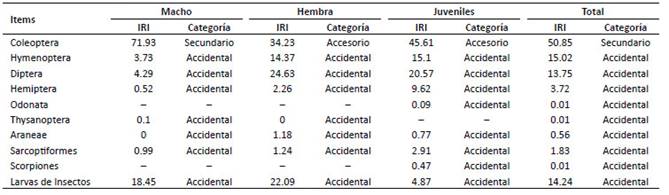
De la revisión de los 14 estómagos en machos, 11 presentaron contenido volumétrico vegetal superior al 70% respecto al contenido animal; de los tres restantes, uno no presentó contenido vegetal ni animal, el segundo no presentó contenido vegetal, pero sí animal, y el tercero obtuvo un porcentaje de 1.1% de contenido vegetal. En el caso de las hembras, de los 23 estómagos revisados, diez presentaron contenido volumétrico vegetal superior al 70% respecto al contenido animal, cinco presentaron contenido volumétrico vegetal inferior al 55% y ocho no presentaron contenido vegetal. Mientras que, en el caso de los juveniles, de los diecisiete estómagos revisados, doce presentaron contenido volumétrico vegetal superior al 60% respecto al contenido animal, cuatro inferiores al 40% y uno no presentó contenido vegetal. En total, de 54 estómagos revisados, se reportaron 33 con contenido volumétrico vegetal superior al 60%. Asimismo, para el análisis global del acumulado de contenidos volumétricos vegetales, en machos se reportó el 87.5%, en hembras el 74% y en juveniles el 62.5%, superando en todos los casos el 60%. Esto indica la preferencia por el consumo de plantas, tanto para individuos de sexos distintos como para individuos de diferentes estadios etarios. Si bien, aparentemente los adultos estarían consumiendo mayor contenido vegetal, bajo las pruebas estadísticas realizadas no se reportó diferencias en los contenidos volumétricos vegetales (Wilcoxon; W= 500.50; NAxJ =54, p= 0.5371); sin embargo, si se reportó diferencias entre los contenidos volumétricos vegetales entre hembras y machos, siendo mayor en machos (Wilcoxon; W= 339; NHxM =37, p= 0.0210) (Tabla 1). De acuerdo con los valores de los índices de importancia relativa (IRI), ningún ítem alimenticio obtuvo la categoría de fundamental, siendo la única de relevancia Coleóptera (IRI= 50.85) como un alimento del tipo secundario (Tabla 2).
Este valor se soporta en los IRIs de Coleoptera obtenidos para machos (IRI= 71.93; secundario) en contraste con las de las hembras (IRI= 34.23; accesorio) y juveniles (IRI= 45.61; accesorio).
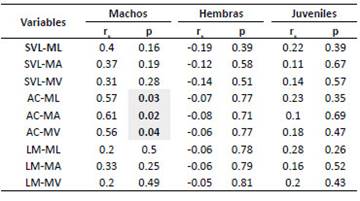
No se reportaron diferencias respecto al número total de presas consumidas entre machos y hembras (Wilcoxon; W= -1.53; NM x H=10, p= 0.17), machos y juveniles (Wilcoxon; W= -1.23; NM x J=10; p= 0.28) y hembras y juveniles (Wilcoxon; W= -1.02; NHx J=10, p= 0.35), por lo que aparentemente tendrían la misma disponibilidad y probabilidad de obtención de alimentos. Sin embargo, la amplitud de nicho trófico, respecto al número total de presas consumidas, fue para machos (NB= 0.50) ligeramente menor que para hembras (NB= 0.78) y juveniles (NB= 0.78). Por otro lado, los datos biométricos no mostraron relación con el tamaño y volumen de las presas consumidas tanto para machos, hembras como juveniles, con excepción del ancho de la cabeza (AC) en machos, donde hubo correlación con la máxima longitud de la presa (AC-ML: rs = 0.57, p= 0.03), máximo ancho de la presa (AC-MA: rs= 0.61, p= 0.02) y con el máximo volumen de la presa (AC-MV: rs= 0.56, p= 0.04) (Tabla 3).
Tabla 3 Correlación de Spearman entre medidas biométricas de Liolaemus polystictus y valores máximos de ancho, longitud y volumen de presas. SVL= Longitud hocico-cloaca, AC= Ancho de la cabeza, LM= Longitud de la mandíbula; ML= Máxima longitud de la presa, MA= Máximo ancho de la presa, MV= Máximo volumen de la presa. rs= Correlación de Spearman. Valores de p < 0.05 se muestran en negritas.
Además, los machos presentaron el ancho de la cabeza (AC) mayor que el de las hembras (Wilcoxon; W= 427; NM x H=47, p < 0.0001) .
A partir de la recopilación de datos bibliográficos, se reportaron 59 especies de Liolaemus pertenecientes al grupo L. montanus, de las cuales ocho fueron herbívoras, nueve artropófagas, 24 omnívoras, y 18 especies no cuentan con información de su dieta.
Discusión
Los resultados obtenidos muestran que Liolaemus polystictus es una especie con tendencia hacia la herbivoría. Asimismo, la dieta concuerda con los hábitos alimenticios de las especies del género Liolaemus, los cuales consumen cantidades considerables de material vegetal (Espinoza et al. 2004, Abdala et al. 2013), siendo en su mayoría omnívoros (Pincheira 2008). Además, se conoce para el grupo L. montanus siete especies herbívoras: L. cazianiaeLobo et al. 2010; L. huayra Abdala et al. 2008; L. inti Abdala et al. 2008; L. orientalis Müller 1924; L. pulcherrimusLaurent 1992 (Abdala et al. 2012), L. huacahuasicus (Halloy & Laurent 1988) y L. molinaei (Valladares et al. 2002). En estas especies, si bien se reportaron cantidades de contenido animal (artrópodos), estas fueron en porcentajes medios a bajos. Pough (1973), Zimmerman y Tracy (1989) y Wilson y Lee (2016) indican que la condición herbívora es incompatible con organismos pequeños, de hábitats fríos y que además posean temperaturas corporales bajas. Sin embargo, es probable que L. polystictus esté seleccionando este tipo de alimento, debido a que en la ecorregión Puna (>3800 msnm, Brack 1986) existe limitada disponibilidad de artrópodos (Hurtubia & Di Castri 1973, Gonzalez et al. 2012, Guo et al. 2013), obligándolos a consumir material vegetal. Adicional a ello, una adaptación de los Liolaemus para sobrevivir a elevadas altitudes y latitudes es el tamaño corporal reducido, el cual permite el calentamiento corporal más rápido durante las horas de mayor disponibilidad térmica, facilitando el alcance de temperaturas corporales altas y con ello la posibilidad de poder digerir material vegetal (Espinoza et al. 2004).
Respecto al contenido animal consumido por L polysticus, el orden Coleoptera fue el más representativo,especialmente para los machos. Ello se debe, a que losescarabajos e insectos en general, tienden a desplazarsemenos en ambientes fríos (Strathdee & Bale, 1998), porlo cual se facilita su captura por medio del forrajeo pasivo(sit and wait). Por otro lado, no se reportaron diferenciasen los tipos de ítems alimenticios empleados por machos,hembras y juveniles, infiriéndose que los recursos alimenticios no presentan diferencia en disponibilidad, nipor estadio etéreo ni por sexo. En contraste, sí se reportaron diferencias entre machos y hembras con respectoal contenido volumétrico vegetal, pero no entre estadiosetéreos. Ello puede deberse a la mayor tasa de crecimiento de los juveniles, los cuales requieren mayores cantidades proteínicas (Andrews 1976, Stamps et al. 2013).
El nicho trófico para machos (NB= 0.50) fue relativamente más bajo que para hembras y juveniles (ambos con NB= 0.78), ello debido al alto porcentaje volumétrico de coleópteros reportados en comparación al resto de ítems alimentarios; sin embargo, en términos generales los valores fueron bajos. De acuerdo con Gonzalez et al. (2012) y Guo et al. (2013), la diversidad de artrópodos se reduce a elevadas altitudes, y ello se refleja en el menor consumo de invertebrados en especies de Liolaemus del grupo montanus. Por otro lado, la correlación entre el ancho de la cabeza (AC) en machos con las máximas medidas de las presas (MA, ML y MV), puede deberse también al mayor consumo de coleópteros. Al parecer, los Liolaemus machos poseen cabezas más anchas que las hembras, y ello les permitiría capturar presas más grandes (Vanhooydonck et al. 2010), como los coleópteros.
En general, las lagartijas del grupo Liolaemus montanus muestran una dieta con considerable consumo de material vegetal, especialmente las distribuidas sobre los 4000 msnm que en su mayoría son omnívoras y herbívoras (Tabla 4) (Pincheira et al. 2008; Espinoza et al. 2004). El aumento del consumo vegetal con la altura apoya lo hipotetizado por Espinoza et al. (2004), sugiriendo que la menor disponibilidad, quien alega que la menor disponibilidad de artrópodos en las punas impulsa al grupo a buscar otras alternativas alimentarias. Además, para Espinoza et al. (2004) el tamaño corporal es una importante adaptación para la obtención de recursos térmicos y con ello la mejor digestión de material vegetal. Siguiendo la hipótesis de Espinoza et al. (2004), se podría suponer una probable relación directa entre el tamaño corporal de las especies del grupo L. montanus y la altura, asimismo, un mayor grado de consumo de material vegetal con la altura. Específicamente si nos referimos al tamaño corporal, se podría hipotetizar que a elevadas altitudes sería beneficioso ser de mayor tamaño, en relación con otras especies de lagartijas del mismo grupo que viven a elevaciones menores, ya que permitiría la mayor retención de calor y con ello facilitaría la digestión de material vegetal. De manera análoga, se podría hipotetizar que el tipo de dieta de otros grupos de lagartijas simpátridas más pequeñas como por ejemplo los del clado L. walkeri y grupo L. alticolor, serían principalmente insectívoras debido a que no llegan a alcanzar las distribuciones altitudinales del grupo L. montanus, pero sí están presentes a elevaciones menores (Aguilar et al. 2013; Aguilar et al. 2017c).
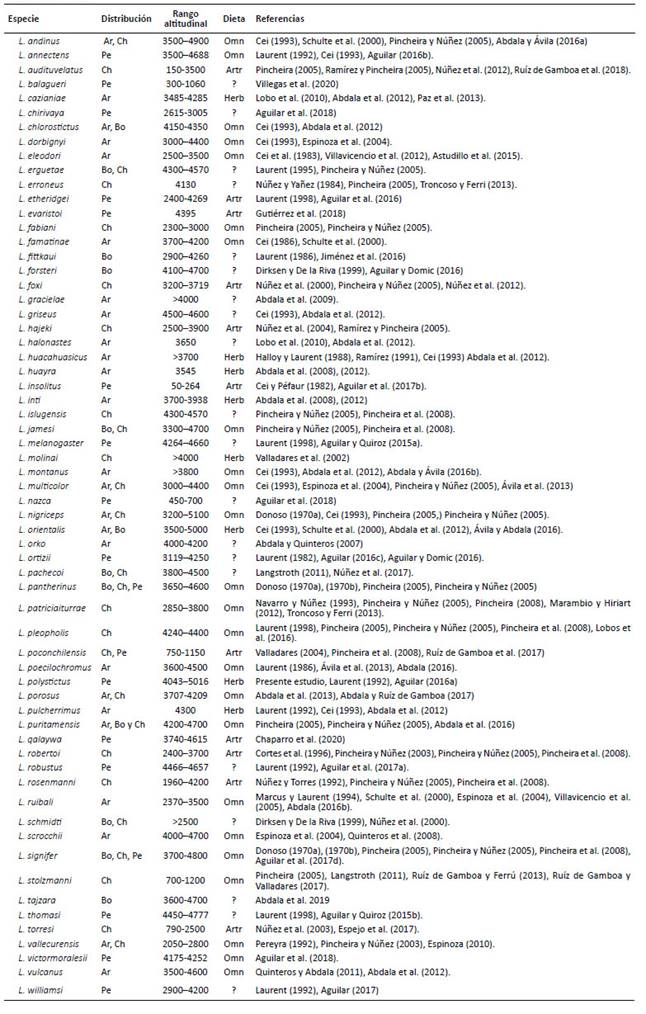
Tabla 4 Distribución y patrones de dieta en las especies del grupo Liolaemus montanus. Abreviaciones para países son Argentina (Ar), Bolivia (Bo), Chile (Ch) y Perú (Pe). La tabla es una adaptación de los datos proveídos por Pincheira et al. (2008), la cual ha sido actualizada hasta el año 2020.












 uBio
uBio 


