Introducción
La placenta que se encuentra anormalmente adherida al útero y que no logra separarse espontáneamente luego del nacimiento del feto, abarca una amplia variedad de presentaciones; por lo que, en la actualidad, se la denomina espectro de placenta acreta (EPA) 1. El EPA consiste en la inserción anormal de parte o toda la placenta, con ausencia total o parcial de la decidua basal, anormalidad de la caduca verdadera y penetración de las vellosidades coriales al miometrio2. La morbimortalidad materna puede ocurrir por hemorragia grave. Las pacientes con EPA son más propensas a requerir histerectomía obstétrica y estancias hospitalarias prolongadas3). Las tasas de EPA están aumentando; los estudios observacionales a partir de los años 1970 y 1980 describen la prevalencia de la placenta adherida entre 1 en 2 510 y 1 en 4 017, en comparación con una tasa de 1 en 533 entre 1982 y 20024. Este aumento es probablemente secundario a la tasa creciente de cesáreas; en los EE. UU. se incrementó de 5% en 1970 a 32,8% en 20105.
Hay varios factores de riesgo para el EPA: cesárea previa, placenta previa, edad materna mayor de 35 años y multiparidad. En una revisión sistemática, la tasa de EPA aumentó de 0,3% en las mujeres con una cesárea previa a 6,74% en las mujeres con cinco o más cesáreas6.
Existen tres variedades de EPA: acreta (sin penetración al miometrio), increta (con penetración el miometrio) y percreta (que sobrepasa la serosa uterina). Por su extensión, se las reconoce como: focal (pequeñas áreas placentarias), parcial (uno o más cotiledones adheridos) y total (toda la placenta anormalmente adherida).
La hipótesis de la etiología del EPA es que un defecto de la interfaz endometrio-miometrio conduce al fracaso de la decidualización normal en el área de una cicatriz uterina, permitiendo el anclaje placentario anormalmente profundo y la infiltración del trofoblasto7.
El pilar del diagnóstico prenatal sigue siendo el ultrasonido Doppler; la resonancia magnética es coadyuvante en casos aislados(8). El Grupo de Trabajo Europeo para EPA, en el año 20169, propuso la creación de criterios ecográficos diagnósticos a partir de 23 revisiones sistemáticas, siendo los más relevantes la pérdida de la ‘zona clara’, las lagunas placentarias; y en el Doppler color, la hipervasculatura útero-vesical asociada a puentes placentarios.
La confirmación anatomo-patológica al microscopio para EPA es la ausencia de la decidua basal; sin embargo, su diagnóstico no resulta fácil por la distorsión que ocurre en el momento del alumbramiento, salvo que se realice una histerectomía y así se obtenga la muestra del tejido. La Sociedad Internacional para la Placenta Anormalmente Invasiva (SIPAI) 10 reconoce el diagnóstico clínico de EPA según hallazgos reportados por el médico.
El tratamiento universalmente aceptado es la histerectomía abdominal total, aunque ha surgido una corriente conservadora para evitar las complicaciones de la histerectomía y/o preservar la fertilidad. En paciente estable, con sangrado no profuso y previa solicitud materna se puede plantear tratamiento conservador de EPA, dejando la placenta total o parcialmente in situ11. Los procedimientos adicionales para disminuir la morbilidad o acelerar la resorción placentaria no cuentan con ensayos controlados aleatorios que los respalden12.
Un análisis de decisión sugiere que 34 a 35 semanas de gestación son óptimas -dependiendo de la capacidad hospitalariapara manejar las complicaciones neonatales, y por un mayor riesgo de sangrado después de las 36 semanas13. La maduración pulmonar fetal con corticosteroides prenatales es apropiada en mujeres con diagnóstico de EPA14.
Métodos
Para el presente estudio descriptivo, retrospectivo, se realizó la búsqueda de casos de EPA en el registro de pacientes del Departamento de Gineco-Obstetricia del Hospital San Bartolomé, Lima, Perú, hallándose 36 casos atendidos del 01/01/2014 al 31/12/2018. El objetivo fue conocer las características epidemiológicas, quirúrgicas y posquirúrgicas de las pacientes con EPA. Se recabaron las historias clínicas y se recogió información del sistema de historias clínicas electrónicas (SIGHOS y SIP). El diagnóstico de EPA se confirmó con los hallazgos intraoperatorios y/o de anatomía patológica. La información fue sometida a técnicas de estadística descriptiva (cálculo de medias y medidas de tendencia central para variables cuantitativas; frecuencias y porcentajes para variables cualitativas), para lo que se empleó el programa SPSS V22.0 y Excel 2010 para Windows. Se reservó en estricto privado la identidad de cada paciente y no se vulneró el principio de autonomía de las pacientes
Resultados
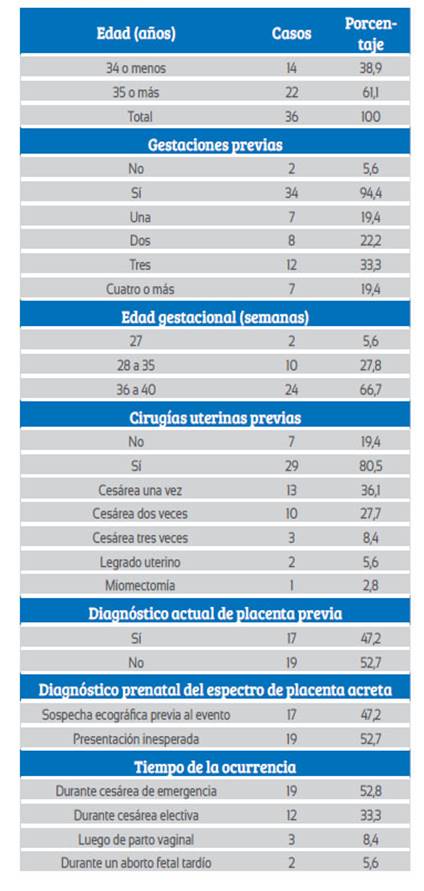
Del total de 30 618 nacimientos atendidos, se presentaron 36 casos de EPA, con tasa de 1,2 casos por mil nacimientos. En la Tabla 1 se detalla las características epidemiológicas de las pacientes, observando que 61% tenía 35 o más años de edad, 94% presentaba al menos un embarazo previo, 66,7% alcanzaron 36 o más semanas de embarazo y 80,6% tenía antecedente de cirugía uterina previa, siendo la cesárea el antecedente más frecuente (72%). El 47,2% tuvo diagnóstico actual de placenta previa, habiendo sido consideradas como casos sospechosos de presentar EPA por los hallazgos ecográficos. La presentación de EPA se produjo inesperadamente en 52,7% durante la cesárea de emergencia por otra causa.
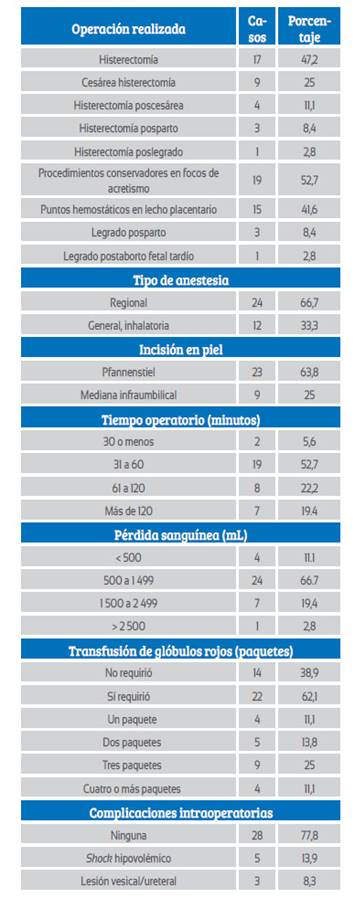
En la Tabla 2 se muestra que 47,2% de las pacientes con EPA terminaron en histerectomía, de las cuales 9 fueron cesáreas-histerectomía (25%), 4 histerectomías poscesárea (11,1%), 3 histerectomías posparto (8,4%) y 1 histerectomía poslegrado uterino (2,8%). Se realizaron procedimientos conservadores en 52,7% de los casos con EPA focal, colocando puntos hemostáticos en el lecho placentario en 19 casos y realizando legrado uterino en 4, logrando controlar la hemorragia. De 32 pacientes sometidas a laparotomía, la incisión fue Pfannenstiel en 63,8%. El tiempo operatorio fue entre 31 y 60 minutos en 52,7%; 77,8% tuvo sangrado menor a 1 500 mL (volumen promedio 1 100 mL), requiriéndose transfusión de paquetes globulares en 62,1%. No registró complicaciones intraoperatorias el 77,8%.
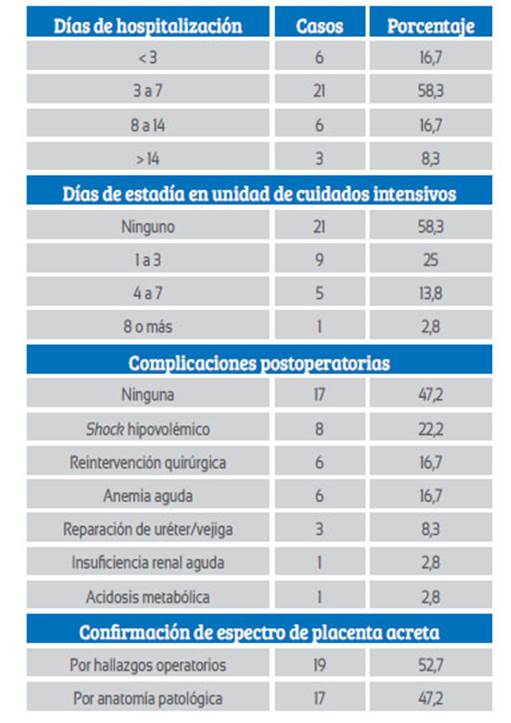
En la Tabla 3 se observa que 58,3% de las pacientes permaneció hospitalizada entre 3 y 7 días, 41,7% ingresó a la UCI, donde 25% se quedó entre 1 y 3 días. Entre las complicaciones posquirúrgicas (52,8%), el shock hipovolémico con 22,2% fue la más frecuente. Los hallazgos operatorios confirmaron el EPA en 52,7% y la histopatología en los 17 casos de histerectomía, de los cuales 15 fueron acreta y 2 increta. No hubo muerte materna relacionada a EPA.
Discusión
La evolución de la obstetricia ha llevado a descubrimientos benéficos y a nuevas enfermedades, como las anomalías de la inserción placentaria. En la actualidad, el EPA es un problema de salud pública debido a su notable aumento en las últimas décadas15. En nuestra serie de casos obtuvimos una tasa de EPA de 1,2/1 000 nacimientos. Gonzales y col. informaron recientemente una incidencia de 1 en 3 42016. El aumento en las tasas de cesáreas en una población tendrá influencia sustancial en el riesgo de acretismo placentario, tanto directa como indirectamente, por mayor riesgo de placenta previa. La tasa de cesárea de nuestro estudio fue 40,6%.
Al analizar las características epidemiológicas de nuestras pacientes, observamos que 94% eran multíparas, 80,5% tenía antecedente de cirugía uterina, 72% cesárea previa, 61% tenía 35 o más años de edad y 47,2% portaba placenta previa. Wu y col.4) encontraron que las tasas de EPA aumentan en conjunto con los partos por cesárea, siendo los factores de riesgo más importantes la cesárea previa (49%) multiparidad (39%), edad materna avanzada (32%) y placenta previa (31%). Para Thurn y col. 17, el factor de riesgo más importante fue la placenta previa (49%). El antecedente de cesárea y el diagnóstico de placenta previa tienen relación muy importante en 88% de los casos con EPA, aumentando en función del número de cesáreas(18). En un metaanálisis se encontró que la tasa de histerectomía, transfusiones de sangre, adherencias y lesiones quirúrgicas incrementó con el número de cesáreas. Así mismo, el riesgo de acretismo placentario aumentó significativamente con dos cesáreas previas18. Se sugiere que el tiempo preferido para el parto en pacientes con evidencia ultrasonográfica de placenta previa y de EPA es a las 34 o 35 semanas de gestación19,20. En nuestra serie, 66,7% alcanzó edad gestacional de 36 o más semanas de embarazo, evidenciando un diagnóstico tardío o ausente hasta el momento del nacimiento: 52,7% se presentó con hemorragia inesperada y durante cesáreas no electivas. No se recomienda esperar más de 36 semanas de gestación, porque aproximadamente la mitad de las pacientes con EPA requiere un parto de emergencia por hemorragia1. Las mujeres con factores de riesgo de placenta previa, cesárea previa, ablación endometrial u otra cirugía uterina, deben someterse a una ecografía en el segundo trimestre para descartar EPA(22). El diagnóstico prenatal permite el parto planificado y, si está indicado, la derivación a un centro con un equipo multidisciplinario experimentado20.
El diagnóstico de EPA durante una cesárea representa casi un tercio de los casos, por lo que se requiere vigilancia intraoperatoria sobre la necesidad de histerectomía de emergencia imprevista23. Nosotros hallamos que 52,7% de los casos fueron de presentación inesperada, terminando en histerectomía en 47,2%. Hernández24 informó que 90,5% requirió histerectomía, a pesar que el tipo de acretismo más frecuente fue el focal (33,3%). De manera similar, Gonzales y col. (16) mencionan que realizaron histerectomías en todos sus casos de EPA. Pero, se encuentra procedimientos conservadores para el manejo de EPA focal y poco profundo en 52,7%, con colocación de puntos hemostáticos del lecho placentario en 41,6%. Wortman y col.(15) señalan que en acretismo focal o parcial que no involucre una gran superficie placentaria se puede realizar el alumbramiento y suturar el lecho placentario.
De 32 pacientes sometidas a laparotomía, se realizó incisión tipo Pfannenstiel en 23. La razón para privilegiar dicha incisión fue para repetir la incisión previa, y que la EPA aún no había sido diagnosticada. La elección de incisión en la piel queda a criterio del operador, aunque muchos usan incisiones verticales para mejor acceso y visualización. Son alternativas razonables las incisiones transversales amplias(1). En nuestra serie, 13 pacientes fueron sometidas a histerectomía; en 7 de ellas se realizó histerotomía corporal, a diferencia de lo recomendado (histerotomía vertical por arriba del nivel de la placenta, evitando disrupciones de la misma para extraer al feto, y posterior histerectomía con la placenta in situ(25). Por otro lado, encontramos una pérdida sanguínea promedio de 1 100 mL, requiriéndose transfusión de paquetes globulares en 62,1%. Gonzales O.(16) comunicó que la media de sangrado fue 2 230 mL y utilizó una cantidad importante de hemoderivados, con media de 5,8 U de paquetes globulares.
Siendo el EPA una patología de elevada morbimortalidad, está asociada a importantes complicaciones intraoperatorias; nosotros las encontramos en 22% de los casos, con shock hipovolémico en 13,9% y lesión ureteral/vesical en 8%. El EPA es la segunda causa de hemorragia obstétrica generadora de morbilidad asociada, representada por coagulación intravascular diseminada, síndrome de dificultad respiratoria del adulto, insuficiencia renal aguda, síndrome de Sheehan y, finalmente, la muerte en 7% de los casos(26). Tradicionalmente, el EPA requiere histerectomía posparto y, a menudo, demanda transfusión sanguínea, ingreso a la unidad de cuidados intensivos (UCI), con estancia hospitalaria prolongada(27). En nuestra serie, el 58,3% permaneció entre 3 y 7 días hospitalizadas, ingresaron a UCI 41,7%, y se presentaron complicaciones posquirúrgicas en 52,8%; el shock hipovolémico (22,2%) fue la complicación más frecuente. El 57,1% mostró complicaciones en el estudio de Hernandez(24). La preparación de toda gestante para una probable hemorragia importante está indicada luego de cualquier embarazo anterior complicado por hemorragia o tratamiento conservador del EPA(28). La confirmación del EPA fue por hallazgos operatorios en 19 casos, y por estudio de anatomía patológica en 17 casos (todas estas histerectomizadas), siendo 15 placenta acreta (88%) y solo 2 placenta increta (12%). Gonzales y col.(16) encontraron acreta 61%, increta 27% y percreta 11%.
En casos de manejo conservador del EPA, es importante ofrecer a las pacientes un método anticonceptivo definitivo (previo consentimiento), para impedir próximos embarazos, pues se ha observado que pacientes con antecedente de EPA y que vuelven a gestar tienen mayor riesgo de rotura uterina, necesidad de cesárea-histerectomía y transfusiones28.
Concluimos que el EPA en nuestra serie estuvo altamente asociado con cesáreas previas. Aunque hubo un número significativo de casos con hemorragia severa y shock hipovolémico, las intervenciones quirúrgicas oportunas y un banco de sangre bien provisto evitaron muertes maternas. El manejo conservador del acretismo focal se mostró como una alternativa válida para evitar la histerectomía y sus complicaciones.