INTRODUCCIÓN
Hylocereus undatus “pitahaya”, es una fruta exótica perteneciente a la familia de las Cactaceae, es nativa de las zonas tropicales de México, América del sur y América central, la cual luego fue introducida y cultivada en el Asia y Medio Oriente (Ortiz & Carrillo, 2012; PromPerú, 2017; Trivellini et al., 2020; Vite, 2014; Zamora, 2018).
Actualmente en el Perú se cuenta actualmente con 750 a 800 hectáreas de pitahaya, las cuales se duplican cada año debido a la demanda creciente, por otro lado es evidente su buen desarrollo y producción en suelos arenosos de la costa peruana desde los 0 msnm hasta los 1,200 msnm ( Abatal et al., 2022; León, 2020; Litardo et al., 2020).
Existen más de 20 variedades de pitahaya que se diferencian por el color de la cáscara (roja, amarilla y verde) y por el color de la pulpa (roja, rosada y blanca) (Ministerio de Desarrollo y Riego, 2020; Ochoa et al., 2012). Siendo la variedad de pulpa roja la más preferida en el mercado, por brindar numerosos beneficios para la salud (Pohlan et al., 2007). En su composición nutricional de H. undatus “pitahaya”, destaca la presencia de glucosa, betalaínas, vitaminas C, ácidos orgánicos, fibra soluble dietética, fitoalbúminas y minerales cons-tituyentes. Además de antocianinas, flavonoides betacianinas y betaxantinas de los cuales se ha demostrado su efectividad como potentes anti-oxidantes de alto valor nutricional y de beneficio para la salud (Sotomayor et al., 2019; Tang et al., 2021; Verona et al., 2020; Wichienchot et al., 2010; Wu et al., 2006). A su vez diferentes estudios han demostrado los beneficios de la cascara y la pulpa de la pitahaya para la salud, como la quimio prevención del cáncer, efectos antiinflamatorios y antidiabéticos, y la reducción del riesgo de mortalidad por enfermedades cardiovasculares (Bauer et al., 2017; Cos et al., 2004; Kim et al., 2010; Ribeiro et al., 2021; Stintzing & Carle, 2007). Por otro lado el uso de la pulpa y cascara tiene un alto potencial para su uso en la industria alimentaria, farmacéutica y cosmética (Trivellini et al., 2020).
La propagación de H. undatus “pitahaya”, se realiza empleando semilla botánica o esquejes. El empleo de semilla botánica, en este cultivo presenta una serie de inconvenientes ya que requiere cuidados constantes, su desarrollo es muy lento, la produc-ción de frutos es tardía y con rendimientos muy variables. Por tanto, la propagación vegetativa por esquejes es la que se emplea con mayor frecuencia ya que las plantas propagadas crecen y producen en menor tiempo, garantizándose un mayor estabilidad genética ,la cual se verá reflejada en una buena producción y rentabilidad del cultivo (Colombo, 2019; Garbanzo et al., 2021; Zamora, 2018).
Un esqueje consiste en una porción de tallo, raíz u hoja, a partir del cual se puede formar una planta completa (Raven et al., 1992; Villar et al., 2018). Su longitud puede influir tanto en las reservas de carbohidratos como en el volumen de auxinas endógenas, que proporciona mayor supervivencia, precocidad en la emisión de raíces, el número y tamaño de los brotes (Braga et al., 2006; Lima, 2013). La siembra de esquejes debe realizarse en suelos que ofrezcan las mejores condiciones para el desarrollo de las plantas con pH entre 5,5 y 6,5, ricos en materia orgánica, buen drenaje y una textura suelta (Cabrera et al., 2018; Pollnow, 2018; Zamora, 2018). Las plantas de H. undatus “pitahaya”, originadas por este método comienzan a florecer uno o dos años después de su plantación (Andrade et al., 2007; Cardoso et al., 2011; Marques et al., 2012).
La formación de raíces en la propagación asexual es un proceso complejo, tanto del punto de vista anatómico y fisiológico, la presencia de carbo-hidratos, proteínas, aminoácidos, vitaminas, compuestos fenólicos, otras sustancias y auxinas contribuyen la inducción de raíces adventicia. Las auxinas, citoquininas y particularmente gibere-linas, influyen directamente sobre el inicio de la formación de raíces, ya que proporcionan mayor porcentaje, velocidad, cualidad y uniformidad de enraizamiento, aunque la sensibilidad de las células varía entre especies, dependiendo de un conjunto de factores intrínsecos. Sin embargo, no todas las plantas tienen la capacidad de enraizar espontáneamente, motivo por el cual es necesario aplicar fitohormonas o fitorreguladores que estimulen la formación de raíces. Las auxinas son hormonas reguladoras del crecimiento vegetal por lo que, en dosis muy pequeñas, regulan los procesos fisiológicos de las plantas, entre las más empleadas destaca el ácido indolacético (AIA), el ácido indolbutírico (AIB) y el ácido naftalenacético (ANA) (Bertsouklis et al., 2022; Fontanetti et al., 2021; Maroto, 2008; Xu et al., 2022). La aplicación de auxina exógena en esquejes, es una práctica utilizada para promover y/o mejorar el proceso de rizogénesis. Logrando estimular la iniciación y uniformidad del enraizamiento (Garay et al., 2014; Kumari, 2023; McLeod et al., 2022).
Ante ello se propuso como objetivo de investí-gación determinar el efecto del ácido indolbutírico en la propagación de H. undatus “pitahaya” bajo condiciones de invernadero.
MATERIAL Y MÉTODOS
La investigación se realizó en el Laboratorio de Biotecnología del Instituto de la Papa y Cultivos Andinos de la Facultad de Ciencias Biológicas, Universidad Nacional de Trujillo. El material biológico (esquejes) se obtuvo de plantas madre (plantas de más de un año de edad) existentes en la estación experimental. Las coordenadas de la ciudad universitaria son: 8°06′53″″ S 79°02′19″″O, mientras que las condiciones ambientales en el predio fueron de una humedad relativa de 80 ± 5% y una temperatura de 19 ± 5 °C.
Selección y desinfección de los esquejes de H. undatus “pitahaya”
El sustrato utilizado estuvo compuesto por compost (marca cuatro estaciones) y arena fina (0,05 cm de diámetro) en una proporción de 1:1. Este fue solarizado (30 - 33 °C) por 4 semanas, con la finalidad de elevar la temperatura y destruir la mayoría de patógenos y semillas de malezas que se encuentren en los sustratos (INIA, 2018). Se utilizaron bolsas de 7x12 pulgadas, las cuales se llenaron con sustrato hasta cubrir las dos terceras partes. Se seleccionaron plantas madre sanas (libres de plagas y enfermedades) y vigorosas ubicadas en la estación experimental, de donde se obtuvieron esquejes. Para ello, se utilizó una tijera podadora, previamente desinfección con legía al 1%. Una vez obtenido los esquejes estos fueron desinfectados con fungicida Benzomil en una solución al 1%. Luego los esquejes fueron colocados en un ambiente fresco y ventilado por un periodo de 8 días, con la finalidad de dejar secar las heridas causadas por el corte (Figura 1).
Siembra de los esquejes de H. undatus “pitahaya”
Después de 8 días se procedió a la siembra, para ello se humedeció toda la zona basal del esqueje, para luego poner en contacto con el polvo compuesto por ácido indolbutírico (AIB), empleándose las concentraciones de 0, 5000, 10000 mg/L. Luego se procedió a sembrar los esquejes en las bolsas de 7x12 pulgadas. Considerándose como variables a evaluar el número, longitud y peso de raíces a los 45 días después de la siembra de los esquejes, además de evaluarse el peso y longitud del tallo (Figura 2).
Análisis estadístico
Se utilizó el diseño experimental completamente al azar, evaluándose la longitud de raíz mayor, número de raíces primarias, peso de masa radi-cular, peso seco de la raíz, peso del tallo y longitud del tallo (Figura 2).

Figura 1 Enraizamiento de esquejes de Hylocereus undatus “pitahaya”, a evaluar el efecto del ácido indolbutírico a la concentración de 0, 5000, 10000 mg/L, a los 45 días de siembra.

Figura 2 Esquejes de Hylocereus undatus “pitahaya”, a evaluar el efecto del ácido indolbutírico a la concentración de 0, 5000, 10000 mg/L.
El diseño estuvo conformado por 3 tratamientos y 24 repeticiones, dando un total de 72 unidades experimentales. Los resultados fueron analizados con el software R versión 4.1.2; aplicándose la prueba de Anova de Welch y Post hoc Games-Howell. A su vez se empleó la prueba Post hoc Tukey’s, para identificar el mejor tratamiento.
RESULTADOS Y DISCUSIÓN
Según la Figura 3a, la prueba de Anova de Welch, presentó un p-valor menor mayor que 0,05 (p = 0,117 > 0,05), dando a conocer que no existió diferencia significancia entre los tratamientos para la variable longitud de raíz mayor, del mismo modo para las variables peso y la longitud de tallo.
El p-valor de significancia de la prueba de Anova de Welch, para la variable N° de raíces primarias, resultó ser menor que 0,05 (p = 0,000 < 0,05), demostrándose la existencia de diferencias significativa entre los tratamientos (Figura 3b). Mientras que para la variable peso de masa radicular, según la prueba Post Hoc Games-Howell, no se presentó diferencia significativa entre los tratamientos T1 y T2, siendo el tratamiento T2, quien presentó el mayor peso de masa radicular promedio (Figura 3c).
La generación de raíces abundantes y uniformes es indicador de la influencia del ácido indolbutírico debido a que la concentración endógena de auxinas de los cladodios se encuentra en un nivel inferior, por tanto, la aplicación exógena del ácido indolbutírico (AIB), favorece considerablemente al enraizamiento (Bastos et al., 2006; Ringphawan & Pauline, 2019). Sin embargo, según lo observado en el análisis estadístico para evaluar el efecto del ácido indolbutírico en la propagación de H. undatus “pitahaya” bajo condiciones de invernadero, no se evidenció diferencia significativa en la prueba de Anova de Welch (p = 0,000 < 0,05), para la variable longitud de raíz mayor, peso y la longitud de tallo. Por otro lado, se evidenció la existencia de diferencia significativa para la variable n° de raíces primarias, mientras que para variable peso de masa radicular, no presentó diferencia significativa entre los tratamientos T1 y T2 (Figura 3d). De todo ello se infiere que las concentraciones de 5000, 10000 mg/L de ácido indolbutírico (AIB), no son representativos en generar un efecto significativo en la propagación de H. undatus “pitahaya” bajo condiciones de invernadero (HR: 80 ± 5% y T: 19 ± 5 °C), por tanto, para su propagación no es imprescindible el empleo del ácido indolbutírico (Bozkurt et al., 2020).
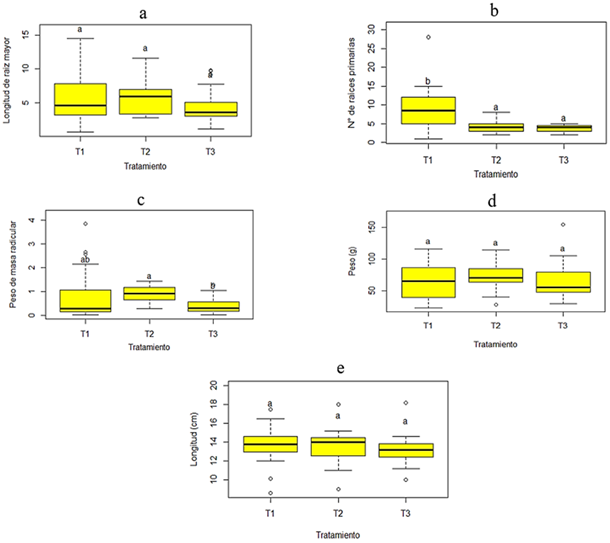
Figura 3 Análisis estadístico para evaluar el efecto del ácido indolbutírico en la propagación de H. undatus “pitahaya” bajo condiciones de invernadero.(a) Longitud de raíz mayor, Anova de Welch, p=0,117 y prueba Post hoc Games-Howell, (b) N° de raíces primarias, Anova de Welch, p=0,000 y prueba Post hoc Games-Howell, (c) Peso de masa radicular, Anova de Welch, p=0,000 y prueba Post hoc Games-Howell, (d) Peso de tallo (g), Anova, p=0,290 y prueba Post hoc Tukey’s, (e) Longitud de tallo (cm), Anova, p=0,656 y prueba Post hoc Tukey’s
Nota: Las letras iguales no presentan diferencia significativa entre los tratamientos.
Sin embargo, investigaciones de Balaguera et al. (2010), demostraron que la dosis de 4,500 mg/L resultó ser favorable para la longitud de raíz de los cladodios, existiendo una relación directamente proporcional con respecto al aumento del AIB. Dicho resultado concuerda con Rodríguez (2019), quién reportó un menor desarrollo radicular empleando menores dosis de AIB a 4000 mg/L, 3000mg/L. A su vez Balaguera et al. (2010), sostiene que al emplear menores concentraciones (0, 1,500, 3,000 mg/L) de AIB en la propagación pitahaya, no evidencian diferencias significativas para cada uno de los tratamientos. Por lo tanto, un buen balance hormonal entre la cantidad y disposición de AIB en el tejido vegetal, estimulan la elongación de células específicas e inhiben el crecimiento de otras Díaz, 2016; Pasqual et al., 2001).
Cabe mencionar que otros enraizaste naturales que han demostrar un efecto favorable en el enraizamiento de H. undatus “pitahaya” son el extracto de Cyperus rotundus L. y el extracto de algas (Binsfeld et al., 2019; Diéguez et al., 2020).
La composición del sustrato estuvo conformado por compost y arena fina en una proporción de 1:1. Investigaciones más recientes hacen hincapié en dejar de prescindir del ácido indolbutírico, ya que factores como el tipo de sustrato son aspectos determinantes en el proceso de enraizamiento como sugiere Malqui (2021), quien afirma que el empleo de Compost 50% + tierra de bosque 50%, y Tierra de bosque 100% es favorable para el desarrollo radicular de la pitahaya. De la misma manera Ortiz (2022), sostiene que el empleo de 3 Arena: 1 Turba: 1 Humus, permite obtener esquejes de pitahaya amarilla enraizados mucho más desarrollados, por tanto los resultados obtenidos se fundamentan en la empleabilidad del humus como agente inductor al enraizamiento , debido a la presencia de ácidos húmicos y fúlvicos (Guaita, 2018). Por otro lado Borini & Assari (2019), sostienen que factores ambientales como la temperatura ≤ 25 °C favorecen el porcentaje de enraizamiento, número de raíces y longitud promedio de raíces (Matías et al., 2019).
CONCLUSIONES
Se concluye que el tratamiento 1, constituido por 0 mg/L de AIB es el mejor, ya que evidencio una mejor respuesta con relación a la longitud de raíz mayor, n° de raíces primarias y peso de masa radicular, de la misma manera para el peso y longitud de tallo de H. undatus “pitahaya”. Por tanto, se recomienda que para su propagación no es necesario el empleo del ácido indolbutírico.












 uBio
uBio 


