INTRODUCCIÓN
Escherichia coli forma parte del microbiota intestinal de la mayoría de las especies animales y del hombre y es uno de los organismos modelo más explorados para la investigación de la evolución y adaptación bacteriana en diferentes condiciones de crecimiento (Kaper et al., 2004; Morales et al., 2007; Alteri y Mobley 2012; Leimbach et al., 2013; Dellepiane y Morales-Cauti, 2018). Este microorganismo puede desarrollarse en diferentes nichos, pudiendo encontrase en los hospederos vivos, el medio ambiente y los alimentos, por lo que también se le considera un indicador de contaminación fecal y, por ende, de prácticas deficientes de higiene (Lucas et al., 2016b; Corzo-Ariyama et al., 2019). Una de las especies bacterianas más versátiles, ya que además de las cepas comensales, presenta cepas específicas que tienen el potencial de causar numerosas patologías intestinales y extraintestinales (Gordon y Cowling, 2003; Morales et al., 2007; Croxen y Finlay, 2010; Tenaillon et al., 2010; Alteri y Mobley, 2012).
La gran versatilidad de E. coli se explica en su alto potencial de recombinación (Tenaillon et al., 2010), lo que resulta, además, en una enorme variabilidad genética, por lo que su tipificación juega un papel crítico en el avance de la comprensión de la evolución (Morales et al., 2017), capacidad de causar enfermedad, transmisión y vigilancia de este microorganismo. La tipificación molecular de E. coli puede ser realizada mediante metodologías como la electroforesis de enzimas multilocus (multilocus enzyme electrophoresis, MLEE), tipificación multilocus de secuencias (Multilocus sequence typing, MLST), por reacción en cadena de la polimerasa (Polymerase chain reaction, PCR) y por la secuenciación del genoma (Clermont et al., 2015).
Se ha demostrado que las cepas de E. coli pueden dividirse en cuatro grupos filogenéticos principales: A, B1, B2 y D. Esta tipificación, además, se relaciona con el carácter virulento de las cepas de E. coli, pues las cepas virulentas extraintestinales (ExPEC) pertenecen principalmente al filogrupo B2 y, en menor medida, al grupo D (Herzer et al., 1990; Clermont et al., 2000, 2015; Wirth et al., 2006; Bok et al., 2020); por otro lado están las cepas que pertenecen a los grupos B1 y A, descritas normalmente como cepas comensales (Bok et al., 2020). Entre los métodos que permiten realizar esta tipificación existe uno que se destaca por su sencillez y rapidez, denominado «método Clermont» (Clermont et al., 2000), el cual se basa en la detección de tres marcadores genéticos (chuA, yjaA y TSPE4.C2) mediante PCR, mostrando una excelente congruencia con métodos de referencia como el MLST en la asignación de filogrupos (Gordon et al., 2008; Clermont et al., 2015).
En la región central de los Andes peruanos, por encima de los 3500 msnm, se desarrolla una crianza de alpacas que resulta crucial en la seguridad alimentaria, ya que estos animales convierten los forrajes silvestres (de limitado potencial nutricional) en recursos de alta calidad como carne y fibra, pero cuyo estado sanitario se ve amenazado por diversos agentes patógenos, entre los que destaca E. coli; patógeno que ha sido involucrado con cuadros severos en las crías de estos animales (Morales et al., 2007, 2017; Lucas et al., 2016a; Rodríguez et al., 2017; Dellepiane y Morales-Cauti, 2018). A pesar de ello, no existen reportes sobre la determinación de grupos filogenéticos en camélidos sudamericanos, por lo que el objetivo del presente estudio fue aplicar el método de Clermont para identificar grupos filogenéticos de las cepas aisladas obtenidas de casos de diarrea en crías de alpaca.
MATERIALES Y MÉTODOS
Lugar de Estudio
La toma de muestras se realizó en las comunidades alpaqueras de Ninacaca, Huayllay y Cochamarca, Pasco, situadas en la sierra central del Perú, por encima de los 3500 msnm. El aislamiento de las cepas se llevó a cabo en el Laboratorio de Microbiología de la Estación Experimental IVITA El Mantaro (Junín, Perú) en febrero y marzo de 2014, y la clasificación filogenética se realizó en la Universidad Autónoma de México en agosto de 2014.
Animales y Muestras
Se evaluaron hisopados rectales de 150 crías de alpacas (105 machos y 45 hembras) de 1-4 meses de edad con cuadros diarreicos. Los hisopos fueron conservados en tubos con medios de transporte bacteriano Stuard (Merck, Alemania) a 4 ºC hasta su remisión y posterior procesamiento en el laboratorio.
Aislamiento de E. coli
El aislamiento de las cepas de E. coli se realizó de forma convencional. Las muestras fueron sembradas directamente en agar MacConkey (Merck, Alemania) a 37 ºC por 24 horas. Los aislados de colonias presuntivas de E. coli fueron identificadas a través de pruebas bioquímicas: indol, motilidad, sulfidrilo, malonato, urea, citrato de Simmons, lisina y orinitina. Las cepas aisladas de E. coli fueron colocadas en agar tripticasa de soya (Merck, Alemania) para su mantenimiento hasta su remisión y ensayos posteriores.
Extracción de ADN
Las cepas de E. coli fueron cultivadas en caldo Luria Bertani (Merck, USA) a 37 ºC por 24 horas. El cultivo (1.5 ml) fue centrifugado a 16 500 g durante 5 minutos, tras lo cual se colocó en baño maría a 100 ºC por 10 minutos. Luego fueron introducidas en frío por 5 minutos para ocasionar una lisis celular por shock térmico. Finalmente se centrifugó a 16 500 g por 5 minutos y se conservó el sobrenadante (que contenía el ADN extraído) de cada muestra para su posterior uso.
Análisis Filogenético
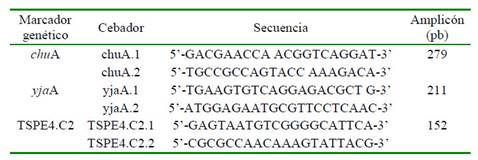
Para la tipificación de E. coli se utilizó el método de Clermont (Clermont et al., 2000), el cual consiste en la amplificación del ADN mediante un PCR triplex. El volumen final de cada ensayo fue de 20 µl, conteniendo 2 µl de buffer tampón 10x, 20 pmol de cada cebador (Cuadro 1), cada uno de los desoxinucleósido trifosfato (dNTPs) al 2 mM, 2.5 U de Taq polimerasa (ATGC Biotechnologie, Francia) y 200 ng del ADN extraído en cada muestra, ajustando el volumen final con agua bidestilada estéril. Las condiciones de los PCR fueron las descritas por Clermont et al. (2000).
Cuadro 1 Cebadores usados para la detección de grupos filogenéticos de E. coli (Clermont et al., 2000)
Análisis de Resultados
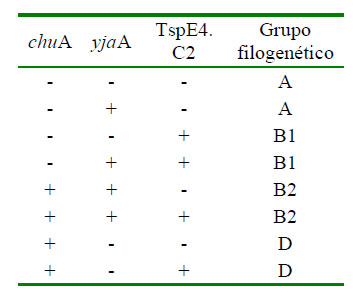
La clasificación filogenética de E. coli se realizó siguiendo el esquema dicotómico realizado por Clermont et al. (2000) con relación a la amplificación de los genes estudiados (Cuadro 2). Los resultados fueron expresados como frecuencias de E. coli pertenecientes a un grupo filogenético (número de muestras positivas / total muestras evaluadas x 100).
RESULTADOS Y DISCUSIÓN
E. coli estuvo presente en el 79.3% (119/150) de los animales con diarrea, pudiendo clasificarse en los grupos filogenéticos A, B1, B2 y D, cuyas frecuencias se muestran en el Cuadro 3.
Cuadro 3 Frecuencia de grupos filogenéticos de E. coli aislados de crías de alpacas (Vicugna pacos) con diarrea

Existen diversos factores que influyen en la prevalencia y densidad de E. coli, pero los principales son el medio ambiente y las características del hospedero vivo (tamaño corporal, morfología intestinal, tiempo de retención de la ingesta y la microflora) (Jang et al., 2017). Una prevalencia similar a la determinada en este estudio es la mostrada por Lucas et al. (2016a), quienes determinaron que este agente estuvo presente en el 80% de los casos fatales de diarrea en crías de alpacas de la sierra central del Perú.
Las infecciones por E. coli en alpacas suelen presentarse como infecciones secundarias, aunque se ha descrito la presencia de algunos patotipos de E. coli diarrogénicos involucrados a trastornos gastrointestinales en estos animales (Cid et al., 2012; Morales et al., 2007, 2017; Luna et al., 2012; Silvera et al., 2012). Las E. coli diarrogénicas podrían pertenecer a cualquiera de los grupos filogenéticos detectados puesto que la transferencia horizontal de genes de virulencia codificados por plásmidos, incluidas las enterotoxinas y los factores de colonización, podría efectuarse entre cepas de diferentes grupos filogenéticos (Gordon et al., 2008; Rúgeles et al., 2010; Løbersli et al., 2012).
Sin embargo, las cepas diarrogénicas, así como las comensales y poco virulentas de E. coli, están asociadas a los grupos A y B1 (Clermont et al., 2000, 2015; Wirth et al., 2006).
Por otro lado, las cepas ExPEC pertenecen principalmente al grupo B2 y en menor proporción al grupo D (Bingen et al., 1994; Boyd y Hartl, 1998; Johnson y Stell, 2000; Escobar-Paìramo et al., 2004; Gordon, 2004). La prevalencia de las infecciones urinarias causadas por cepas ExPEC de E. coli son cada vez más frecuente en muchos países (Clermont et al., 2013). En el presente estudio se evidencia que las cepas ExPEC podrían estar presentes en el 21% de los aislados de E. coli, confirmando a la alpaca como una fuente potencial de estas cepas, y esbozando un posible vínculo con las infecciones extraintestinales de E. coli en el poblador Además, diversos reportes en el Perú han descrito el manejo sanitario deficiente que se hace durante el sacrificio (Morales et al., 2007, 2017; Dellepiane y Morales-Cauti, 2018) y expendio (Lucas et al., 2016b) de la carne de otras especies animales, y que tambien podrían extenderse al comercio de carne de alpaca, por lo que se debería evaluarse la posible transmisión por alimentos de estas cepas.
En el presente estudio también se determinó que el grupo filogenético B1 era el predominante (65.55%), seguido del grupo D, representando los grupos A y B2 menos del 15% de los aislados. No existen reportes sobre la distribución filogenética de E. coli en alpacas, pero es muy particular de esta especie por los ambientes extremos en los que se desarrollan y las características de alimentación muy particulares que presenta. En humanos, las cepas del grupo A son predominantes (40.5%), seguido por cepas del grupo B2(25.5%) (Duriez et al., 2001; EscobarPaìramo et al., 2004; Nowrouzian et al., 2006). En animales predominan las cepas del grupo B1, con una frecuencia hasta de 48.2%, seguidas por A (hasta 48.2%), B2 (hasta 21%) y D (hasta 16%) (Escobar-Paìramo et al., 2004; Gordon y Cowling, 2003; Skurnik et al., 2006; Baldy-Chudzik et al., 2008; Bok et al., 2020). Estas diferencias pueden deberse a características de la especie en términos de morfología y fisiología intestinal; no obstante, los hábitos alimenticios y el nivel de higiene son los principales factores que explican las distribuciones de los grupos filogenéticos en humanos (Gordon et al., 2005; Skurnik et al., 2008; Tenaillon et al., 2010).












 uBio
uBio