INTRODUCCIÓN
El término “acceso vascular” implica tanto el catéter venoso central (CVC), la fístula arterio-venosa (FAV) y el injerto protésico vascular, los cuales son elementos fundamentales para realizar la hemodiálisis 1. La infección asociada al acceso vascular para hemodiálisis crónica ocurre hasta en un 40% de los pacientes que se dializan a través de un CVC permanente 2 y hasta 15 veces más en CVC en comparación con los pacientes que se dializan con FAV 3. Además de ello se reporta que el 50% de los CVC permanentes son cambiados en el primer año por complicaciones infecciosas 4. En consecuencia, debido al menor riesgo de infecciones asociadas al acceso vascular de hemodiálisis, se considera que el primer acceso vascular debe ser una FAV y, en casos en los que haya dificultades anatómicas para su creación, se podría considerar los injertos arteriovenosos de uso temprano 5.
En el Perú, se reporta que, aproximadamente, el 80% de los pacientes ingresan a hemodiálisis con CVC temporal, 15% con un CVC permanente y solo el 5% de los pacientes en hemodiálisis utilizan una FAV como acceso vascular 6. Ello podría deberse a la falta de personal capacitado para su creación o a la imposibilidad de realizar el procedimiento en algunas localizaciones anatómicas 7.
Considerando que el CVC es la modalidad de acceso vascular para hemodiálisis crónica más utilizada en el contexto peruano y que esta modalidad tiene un mayor riesgo de complicaciones infecciosas, el Seguro Social de Salud del Perú (EsSalud) priorizó la realización de la presente guía de práctica clínica (GPC) con el objetivo de brindar recomendaciones para la prevención, diagnóstico y manejo de las infecciones asociadas al acceso vascular de hemodiálisis, y contribuir a la reducción de la morbimortalidad relacionada.
METODOLOGÍA
El procedimiento seguido para la elaboración de la presente GPC está detallado en su versión extensa, la cual puede descargarse de la página web del IETSI de EsSalud (http://www.essalud.gob.pe/ietsi/guias_pract_clini.html). En resumen, se aplicó la siguiente metodología:
Conformación del grupo elaborador de la guía local (GEG): Se conformó un GEG, que incluyó metodólogos, médicos nefrólogos, infectólogos e internistas.
Formulación de preguntas: En concordancia con los objetivos y alcances de esta GPC, el GEG formuló 7 preguntas clínicas (Tabla 1), cada una de las cuales pudo tener una o más preguntas PICO (Population, Intervention, Comparator, Outcome). A su vez, cada pregunta PICO pudo tener uno o más desenlaces (outcomes) de interés.
Búsqueda y selección de la evidencia: Para cada pregunta PICO, se realizó la búsqueda y selección de la evidencia. Para ello, entre noviembre del 2019 y marzo del 2020, se buscó revisiones sistemáticas (RS) publicadas como artículos científicos (mediante búsquedas sistemáticas en PubMed y Central de Cochrane) o realizadas como parte de una GPC previa (mediante una búsqueda sistemática de GPC sobre el tema) (Material suplementario 1). Cuando se encontraron RS de calidad aceptable, se escogió una RS para la toma de decisiones, la cual fue actualizada cuando el GEG lo consideró necesario. Cuando no se encontró ninguna RS de calidad aceptable, se realizó una búsqueda de novo de estudios primarios.
Evaluación de la certeza de la evidencia: La certeza de la evidencia para cada desenlace de cada pregunta PICO pudo ser alta, moderada, baja, o muy baja (Tabla 2). Para evaluar la certeza de la evidencia, se siguió la metodología de Grading of Recommendations Assessment, Development, and Evaluation (GRADE) 8. Para presentar el resumen de los estudios, se usó tablas de resumen de evidencias (Summary of Findings [SoF]) de GRADE.
Formulación de las recomendaciones: El GEG revisó la evidencia seleccionada para cada pregunta clínica en reuniones periódicas, y formuló recomendaciones fuertes o condicionales (Tabla 2) usando la metodología GRADE 8. Para ello, se tuvo en consideración: 1) Beneficios y daños de las opciones, 2) Valores y preferencias de los pacientes, 3) Aceptabilidad por parte de los profesionales de salud, 4) Factibilidad de las opciones en los establecimientos de salud de EsSalud, y 5) Uso de recursos. Luego de discutir estos criterios para cada pregunta, el GEG formuló las recomendaciones por consenso o por mayoría simple. Se le asignó a cada recomendación el nivel de certeza más bajo alcanzado por alguno de los desenlaces críticos de su pregunta.
Puntos de buena práctica clínica: El GEG formuló buenas prácticas clínicas (BPC), usualmente en base a su experiencia clínica. Las BPC se presentan en la Tabla 2 y su justificación se halla disponible en la versión extensa de la presente GPC.
Revisión por expertos externos: La presente GPC fue revisada en reuniones con médicos especialistas representantes de otras instituciones y tomadores de decisiones. Asimismo, su versión extensa fue enviada por vía electrónica a expertos externos para su revisión (mencionados en la sección de agradecimientos). El GEG tuvo en cuenta los resultados de estas revisiones para modificar las recomendaciones finales.
Aprobación de la GPC: La presente GPC fue aprobada para su uso en EsSalud, con Resolución N° 116-IETSI-ESSALUD-2020.
Actualización de la GPC: La presente GPC tiene una vigencia de tres años. Al acercarse al fin de este período, se procederá a realizar una RS de la literatura para su actualización, luego de la cual se decidirá si se actualiza la presente GPC o se procede a realizar una nueva versión.
Recomendaciones
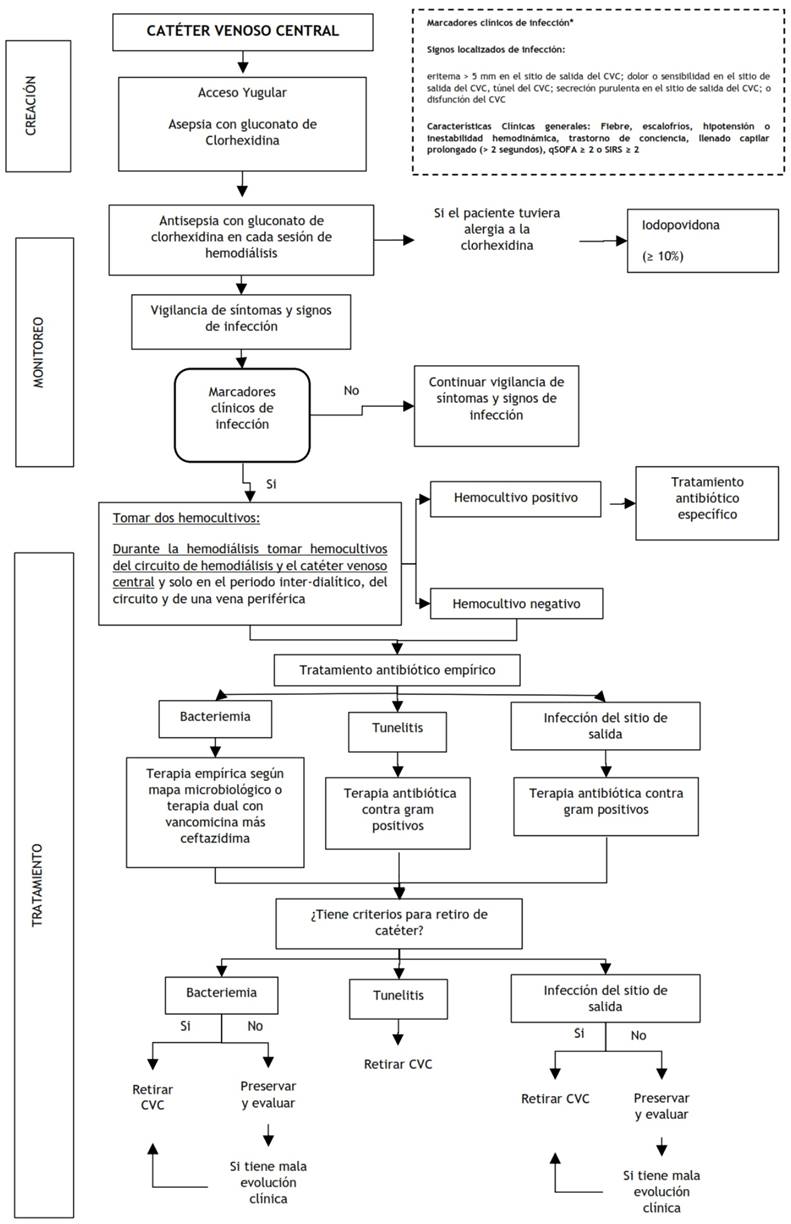
La presente GPC abordó 7 preguntas clínicas sobre prevención, diagnóstico y tratamiento. En base a dichas preguntas se formularon 12 recomendaciones (11 fuertes y 1 condicional), 33 BPC, y 02 flujogramas de manejo (Tabla 1, Figura 1) .
La presente GPC se enfoca en pacientes en hemodiálisis con catéter, fístula o injerto. A continuación, se expondrán las recomendaciones para cada pregunta clínica, así como un resumen del razonamiento seguido para llegar a cada recomendación. Todos los enunciados (recomendaciones o BPC) se encuentran enumerados en la Tabla 1, por lo cual en el texto solo se mencionará el número del enunciado al cual se hace referencia. Los datos numéricos de los beneficios y daños para cada pregunta se exponen en las tablas SoF, que se pueden consultar en el Material Suplementario 2 .
Pregunta 1: En los pacientes con indicación de hemodiálisis, ¿se debería administrar profilaxis antibiótica previa a la colocación del catéter, creación de fístula o injerto?
Se hallaron 2 RS, la de Wetering 2013 9 incluyó pacientes con indicación de CVC de tiempo prolongado, mientras que la RS de Stewart 2006 10 incluyó pacientes con indicación de reconstrucción arterial con o sin material protésico. Ambas RS tenían una calidad aceptable. Dado que se consideró que ambas RS evaluaban poblaciones distintas de la población objetivo, se decidió realizar una búsqueda de novo de estudios primarios que incluyeran la población objetivo. Se encontraron 2 ensayos clínicos aleatorizados (ECA): Huddam 2012 11 y Zibari 1997 12.
La RS de Wetering 2013 9 encontró que la profilaxis antibiótica sistémica no ofreció protección contra la sepsis relacionada al CVC. El ECA de Huddam 2012 11) encontró que la profilaxis antibiótica no tuvo efecto sobre la bacteriemia o la infección del sitio de salida en pacientes en hemodiálisis crónica con CVC. Por ello, se decidió emitir una recomendación en contra de esta intervención. A pesar de que la evidencia fue de baja certeza se decidió emitir una recomendación fuerte debido a que la evidencia fue consistente y a que consideró que someter a los pacientes a una intervención que no ha mostrado ningún beneficio y que posiblemente tenga efectos adversos sería dañino.
La RS de Stewart 2006 10 encontró que la profilaxis antibiótica previa a la creación de FAV o injerto resultó en menor probabilidad de infección temprana del injerto y el ECA de Zibari 1997 12 encontró que la profilaxis antibiótica previa a la creación de FAV resultó en una menor probabilidad de infección de la herida. Considerando que el balance entre beneficios y daños favorece la intervención, y que esta intervención es además aceptada y factible, se decidió emitir una recomendación a favor . A pesar que la evidencia fue de baja certeza, la consistencia de los resultados, la posibilidad de aumentar la equidad y el bajo costo de la intervención inclinó a emitir una recomendación fuerte .
Pregunta 2: En pacientes con indicación de colocación de CVC para hemodiálisis, creación de fístula o injerto, o que se encuentran en hemodiálisis crónica, ¿Cuál es la solución antiséptica más efectiva y segura para prevenir la infección del acceso vascular?
Se halló la RS de Shi 2019 13 que incluyó estudios de pacientes en unidad de cuidados intensivos (UCI), con indicación de colocación de CVC de bajo flujo y un tiempo corto de permanencia del acceso vascular (menor de 3 meses). Solo 1 estudio incluyó a pacientes en hemodiálisis. Por ello, se decidió realizar una búsqueda de ECA para tener una evidencia directa. En esta búsqueda, se encontró el ECA de McCann 2016 14 que evaluó pacientes en hemodiálisis por CVC.
La RS de Shi 2019 13 encontró que el uso de clorhexidina redujo la probabilidad de bacteriemia relacionada a CVC, colonización del CVC y la incidencia de reacciones cutáneas. El ECA de McCann 2016 (14 encontró que el uso de clorhexidina redujo la probabilidad de infección relacionada a CVC. Debido a que, los beneficios son mayores frente a los posibles daños, se optó por emitir una recomendación a favor del uso de gluconato de clorhexidina durante la colocación del CVC, así como durante la antisepsia local previa a cada sesión de hemodiálisis. Por otra parte, el uso de gluconato de clorhexidina, disminuye el riesgo de infecciones relacionadas al CVC y con ello se reduce la morbimortalidad asociada y el uso de recursos. Por tal motivo, a pesar de que la certeza de la evidencia fue muy baja, se decidió emitir una recomendación fuerte .
Pregunta 3: En pacientes en hemodiálisis ¿Cuáles marcadores clínicos o laboratoriales son útiles para identificar a los pacientes con sospecha de infección asociada al acceso de hemodiálisis?
No se encontraron RS ni ensayos clínicos aleatorizados referidos con esta pregunta clínica, por lo cual, se decidió emitir por consenso BPC que se enuncian en la Tabla 1.
Pregunta 4: En pacientes en hemodiálisis, ¿Cuál es la mejor prueba clínica o laboratorial para confirmar el diagnóstico de infección asociada al acceso de hemodiálisis?
Se encontró una RS al respecto: Safdar 2005 15. Adicionalmente se encontró una guía de práctica clínica con referencias potencialmente útiles y se seleccionó la que respondía a la pregunta PICO: Quittnat Pelletier 2016 16. La evidencia evaluada resume la sensibilidad y especificidad de los hemocultivos tomados de diferentes localizaciones: venoso periférico, directo del circuito, o del dispositivo intravascular.
La RS de Safdar 2005 15 encontró que los hemocultivos pareados tenían una sensibilidad del 79% y una especificidad del 99%. Por tal motivo, se optó por emitir una recomendación a favor de tomar hemocultivos pareados ante la sospecha de bacteriemia asociada a CVC. Por otra parte, teniendo en cuenta que, la implementación de la toma de hemocultivos pareados ante la sospecha de bacteriemia en pacientes en hemodiálisis, generaría ahorros a largo plazo ya que evitaría las complicaciones asociadas al tratamiento de sepsis, disminuiría la morbilidad secundaria y la mortalidad global en este grupo de pacientes (15, 17), se decidió emitir una recomendación fuerte .
La GPC de Quittnat Pelletier 2016 16 encontró que para el hemocultivo de sangre venosa periférica la sensibilidad era de 93.9% y la especificidad de 92.5% y que para el hemocultivo tomado directo del circuito de hemodiálisis se encontró una sensibilidad de 93.5% y una especificidad de 100%. En consecuencia, se optó por emitir una recomendación a favor de tomar hemocultivos del CVC y del circuito durante la diálisis, sólo considerándose la toma de un hemocultivo de la vena periférica y otro del lumen del catéter durante el periodo interdialítico. Por otra parte, teniendo en cuenta que, la implementación de este procedimiento evitaría la venopunción, permitiendo la preparación adecuada de estos pacientes para la inserción de accesos vasculares permanentes y además facilita la toma del mismo teniendo en cuenta que esta población es de difícil acceso periférico 16 se decidió emitir una recomendación fuerte .
Pregunta 5: En pacientes con infección asociada al acceso de hemodiálisis, ¿cuál es la terapia antibiótica empírica más efectiva y segura a usar?
Se encontraron 2 RS publicadas como artículo científico: Aslam 2014 18 que valoró la proporción de curación y eventos adversos, y Allon 2004 19 que valoró la prevalencia de infección. Se decidió realizar una búsqueda de ECA para evaluar la eficacia de las terapias antibióticas empíricas en pacientes con infección relacionada al acceso de hemodiálisis; sin embargo, no se encontró ningún estudio. Por este motivo, se decidió realizar una búsqueda de estudios observacionales (EO) y se encontró el estudio de Mohamed 2019 20).
La RS de Aslam 2014 18 encontró que para los casos de infección relacionada al CVC, había una mayor proporción de curados en los pacientes en los que se administraba cobertura para gram positivos y gram negativos. Por su parte, la RS de Allon 2004 19 encontró que en pacientes en hemodiálisis con infección del acceso vascular (bacteriemia relacionada con el catéter, infección del sitio de salida, infección de la fístula o injerto), la prevalencia de gram positivos fue de 77.37% y de los gram negativos fue de 28.62%. Por su parte, la RS de Aslam 2014 18 reportó una menor frecuencia de shock séptico en los pacientes a los que se les administró antibiótico sistémico por infección relacionada con el acceso vascular de hemodiálisis. En consecuencia, en sospecha de bacteriemia asociada a CVC, los beneficios, al administrar terapia según la epidemiología microbiológica de cada institución o terapia dual con vancomicina y ceftazidima como terapia empírica de primera elección, son mayores a los posibles daños. Por este motivo, se optó por emitir una recomendación a favor del uso de la terapia según la epidemiología microbiológica o terapia dual, en caso de que no se disponga de esta información. Por otra parte, a pesar de que la certeza de la evidencia fue muy baja, se consideró que los pacientes y profesionales de la salud aceptarían el tratamiento antibiótico. Además, su implementación es factible de realizar. Por ello se decidió emitir una recomendación fuerte .
El estudio de Mohamed 2019 20 encontró que en pacientes con infección del sitio de salida del CVC o tunelitis, la prevalencia de infección de microorganismos gram positivos fue del 95,7%. Por su parte, la RS de Aslam 2014 18 reportó una menor frecuencia de shock séptico en los pacientes a los que se les administró antibiótico sistémico por infección relacionada con el acceso vascular de hemodiálisis. Por tal motivo, teniendo en cuenta que los posibles beneficios, al administrar la terapia antibiótica empírica contra Gram positivos (cefalosporinas de primera generación, dicloxacilina, clindamicina u oxacilina), son mayores a los posibles daños, se optó por emitir una recomendación a favor del uso de esta terapia. Por otra parte, a pesar que la certeza de la evidencia fue muy baja, se consideró que los pacientes y profesionales de la salud aceptarían el tratamiento antibiótico. Además, su implementación es factible de realizar. Por ello se decidió emitir una recomendación fuerte.
La RS de Allon 2004 19 encontró que en pacientes en hemodiálisis con infección del acceso vascular (bacteriemia relacionada con el catéter, infección del sitio de salida, infección de la fístula o injerto), la prevalencia de gram positivos fue de 77.37% y de los gram negativos fue de 28.62%. El estudio de Mohamed 2019 20 encontró que en pacientes con infección del sitio de salida del CVC o tunelitis, la prevalencia de infección de microorganismos gram positivos fue del 95,7%. Por su parte, la RS de Aslam 2014 18 reportó una menor frecuencia de shock séptico en los pacientes a los que se les administró antibiótico sistémico por infección relacionada con el acceso vascular de hemodiálisis. Por tal motivo, en pacientes con tunelitis, se consideró que los posibles beneficios, al administrar la terapia antibiótica empírica contra Gram positivos (oxacilina, cefalosporina de primera generación), son mayores a los posibles daños. Por este motivo, se optó por emitir una recomendación a favor del uso de esta terapia. Por otra parte, en base a la microbiología local, existe una mayor predominancia de microorganismos Gram positivos en pacientes con tunelitis. A pesar que la certeza de la evidencia fue muy baja, se consideró que los pacientes y profesionales de la salud aceparían el tratamiento antibiótico. Además, su implementación es factible de realizar. Por ello se decidió emitir una recomendación fuerte .
La RS de Allon 2004 19 encontró que en pacientes en hemodiálisis con infección del acceso vascular (bacteriemia relacionada con el catéter, infección del sitio de salida, infección de la fístula o injerto), la prevalencia de gram positivos fue de 77.37% y de los gram negativos fue de 28.62%. Por su parte, la RS de Aslam 2014 18 reportó una menor frecuencia de shock séptico en los pacientes a los que se les administró antibiótico sistémico por infección relacionada con el acceso vascular de hemodiálisis. En sospecha de infección de la fístula o injerto, se consideró que los posibles beneficios, al administrar la terapia antibiótica empírica contra Gram positivos (cefalosporinas de primera generación, dicloxacilina, clindamicina u oxacilina), son mayores a los posibles daños. Por este motivo, se optó por emitir una recomendación a favor del uso de esta terapia. Por otra parte, en base a la microbiología local, existe una mayor predominancia de microorganismos Gram positivos para la sospecha de infección de la fístula o injerto. A pesar que la certeza de la evidencia fue muy baja, se consideró que los pacientes y profesionales de la salud aceptarían el tratamiento antibiótico; y que su implementación es factible de realizar; por lo cual se decidió emitir una recomendación fuerte .
Pregunta 6: En pacientes con infección asociada a catéter de hemodiálisis, ¿se debe retirar o preservar el catéter?
Para valorar si el catéter retirado se debe cambiar inmediatamente o posteriormente en pacientes con infección o bacteriemia de catéter se encontró una RS que valoró el desenlace resolución de infección o bacteriemia: Aslam 2014 21. Se encontró un ECA que abordó la población y el desenlace de mortalidad: Rijnders 2004 (22).
La RS de Aslam (2014) 21 encontró que el retiro con recambio inmediato del catéter mejora la probabilidad de resolver la infección respecto al retiro del catéter sin recambio inmediato. Por otra parte, el estudio de Rijnders (2004) 22) encontró que retirar el catéter ante la sospecha de infección no tiene un efecto sobre la mortalidad con respecto a retirar el catéter cuando la bacteriemia está confirmada. Por este motivo se optó por emitir una recomendación a favor del retiro del catéter ante una bacteriemia confirmada. A pesar de que el retiro del catéter con bacteriemia confirmada generaría ahorros al sistema de salud, el retiro del catéter tendría que ser inmediato en algunos contextos y en algunas situaciones se preferirá preservar el catéter En tal contexto, ya que solo algunos pacientes podrían beneficiarse por la recomendación, la fuerza de recomendación será condicional .
Pregunta 7: En pacientes que se encuentran en hemodiálisis, con infección asociada a la fístula o injerto ¿se debe cerrar/retirar o preservar la fístula o el injerto?
Respecto a la remoción del injerto, al no encontrarse ninguna RS, se realizó una búsqueda de novo de ECA o EO. Se encontraron dos estudios observacionales que responden a la pregunta: Calligaro 1994 23) y Lentino 2000 24
El estudio de Calligaro 1994 23) reportó que la remoción del injerto tuvo mayor frecuencia de amputación y no tuvo beneficios para el desenlace mortal, en los pacientes con infección asociada al injerto. El estudio de Lentino 2000 24 reportó que el efecto sobre la mortalidad en los casos en los que se preservó el injerto varió según el grado de severidad de la infección en los pacientes (de 5% a 23%). Además, considerando que el efecto de la remoción del injerto se desconoce para el desenlace de mortalidad a largo plazo y que este, podría ser tener mayores beneficios, se decidió emitir una recomendación a favor de la remoción del injerto. Por otra parte, se consideró que la implementación de la intervención generaría ahorros a largo plazo ya que evitaría futuras complicaciones como isquemia, hemorragia, sepsis, infección, entre otras. Además, debido a que el procedimiento quirúrgico se realiza actualmente, no sería necesario la implementación de nuevos equipos o instrumentos, por lo que sería factible y potencialmente evaluable. Por ello, se decidió emitir una recomendación fuerte .
No se encontró evidencia respecto a la remoción de la fístula; por lo cual, se planteó un BPC (Tabla 1).
Tabla 1 Lista de recomendaciones y puntos de buena práctica clínica
| Enunciado | Tipo * | Certeza ** | |
| Prevención | |||
| Pregunta 1: En los pacientes con indicación de hemodiálisis, ¿se debería administrar profilaxis antibiótica previa a la colocación del catéter, creación de fístula o injerto? | |||
| 1.1 | En pacientes en quienes se decide iniciar hemodiálisis, recomendamos no administrar profilaxis antibiótica sistémica previo a la colocación del catéter venoso central. | Recomendación fuerte en contra | Baja (⊕⊕◯◯) |
| 1.2 | En pacientes en quienes se decide crear fístula o injerto para hemodiálisis, recomendamos administrar profilaxis antibiótica sistémica previa al procedimiento quirúrgico. | Recomendación fuerte a favor | Baja (⊕⊕◯◯) |
| 1.3 | En pacientes en quienes se les colocará un catéter venoso central para hemodiálisis, es preferible usar la vena yugular interna como acceso vascular de elección. | BPC | |
| 1.4 | En pacientes en quienes se creará una fístula o injerto para hemodiálisis, se debe administrar una dosis de cefazolina 2 gr EV 30 minutos antes del procedimiento quirúrgico. En pacientes alérgicos a los betalactámicos, se puede optar por vancomicina 1 gr EV 60 minutos antes del procedimiento. | BPC | |
| Pregunta 2: En pacientes con indicación de colocación de CVC para hemodiálisis, creación de fístula o injerto, o que se encuentran en hemodiálisis crónica, ¿Cuál es la solución antiséptica más efectiva y segura para prevenir la infección del acceso vascular? | |||
| 2.1 | En pacientes en quienes se le colocará un catéter venoso central temporal o de larga permanencia para hemodiálisis, recomendamos realizar la antisepsia de la zona de punción con solución de gluconato de clorhexidina. | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 2.2 | En pacientes que se hemodializan a través de un catéter venoso central temporal o de larga permanencia, recomendamos realizar la antisepsia del mismo con solución de gluconato de clorhexidina en cada sesión de hemodiálisis. | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 2.3 | En pacientes que se encuentran en hemodiálisis a través de fístula o injerto, se debe realizar la antisepsia con solución de gluconato de clorhexidina durante cada sesión de hemodiálisis. | BPC | |
| 2.4 | Previa a la aplicación de la solución antiséptica se debe realizar un lavado con agua y jabón en el área donde se colocará el acceso vascular. | BPC | |
| 2.5 | Si el paciente es alérgico al gluconato de clorhexidina o se observa reacciones cutáneas importantes por su uso, se puede usar solución de yodopovidona espuma. | BPC | |
| 2.6 | La concentración a usar del gluconato de clorhexidina debe ser ≥ 0.5 % y la de yodopovidona espuma debe ser ≥ 10% | BPC | |
| 2.7 | Al aplicar la solución de gluconato de clorhexidina, se debe dejar un tiempo de secado de al menos 3 minutos. | BPC | |
| 2.8 | Al aplicar la solución la solución de yodopovidona se debe dejar un tiempo de secado de al menos 2 minutos | BPC | |
| Diagnóstico | |||
| Pregunta 3: En pacientes en hemodiálisis ¿Cuáles marcadores clínicos o laboratoriales son útiles para identificar a los pacientes con sospecha de infección asociada al acceso de hemodiálisis? | |||
| 3.1 | En pacientes en hemodiálisis, se deben evaluar en cada sesión los siguientes marcadores clínicos de infección: Signos localizados de infección: eritema > 5 mm en el sitio de salida del CVC, en la zona de la fístula, o zona del injerto; dolor o sensibilidad en el sitio de salida del CVC, túnel del CVC, zona de la fístula, o zona del injerto; secreción purulenta en el sitio de salida del CVC; o disfunción del CVC Características Clínicas generales: Fiebre, escalofríos, hipotensión o inestabilidad hemodinámica, trastorno de conciencia, llenado capilar prolongado (> 2 segundos), qSOFA ≥ 2 o SIRS ≥ 2 | BPC | |
| 3.2 | Si se sospecha de infección asociada al acceso vascular de hemodiálisis, primero se debe descartar otros focos probables de la infección. | BPC | |
| 3.3 | El área del acceso vascular debe protegerse con una gasa o un apósito transparente y se debe vigilar la higiene e integridad de la piel circundante. | BPC | |
| 3.4 | Se debe brindar educación constante al paciente y/o cuidadores acerca de la preservación y cuidados del acceso de hemodiálisis. | BPC | |
| 3.5 | En pacientes en hemodiálisis, debido al riesgo de infección del acceso vascular, la elección del tipo de acceso se escogerá en el siguiente orden: fístula nativa (primera elección), injerto autólogo, injerto protésico, y como última opción el catéter venoso central. | BPC | |
| 3.6 | Si se decide utilizar un catéter venoso central para hemodiálisis, de preferencia usar uno tunelizado, siempre y cuando sea factible y no existan contraindicaciones. | BPC | |
| 3.7 | En los pacientes en hemodiálisis a través de catéter venoso central, se debe realizar el cambio a fístula tan pronto como sea posible, siempre y cuando sea factible y no existan contraindicaciones. | BPC | |
| Pregunta 4: En pacientes en hemodiálisis, ¿Cuál es la mejor prueba clínica o laboratorial para confirmar el diagnóstico de infección asociada al acceso de hemodiálisis? | |||
| 4.1 | Para establecer el diagnóstico de infección asociada al acceso de hemodiálisis, se debe tener sospecha clínica de infección y haberse descartado otros focos. | BPC | |
| 4.2 | En pacientes en hemodiálisis con sospecha de bacteriemia asociada a catéter venoso central, recomendamos tomar 2 hemocultivos para establecer el diagnóstico. | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 4.3 | Durante la hemodiálisis, un hemocultivo debe ser tomado del catéter venoso central y otro del circuito de hemodiálisis, y solo en el periodo inter-dialítico, los hemocultivos se tomarán del circuito de hemodiálisis y de una vena periférica. | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 4.4 | Para confirmar el diagnóstico de bacteriemia por infección de la fístula o el injerto, considerar la toma de dos hemocultivos. De haber exudado realizar un hisopado y cultivar en un medio apropiado. | BPC | |
| 4.5 | El volumen mínimo de muestra de sangre para realizar un hemocultivo debe ser 10 ml | BPC | |
| 4.6 | El hemocultivo que se realice a través del catéter venoso central debe ser por el lumen venoso. | BPC | |
| 4.7 | Se debe iniciar la antibioticoterapia empírica inmediatamente después de haberse tomado el cultivo. | BPC | |
| 4.8 | Para establecer el diagnóstico de sepsis del acceso vascular, se debe de cumplir con los criterios de sepsis (sospecha de foco de infección: acceso vascular + score SOFA ≥ 2) | BPC | |
| 4.9 | Cuando existan los siguientes tipos de infección (tromboflebitis, endocarditis, artritis séptica, osteomielitis y abscesos), se debe descartar infección del acceso de hemodiálisis como foco primario | BPC | |
| Tratamiento | |||
| Pregunta 5: En pacientes con infección asociada al acceso de hemodiálisis, ¿cuál es la terapia antibiótica empírica más efectiva y segura a usar? | |||
| 5.1 | En pacientes en hemodiálisis que tengan sospecha de bacteriemia asociada al catéter de hemodiálisis, se recomienda administrar antibioticoterapia empírica según la epidemiología microbiológica del establecimiento de salud. De no disponerse, recomendamos administrar terapia dual con vancomicina y ceftazidima como tratamiento empírico de primera elección. | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 5.2 | En pacientes en hemodiálisis que tengan sospecha de infección en el sitio de salida, recomendamos administrar terapia antibiótica contra gram positivos (cefalosporinas 1era generación, dicloxacilina, clindamicina u oxacilina) como tratamiento empírico de primera elección | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 5.3 | En pacientes en hemodiálisis que tengan sospecha de infección de la fístula o injerto recomendamos administrar terapia antibiótica contra gram positivos (cefalosporinas 1era generación, dicloxacilina, clindamicina u oxacilina) como tratamiento empírico de primera elección. | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 5.4 | En pacientes en hemodiálisis que tengan tunelitis, recomendamos administrar terapia antibiótica contra gram positivos (oxacilina, cefalosporina de 1era generación) como tratamiento empírico de primera elección. | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 5.5 | Todos los centros de HD deberían tener un mapa microbiológico actualizado, de ser posible, cada 6 meses. | BPC | |
| 5.6 | En pacientes en hemodiálisis ambulatoria, considerar la epidemiología microbiológica local para orientar la elección de la terapia antibiótica empírica. | BPC | |
| 5.7 | Una vez que se identifique el germen y su patrón de resistencia, debe de-escalar a una terapia más selectiva. | BPC | |
| 5.8 | La vancomicina debe ser administrada en 2 horas y nunca en un tiempo < 1 hora. | BPC | |
| 5.9 | La primera dosis de vancomicina debe ser dosis de carga (25-30 mg/kg). | BPC | |
| 5.10 | La duración del tratamiento antibiótico para la bacteriemia asociada a catéter venoso central dependerá del agente microbiano aislado: Para Staphylococcus aureus el tratamiento debe ser no menor a 4 semanas. Considerar la realización de un ecocardiograma. Para estafilococos coagulasa negativos, bacilos gram negativos o enterococos el tiempo de tratamiento será no menor a 1 semana ni mayor a 2 semanas. Para especies de candida el tiempo de tratamiento será no menor a 2 semanas. En infecciones por Staphylococcus aureus y especies de cándida considerar la búsqueda de infecciones metastásicas. Otros aspectos que determinarán la duración del tratamiento serán el patrón de resistencia, la evolución clínica y el criterio clínico del médico tratante. | BPC | |
| Pregunta 6: En pacientes con infección asociada a catéter de hemodiálisis, ¿se debe retirar o preservar el catéter? | |||
| 6.1 | En pacientes en hemodiálisis con bacteriemia asociada a catéter, sugerimos retirar el catéter. | Recomendación condicional a favor | Muy Baja (⊕◯◯◯) |
| 6.2 | Si el paciente tiene alta sospecha o diagnóstico establecido de bacteriemia asociada a catéter de hemodiálisis, se debe retirar inmediatamente el catéter en las siguientes circunstancias: Sepsis o shock séptico Evidencia de infección metastásica. Tunelitis Pus en el sitio de salida del catéter. Si la fiebre y / o bacteriemia persistente de 48 a 72 horas después del inicio de antibióticos a los que el organismo es susceptible. Cuando la infección se debe a patógenos difíciles de curar, como S. aureus, Pseudomonas, Candida u otros hongos o bacterias multidrogoresistentes. | BPC | |
| 6.3 | Cuando exista bacteriemia asociada a CVC no tunelizado, este debe retirarse y no intentar la preservación del mismo. | BPC | |
| 6.4 | En ciertas circunstancias es posible preservar el catéter venoso central tunelizado, tales como: imposibilidad de otros accesos vasculares, dificultades físicas o anatómicas para la colocación del nuevo catéter. | BPC | |
| 6.5 | Se puede insertar un nuevo catéter de diálisis tunelizado una vez que se obtienen hemocultivos con resultados negativos. | BPC | |
| Pregunta 7: En pacientes que se encuentran en hemodiálisis, con infección asociada a la fístula o injerto ¿se debe cerrar/retirar o preservar la fístula o el injerto? | |||
| 7.1 | En pacientes en hemodiálisis con infección asociada al injerto, se recomienda remover el injerto. | Recomendación fuerte a favor | Muy Baja (⊕◯◯◯) |
| 7.2 | En pacientes con infección asociada a la fístula, se debe intentar siempre que sea posible la preservación de la fístula mediante desbridamiento quirúrgico de las colecciones existentes. | BPC | |
* Recomendación (R) o buenas prácticas clínicas (BPC)
** La certeza de la evidencia solo se establece para las recomendaciones, mas no para los puntos de BPC
Tabla 2 Significado de los niveles de certeza de la evidencia y de la fuerza de la recomendación
| Categorías | Significado |
|---|---|
| Certeza de la evidencia | |
| (⨁⨁⨁⨁) Alta | Es muy probable que el verdadero efecto sea similar al efecto estimado. |
| (⨁⨁⨁◯) Moderada | Es moderadamente probable que el verdadero efecto sea similar al efecto estimado, pero es posible que sea sustancialmente diferente |
| (⨁⨁◯◯) Baja | Nuestra confianza en el efecto es limitada. El verdadero efecto podría ser sustancialmente diferente al efecto estimado |
| (⨁◯◯◯) Muy baja | Nuestra confianza en el efecto es pequeña. El verdadero efecto probablemente sea sustancialmente diferente al efecto estimado |
| Fuerza de la recomendación | |
| Recomendación fuerte | El GEG considera que todos o casi todos los profesionales que revisan la evidencia disponible seguirán esta recomendación. En la formulación de la recomendación se usa el término “se recomienda” |
| Recomendación Condicional | El GEG considera que la mayoría de los profesionales que revisan la evidencia disponible seguirán esta recomendación, pero un grupo de profesionales podría optar por no aplicarlas en alguna población particular, siempre que sea justificado. En la formulación de la recomendación se usa el término “se sugiere” |
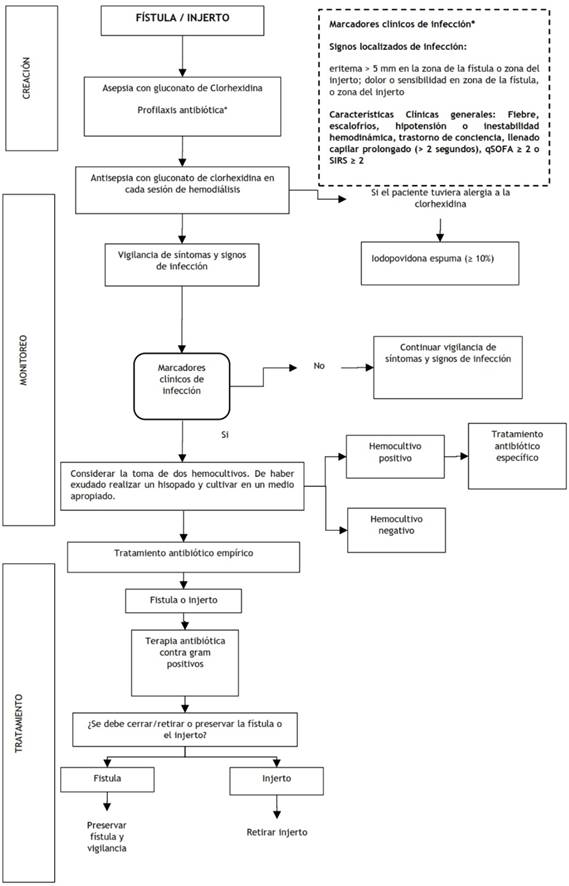
Figura 1 Flujograma de prevención, diagnóstico y manejo de infección de fístula/injerto de hemodiálisis.