INTRODUCCIÓN
El sentido del gusto es esencial para la vida, porque, además de prevenir la ingestión de sustancias tóxicas, activa las vías neuronales para la digestión, la absorción y el almacenamiento de nutrientes. Una disfunción de la percepción del gusto puede repercutir en la calidad de vida al afectar el apetito, el peso corporal y el bienestar psicológico 1 En consecuencia, el cambio en la percepción de este sentido puede influir en el estado de salud y en el riesgo de enfermedades crónicas, como obesidad 2 aterosclerosis, diabetes, enfermedades hepáticas, hipertensión 3 cáncer 4 etc.
Hay varios factores que pueden afectar la percepción del gusto, como malnutrición, cáncer, hepatitis crónica, disfunción renal, SIDA, traumatismo encefalocraneano, exposición a químicos tóxicos, exposición a agentes industriales, medicación, envejecimiento, infecciones orales y periorales, parálisis de Bell, uso de prótesis dental, tratamientos de conducto, etc. 5. Se ha reportado que también puede ser causada por exodoncias de las muelas del juicio mandibulares (6, 7), o como secuela por la administración de anestesia dental para el procedimiento quirúrgico (8, 9). Sin embargo, los déficits gustativos que siguen a la exodoncia de otras piezas dentales (molares superiores, incisivos, etc.) o tratamientos de conducto radicular no pueden explicarse por el daño del nervio cuerda del tímpano o glosofaríngeo, ya que las fibras nerviosas de estos nervios no inervan ni atraviesan el sitio quirúrgico anterior 10-12
La desaferentación dental (DD) se define como la eliminación o reducción de las entradas neurales aferentes periféricas relacionadas con los aparatos dentales y masticatorios. Los ejemplos de DD incluyen pérdida de dientes, desprendimiento periodontal local y/o generalizado, restauraciones quirúrgicas o protésicas inadecuadas, tratamientos de ortodoncia, tratamientos de conducto, masticación defectuosa, etc. (11, 13).
Los seres humanos y los animales, como las ratas y los ratones, tienden a consumir en exceso alimentos ricos en calorías. La «recompensa» se ha subdividido en tres procesos psicológicos interdependientes: hedonia (gustar una comida: liking), refuerzo (formación de asociaciones entre estímulos, acciones y/o la comida) y motivación (querer la comida: wanting) 14 El wanting se evalúa en animales mediante pruebas de ingesta, como masa total o volumen consumido durante un período designado; no obstante, evitar el consumo de una solución no necesariamente implica el disgusto por la misma, así como tampoco el consumo exacerbado supone mayor agrado hacia una sustancia. En consecuencia, las medidas de ingesta por sí solas son interpretativamente limitadas. Para subsanar este problema, Grill y Norgren desarrollaron el test de reactividad gustativa (TRG), capaz de sondear el liking en ausencia del wanting 15 La reactividad gustativa (RG) se refiere a las respuestas orofaciales estereotipadas provocadas por un estímulo gustativo en animales, incluidos los roedores y los seres humanos. Para aplicar este procedimiento en los animales, se les coloca quirúrgicamente cánulas intraorales a través de las cuales se puede infundir directamente los estímulos del gusto y grabar en video las respuestas para el análisis cuadro por cuadro. La RG se puede clasificar generalmente como ingestiva, aversiva o ambigua (16, 17).
El objetivo del presente estudio fue evaluar la influencia de la DD en el sentido del gusto de ratas Wistar machos mediante el TRG.
MATERIALES Y MÉTODOS
Estudio experimental que siguió las directrices de ARRIVE 2.0 (Animal Research Reporting of In Vivo Experiments). Fue realizado con diez ratas Wistar, en buenas condiciones sanitarias sistémicas, las cuales fueron obtenidas del bioterio de la Facultad de Medicina de la Universidad Peruana Cayetano Heredia (UPCH). Las ratas se alojaron en jaulas individuales de 35 × 23 × 18 cm, en donde recibieron alimentación habitual, consistente en dieta de granos y proporcionada ad libitum y acceso ilimitado al agua. Además, durante los experimentos, se las mantuvo en condiciones óptimas de un ciclo día-noche de 12 horas, con temperatura (22 ºC) y humedad (60-70 % HR) constantes.
El cálculo del tamaño de la muestra se realizó utilizando el software OpenEpi con base en una investigación previa 18 que estableció que la diferencia de medias del número de respuestas aversivas a quinina al 0,003 % en el TRG entre el grupo control y el grupo con sección del nervio glosofaríngeo fue de 8,2 (DE 3,4 y 2,1, respectivamente); asimismo, utilizando una potencia de 90 % y un nivel de significancia del 5 %, se calculó que tres ratas en cada grupo serían suficientes para poder rechazar la hipótesis nula. Este número se incrementó a cinco en cada grupo para compensar la posible pérdida de cánulas o muerte durante la fase experimental. Se aleatorizó y asignó a las ratas a uno de los dos grupos: control y experimental.
Para asegurar la homogenización de los grupos, todos los sujetos de investigación fueron machos, de 8 a 12 semanas de edad y con un peso estadísticamente no significativo al comparar el grupo control con el grupo experimental (tabla 1).
Tabla 1 Peso de los sujetos de investigación antes de iniciar el estudio.
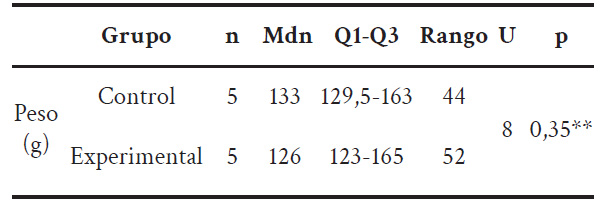
Nota: Nivel de significancia p < 0,05: * significativo; ** no significativo.
La implantación de cánulas intraorales para TRG en ambos grupos se hizo bajo sedación profunda, mediante una combinación de ketamina 40 mg/kg y xilazina 5 mg/kg intraperitoneal. Una vez que las ratas no respondían al pellizco de la pata, se dio inicio a la cirugía usando una técnica similar a la de Parker (19, 20), pero usando cánulas Clay Adams PE-50. Para prevenir la pérdida o la obstrucción de la cánula, se realizó el mismo procedimiento en el lado opuesto. Asimismo, aprovechando la anestesia, en el grupo experimental se realizó la exodoncia de los tres molares superiores del lado derecho. Se alojó individualmente a las ratas en jaulas inmediatamente después de la cirugía. Se administró una inyección del analgésico meloxicam 1 mg/kg y penicilina-estreptomicina 0,1 mg/kg vía subcutánea. Para mantener la permeabilidad de las cánulas se infundió agua destilada cada tres días. Para la infusión de soluciones que se usaron en el TRG se conectó a la cánula que sobresalía por la nuca una aguja 23G × 1” cortada, la cual, a su vez, se adaptó a una extensión DIS de 30 cm y una llave de triple vía con extensión de 50 cm. Finalmente, se conectó a la llave de triple vía una jeringa de 3 cc con la solución a infundir.
Al tercer día de la cirugía, se dio inicio al TRG (día 1) en una cabina trapezoidal espejada, en la cual se colocó individualmente a las ratas de ambos grupos y se registró con una videocámara a 60 fotogramas por segundo las reacciones orofaciales y corporales ante la infusión intraoral de dos saborizantes: 1 M de sacarosa (ingestiva) y 3 mM de benzoato de denatonio (BD), la cual es aversiva, a razón de 1 mL en 1 minuto. Este TRG se repitió en los días 7, 14 y 21. Se registró el número total de respuestas ingestivas y aversivas durante el período de infusión de un minuto y durante los 30 segundos siguientes.
Las respuestas ingestivas consideradas en la presente investigación fueron las siguientes: 1) movimientos de la boca: aberturas rítmicas de baja amplitud de la mandíbula, generalmente durante la ingestión de fluidos; 2) protrusión lingual (medial y lateral): protrusiones rítmicas de la lengua en la línea media, cubriendo los incisivos superiores, y extensiones no rítmicas de la lengua, la cual emerge a ambos lados de la boca, dando como resultado una separación asimétrica de los labios; 3) lameteo de las patas delanteras: extensiones rítmicas de gran amplitud de la lengua en la línea media dirigidas a las patas delanteras (figura 1).
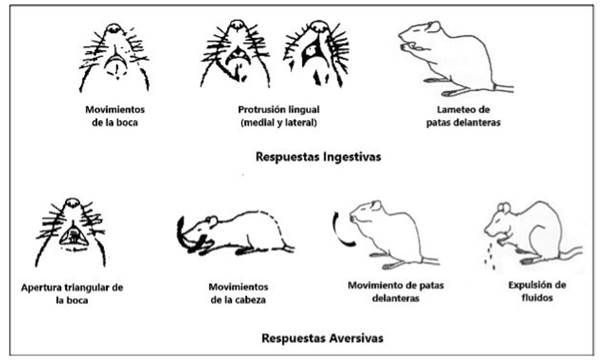
Figura 1 Comportamiento durante el test de reactividad gustativa. Adaptada a partir de Grill et al. 18
Las respuestas aversivas fueron las siguientes: 1) aperturas triangulares de la boca: aberturas de gran amplitud de la mandíbula que revelan los incisivos superiores e inferiores con retracción concomitante de las comisuras de la boca; 2) movimiento de la cabeza: ráfaga de movimientos de lado a lado de la cabeza de alta frecuencia; 3) movimiento de las patas delanteras: ráfaga de movimientos de alta frecuencia de una o ambas extremidades anteriores; 4) expulsión de fluidos: acumulación de líquido fuera de la boca, el fluido gotea a la cabina del TRG 21 (figura 1).
Por último, para el análisis, se puntuaron las reacciones registradas durante los últimos 30 segundos de la fase de infusión y durante los primeros 30 segundos de la fase de post-infusión.
La información obtenida se incorporó en una hoja de cálculo de MS-Excel. Luego fue procesada en el paquete estadístico SPSS versión 26. En vista de que no todas las variables tenían distribución normal, y se tienen menos de 50 datos en cada grupo, se usó una prueba no paramétrica (U de Mann-Withney) para identificar diferencias entre dos muestras independientes. Finalmente, la magnitud de la diferencia se calculó mediante la r de Rosenthal.
Todos los experimentos fueron aprobados por el Comité de Ética en Investigación de la Facultad de Medicina de la Universidad Nacional Mayor de San Marcos (código de estudio n.° 0054-2022).
RESULTADOS
Los resultados son presentados con el intervalo de confianza del 95 %. En todo momento, el nivel de significancia se estableció en p ≤ 0,05 (tabla 2).
Tabla 2 Comparación del número de respuestas del TRG.
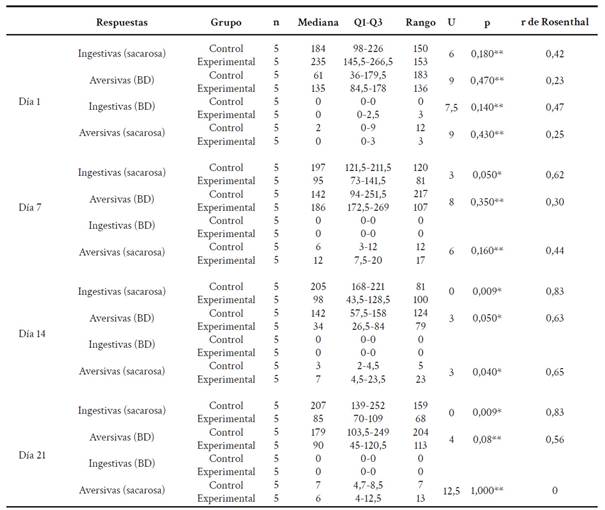
Nota: Nivel de significancia p < 0,05: * significativo; ** no significativo.
En la comparación del número de respuestas al TRG entre el grupo control y el grupo experimental en el día 1, no se encontraron diferencias estadísticamente significativas en las respuestas ingestivas y aversivas a sacarosa (p = 0,18 y 0,43, respectivamente). En el mismo sentido, no se encontraron diferencias estadísticamente significativas en las respuestas aversivas e ingestivas a BD (p = 0,47 y 0,14, respectivamente). En todos los casos se mantuvo una magnitud de la diferencia (r de Rosenthal) < 0,5, considerada como efecto pequeño.
Al comparar el número de respuestas al TRG en el día 7, no se encontraron diferencias estadísticamente significativas en las respuestas aversivas a BD y a sacarosa (p = 0,35 y 0,16, respectivamente). En cambio, sí se hallaron diferencias estadísticamente significativas en las respuestas ingestivas a sacarosa, donde las puntuaciones del grupo control (Mdn = 197; Rango = 120) fueron mayores que las del grupo experimental (Mdn = 95; Rango= 81); con U = 3, p = 0,05, y una magnitud de la diferencia de 0,623, que en la escala de Cohen se considera como efecto intermedio. No se obtuvo respuestas ingestivas a BD.
Al evaluar el número de respuestas al TRG en el día 14, se encontraron diferencias estadísticamente significativas en las respuestas ingestivas a sacarosa, donde las puntuaciones del grupo control (Mdn = 205; Rango = 81) fueron mayores que las del grupo experimental (Mdn = 98; Rango = 100); con U = 0, p = 0,009, y una magnitud de la diferencia de 0,83, que en la escala de Cohen se considera como gran efecto. En el mismo sentido, se encontraron diferencias estadísticamente significativas en las respuestas aversivas a BD, donde las puntuaciones del grupo control (Mdn = 142; Rango = 124) fueron mayores que las del grupo experimental (Mdn = 34; Rango = 79); con U = 3, p = 0,05, y una magnitud de la diferencia de 0,63, que en la escala de Cohen se considera como efecto intermedio. Asimismo, se encontraron diferencias estadísticamente significativas en las respuestas aversivas a sacarosa, donde las puntuaciones del grupo experimental (Mdn = 7; Rango= 23) fueron mayores que las del grupo control (Mdn = 3; Rango = 5); con U = 3, p = 0,04, y una magnitud de la diferencia de 0,65, que en la escala de Cohen se considera como efecto intermedio.
Por último, en la comparación del número de respuestas al TRG en el día 21, no se encontraron diferencias estadísticamente significativas en las respuestas aversivas a BD (p = 0,08) ni en las respuestas aversivas a sacarosa (p = 1). Asimismo, no se obtuvieron respuestas ingestivas a BD, tal como ocurrió en los días 7 y 14. En cambio, sí se hallaron diferencias estadísticamente significativas en las respuestas ingestivas a sacarosa, donde las puntuaciones del grupo control (Mdn = 207; Rango = 159) fueron mayores que las del grupo experimental (Mdn = 85; Rango = 68); con U = 0, p = 0,009, y una magnitud de la diferencia de 0,83, que en la escala de Cohen se considera como gran efecto.
DISCUSIÓN
Se han realizado múltiples estudios de DD en roedores para reducir su capacidad masticatoria, ello mediante la extracción de molares (22, 23), el tratamiento de conducto radicular 24 la alimentación con dieta blanda (25, 26), o la colocación de placas de mordida (27, 28). En la presente investigación, se provocó la DD en los sujetos de estudio mediante la exodoncia de los tres molares superiores del lado derecho.
Un aspecto poco conocido es que la DD afecta el sentido del gusto debido a que las entradas somatosensoriales del trigémino y gustativas convergen en la corteza, el tálamo, el núcleo parabraquial, etc., y los estudios anatómicos han revelado proyecciones del V par a la región rostro-lateral del núcleo del tracto solitario (NTS), primer relevo gustativo a nivel central, que recibe proyecciones del nervio cuerda del tímpano (CT) del facial (29, 30) o glosofaríngeo (GL). En un estudio se determinó que las respuestas a los saborizantes aplicados en la lengua de la rata se registraron electrofisiológicamente en unidades del NTS mientras se manipulaban los nervios lingual y mandibular. La sección de cualquiera de estos nervios resultó en una disminución significativa de la respuesta gustativa; sin embargo, fue aún mayor cuando se cortó el nervio dentario. Por lo tanto, los parámetros de las propiedades de textura de los alimentos monitoreados por los dientes que funcionan como sensores de fuerza contribuyen claramente a la señalización del «sabor» 31
Se ha estudiado la relación entre la DD y los problemas cognitivos como demencias tipo alzhéimer, deterioro de memoria espacial, enfermedad de Parkinson, cardiopatías, osteoporosis, depresión y ansiedad 11 Sin embargo, hay pocos estudios que analizan la relación entre la DD y la disfunción gustativa sin lesión directa del nervio cuerda del tímpano o glosofaríngeo. El estudio de Boucher et al. 10 es interesante porque correlaciona las disfunciones gustativas y la DD en humanos mediante electrogustometría (EGM). En este trabajo se determinó que cuanto mayor era el número de dientes perdidos, mayor era el umbral de EGM, independientemente de la edad del sujeto; como se sabe, a mayor umbral menor sensación gustativa. Sin embargo, los déficits gustativos que siguen a otro tipo de DD, como la exodoncia de otras piezas dentales (molares superiores, incisivos, etc.) o tratamientos de conducto radicular, no pueden explicarse por el daño del nervio CT o GL, porque las fibras nerviosas de estos nervios no inervan ni atraviesan el sitio quirúrgico anterior (10, 12).
El TRG se usa con mayor frecuencia en paradigmas de aversión al gusto condicionada 32 sin embargo, también se usa en una amplia gama de situaciones experimentales, incluida la investigación sobre la palatabilidad gustativa, la saciedad, el agotamiento de sodio 16 y en estudios relacionados con el aprendizaje y la memoria mediante la conducta consumatoria y el condicionamiento clásico 33 En el trabajo pionero de Grill y Norgren (34, 35) se describieron minuciosamente las conductas que componen el patrón hedónico (ingestivo) y el aversivo en ratas adultas. Inicialmente, se identificaron 4 componentes orofaciales y 5 de respuesta corporal. El patrón hedónico (ingestivo) incluye movimientos rítmicos de la boca (MB), protrusiones linguales mediales (PLM) y protrusiones linguales laterales (PLL). En cambio, el patrón aversivo incorpora aperturas triangulares de la boca (ATB), frotación de la barbilla contra el piso, movimientos rápidos de la cabeza (MC), movimientos de las patas delanteras hacia adelante (MPD) y limpieza con ambas patas delanteras sobre el hocico (LPD). Algunos trabajos posteriores han reducido el patrón de respuestas aversivas a ATB, MPD y FB, y han añadido al patrón hedónico el lameteo de las patas delanteras (LPD) (18). En nuestro trabajo de investigación se consideró como patrón ingestivo el MB, la protrusión lingual (incluye PLM y PLL) y el LPD. En el patrón aversivo se incluyó ATB, MC, MPD y expulsión de fluidos.
Dado que la cantidad de respuestas aversivas a sacarosa e ingestivas a BD en el TRG fueron insignificantes, solo se consideraron en el análisis final las respuestas ingestivas a sacarosa y aversivas a BD. En este estudio se observó que el número de reacciones ingestivas a sacarosa disminuyó notablemente a partir de la primera semana en el grupo experimental con respecto al grupo control, estadísticamente significativa en todos los casos. En cambio, las reacciones aversivas a BD fueron variables, aumentaron en el grupo experimental la primera semana y disminuyeron en la segunda y tercera semana al ser comparadas con el grupo control, encontrándose diferencias estadísticamente significativas en la segunda semana. En el primer día del TRG no se encontraron diferencias estadísticamente significativas en las respuestas ingestivas a sacarosa o aversivas a BD porque se presume que transcurrió poco tiempo para que se expresen cambios en el sentido del gusto por la DD.
No se pueden comparar estos resultados con otros trabajos de investigación porque, en la revisión de la literatura, no se encontraron estudios que midan estas variables, además las respuestas aversivas no se midieron con BD. Sin embargo, existen reportes de TRG en murinos sometidos a la sección del nervio CT del VII par (lleva información gustativa de los 2/3 anteriores de la lengua) o GL (lleva información gustativa del 1/3 posterior de la lengua), que podría considerarse otra forma de desaferentación. Por ejemplo, en el estudio de Grill y Schwartz (36), al comparar las respuestas ingestivas mediante la infusión de sacarosa a diferentes concentraciones en ratas con sección del nervio CT y GL frente al grupo control, observaron que la puntuación ingestiva aumentó significativamente con el aumento de la concentración de sacarosa en el grupo control (F2,6 = 6,3; p < 0,05); en cambio, las ratas CT + GL mostraron significativamente menos respuestas ingestivas totales que las ratas intactas en cada concentración de sacarosa analizada (F2,6 = 6,7, 5,6, 7,8; p < 0,05). Prácticamente todos los estudios sobre aversión al gusto que hayan empleado el TRG se realizaron con clorhidrato de quinina; no obstante, el BD es 3000 veces más amargo que la quinina.
En el estudio de King et al. 37 en el cual se expusieron a una de tres condiciones quirúrgicas a ratas (sección del GL bilateralmente, extirpación de 8-10 mm del GL bilateralmente y grupo control en el que solo se expusieron los GL), se realizó el TRG mediante la infusión de quinina (3 mM) o agua destilada a los 17, 52 o 94 días después de la cirugía. Los comportamientos aversivos puntuados incluyeron ATB, frotamiento de barbilla, MC y MPD. Un análisis de la varianza de dos factores indicó efectos principales significativos del estímulo (F(1,65) = 92,55; p < 0,001) y la condición nerviosa (F(6,65) = 7,26; p < 0,001), así como una interacción significativa (F(6,65) = 7,713; p < 0,001). Cuando el agua fue el estímulo, ocurrieron muy pocos comportamientos aversivos, independientemente de la condición del GL. Por el contrario, la infusión de quinina provocó muchos comportamientos aversivos, pero solo en animales con los nervios intactos. Dentro de las limitaciones del estudio, tenemos la falta en la homogenización de la muestra, situación que se trató de subsanar con el peso inicial de los sujetos de investigación.
CONCLUSIONES
En la presente investigación se encontró una diferencia en las medianas de las respuestas ingestivas a sacarosa y aversivas a BD en ratas Wistar machos a consecuencia de la DD, siendo esta menor en el grupo experimental el día 7 (ingestivas a sacarosa), el día 14 (ingestivas a sacarosa y aversivas a BD) y el día 21 (ingestivas a sacarosa); y mayor en el grupo experimental el día 14 (aversivas a sacarosa). Se sugiere ampliar esta línea de investigación a través de la evaluación de la función gustativa mediante un estudio histomorfométrico de la papila caliciforme en ratas albinas.
Institución donde se realizó el estudio: Bioterio de la Facultad de Medicina Veterinaria de la Universidad Nacional Mayor de San Marcos y Clínica de Animales Menores de la Facultad de Medicina Veterinaria de la misma universidad











 texto en
texto en 


