Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Gastroenterología del Perú
versión impresa ISSN 1022-5129
Rev. gastroenterol. Perú v.23 n.3 Lima jul./set. 2003
TRABAJOS ORIGINALES
Tratamiento del Helicobacter Pylori con Omeprazol, Amoxilina y Claritromicina en esquemas de 7 y 10 días
Wilson Rodríguez1; Arturo Pareja Cruz2; Luis Yushimito2; Alberto Ramírez Ramos3,4; Robert H. Gilman3,4; José Watanabe Yamamoto4,5; Carlos Rodríguez Ulloa4,5; Daniel Mendoza Requena3; José Guerra Valencia3; Julio Leey Casella3; Erick Chinga Alayo3,6; Billie Velapatiño3; Teresa Valencia3.
1 Hospital Militar Central - Dpto. de Gastroenterología
2 Departamento Médico - MEDCO
3 Universidad Peruana Cayetano Heredia
4 Grupo de Fisiología Gastrointestinal de la Universidad Peruana Cayetano Heredia y Universidad John Hopkins
5 Policlínico Peruano-Japonés.
6 Cook County Hospital - Dpto. de Medicina, Chicago - Illinois
RESUMEN
OBJETIVO: La terapia de un inhibidor de la bomba de protones más dos antibióticos es el tratamiento más aceptado para la infección por el Helicobacter pylori. Sin embargo, no hay consenso sobre su duración. El objetivo fue comparar los porcentajes de erradicación del esquema de omeprazol+claritromicina+amoxicilina administrados durante 7 vs 10 días.
METODOLOGÍA: Seleccionamos pacientes del Hospital Militar Central y Policlínico Peruano-Japonés con síntomas del tracto gastrointestinal superior y Helicobacter pylori. Excluimos aquéllos con úlcera péptica. Para el diagnóstico se tomaron biopsias para la prueba de la ureasa, PCR, cultivo y coloración con plata. Empleamos omeprazol+claritromicina+ amoxicilina, durante 7 días versus 10 días. Realizamos endoscopía control al mes de terminado el tratamiento, y utilizamos técnicas de biología molecular para diferenciar las recurrencias de las reinfecciones. Evaluamos la susceptibilidad a claritromicina.
RESULTADOS: Incluimos 36 pacientes en cada grupo. En ambos la erradicación fue igual: 86.1% (31/36). En varios pacientes en que persistió la bacteria se identificó la misma cepa que la inicial. El 91.18% de nuestras muestras fueron sensibles a claritromicina.
CONCLUSIONES: En el Perú la combinación de omeprazol+claritromicina+amoxicilina para erradicar la infección por el Helicobacter pylori da resultados superiores al 80%. El esquema de 7 y 10 días erradicó a la bacteria en el 86% de nuestros pacientes.
PALABRAS CLAVE: Helicobacter pylori, tratamiento, ensayo clínico.
SUMMARY
AIM: The most accepted treatment for infection by Helicobacter pylori is the proton pump inhibitor based therapy with two antibiotics. However, there is no consensus regarding the duration. The purpose here was to compare eradication percentages in the omeprazole + amoxicillin + clarithromycin regimen administered during 7 days versus 10 days and confront the results with a previous 14-day* experience in Peru.
METHOD: Patients from the Central Military Hospital and Peruvian-Japanese Hospital evidencing chronic upper gastrointestinal tract symptoms were recruited. We excluded patients with peptic ulcer. Biopsies were taken for diagnosis, for urease and PCR tests, culture and coloring with silver. Omeprazole + clarithromycin + amoxicillin was used during 7 days versus 10 days. Control endoscopy was performed one month after treatment had been completed and molecular biology techniques were used to differentiate recurrences from new infections. Susceptibility to clarithromycin was assessed.
RESULTS: 36 patients were included in each group. Eradication was the same in both groups: 86.1% (31/36). In several patients in whom the bacteria persisted, the same initial nucleus was found. In a previous study* using this same regimen during 14 days, a 93% eradication was obtained. 91.18% of our samples were susceptible to clarithromycin.
CONCLUSIONS: In Peru, the omeprazole + clarithromycin + amoxicillin combination gives results higher than 80% in the eradication of infection by Helicobacter pylori. The 7 and 10 days regimens eradicated the bacteria in 86% of our patients.
KEY WORDS: Helicobacter pylori, treatment, clinical trial.
INTRODUCCIÓN
Se acepta que el tratamiento ideal de la infección por el Helicobacter pylori debe ser simple, efectivo en todos los casos, de bajo costo y libre de efectos secundarios. Sin embargo, hasta el presente no hay un esquema terapéutico que cumpla plenamente con estos requisitos, pero sí existen muchos que se acercan al tratamiento ideal (1).
Desde hace cerca de dos décadas el Grupo de Fisiología Gastrointestinal de la Universidad Peruana Cayetano Heredia y de la Universidad de Johns Hopkins ha venido estudiando diversos esquemas de tratamiento. Inicialmente monoterapia, luego terapia doble y terapia triple, cuyos resultados han sido publicados (1-3).
Al presente hay alrededor de un centenar de esquemas que han sido propuestos y estudiados (dobles, triples, cuádruples y de variada duración), teniendo muchos de ellos porcentajes de erradicación por encima del 80% que es el mínimo de erradicación que se ha aceptado como satisfactorio. Los problemas con estos esquemas son de un lado el porcentaje de efectos secundarios, de otro su adecuado cumplimiento por parte de los pacientes y el costo.
La evidencia disponible hasta la fecha, revela que los esquemas de tratamiento con los que se obtienen mayores porcentajes de erradicación son los triples, y entre ellos la combinación de claritromicina + amoxicilina + omeprazol es el que tiene menor número de efectos secundarios, es más simple de administrar, y proporciona elevados porcentajes de erradicación. Sin embargo, la duración del tratamiento no está bien definida. Se han evaluado esquemas de 7, 10 y 14 días con resultados diversos (4-6). En el Perú el esquema de 14 dias de tratamiento ha sido estudiado en un importante número de pacientes con un porcentaje de erradicación de 93% (7).
Merece remarcarse que si no se usan técnicas moleculares, no se puede diferenciar las recurrencias de las reinfecciones luego del tratamiento, lo cual tiene importantes implicancias clínicas y de salud pública, ya que para los pacientes que sufren recurrencias sería recomendable cambiar el esquema de antibióticos utilizados, basado en un análisis de susceptibilidad antimicrobiana, mientras que para los casos con reinfecciones se puede utilizar el esquema inicial. En cuanto al contexto de la salud pública, las recurrencias indican factores asociados a resistencia bacteriana o uso irracional de antibióticos, mientras que las reinfecciones apuntan a una fuente continua de infección, considerando que en nuestro país las principales vías de transmisión son la fecal-oral y a través del agua (2,8).
Considerando los aspectos anteriormente presentados, creímos pertinente realizar este estudio, con el objeto de presentar nuestra experiencia al comparar la eficacia y el perfil de reacciones adversas de un esquema triple aplicado en periodos de tratamiento de 7 y 10 días.
MATERIAL Y MÉTODOS
Pacientes
El presente estudio se realizó en el Hospital Militar Central y en el Policlínico Peruano Japonés, ambos localizados en la ciudad de Lima, Perú, habiéndose incluido los pacientes que eran referidos para esofagogastroduodenoscopía por presentar síntomas crónicos del tracto gastrointestinal superior. Se excluyeron aquéllos con úlcera gástrica o duodenal activa, cáncer gástrico, gastrectomizados, vagotomizados y quienes habían recibido en el curso de las últimas cuatro semanas, antibióticos, bismuto o inhibidores de la bomba de protones.
Se consideró que un paciente tenía infección por el Helicobacter pylori cuando la biopsia gástrica sometida a coloración con plata era positiva, habiéndose realizado además la prueba de la ureasa y PCR. Los pacientes fueron distribuidos al azar para incorporarse al grupo de 7 y 10 días de tratamiento. El estudio fue abierto, sin embargo fue ciego para el patólogo que evaluó las láminas. A partir de las cuatro semanas de terminar la terapia los pacientes fueron reexaminados mediante esofagogastroduodenoscopía y biopsias para evaluar el porcentaje de erradicación.
Determinamos el nivel socioeconómico de los pacientes de acuerdo a un cuestionario.
Grupos de tratamiento
Los pacientes se dividieron en dos grupos de tratamiento con similares características en grupos de edad, sexo, raza y nivel socioeconómico. Al grupo I se le administró Omeprazol 20mg, Amoxicilina 1g. y Claritromicina 500mg bid durante 7 días. Al grupo II se le dio el mismo esquema de medicación con la diferencia que el tratamiento se dio durante 10 días.
Cálculo de la muestra
Considerando una tasa de recaída de 0.3 en el grupo de 7 días, y de 0.058 en el grupo de 10 días, con un poder de 80%, para detectar por lo menos una diferencia de 0.25, obtuvimos una muestra de por lo menos 36 personas en cada grupo. Los datos de recaída los conseguimos de una evaluación piloto que realizamos con los primeros 27 pacientes.
Endoscopía
La endoscopía se realizó como fue descrita anteriormente (9). Los endoscopios flexibles utilizados eran de marca Fujinon modelo EG450 HR. Previo al examen, para prevenir la contaminación, los endoscopios, fueron lavados y esterilizados cuidadosamente con soluciones antimicrobianas (glutaraldehído, endozime).
Se tomó 3 biopsias en cada paciente, una para la coloración con plata, otra para la prueba rápida de la ureasa, y la tercera para el estudio de PCR.
Estudios Histológicos
Las biopsias para estudio histológico se fijaron en formol neutro. Luego de su inclusión en parafina, se efectuaron cortes de 3-4 micras de espesor coloreándose con plata (método de Warthin Starry). Las muestras fueron leídas por un patólogo experto.
Prueba Rápida de la Ureasa
Una biopsia del antro se colocó en agar-úrea procediéndose a realizar la lectura a los 15-30 minutos, y 16, 12 y 24 horas respectivamente. Se consideró la prueba positiva cuando se visualizó la variación de color del amarillo a rojo grosella.
Cultivos bacteriológicos
Se evaluó mediante cultivo a un total de 256 pacientes. En todos los casos, los cultivos fueron obtenidos de las biopsias del antro. Se utilizó el método estándar para el crecimiento de la bacteria en condiciones de microaerofilia (5% de oxígeno, 10% de dióxido de carbono y 85% de nitrógeno), en agar DIFCO BHI (brain Herat infusion) suplementado con 10% de sangre de caballo o de carnero (7).
Susceptibilidad antimicrobiana
La susceptibilidad antimicrobiana fue realizada para el antibiótico claritromicina en 36 muestras mediante el método del E-test (AB Biodisk, Solna, Sweden), según Valdez et al (10). La concentración inhibitoria mínima (MIC) fue definida como la menor concentración del antibiótico que resultó en una inhibición completa (ausencia de colonias). Para la resistencia a claritromicina se consideró un valor mayor o igual a 0.125 ug/ml.
Reacción en Cadena de Polimerasa (PCR)
Los fragmentos de ADN del H. pylori fueron amplificados mediante el uso de primers dirigidos al gen de la Ureasa, en un volumen de reacción de 25 ul que conteniendo 2 mM de MgCl2, 0.25 mM de dNTPs, 0.4 uM de cada primer, 1X de Buffer, 0.02 U/ul Taq Polimerasa, y 5 ul del ADN extraído. Los siguientes oligonucleotidos, los cuales fueron usados como cebadores o primers, fueron derivados de la secuencia del gen de la ureasa (ureB) reportados por Jeong et al (11). UreaseB-F (5'CGTCCGGCAATAGCTGCCATAGT) y UreaseB-R (GTAGGT CCTGCTACTGAAGCCTTA). Las temperaturas que se usaron fueron las siguientes: 1 min a 94°C, 1 min a 67 °C y 1 min a 72 °C. Se realizaron 35 ciclos de amplificación, luego una corrida electroforética en agarosa al 2% con bromuro de etidio en la muestra. Se observó bajo iluminación ultravioleta evidenciándose la presencia de un fragmento de banda amplificado de un tamaño de 467 pares de bases.
Ensayo de RAPD-PCR (Ramdom Amplified Polymorphic DNA-PCR)
Utilizando muestras de los cultivos, se evaluaron 4 pacientes que permanecieron positivos después del tratamiento, mediante la técnica de Amplificación de Polimorfismos de ADN al Azar (RAPD) usando los procedimientos y condiciones descritos en Soto et al (7). Este análisis determinó la diferencia entre cepas comparando los patrones de migración de ADN en un gel de electroforesis usando 4 cebadores diferentes.
Análisis estadístico
Consideramos eficacia como: número de pacientes sin infección por el Helicobacter pylori en la endoscopía control/Número de pacientes que culminaron el tratamiento. Consideramos recurrencia como el hallazgo de la misma cepa que la identificada antes del inicio del tratamiento. Consideramos reinfección como el hallazgo de una cepa diferente a la identificada antes del tratamiento. Las variables que incluimos fueron edad, sexo, condición socioeconómica, y cumplimiento del tratamiento.
Utilizamos la t de students para comparar las variables numéricas, y el chi cuadrado para las variables categóricas. Consideramos como significativo un p<0.05. Para la elaboración de la base de datos y el procesamiento utilizamos el programa estadístico SPSS 9.0.
Aspectos éticos
El estudio fue aprobado por el Comité de Ética del Hospital Militar Central y del Policlínico Peruano Japonés. A todos los pacientes se les solicitó un consentimiento informado y se les explicó el objetivo del estudio, el tratamiento y los posibles efectos secundarios.
RESULTADOS
Pacientes
Evaluamos endoscópicamente a 256 pacientes con síntomas crónicos del tracto gastrointestinal superior (152 en el Policlínico Peruano Japonés y 104 en el Hospital Militar Central). De ellos, encontramos infección por el H. pylori en 105 (41%) pacientes, de los cuales 9 no desearon participar, incluyéndose finalmente en el estudio a 96 pacientes: 48 del Hospital Militar Central (23 en el Grupo I de 7 días y 25 en el Grupo II de 10 días de tratamiento) y 48 del Policlínico Peruano Japonés (25 en el Grupo I y 23 en el Grupo II), asignándose 48 al Grupo I y 48 al Grupo II. Todos ellos recibieron tratamiento completo, pero no acudieron al control 12 (25%) personas de cada grupo, porque no fue posible contactarlos nuevamente, algunos no desearon realizarse la endoscopía control y otros por motivos de viaje.
Al final, realizamos el análisis de las tasas de erradicación en 36 personas en cada grupo. Los grupo I y II fueron comparables en cuanto a edad promedio (42 vs 45 años) (p=NS), y porcentaje de mujeres (50% (18/36) vs 52.6% (20/38), p=NS) respectivamente; todos fueron de raza mestiza y procedentes de nivel socioeconómico medio o alto.
Tasas de erradicación
Logramos la erradicación en el 86.1% (31/36) de pacientes del Grupo I. El mismo valor logramos en el Grupo II. (Tabla 1). Los controles se realizaron después de 1 a 3 meses de culminada la terapia antibiótica. Pudimos realizar el RAPD en 4 de los 10 pacientes en los cuales no se logró erradicar al H. pylori. En todos ellos, las cepas identificadas después del tratamiento fueron las mismas que las iniciales, con lo que se descartó la posibilidad de reinfección.
Susceptibilidad a claritromicina
En 34 (47.2%) de las 72 muestras previas al tratamiento, pudimos realizar análisis de susceptibilidad a claritromicina. 91.18% (31/34) de estas muestras fueron sensibles a claritromicina y 8.82% (3/34) fueron resistentes. En 2 de los 3 pacientes con muestras inicialmente resistentes se erradicó la bacteria después del tratamiento.
También evaluamos 2 de las 72 muestras aisladas después de recibir el tratamiento, de ellas 1 fue sensible, y la otra presentó resistencia intermedia.
Reacciones adversas
Ningún paciente fue retirado del estudio por haber presentado efectos secundarios moderados o severos. Las reacciones adversas fueron similares en los grupos I y II (Tabla 2). Ninguno presentó rash o reacción alérgica. Ninguno fue hospitalizado debido a las reacciones adversas y no fue necesario suspender el tratamiento debido a los efectos secundarios.
DISCUSIÓN
En el presente estudio, empleando este esquema durante 7 y 10 días hemos obtenido 86.1% de erradicación, superando el porcentaje de erradicación de 80%, que es el porcentaje mínimo aceptado que debe de tener un esquema para eliminar al Helicobacter pylori (1). No encontramos diferencia en cuanto a la eficacia de los tratamientos de 7 y 10 días, ni tampoco en la tasa de persistencia de la bacteria post-tratamiento. Disponiendo últimamente de la técnica del RAPD, que permite diferenciar la reinfección de la recurrencia, pudimos realizar esta prueba en el 40% (4/10) de los pacientes en los cuales no se logró la erradicación, determinando que en todos ellos se trataba de la misma cepa que la previa al tratamiento, con lo que se confirmó que el tratamiento no había sido efectivo, no tratándose de una reinfección.
Creemos que las recurrencias se asociaron principalmente a la duración de ambos esquemas de tratamiento, y no a una resistencia intrínseca del Helicobacter pylori a los antibióticos utilizados (claritromicina y amoxicilina), ya que esta combinación ha sido bastante exitosa en nuestro país, en esquemas de 14 días de duración (7).
Nuestros resultados son confiables porque ambos grupos de tratamiento fueron comparables en cuanto a edad, sexo, condiciones socioeconómicas, habiéndonos asegurado que el cumplimiento de la terapia fue óptimo. Ambos grupos presentaron similar frecuencia de reacciones adversas, siendo todas ellas menores, tales como sabor amargo en la boca, dolor abdominal, náuseas, diarrea y cefalea, las cuales remitieron a los pocos días sin requerir la suspensión del tratamiento.
El 8.82% de las muestras evaluadas antes de iniciar la terapia antibiótica fueron resistentes a claritromicina. Nuestros hallazgos son consistentes con los reportados por otros grupos de estudio, donde la prevalencia de resistencia no fue mayor al 10% (12,13), sin embargo contrastan con los de otro trabajo realizado en el Perú, en el cual encuentran una resistencia en el 50% de sus muestras (14). En el estudio de Soto, Bautista, Gilman y col (7), pese a encontrar 27% de resistencia, alcanzaron una erradicación del 93%. Tomando en cuenta estas evidencias, y considerando que: 1) no siempre la resistencia in vitro concuerda con los resultados in vivo (15); 2) la terapia triple que incluye a claritromicina logra altas tasas de erradicación (7,15); 3) la poca frecuencia de reacciones adversas significativas con este esquema; y que 4) la utilización de tres medicamentos asegura una mayor eficacia (1,2,15); creemos que el tratamiento para la infección por el Helicobacter pylori debe ser la terapia triple (amoxicilina, claritromicina y omeprazol), preferentemente durante 14 días. Sin embargo, es prudente realizar un monitoreo del perfil de resistencia a claritromicina en el futuro y continuar con las evaluaciones de eficacia de este esquema de tratamiento.
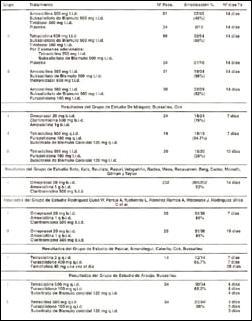
En la Tabla 3 sintetizamos todos los esquemas de tratamiento del Helicobacter pylori que se han investigado en el Perú, remarcando aquéllos con los que se ha obtenido un porcentaje de erradicación superior al 80% y con un número estadísticamente representativo de pacientes.
En el Perú, Soto, Bautista, Gilman y col. reportan un porcentaje de erradicación del 93% con la combinación de omeprazol + amoxicilina + claritromicina administrados durante 14 días a 216 pacientes (7). De Idiaquez, Bussalleu y col. reportaron en un estudio de 24 pacientes con este esquema triple prescrito durante 7 días una erradicación de 75% (17). Explicamos esta diferencia, por el número de pacientes evaluados por estos autores que no llega a las cifras requeridas para que los resultados tengan significación.
En conclusión, los esquemas de tratamiento triple para erradicar al Helicobacter pylori utilizando omeprazol, claritromicina y amoxicilina por 7 y 10 días, son similares en cuanto a eficacia, tasa de recurrencia después de 1 mes de seguimiento y perfil de reacciones adversas. En base a los estudios de Soto, Bautista Gilman y col. creemos recomendable utilizar el esquema de 14 días, pero si esta combinación se administra 7 días se logra también un elevado porcentaje de erradicación, superior al 80%, establecido como mínima eficacia. Debido a la alta tasa de reinfección descrita en nuestro país, es necesaria la búsqueda de otras medidas complementarias al tratamiento antibiótico, tales como el mejoramiento de las prácticas higiene, la eliminación del Helicobacter pylori de fuentes comunes, y el uso de vacunas, lo cual reduciría la alta prevalencia de la infección en nuestro país (20), y probablemente de sus enfermedades asociadas.
Tabla 1. Porcentaje de erradicación en cada grupo
de tratamiento

Tabla 2. Efectos Secundarios (%)
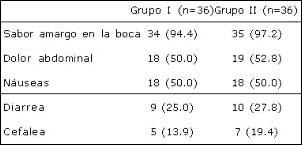
Tabla 3. Resultados del Grupo de Fisiología Gastrointestinal
de la Universidad Peruana Cayetano Heredia y
la Universidad de Jhons Hopkins
AGRADECIMIENTOS
A la Corporación MEDCO SAC por haber financiado los gastos de laboratorio y personal técnico del presente estudio, y proporcionado el omeprazol, la claritromicina y la amoxicilina.
A las Enfermeras Sra. Aurora Cataldo y Srta. Carmen Tamamoto y personal del Servicio de Gastroenterología del Policlínico Peruano Japonés, y a las enfermeras Marianela Oré y Patricia Ávila, y personal del Departamento de Gastroenterología del Hospital Militar Central por su valioso apoyo.
A los doctores María Cristina Segovia y Marcos Chávez por su ayuda en la evaluación y captación de pacientes.
A la Srta. Yenyffer Barreto Tuero, por su soporte secretarial.
BIBLIOGRAFÍA
1. RAMÍREZ RAMOS A, PAREJA CRUZ A, LEEY CASELLA J, MENDOZA REQUENA D. Helicobacter pylori en el Perú. Editorial Santa Ana. 2003. [ Links ]
2. RAMÍREZ RAMOS A, LEEY J, MENDOZA D, GUERRA J. Helicobacter pylori. Epidemiología - Diagnóstico - Tratamiento. Consensos Mundiales. Experiencia en el Perú. Diagnóstico 2003; 42(1):23-37. [ Links ]
3. RAMÍREZ RAMOS A, GILMAN RH, LEÓN BARÚA R, RECAVARREN S, WATANABE J, et al. Rapid recurrente of Helicobacter pylori infection in Peruvian patients after successful eradication. Clin Inf Dis 1997; 25:1027-1031. [ Links ]
4. MISLEWICK JJ, HARRIS AW, BARDHAN KD, LEVI S, MORAIN CO, COOPER BT et al. One week triple therapy for Helicobacter pylori: a multicentre comparative study. Gut 1997; 41:735-739 (December). [ Links ]
5. BROUTET N, MARAIS A, LAMOULIATTE H, DE MASCAREL A, SAMOYEAU R, SALAMON R, et al. CagA Status and Eradication Treatment Outcome of Anti-Helicobacter pylori Triple Therapies in Patients with Nonulcer-Dyspepsia. J Clin Microbiol 2001; 39:1319-1322. [ Links ]
6. DE BOER WA, TYTGAT GNJ. Regular new: Treatment of Helicobacter pylori infection. BMJ 2000; 320:31-34. [ Links ]
7. SOTO G, BAUTISTA C, ROTH DE, GILMAN RH, VELAPATIÑO B, OGURA M et al. Helicobacter pylori Reinfection is Common in Peruvian Adults Following Successful Antibiotic Eradication Therapy. Aceptado para publicación: Journal of Infectious Diseases. [ Links ]
8. KLEIN PD, Gastrointestinal Physiology Working Group, Graham DY, Gaillour A, Opekun AR, Smith EO. Water source as risk factor for Helicobacter pylori infection in Peruvian children. Lancet 1991; 337:1503-1506. [ Links ]
9. GILMAN RH, LEÓN-BARÚA R, COK J et al. Rapid identification of Campylobacter pylori in Peruvians with gastritis. Dis Dis Sci 1986; 31: 1089-94. [ Links ]
10. VALDEZ Y, VELAPATIÑO B, GILMAN RH, GUTIÉRREZ V, LEÓN C. Antimicrobial Susceptibility of Helicobacter pylori Determined by the E test using Tetrazolium Egg Yolk agar. J Clin Microbiol 1998; 36: 2784-5. [ Links ]
11. JEONG JY, MUKHOPADHYAY AK, DAILIDIENE D, WANG Y, VELAPATIÑO B, GILMAN RH et al. Sequential Inactivation of rdxA (HP0954) and frxA (HP0642) Nitroreductase Genes Causes Moderate and High-Level Metronidazole Resistance in Helicobacter pylori. J Bacteriol 2000; 182: 5082-5090 [ Links ]
12. OLSON C, EDWARDS A. Primary susceptibility of Helicobacter pylori to clarithromycin compared to metronidazole in patients with duodenal ulcers associated with Helicobacter pylori. Gastroenterology 1995; 90: 1589. [ Links ]
13. PETERSON WL, GRAHAM DY, MARSHALL B, BLASER MJ, GENTA MR, KLEIN PD et al. Clarithromycin as monotherapy for eradication of Helicobacter pylori: a randomized, double-blind trial. Am J Gastroenterol 88; 1860-1864. [ Links ]
14. VASQUEZ A, VALDEZ Y, GILMAN RH, MCDONALD JJ, WESTBLOM TU, BERG D et al. Metronidazole and clarithromycin resistance in Helicobacter pylori determined by measuring mics of antimicrobial agents in color indicator egg yolk agar in a miniwell format. J Clin Microbiol 1996; 34: 1232-1234. [ Links ]
15. DUNN BE, COHEN H, BLASER MJ. Helicobacter pylori. Clin Microbiol Rev 1997; 10 (4): 720-741. [ Links ]
16. AKOPYANZ N, BUKANOV NO, WESTBLOM TU, KRESOVICH S, BERG DE. DNA diversity among clinical isolates of Helicobacter pylori detected by PCR-based RAPD fingerprinting. Nucleic Acids Res 1992; 20: 5137-42. [ Links ]
17. DE IDIAQUEZ D, BUSSALLEU A, COK J. Nuevos esquemas terapéuticos para el tratamiento de la infección por Helicobacter pylori y evaluación de la reinfección al año post tratamiento exitoso. Lima: CIMAGRAF, 2001. [ Links ]
18. PÁUCAR H, ARRUNÁTEGUI L, CABELLO J, COK J, BUSSALLEU A. Tratamiento de la úlcera péptica duodenal mediante la erradicación del Helicobacter pylori: estudio controlado randomizado. Rev Gastroenterol Perú 1997; 17: 203-13. [ Links ]
19. ARAUJO R. Nuevo esquema ultracorto para erradicar la infección por Helicobacter pylori utilizando tetraciclina, furazolidona y subcitrato de bismuto coloidal en pacientes dispépticos con o sin úlcera péptica en el Hospital Nacional Cayetano Heredia. Tesis para optar el Grado de Bachiller en Medicina. Universidad Peruana Cayetano Heredia. Lima, Perú. 2003. [ Links ]
20. RAMÍREZ RAMOS A, CHINGA E, MENDOZA D, LEEY J, SEGOVIA-CASTRO M, OTOYA C. Variación de la prevalencia del Helicobacter pylori en el Perú. Período 1985-2002, en una población de nivel socioeconómico medio y alto. Rev Gastroenterol Perú 2003; 23: 92-98 [ Links ]