INTRODUCCIÓN
El carcinoma hepatocelular (CHC) es el tipo más frecuente de cáncer primario de hígado, comúnmente, se desarrolla en personas que padecen enfermedades hepáticas crónicas, como cirrosis causada por hepatitis B o C, y la esteatosis hepática no alcohólica 1. Según GLOBOCAN 2022, indica que CHC ocupa el octavo lugar en términos de incidencia y cuarto lugar en términos de mortalidad, a nivel mundial 2. Asimismo en el 2022, el Perú reportó un 4,9% de incidencia y un 4,2% de mortalidad, ambos estandarizados por edad (mundial) por 100 000 respectivamente 2.
La vigilancia es la estrategia clave para la atención oportuna del cáncer, principalmente en los pacientes con factores de riesgo de CHC 3, como la cirrosis hepática que tiene una prevalencia del 85% al 95% en esta población, y recientemente también se consideró a los pacientes con fibrosis hepática avanzada (estadio F3) 4,5.
En ese sentido, el manejo oportuno de la enfermedad podría mejorar el pronóstico de los pacientes con CHC, lo cual ayudaría a reducir la mortalidad, y mejorar la calidad de vida de las pacientes en mención. Por ello, la Dirección de Guías de Práctica Clínica, Farmacovigilancia y Tecnovigilancia del Instituto de Evaluación de Tecnologías en Salud e Investigación (IETSI) del Seguro Social del Perú (EsSalud) elaboró la guía de práctica clínica (GPC) basada en evidencias para el manejo de pacientes con CHC, cuyas recomendaciones y puntos de buena práctica clínica serán aplicadas por profesionales de la salud en EsSalud. El presente artículo es un resumen de dicha GPC.
MATERIALES Y METODOLOGÍA
El procedimiento seguido para la elaboración de la presente GPC está detallado en su versión "in extenso", la cual puede descargarse de la página web del IETSI de EsSalud (https:// ietsi.essalud.gob.pe/gpc-guias-de-practica-clinica/).
En resumen, se aplicó la siguiente metodología:
Conformación del grupo elaborador de la guía (GEG):
Se conformó un GEG, que incluyó metodólogos, médicos gastroenterólogos, oncólogos médicos, cirujanos oncólogos, cirujanos generales, y radiólogos intervencionistas.
Formulación de preguntas:
En concordancia con los objetivos y alcances de esta GPC, el GEG formuló 8 preguntas clínicas (Tabla 1), cada una de las cuales pudo tener una o más preguntas PICO (Population, Intervention, Comparator, Outcome). A su vez, cada pregunta PICO pudo tener uno o más desenlaces (o outcomes) de interés.
Búsqueda y selección de la evidencia:
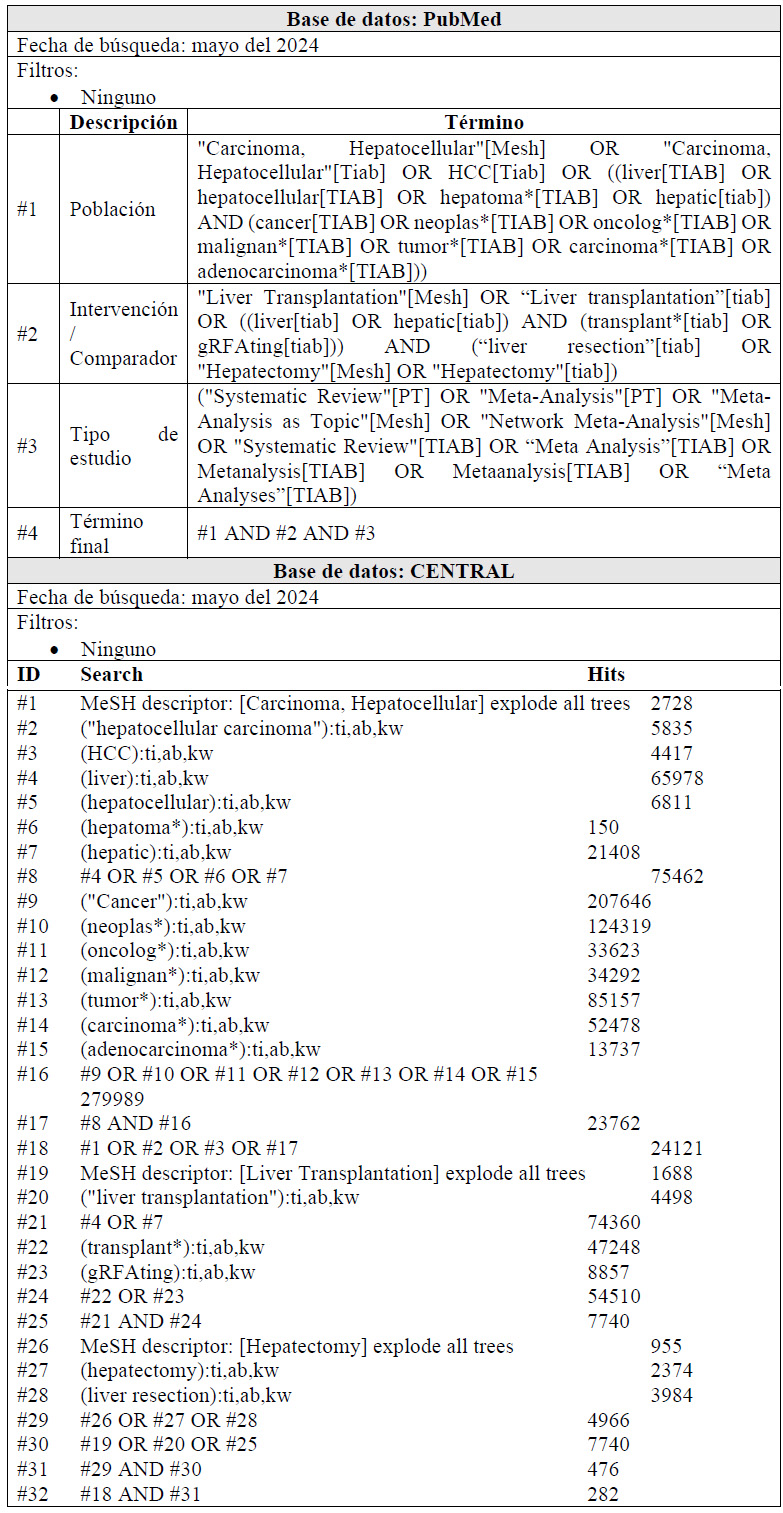
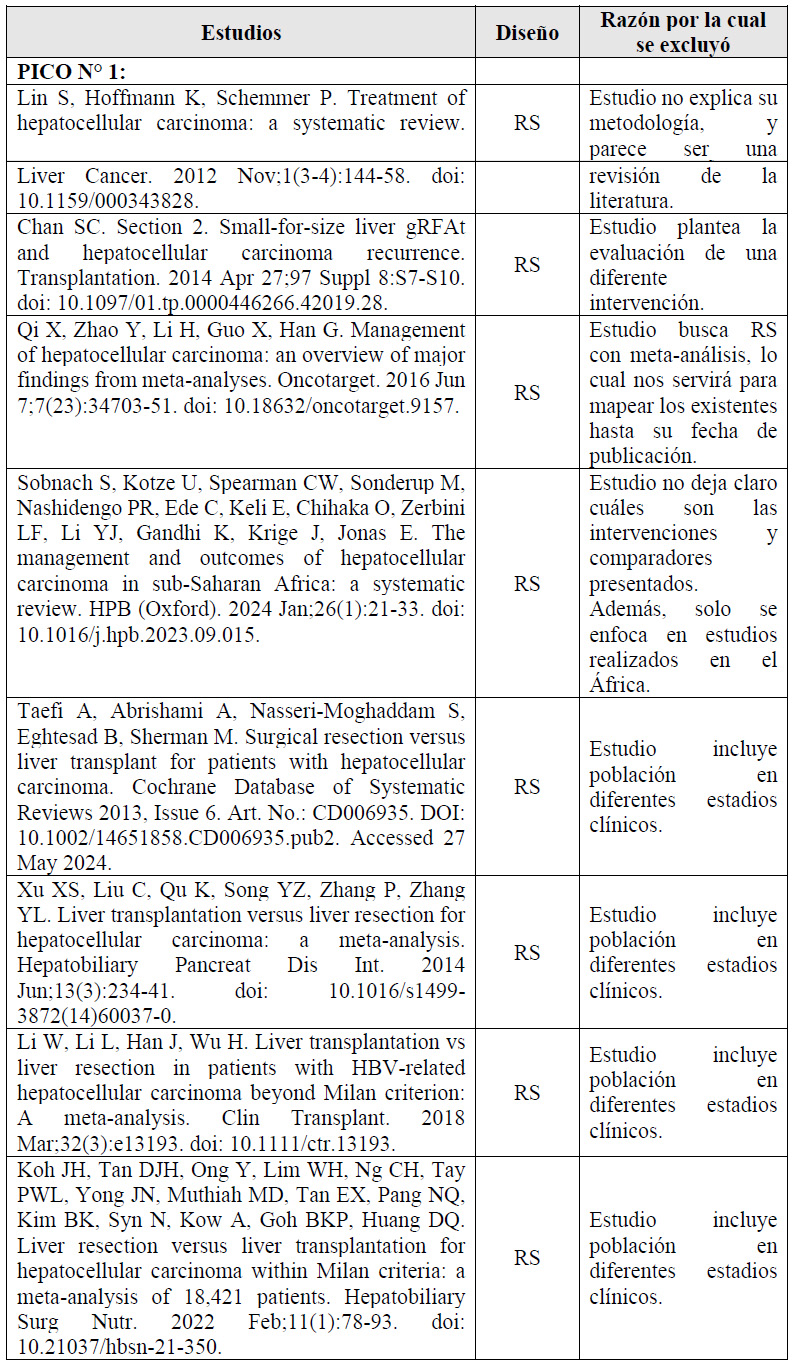
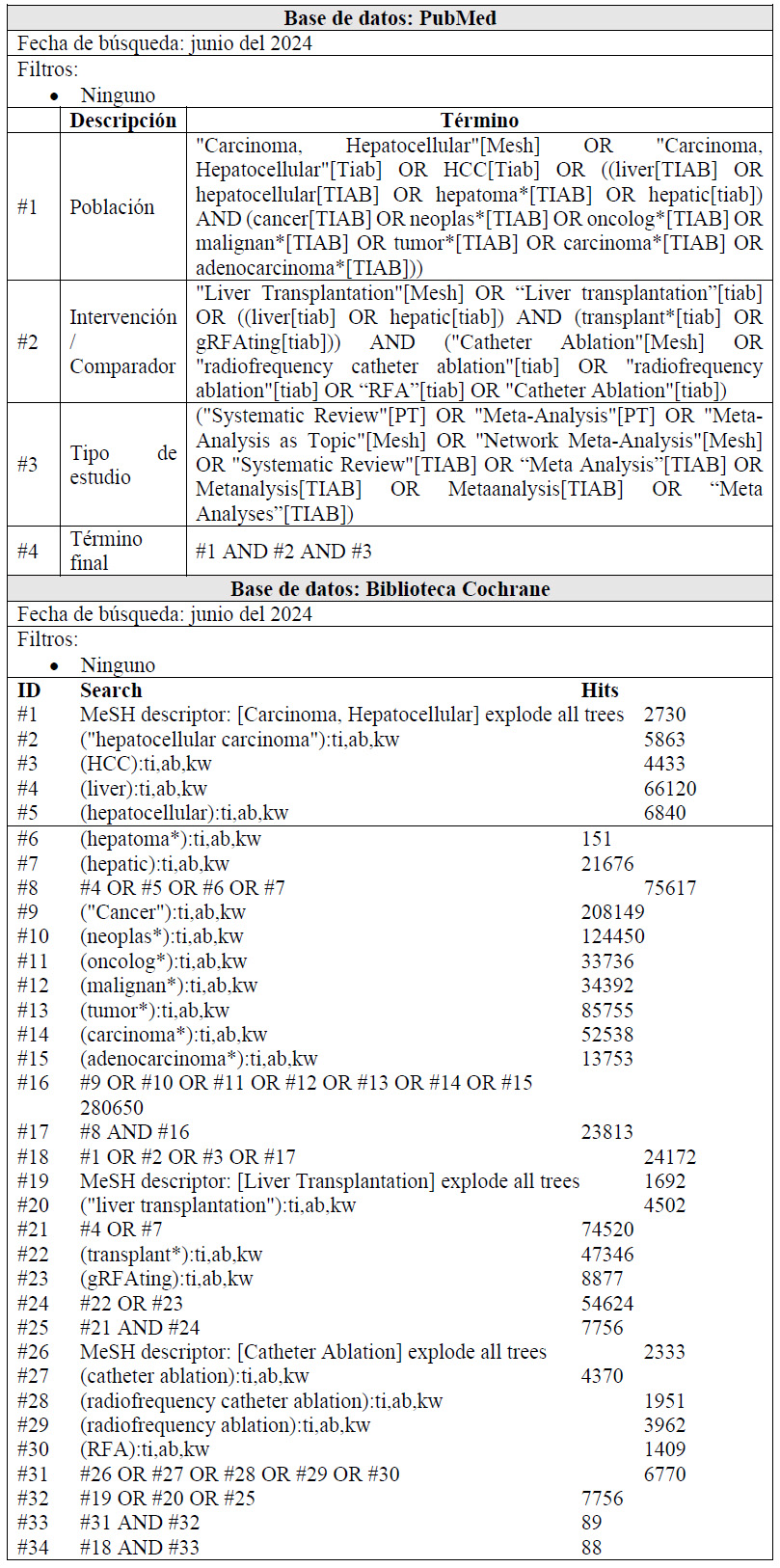
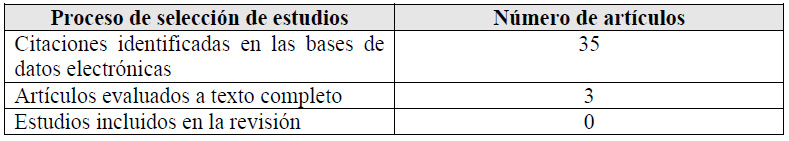
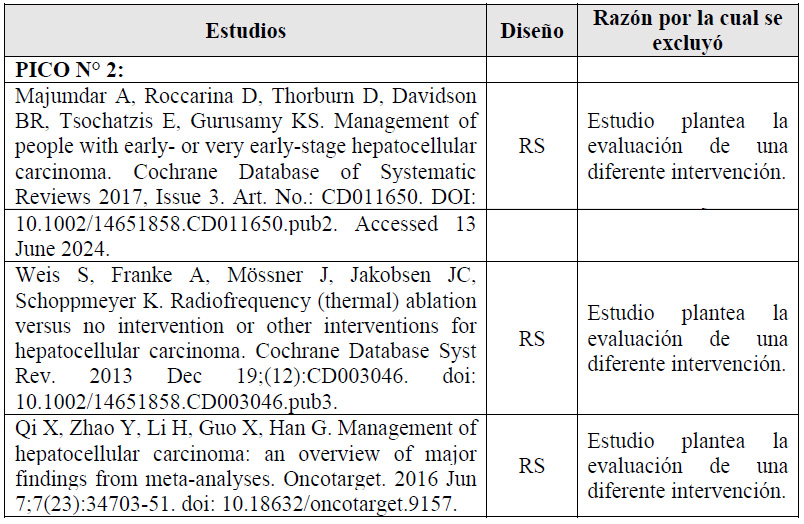
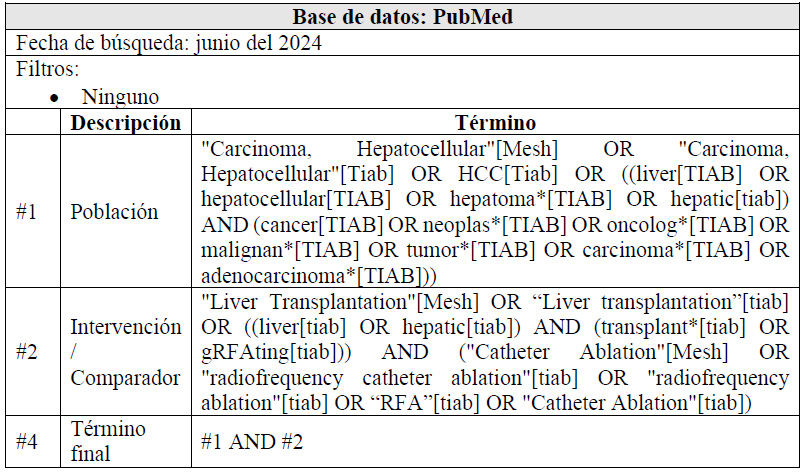
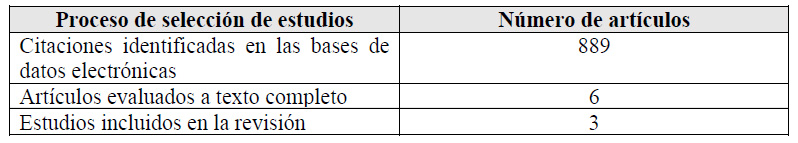
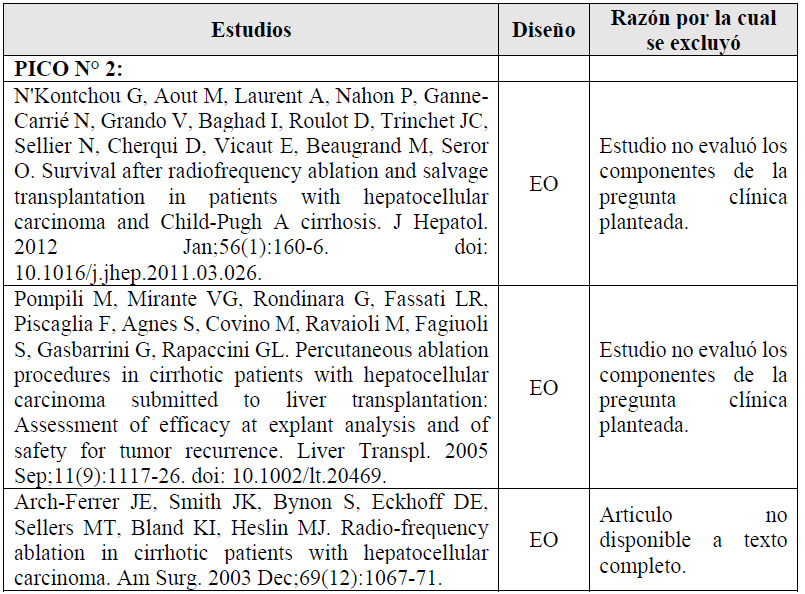
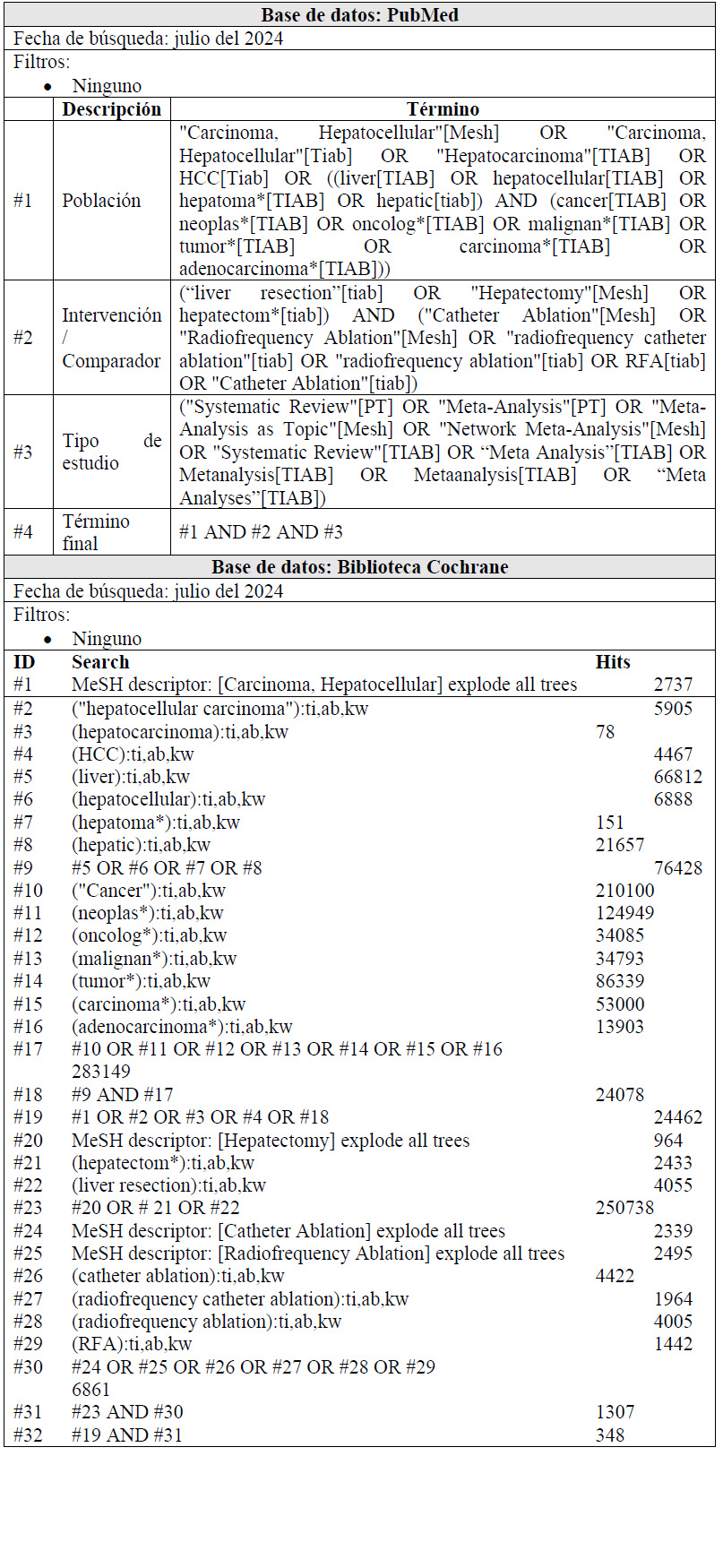
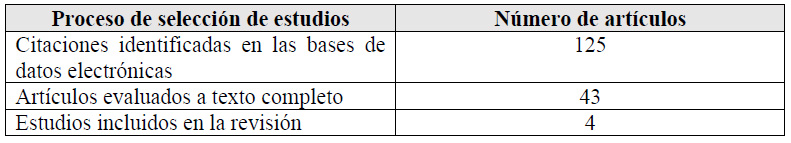
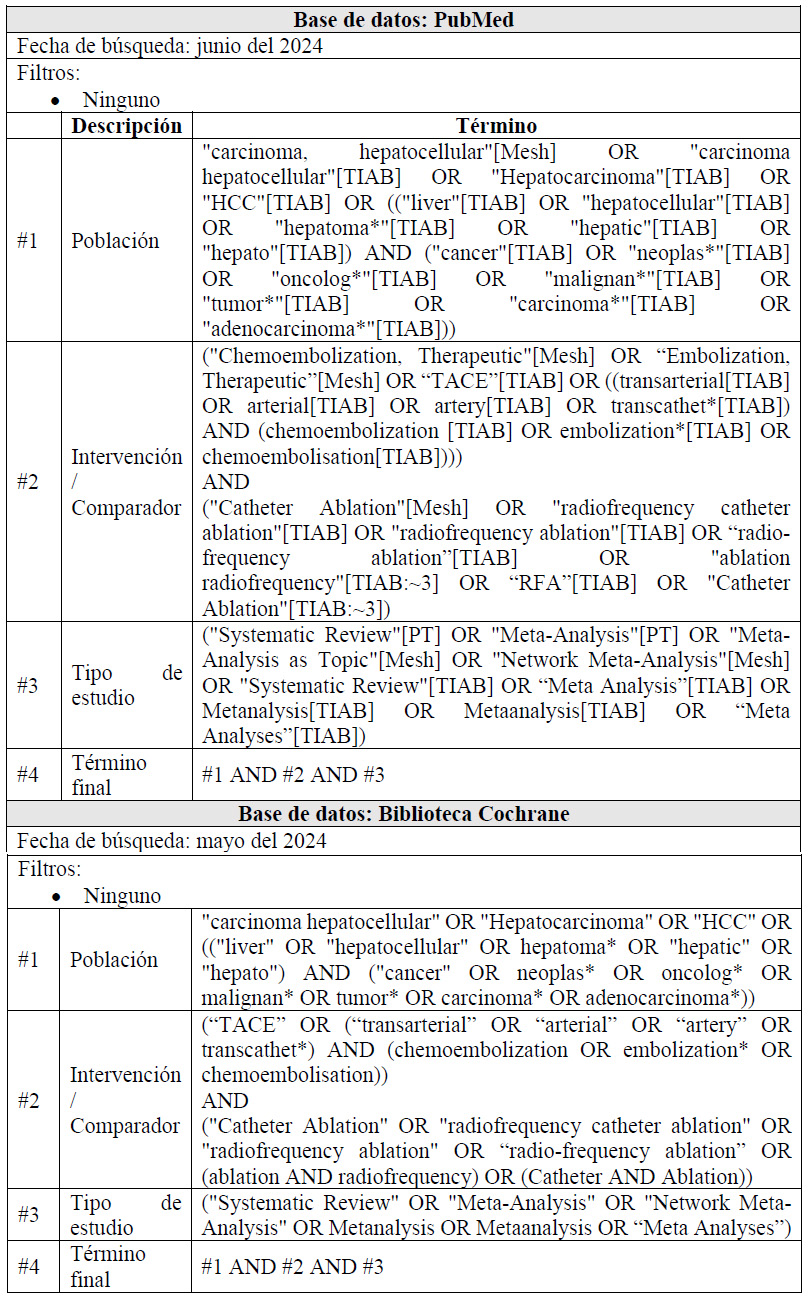
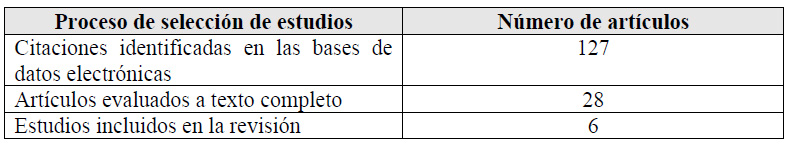
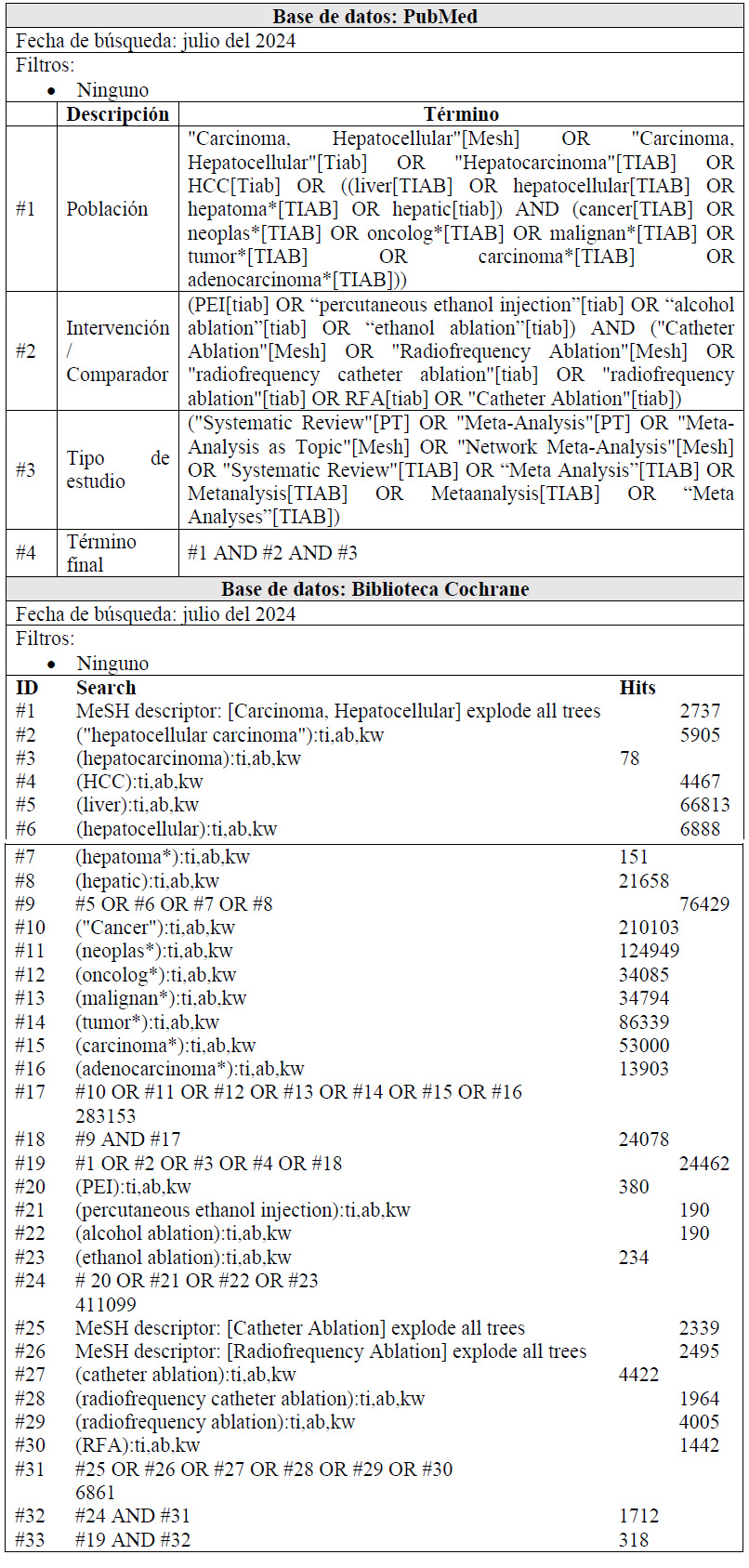
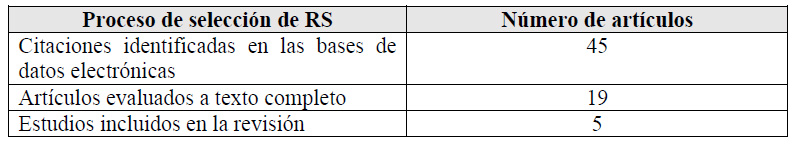
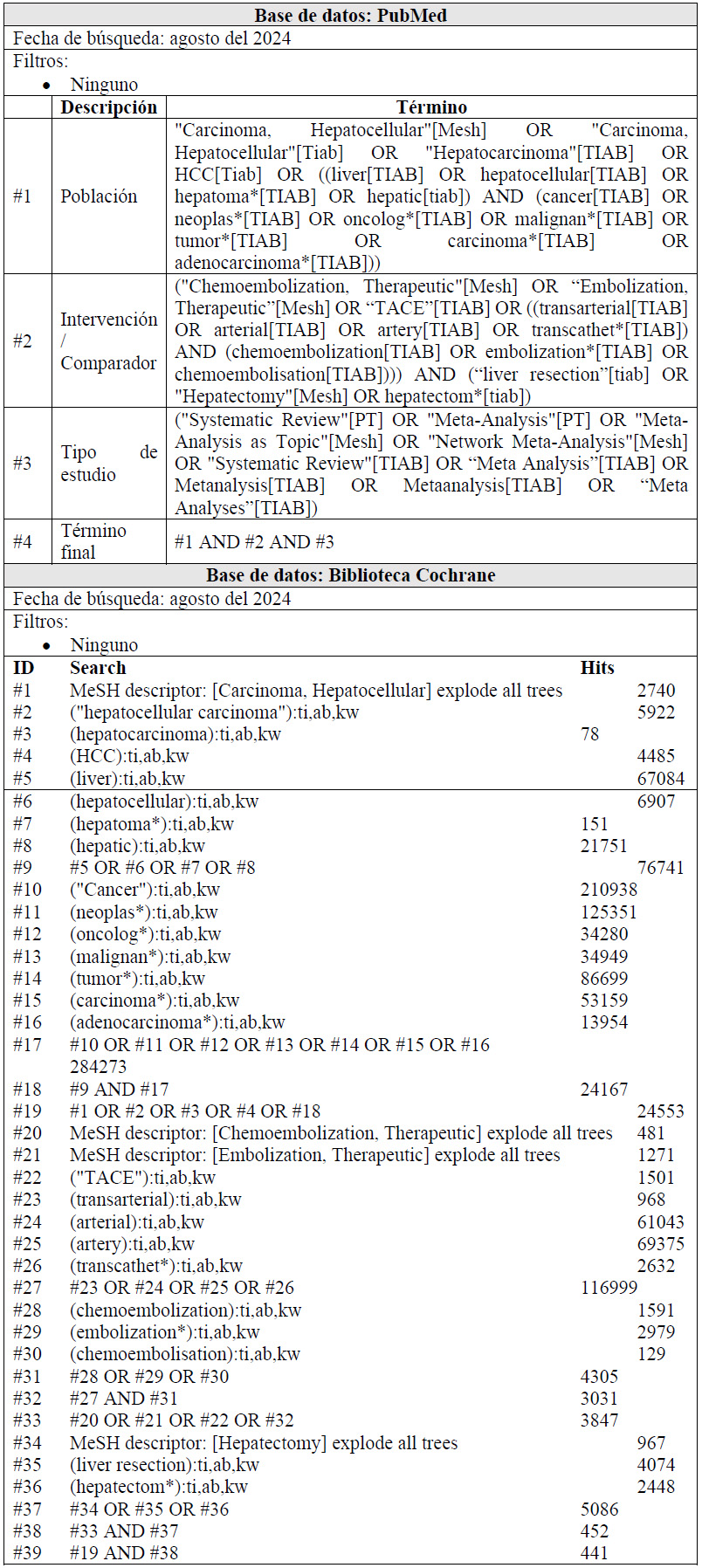
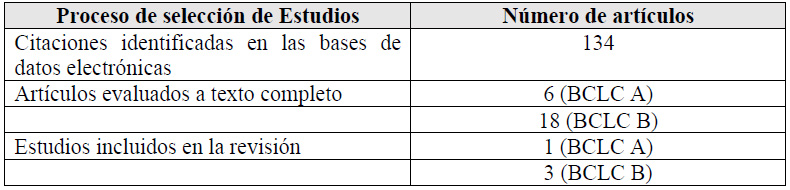
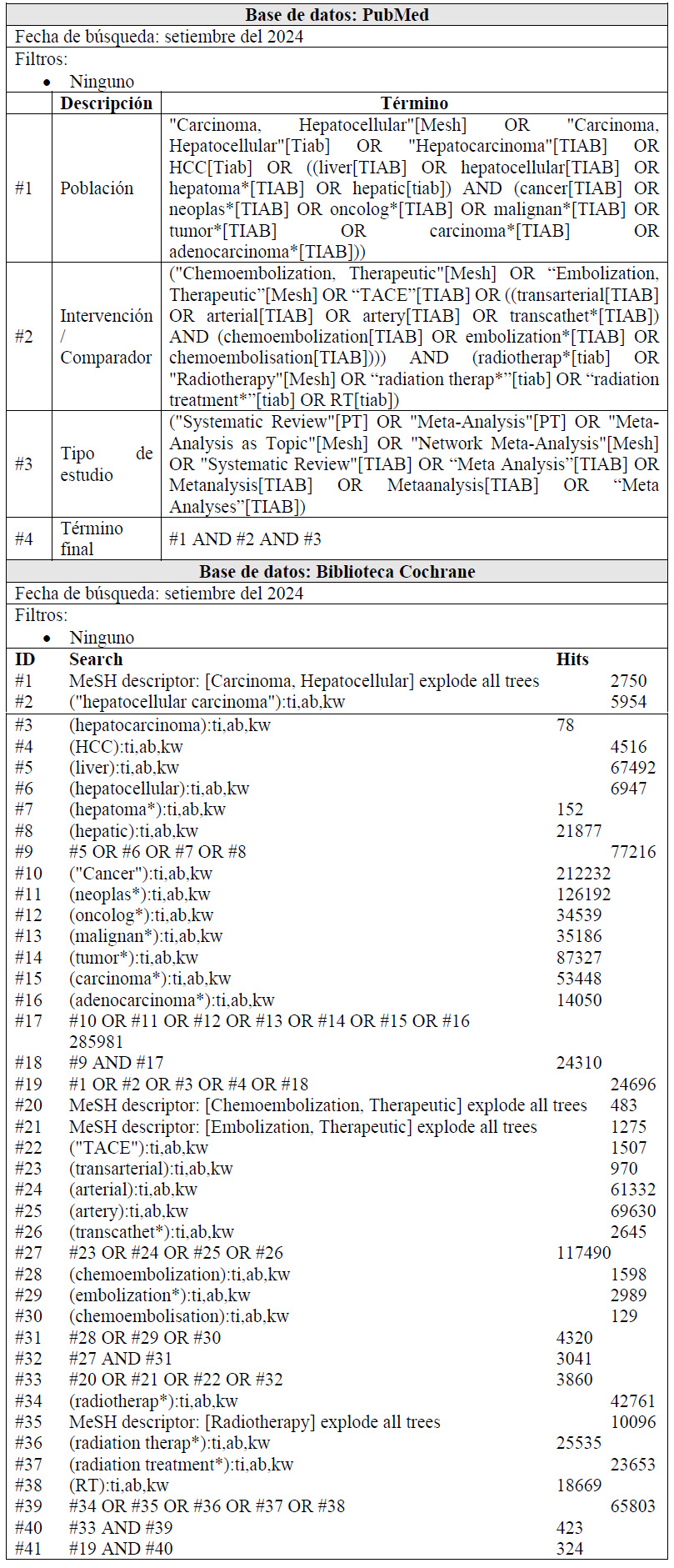
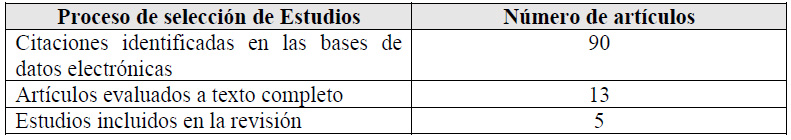
Para cada pregunta PICO, durante mayo del 2024, se buscaron revisiones sistemáticas (RS) publicadas como artículos científicos (mediante búsquedas sistemáticas en PubMed y Biblioteca Cochrane) o realizadas como parte de una GPC previa (mediante una búsqueda sistemática de GPC). Cuando se encontraron RS de calidad aceptable según el instrumento A Measurement Tool to Assess Systematic Reviews-II (AMSTAR II) 6 modificado por IETSI, se escogió una para cada desenlace de interés, la cual fue actualizada cuando el GEG lo consideró necesario. Finalmente, cuando no se encontró ninguna RS de calidad aceptable, se realizó una búsqueda de novo de estudios primarios.
Evaluación de la certeza de la evidencia y cálculo de efectos absolutos:
Para cada desenlace de cada pregunta PICO, se evaluó la certeza de la evidencia siguiendo la metodología de Grading of Recommendations Assessment, Development, and Evaluation (GRADE) 7.
Asimismo, se calcularon los efectos absolutos para cada desenlace (diferencias de riesgos para desenlaces dicotómicos, o diferencias de medias para desenlaces numéricos). Para el cálculo de las diferencias de riesgos, se consideró que la incidencia del desenlace en el grupo control fue la reportada por el cuerpo de la evidencia, salvo se mencione lo contrario para alguna pregunta.
Formulación de las recomendaciones:
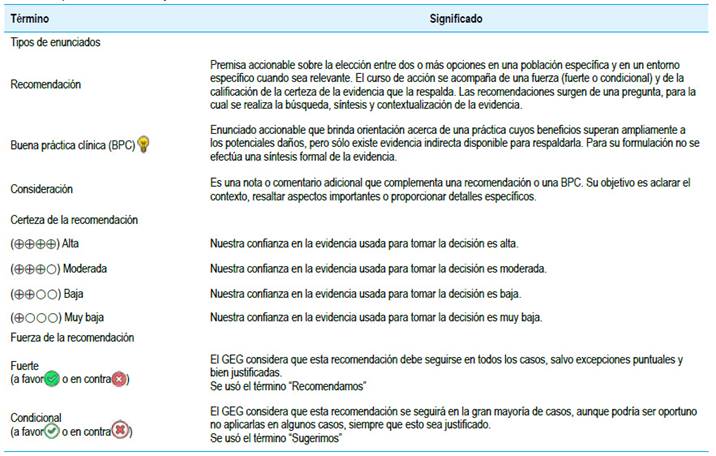
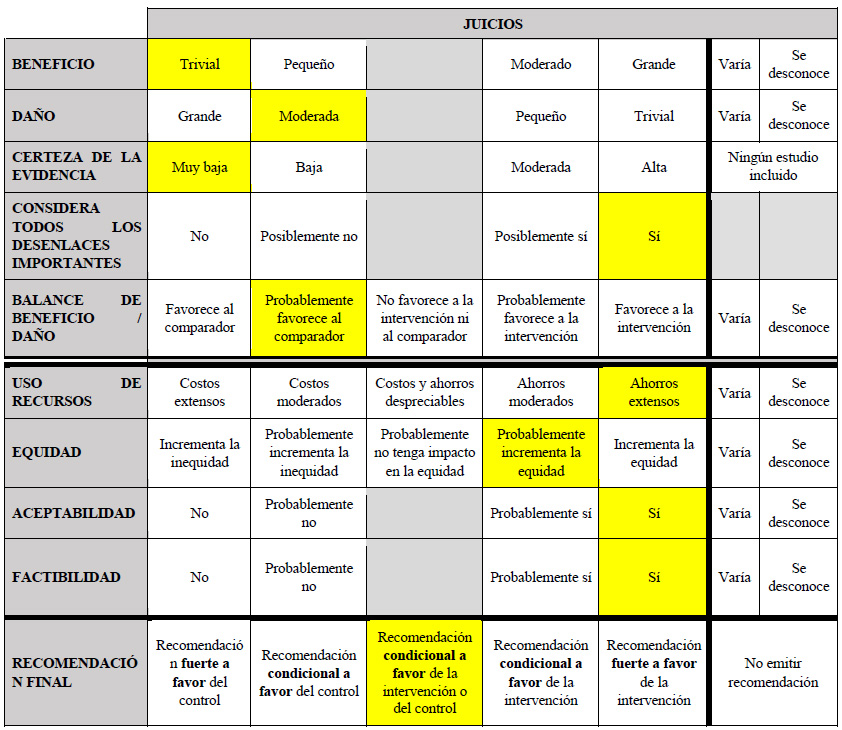
El GEG revisó la evidencia seleccionada para cada pregunta clínica en reuniones periódicas, usando los marcos Evidence to Decision (EtD) de la metodología GRADE 8,9. Para ello, tuvo en consideración: 1) Beneficios y daños de las opciones, 2) Valores y preferencias de los pacientes, 3) Aceptabilidad por parte de los profesionales de salud y pacientes, 4) Equidad, 5) Factibilidad de las opciones en EsSalud, y 6) Uso de recursos. Luego de discutir estos criterios para cada pregunta, el GEG, por consenso o por mayoría simple, formuló cada recomendación, asignándole una fuerza (fuerte o condicional) y una certeza de la evidencia (alta, moderada, baja, o muy baja) cuya interpretación se muestra en la Tabla 2.
Formulación de buenas prácticas clínicas:
El GEG formuló buenas prácticas clínicas (BPC), usualmente en base a su experiencia clínica o a adopciones de otras guías o protocolos (Tabla 1).
Revisión por expertos externos:
La presente GPC fue revisada en reuniones con especialistas representantes de otras instituciones, y tomadores de decisiones de EsSalud. Asimismo, su versión extensa fue enviada por vía electrónica a un experto externo para su revisión (mencionados en la sección de agradecimientos). Cuando fue pertinente, el GEG tuvo en cuenta los resultados de estas revisiones para modificar las recomendaciones finales.
Actualización de la GPC:
La presente GPC tiene una vigencia de cinco años. Al acercarse al fin de este período, se procederá a realizar una RS de la literatura para su actualización, luego de la cual se decidirá si se actualiza la presente GPC o se procede a realizar una nueva versión.
Recomendaciones
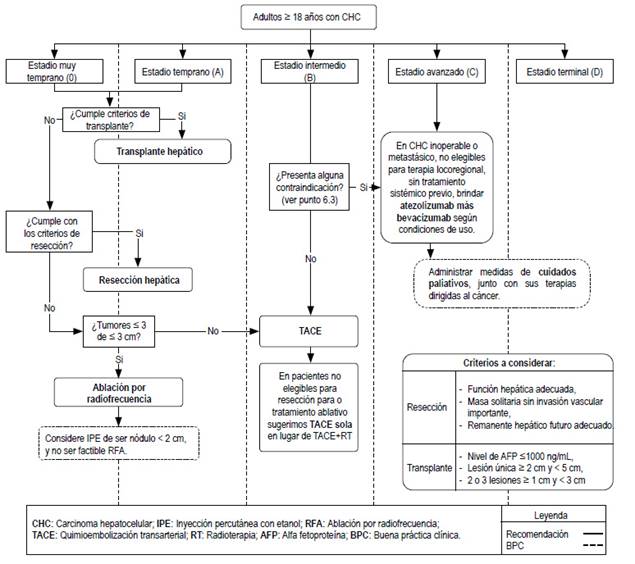
La presente GPC abordó 8 preguntas clínicas, y se formularon 9 recomendaciones (8 condicionales, 1 basada en un Dictamen Preliminar de Evaluación de Tecnología Sanitaria), 12 BPC, y 1 flujograma (Tabla 1, Figuras 1).
A continuación, se expondrán las recomendaciones para cada pregunta clínica, así como un resumen del razonamiento seguido para llegar a cada recomendación. No se incluyó las justificaciones de los puntos de BPC, las cuales se puede leer en el documento in-extenso.
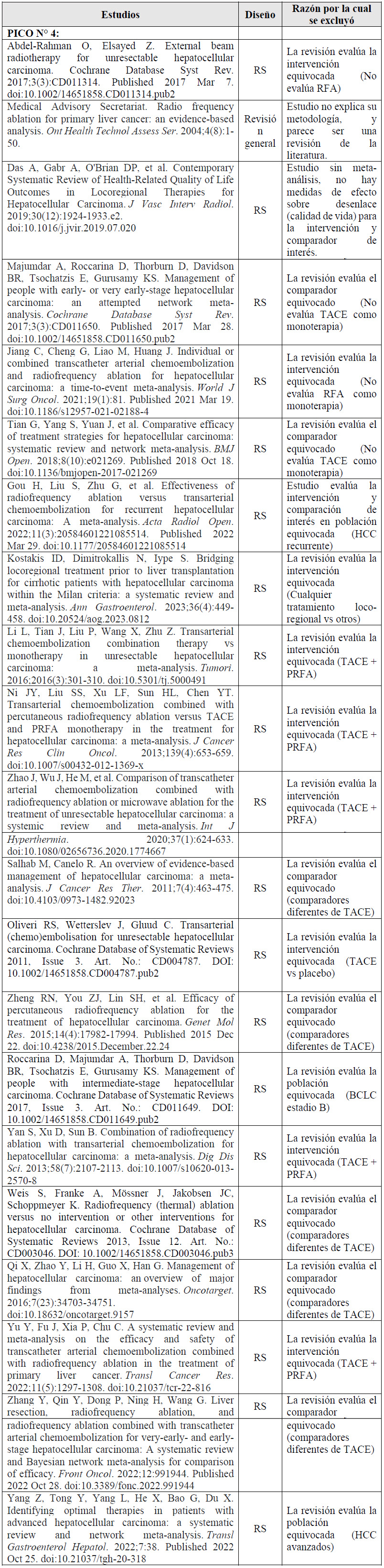
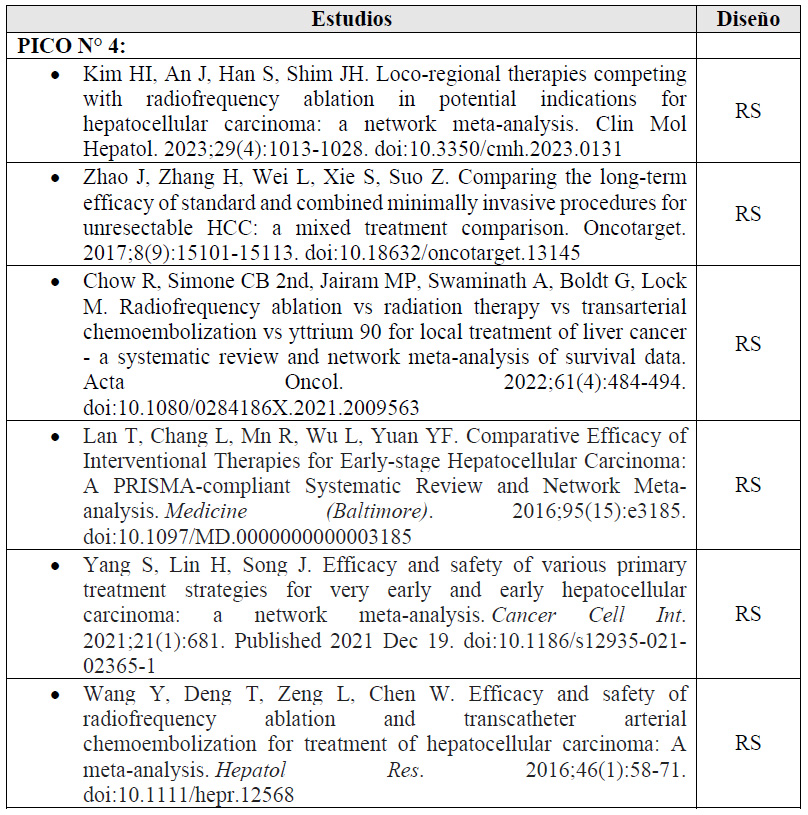
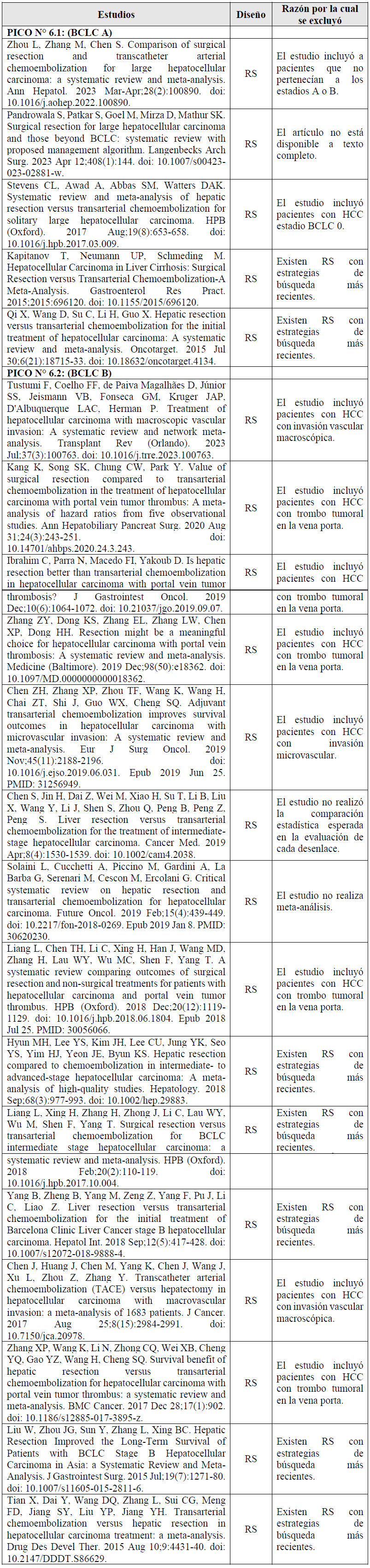
Para cada pregunta, los detalles sobre la búsqueda sistemática se exponen en el Material Suplementario 1. El balance de beneficios daños en forma de tablas Summary of Findings (SoF), así como la justificación en extenso de cada decisión en forma de tablas Evidence to Decision (EtD), se exponen en el Material Suplementario 2.
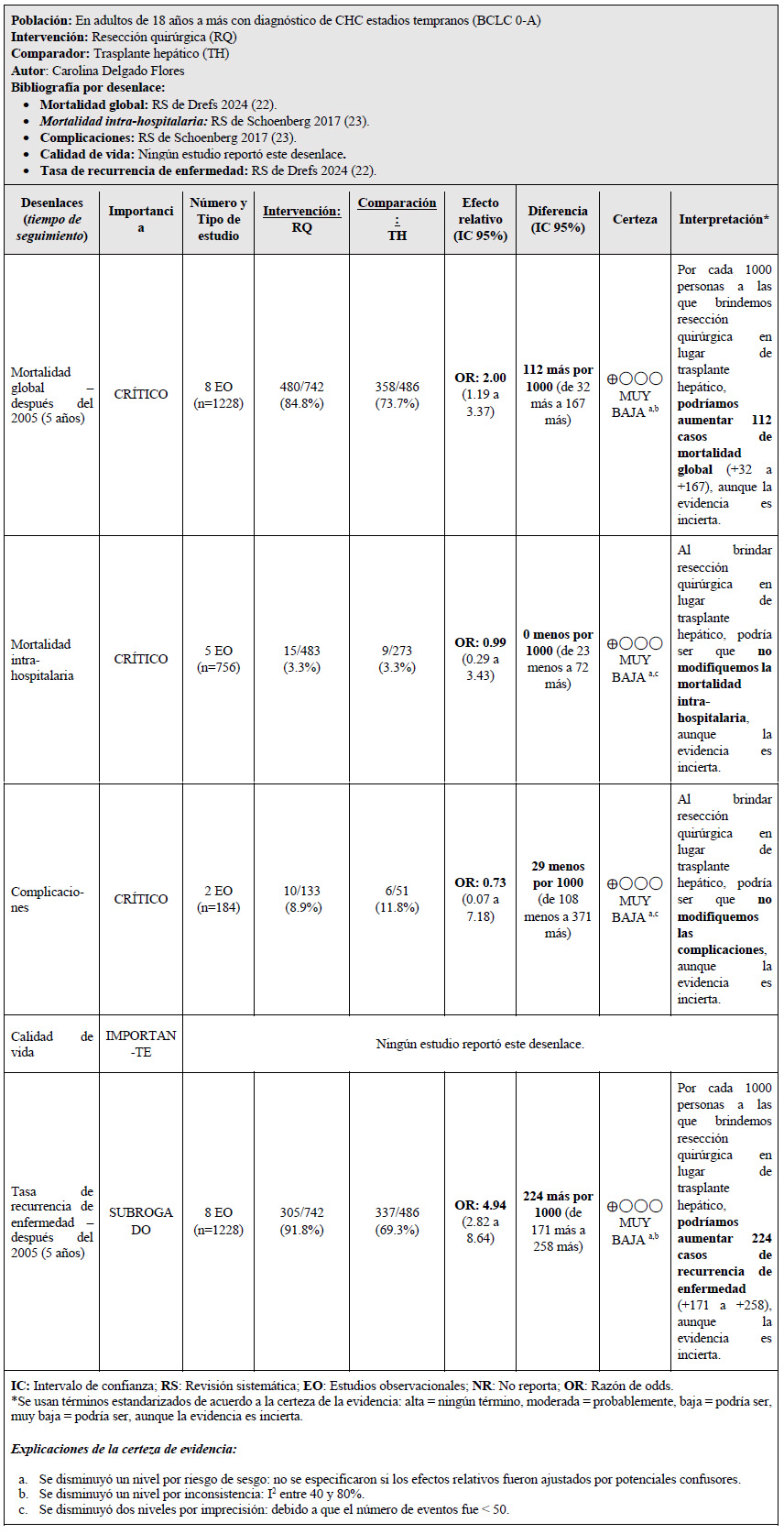
1. En adultos de 18 años a más con diagnóstico de carcinoma hepatocelular (CHC) estadios tempranos (BCLC 0-A), ¿se debería brindar resección quirúrgica o trasplante hepático?
Para los estadios tempranos se estima que el trasplante hepático es la primera opción de tratamiento 10. No obstante, la resección quirúrgica podría ser una opción viable, ya que remueve el tejido canceroso 5. Por ello, se busca valorar los potenciales efectos en ambas intervenciones; considerando también el uso de recursos limitado, la escasez de donadores, y el riesgo asociado de inmunosupresión del paciente.
Se tomaron como referencia las RS de Drefs 2024 11 y Schoenberg 2017 12. En estas se encontró que, si brindamos resección quirúrgica a 100 personas en lugar de brindar el trasplante hepático, podría ser que no modifiquemos la mortalidad intrahospitalaria y complicaciones 12, podría ser que aumentemos 11 casos de mortalidad global (+3 a +17), y aumentemos 22 casos de recurrencia de enfermedad (+17 a +26), aunque todos estos resultados son inciertos 11. Cabe resaltar que ningún estudio reportó el desenlace de calidad de vida.
Si bien este balance de los efectos favoreció al trasplante hepático, el panel reconoce la escasez de donantes de hígado en el Perú, con lo cual se reduce su factibilidad y equidad. En ese sentido, el panel consideró importante ampliar las opciones de tratamiento en estos pacientes, y siendo la resección quirúrgica una opción de tratamiento que ha mostrado beneficios, que es bastante aceptada por los especialistas y pacientes, y que además es menos costosa 13, se emitió una recomendación a favor de brindar la intervención y del comparador. Debido a que la certeza general de la evidencia fue muy baja, esta recomendación fue condicional.
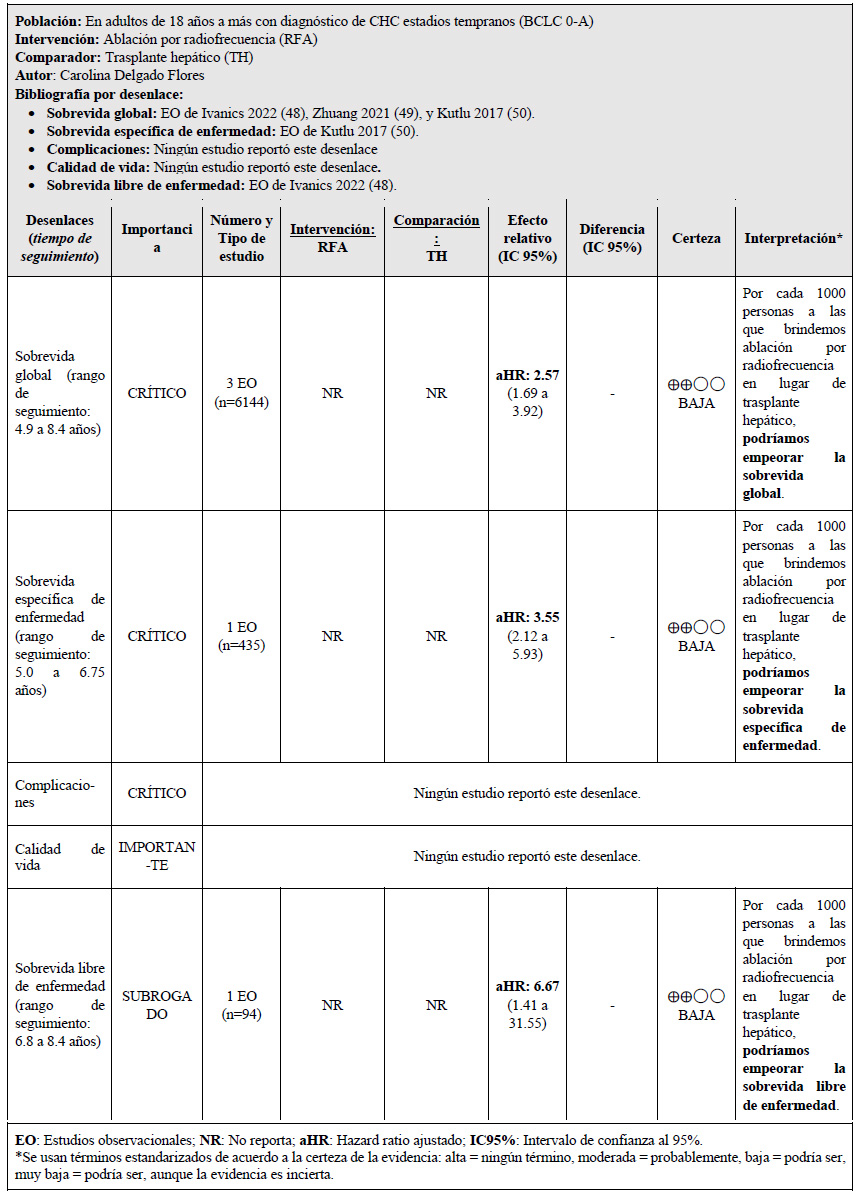
2. En adultos de 18 años a más con diagnóstico de CHC estadios tempranos (BCLC 0-A), ¿se debería brindar trasplante hepático o ablación por radiofrecuencia (RFA)?
La RFA es un procedimiento ablativo que mediante el uso de ondas de radio calienta y destruye células cancerígenas 10. Se busca valorar los potenciales efectos del trasplante hepático comparado con RFA en pacientes con CHC en estadios tempranos (BCLC 0-A).
Se tomaron como referencia los estudios observacionales de Ivanics 2022 14, Zhuang 2021 15, y Kutlu 2017 16. En estas se encontró que, si brindamos la RFA a 100 personas en lugar de brindar trasplante hepático, podría ser que empeoremos la sobrevida global, sobrevida específica de enfermedad y sobrevida libre de enfermedad. Ningún estudio reportó el desenlace de complicaciones y calidad de vida.
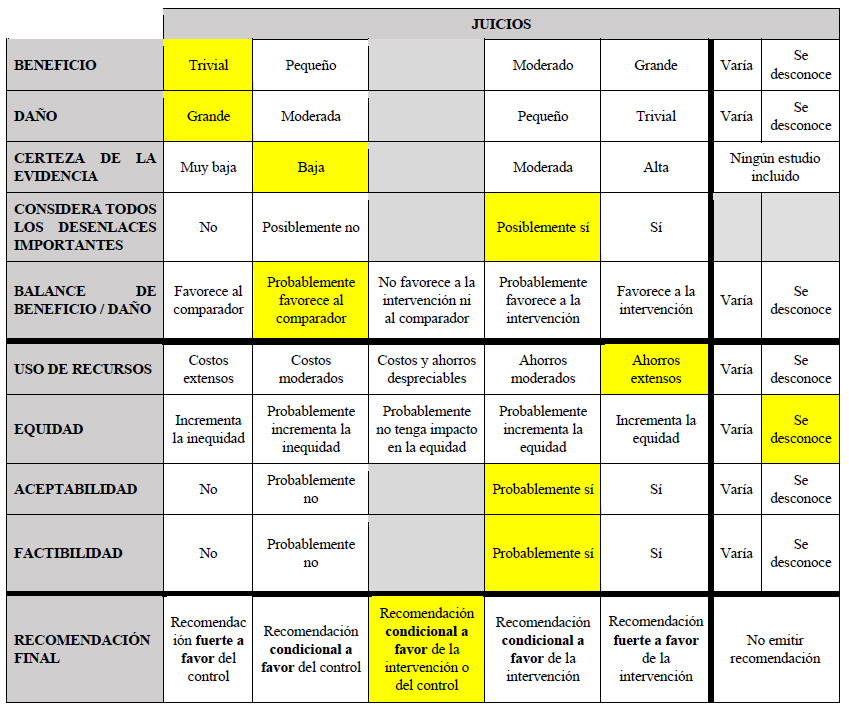
El balance de los efectos favoreció al transplante hepático, no obstante, el panel reconoce la escasez de donantes de hígado en el Perú, con lo cual se reduce su factibilidad. En ese sentido, el panel consideró importante ampliar las opciones de tratamiento en estos pacientes, y siendo la RFA una opción de tratamiento que ha mostrado beneficios, según las características clínicas del paciente; que además es una opción de tratamiento probablemente aceptable por los especialistas y pacientes, y que además es menos costosa 13; se emitió una recomendación a favor de la intervención y del comparador. Debido a que la certeza general de la evidencia fue muy baja, esta recomendación fue condicional.
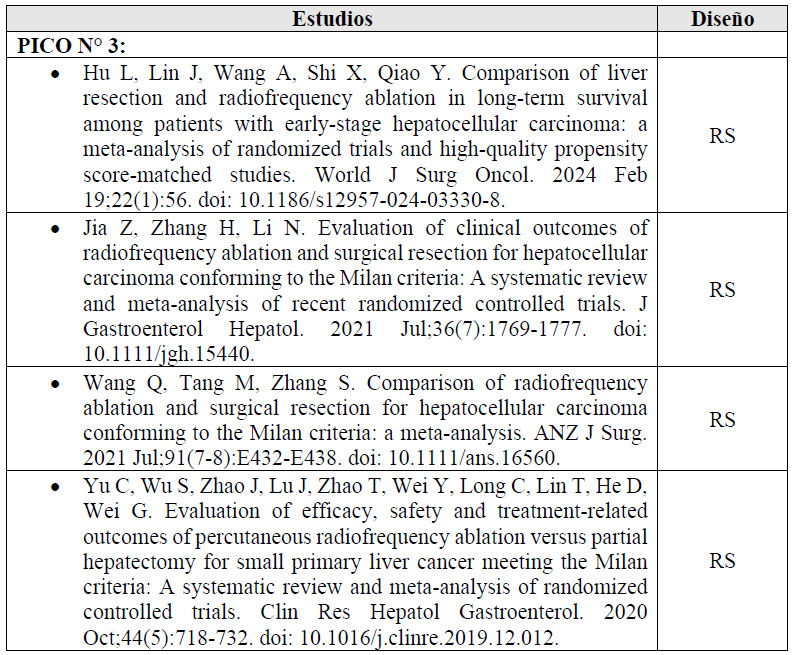
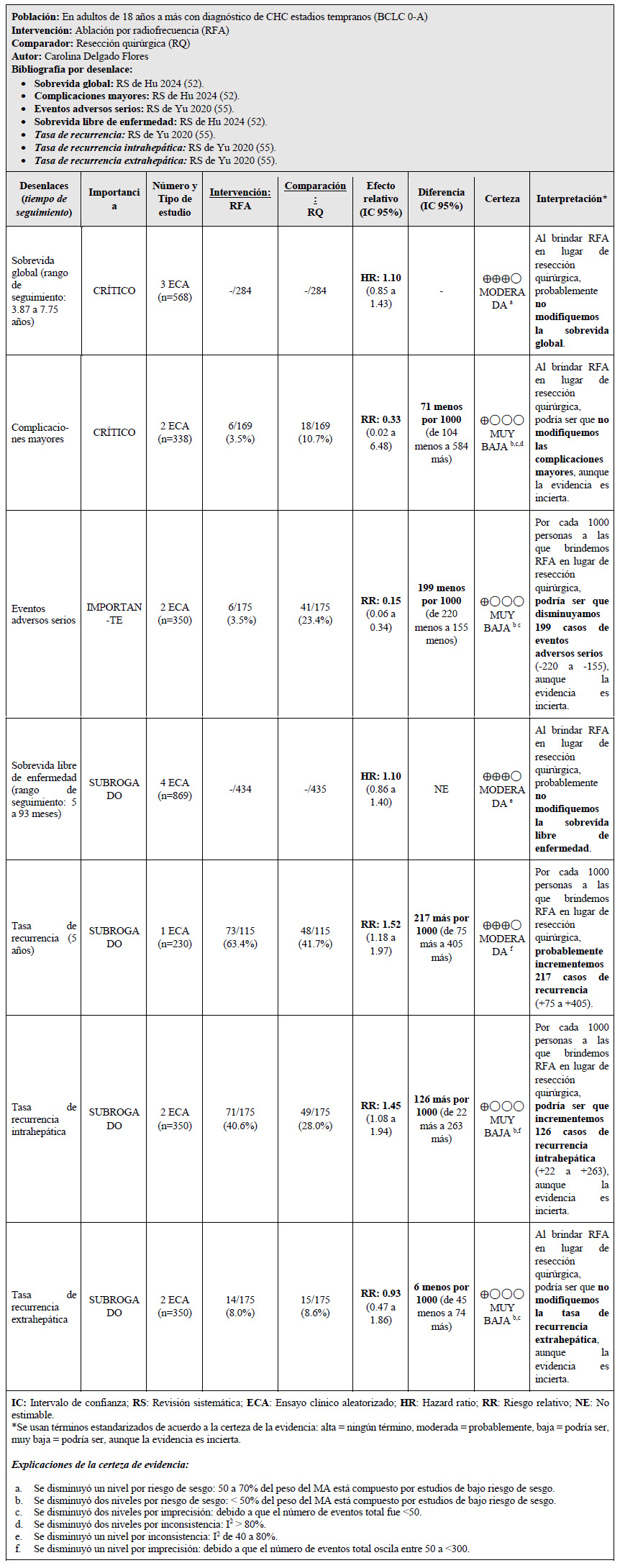
3. En adultos de 18 años a más con diagnóstico de CHC estadios tempranos (BCLC 0-A), ¿se debería brindar RFA o resección quirúrgica?
Se tomaron como referencia las RS Hu 2024 17, y Yu 2020 18. En estas se encontró que, si brindamos la RFA a 100 personas en lugar de brindar la resección quirúrgica, podría ser que disminuyamos 20 casos de eventos adversos serios (-22 a -15) pero esto es incierto 18. En contraste, podría ser que no modifiquemos las complicaciones mayores 18 y la tasa de recurrencia extrahepática 18 pero esto es incierto.
En cuanto a los daños, si brindamos la RFA a 100 personas en lugar de brindar la resección quirúrgica, probablemente aumentemos 22 los casos de recurrencia (+7 a +40), y podría ser que aumentemos 13 casos de recurrencia intrahepática (+2 a +26) pero esto es incierto 18. En contraste, probablemente no modifiquemos la sobrevida global y sobrevida libre de enfermedad 17.
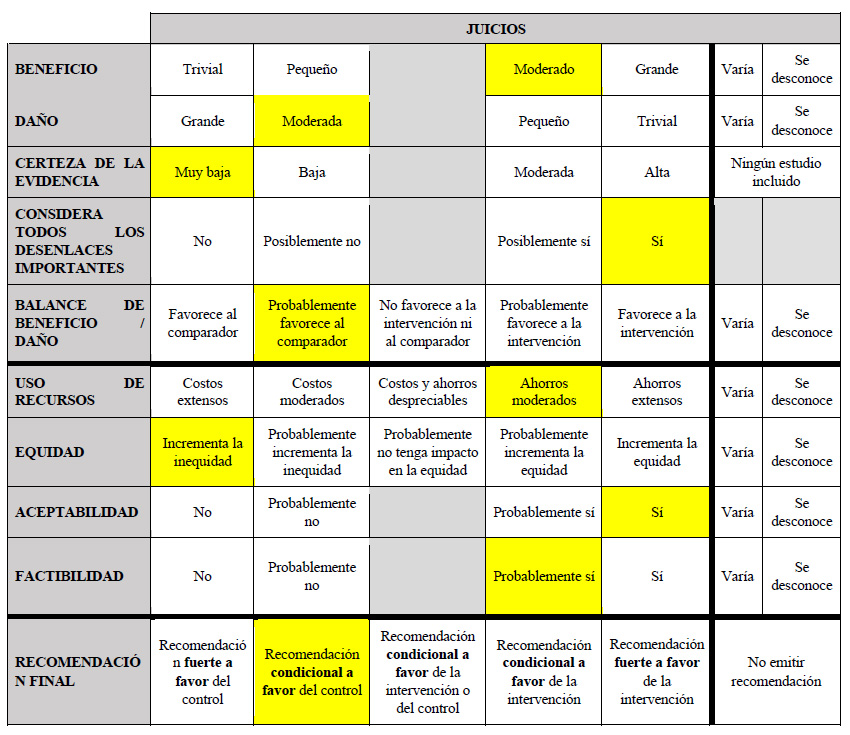
Considerando los juicios emitidos para los beneficios y daños, el GEG precisó que los resultados para los daños fueron probablemente más importantes para los pacientes con CHC; esto sumado a que brindar la intervención, aunque probablemente es factible de implementar, implicaría una reducción de la equidad. Por ello, se emitió una recomendación a favor de brindar el comparador. Debido a que la certeza general de la evidencia fue muy baja, esta recomendación fue condicional.
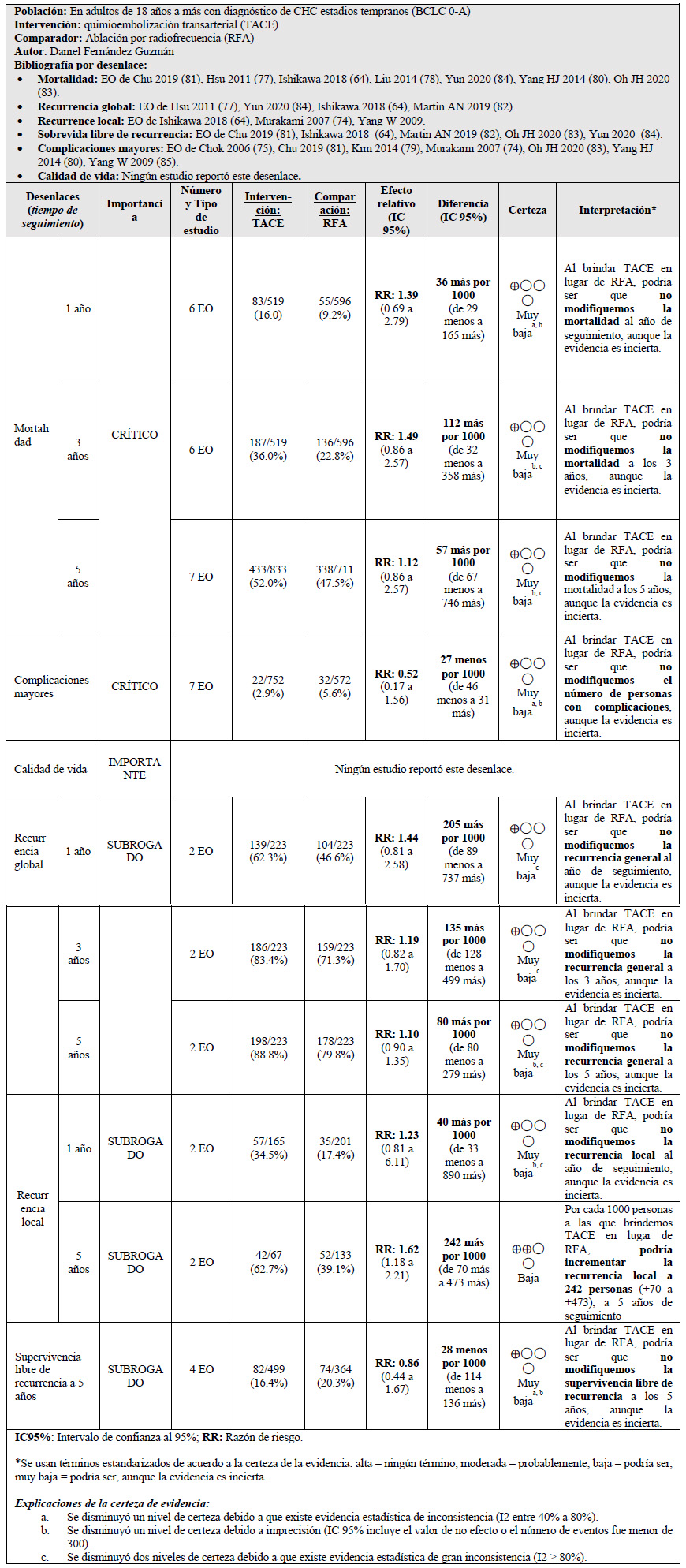
4. En adultos de 18 años a más con diagnóstico de CHC estadios tempranos (BCLC 0-A) no resecables, ¿se debería brindar quimioembolización transarterial (TACE) o RFA?
Entre las opciones no quirúrgicas, la RFA se recomienda en estadios tempranos, debido a su naturaleza menos invasiva, sin embargo, en casos donde la RFA no es factible (como en tumores que se encuentran en la región subcapsular, la cúpula o zonas adyacentes a las asas intestinales o el conducto biliar) 19, la realización de TACE aparecería ocasionalmente en la práctica clínica, aunque sus beneficios y daños siguen siendo inciertos 20.
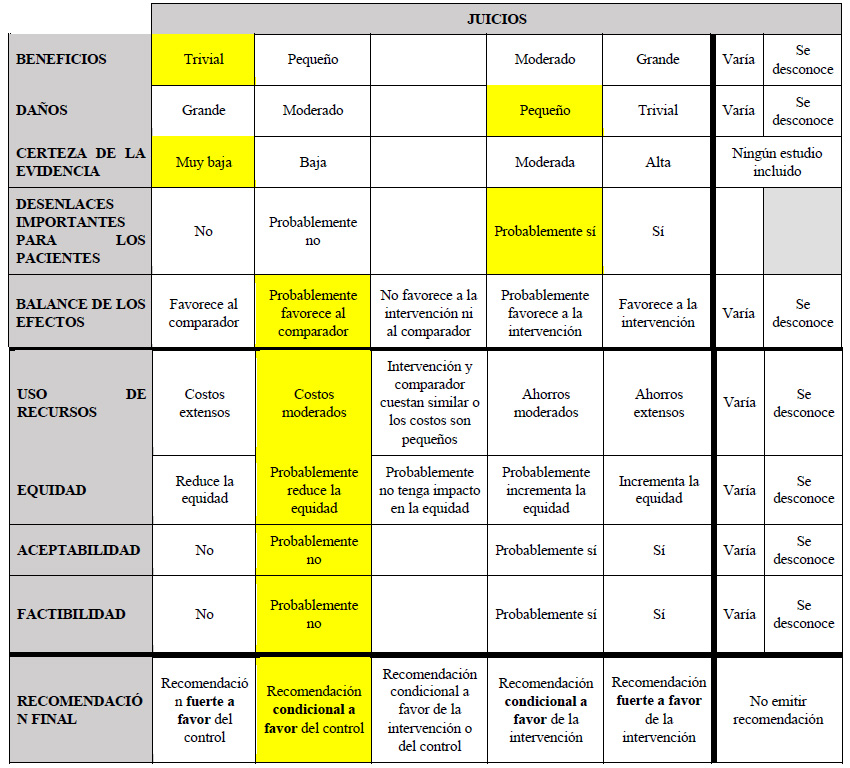
Se tomaron como referencia las RS de Chow 2022 21, y Yang 2021 22. En estas se encontró que, si brindamos TACE a 100 personas en lugar de brindar la RFA, podría ser que incrementemos la recurrencia local a 24 personas (+7 a +47) a los 5 años de seguimiento. En contraste, podríamos no tener efecto sobre mortalidad, recurrencia global, número de complicaciones mayores, y supervivencia libre de recurrencia, pero esto es incierto. Cabe resaltar que ningún estudio reportó resultados para el desenlace de calidad de vida.
Por ello, se emitió una recomendación a favor de brindar el comparador. Debido a que la certeza general de la evidencia fue muy baja, esta recomendación fue condicional.
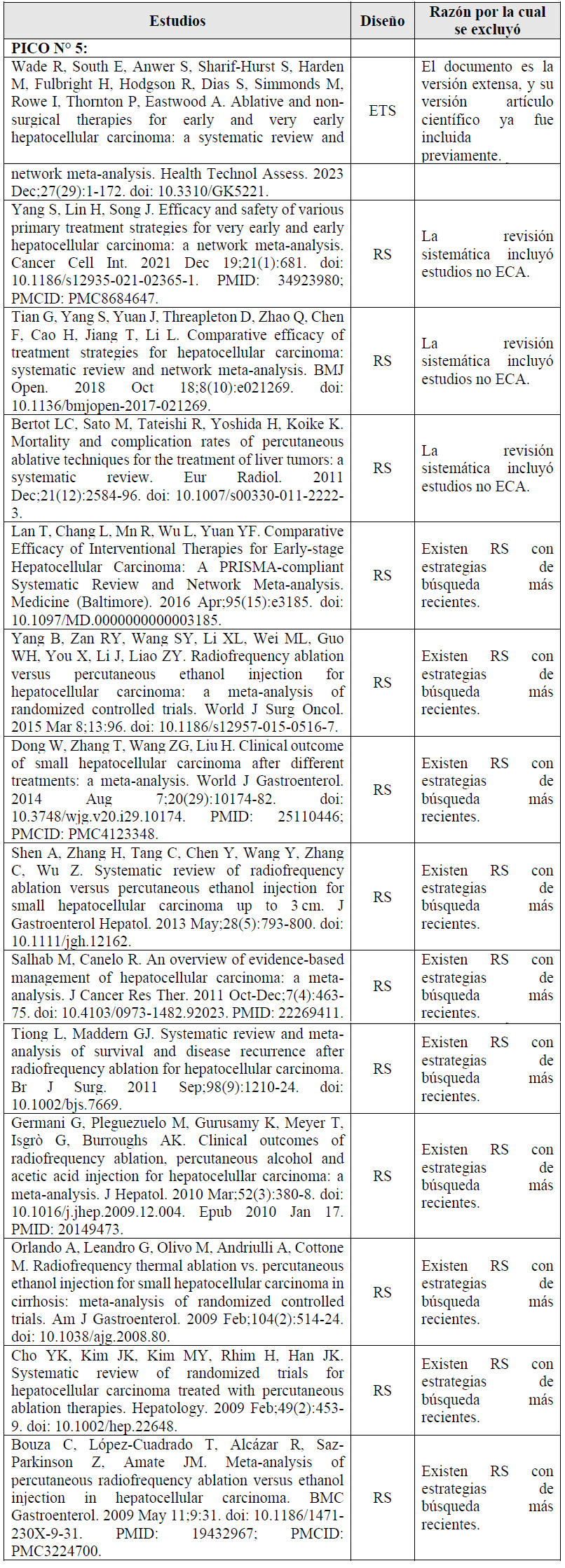
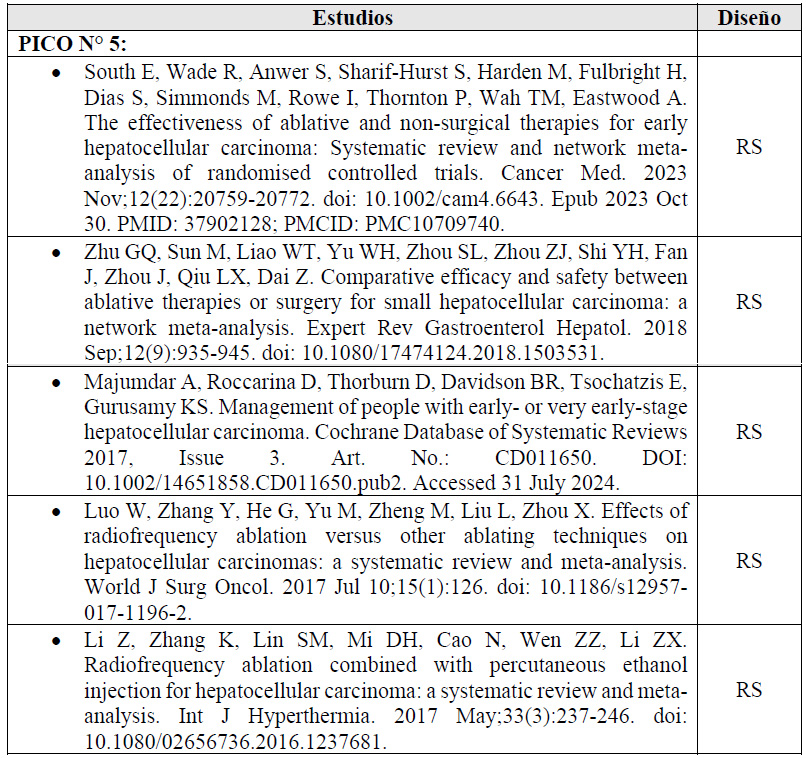
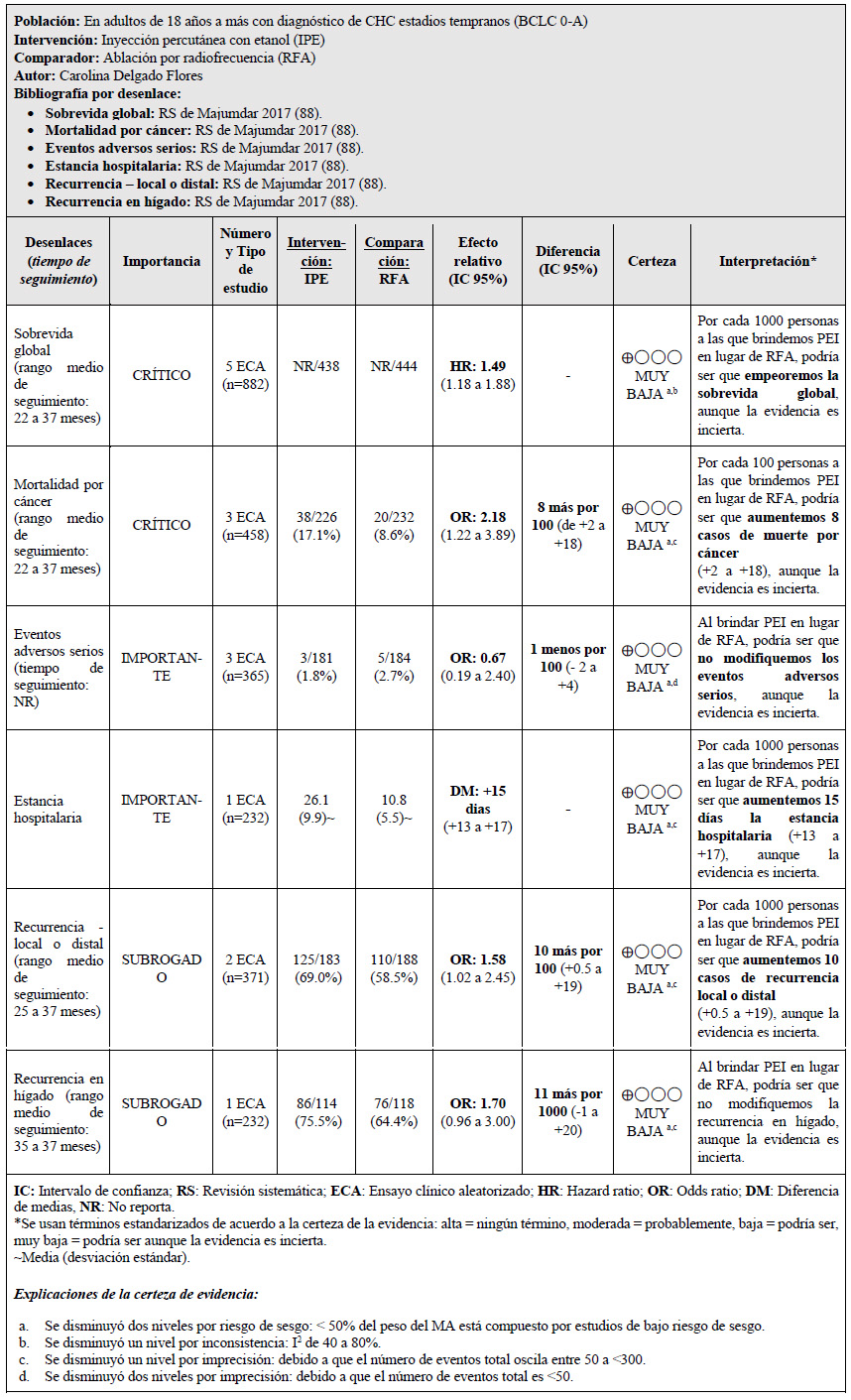
5. En adultos de 18 años a más con diagnóstico de CHC estadios tempranos (BCLC 0-A), ¿se debería brindar inyección percutánea con etanol (IPE) o RFA?
Ambas técnicas ablativas causan la necrotización del tejido tumoral a través de sus mecanismos, por congelación rápida y deshidratación de células químicas; además, podrían causar otros diferentes efectos post-ablativos 23.
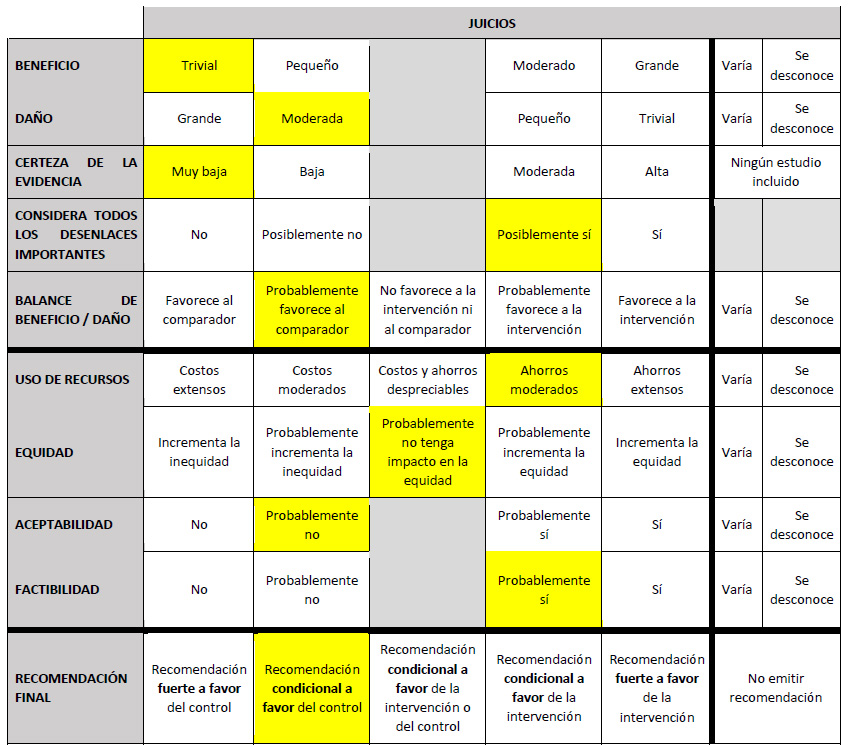
Se tomó como referencia la RS de Majumdar 2017 24. Esta encontró que, si brindamos la IPE a 100 personas en lugar de brindar la RFA, podría ser que no modifiquemos los eventos adversos serios, empeoremos la sobrevida global, aumentemos 8 casos de muerte por cáncer (+2 a +18), aumentemos 15,3 días la estancia hospitalaria (+13,23 a + 17,37) y aumentemos 10 casos de recurrencia local o distal (+1 a +19) pero esto es incierto. Por ello, se emitió una recomendación a favor de brindar el comparador. Debido a que la certeza general de la evidencia fue muy baja, esta recomendación fue condicional.
6. En adultos de 18 años a más con diagnóstico de CHC estadio temprano o intermedio (BCLC A-B), ¿se debería brindar resección quirúrgica o TACE?
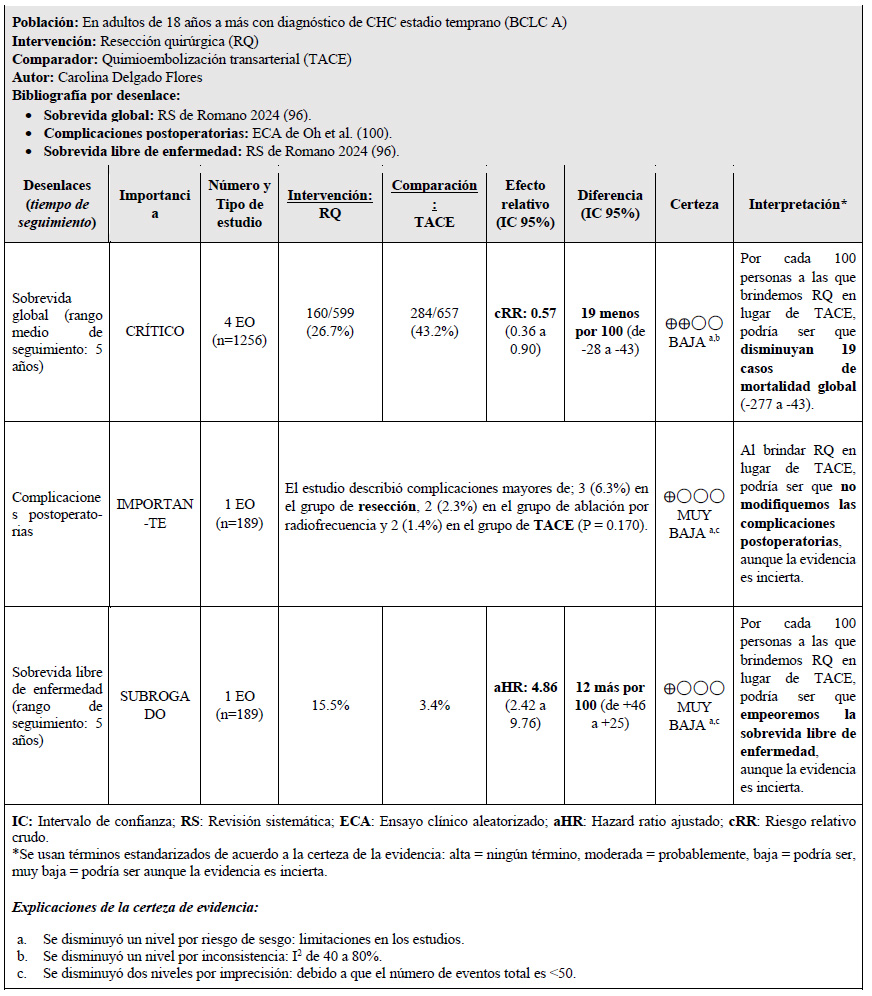
Sub-población de pacientes con CHC estadio temprano (BCLC A)
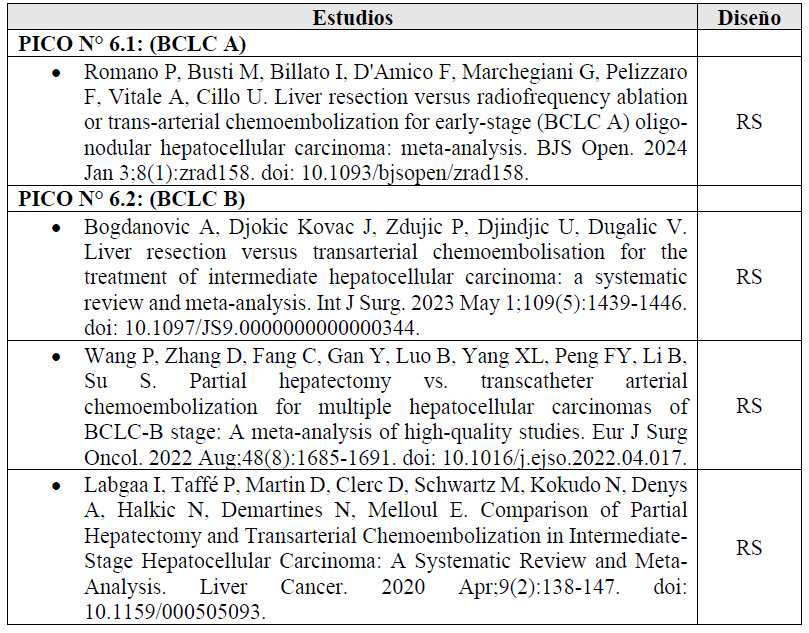
Se tomó como referencia la RS de Romano 2024 25. Este encontró que, si brindamos la resección quirúrgica a 100 personas en lugar de brindar TACE, podría ser que disminuyan 19 casos de mortalidad global (-28 a -43), y podría ser que empeoremos la sobrevida libre de enfermedad pero esto es incierto. Por otro lado, podría ser que no modifiquemos las complicaciones postoperatorias pero esto es incierto.
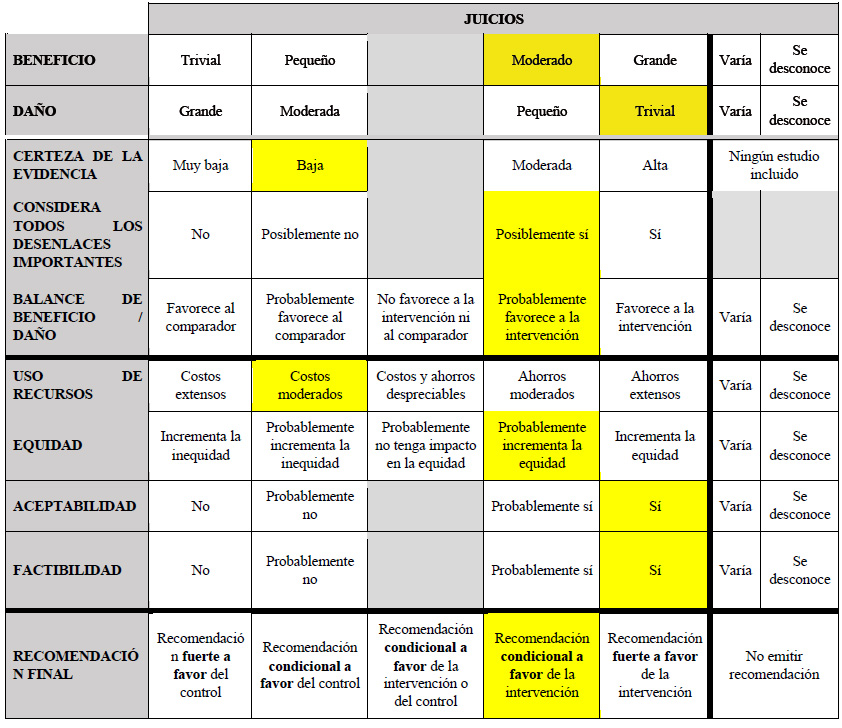
Considerando los juicios emitidos para los beneficios y daños, además del probable incremento de la equidad de brindar la intervención, su aceptabilidad y factibilidad de implementación; se emitió una recomendación a favor de la intervención. Debido a que la certeza general de la evidencia fue baja, esta recomendación fue condicional.
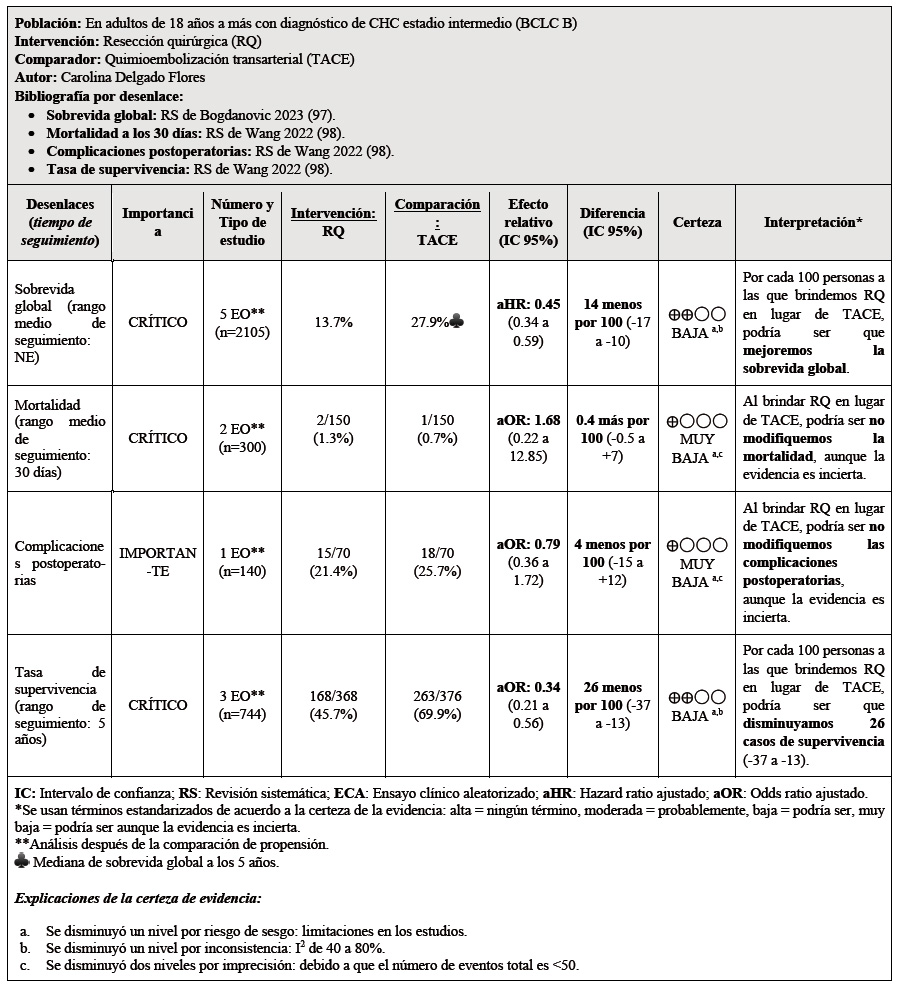
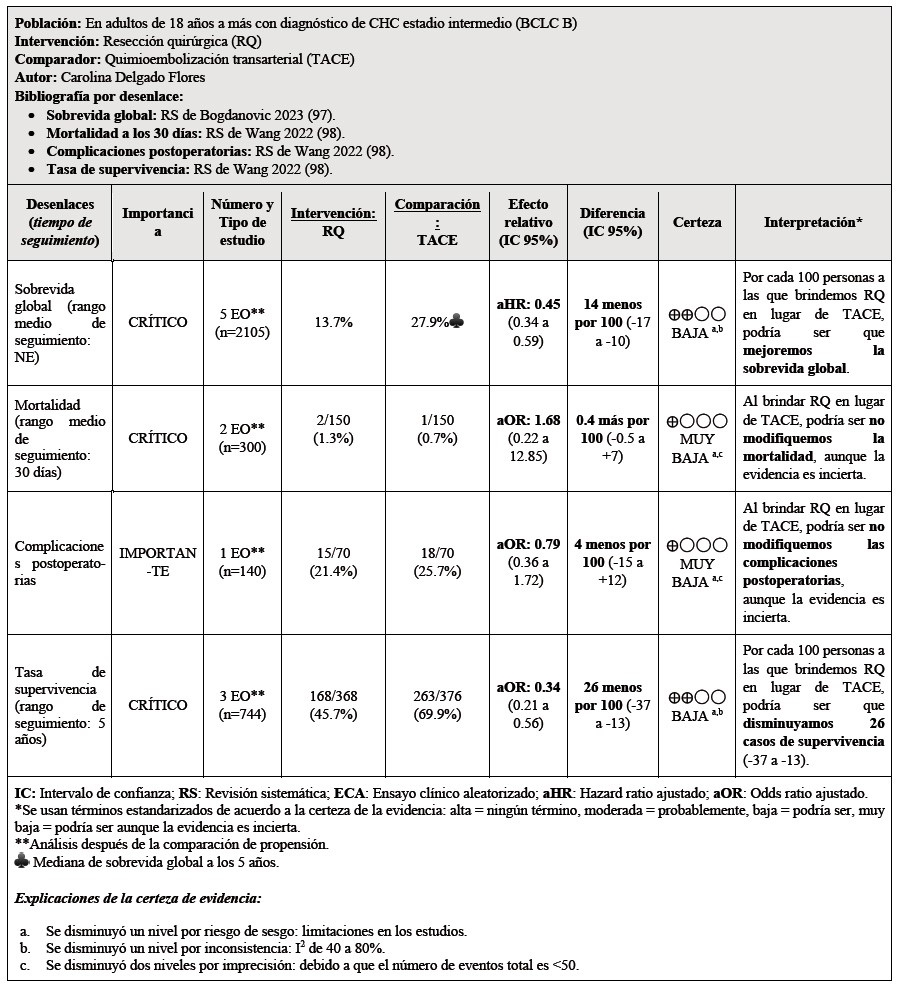
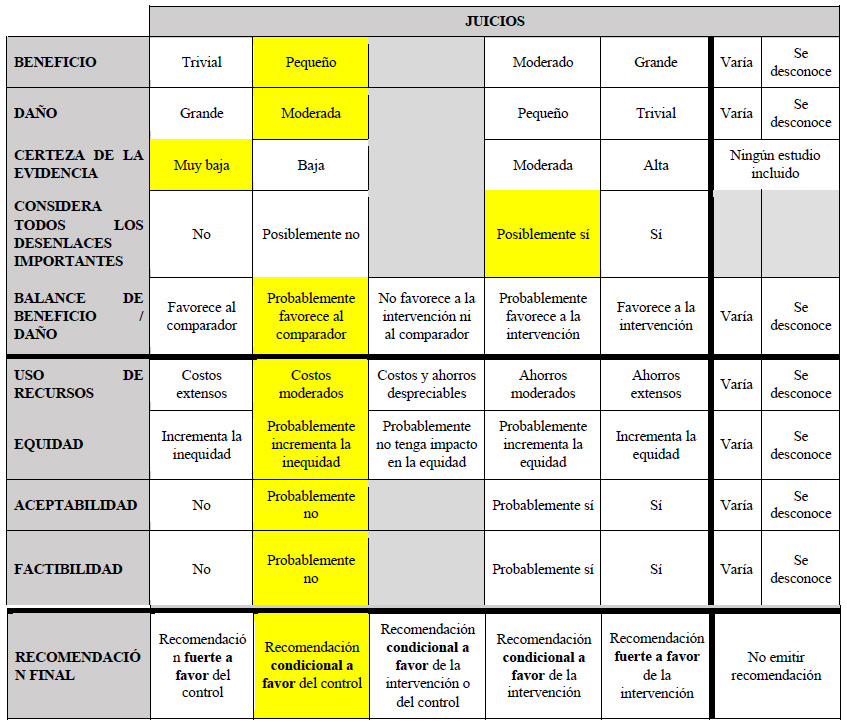
Sub-población de pacientes con CHC estadio intermedio (BCLC B)
Respecto a los pacientes en estadio intermedio, existe variabilidad en la estrategia a brindar en los pacientes de este estadio. Mientras el algoritmo actualizado de la BCLC 2022 recomienda TACE, guías como la ESMO 2021 26 y asiáticas del 2014 27,28 recomiendan la resección quirúrgica.
Se tomaron como referencia las RS de Bogdanovic 2023 29, y Wang 2022 30. En estas se encontró que, si brindamos la resección quirúrgica a 100 personas en lugar de brindar TACE, podría ser que mejoremos la sobrevida global, disminuyamos 26 casos la tasa de supervivencia (-37 a -13). Por otro lado, podría ser que no modifiquemos la mortalidad a los 30 días, complicaciones postoperatorias pero esto es incierto.
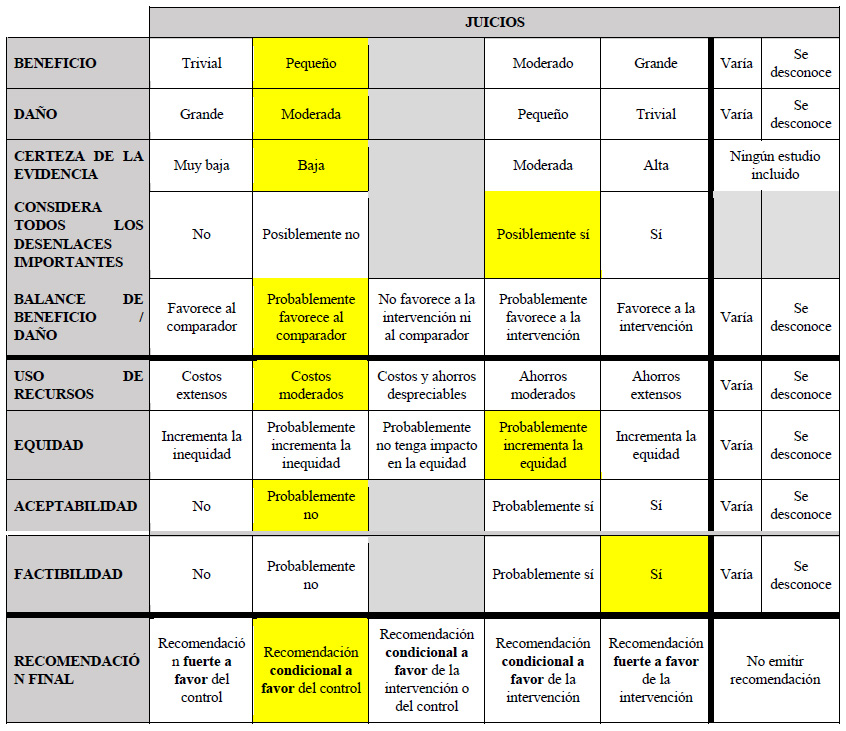
Considerando los juicios emitidos para los beneficios y daños, además del incremento moderado del uso de recursos, y su probable no aceptabilidad después del balance de los efectos; se emitió una recomendación a favor del comparador. Debido a que la certeza general de la evidencia fue baja, esta recomendación fue condicional.
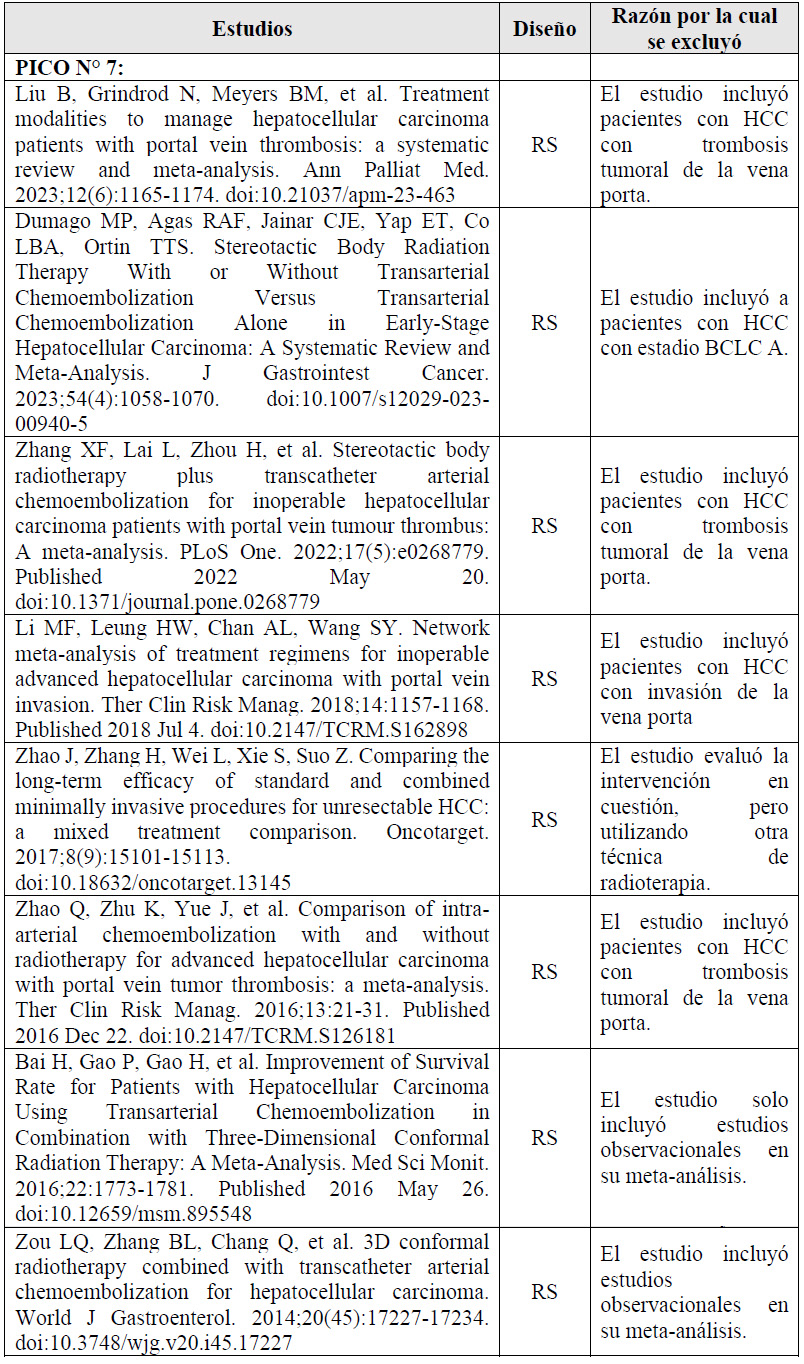
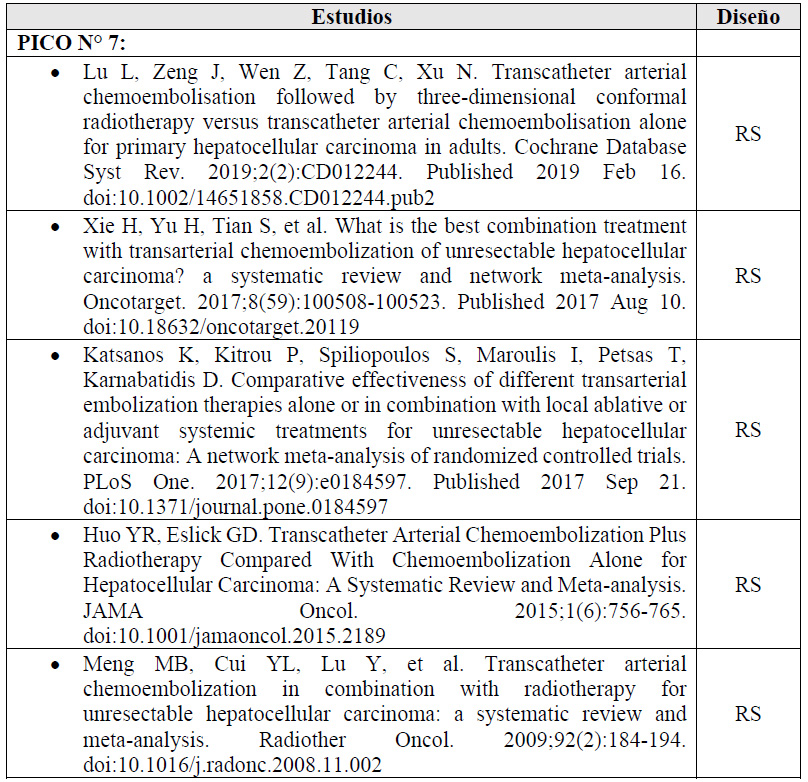
7. En adultos de 18 años a más con diagnóstico de CHC estadio intermedio (BCLC B) no elegible para resección o tratamiento ablativo, ¿se debería brindar TACE más radioterapia (RT) o TACE sola?
Con el avance de la tecnología médica se ha venido estudiando los potenciales efectos de incluir la radioterapia en el tratamiento de pacientes con CHC en estadio intermedio 31. Existen diversas técnicas para brindar radioterapia, sin embargo, para efectos del desarrollo de esta pregunta clínica nos centraremos en la radioterapia conformal tridimensional (3-DCRT), puesto que esta es la técnica utilizada en la institución.
Se tomó como referencia la RS de Lu 2019 31. Esta encontró que, si brindamos TACE más RT a 100 personas en lugar de brindar TACE sola, podría ser que disminuyamos 17 casos de mortalidad por todas las causas (-23 a -10), disminuyamos 25 casos la proporción sin respuesta tumoral (CR+PR) (-30 a -19), se mejore la calidad de vida, pero esto es incierto.
En cuanto a los daños, si brindamos TACE más RT a 100 personas en lugar de brindar TACE sola, podría ser que incrementemos 18 casos de elevación de bilirrubina total (+37 a +48), y se disminuya la tasa de participantes con AFP sérica sin disminución o normalización, pero esto es incierto. Por otro lado, podría ser que no modifiquemos la leucopenia y la elevación de transaminasas séricas, pero esto es incierto.
Esto sumado al hecho de que brindar la intervención implicaría un mayor costo, la reducción de la equidad, la probable no aceptabilidad ni factibilidad; por ello, se emitió una recomendación a favor del comparador. Debido a que la certeza general de la evidencia fue muy baja, esta recomendación fue condicional.
8. En pacientes de 18 años a más con diagnóstico de CHC inoperable o metastásico, Child-Pugh Clase A, no tributario a tratamientos locoregionales, y sin tratamiento sistémico previo, ¿se debería brindar atezolizumab más bevacizumab o sorafenib?
El atezolizumab es un anticuerpo monoclonal humanizado IgG1 que se dirige a PD-L1 e inhibe la interacción entre PD-L1 y sus receptores, PD-1 y B7-1. Su efecto sobre los pacientes con CHC se ha estudiado en combinación con bevacizumab, el cual es un anticuerpo monoclonal humanizado recombinante que se une al factor de crecimiento endotelial vascular (VEGF) e inhibe su actividad biológica. De modo que, se presume que su uso combinado aumenta la eficacia del bevacizumab en la inhibición del VEGF 32,33.
Se tomó como referencia el Dictamen Preliminar de Evaluación de Tecnología Sanitaria N.° 035-DETS IETSI-2022 34 que respondía a la pregunta clínica planteada. Este incluyó como evidencia principal al ECA de IMbrave150 35,36, el cual presenta sus resultados en dos publicaciones de resultados al 51,6% de los eventos requeridos (Finn 2020), y al 89,7% (Cheng 2022). Se encontró que, si brindamos atezolizumab más bevacizumab en lugar de sorafenib, se mejora la sobrevida global, se prolonga la sobrevida libre de progresión, se incrementa la tasa de respuesta objetiva, y se incrementa el tiempo hasta el deterioro de la calidad de vida.
En cuanto a los daños, si brindamos atezolizumab más bevacizumab en lugar de sorafenib, se incrementa la tasa de eventos adversos serios, y se incrementa el porcentaje de pacientes que discontinuaron el tratamiento debido a eventos adversos.
En ese sentido, los especialistas consideraron que los eventos adversos con atezolizumab más bevacizumab que conducen a la discontinuación del tratamiento son poco frecuentes y manejables, y el potencial para prolongar la vida y mejorar la calidad de vida de los pacientes supera con creces los riesgos asociados con el tratamiento. Por ello, emitió una recomendación basada en Dictamen Preliminar de Evaluación de Tecnología Sanitaria de IETSI - EsSalud.