INTRODUCCIÓN
La deficiencia de hierro (DH) se caracteriza por niveles disminuidos, pero no extremos del hierro corporal total, con preservación en los glóbulos rojos y precede a la anemia por deficiencia de hierro. Ésta última cursa con una disminución grave del hierro corporal total con presencia de glóbulos rojos hipocrómicos y microcíticos 1. La DH ocasiona la mitad de los casos de anemia 2,3 y es más frecuente en preescolares, mujeres premenopáusicas, gestantes y es observado también en donantes de sangre, convirtiéndose en un hallazgo frecuente en la práctica médica diaria 4,5.
El estudio RISE (evaluación del estado de hierro en donantes) demostró que el 66% de mujeres y el 49% de hombres que donaban frecuentemente presentaban DH 6. Ante esto, se puede inferir que la donación de sangre es una causa importante de pérdida de hierro. En este procedimiento cada unidad recolectada equivale a 450 mL pudiendo generar una pérdida de 200 a 250 mg de hierro, la cual predispone a alteraciones en las reservas de hierro si no se monitorea de manera temprana 7.
En la mayoría de los bancos de sangre del Perú, la concentración de hemoglobina es la prueba de detección recomendada antes de cada donación, y los valores aceptados son ≥12,5 g/dL en mujeres y ≥13,5 g/dL para donantes varones 8. En la literatura se aconseja el uso de ferritina como marcador del estado de hierro 9, sin embargo, no existe una recomendación para la detección de DH.
La seguridad del diagnóstico de DH requiere diferentes pruebas hematológicas e inmunológicas, dentro de ellas el conteo completo de sangre, la ferritina, la saturación de transferrina, el receptor soluble de transferrina, entre otros 10. Los índices eritrocitarios como el volumen corpuscular medio (VCM), la hemoglobina corpuscular media (HCM) y la concentración de hemoglobina corpuscular media (CHCM) tienen una baja sensibilidad para valorar estados deficientes de hierro, a menos que ya se desarrolle la anemia 11. La concentración de ferritina es el marcador más usado para el diagnóstico de ferropenia, teniendo como limitación que ve afectado por cuadros inflamatorios 12. El receptor soluble de transferrina puede ser usado cuando la ferritina tenga un uso limitado, pero el costo y el tiempo de proceso no hacen que sea lo más recomendado 13. Las limitantes de estos marcadores hacen que estas herramientas no sean apropiadas en el contexto de la selección de donantes de sangre.
Dentro de los parámetros hematológicos calculados por los analizadores Beckham Coulter tenemos al factor de anemia microcítica (Maf®) como herramienta de detección temprana de DH 14. Dopsaj et al.2 realizó un estudio en atletas sanos demostrando que el Maf® tenía una buena discriminación diagnóstica para DH con una sensibilidad y especificad del 61,5% y 93%, respectivamente. Estudios muestran además su utilidad en diferentes patologías como cardiopatías congénitas y enfermedad renal crónica para diferenciar estadios de deficiencia de hierro 15,16. Singh et al.17 plantea la posibilidad del uso del Maf® como cribado en donantes de sangre para detección de DH, teniendo como limitante que no pudo comparar su utilidad entre donantes masculinos y femeninos.
Dada la fuerte asociación entre DH y marcadores de estatus de hierro como ferritina, y la creciente evidencia sobre la necesidad del monitoreo en la selección de donantes de sangre 5, el Maf® podría utilizarse como una prueba de cribado rentable al ser un parámetro calculado. Por lo tanto, el objetivo de este estudio es determinar la relación entre la deficiencia de hierro y el Maf®, y evaluar el rendimiento diagnóstico en la detección de deficiencia de hierro en postulantes diferidos a donar sangre.
MÉTODOS
Diseño y ámbito de estudio
Se realizó un estudio transversal para evaluar la relación de la DH y el Maf® en postulantes de sangre diferidos que acudieron al Servicio de Hemoterapia y Banco de Sangre del Hospital Nacional Cayetano Heredia en Lima, Perú durante el mes de enero del 2023.
Participantes
Este estudio incluyó postulantes a donar sangre entre 18 y 65 años los cuales fueron seleccionados aleatoriamente de las historias clínicas de aquellos que fueron diferidos por presentar valores de hemoglobina menores de 12,5 g/dL (mujeres) y menores de 13,5 g/dL (varones). Como parte del proceso de selección del donante de sangre; los candidatos fueron registrados en un inicio tomando sus datos sociodemográficos básicos (edad y sexo), luego se recolectó una muestra de sangre venosa para la realización del hemograma y pruebas infecciosas. Posteriormente, se administró un cuestionario de selección de donantes con la realización de un breve examen físico de acuerdo con los procedimientos normalizados por la institución y de PRONAHEBAS 8.
Los postulantes con alteraciones en los leucocitos, con volumen corpuscular medio (VCM) > 96 fL, sujetos diferidos por otra causa que no sea por los valores de hemoglobina y consumo de suplementos de hierro en los últimos 6 meses fueron excluidos del estudio.
Recopilación de datos y variables
Los datos demográficos (edad y sexo) y clínicos como el índice de masa corporal (IMC) fueron obtenidos de las historias clínicas. A todo postulante a donar sangre se le realizó un hemograma y pruebas serológicas infecciosas, para lo cual se recogió 9 mL de sangre venosa en un tubo con anticoagulante ácido etilendiaminotetraacético tripotásico (EDTA K3) y en un tubo con gel separador, respectivamente. El conteo sanguíneo se realizó en el analizador hematológico CELL-DYN Emerald System (Abbott Diagnostics), el cual da resultados impresos para el número absoluto de hemoglobina (g/dL), hematocrito (%), VCM (fL), HCM (pg), CHCM (g/dl). Del tubo con gel separador se obtuvo 1 mL de suero para la realización de la prueba de ferritina en el analizador automatizado ARCHITECT 1000 mediante la técnica de quimioluminiscencia. Para la garantizar la fiabilidad de los resultados, se realizaron calibraciones y se corrieron controles a diario antes del análisis de las muestras, según las instrucciones del fabricante. El Maf® fue calculado mediante la fórmula Maf® = ((Hb x VCM) /100)) 17.
Análisis estadístico
Se evaluó la distribución de las variables utilizando métodos numéricos y gráficos. Las variables numéricas fueron resumidas como medias y desviación estándar si cumplían con criterios de normalidad, o como mediana y rango intercuartil (RIC) en caso correspondió. En el análisis bivariado, se comparó las características sociodemográficas clínicas y de laboratorio (incluyendo el Maf®) con la ferritina categorizada según un punto de corte de 30 ng/mL (1) mediante la prueba de U de Mann-Whitney para variables continuas y la prueba de Chi-cuadrado. Se utilizó el coeficiente de correlación de Spearman para hallar la correlación entre ferritina y Maf®. La interpretación del coeficiente de correlación rho de Spearman fue según Prion y Haerling (2014) 18.
Se utilizó el análisis de la curva característica operativa del receptor (ROC) para evaluar el rendimiento diagnóstico del Maf® para la evaluación de la DH utilizando a la ferritina como parámetro de medida. Se obtuvieron los puntos de corte en función de la combinación óptima de la sensibilidad y especifidad. Las pruebas estadísticas fueron bilaterales y se consideró un nivel de significancia del 5%. Los valores de Maf® fueron calculados en el programa Microsoft Excel para Windows 10. El análisis estadístico se realizó usando el programa estadístico STATA versión 16 para Windows (StataCorp LP, College Station, Texas, Estados Unidos). Los gráficos se realizaron en el programa GraphPad Prism Versión 8.
Aspectos éticos
Este estudio fue aprobado por el Comité de Ética de la Universidad Peruana Cayetano Heredia (código: 209775) y por el Comité de Ética Institucional del Hospital Nacional Cayetano Heredia (código: 054-2022). Los participantes firmaron un consentimiento informado por escrito antes de la realización de los procedimientos del estudio.
RESULTADOS
159 postulantes diferidos a donar sangre entre 18 a 65 años participaron en el estudio. La media (desviación estándar) de la edad y el IMC de los participantes del sexo masculino fue mayor con 38,2 (11,4) y 28,4 (4,6), respectivamente. La mediana (RIC) de las concentraciones de hemoglobina, ferritina y Maf® en mujeres fueron 11,3 (10-12) gr/dL, 34,4 (18-93) ng/mL y 9,3 (8-10) siendo menores que en varones (Tabla 1).
Tabla 1. Características demográficas, clínicas y hematológicas de postulantes diferidos a donar sangre según sexo en el Servicio de Hemoterapia y Banco de Sangre del Hospital Nacional Cayetano Heredia
| Característica | Total | Femenino (n = 134) | Masculino (n = 25) |
|---|---|---|---|
| Edad (años) - Media (DE) | 34,4 (10,3) | 33,7 (10,0) | 38,2 (11,4) |
| IMC (Kg/m2) - Media (DE) | 26,9 (3,4) | 26,7 (3,1) | 28,4 (4,6) |
| Hemoglobina (g/dL) - Mediana (RIC) | 11,4 (10-12) | 11,3 (10-12) | 12,6 (12-13) |
| Hematocrito (%) - Mediana (RIC) | 35,9 (33-37) | 35,2 (33-37) | 38,8 (37-40) |
| VCM (fL) - Mediana (RIC) | 83,1 (74-88) | 82,9 (73-89) | 83,1 (76-86) |
| CHM (pg) - Mediana (RIC) | 26,2 (23-29) | 26,1 (23-29) | 26,3 (23-27) |
| CHCM (g/dL) - Mediana (RIC) | 31,7 (31-32) | 31,7 (31-32) | 31,5 (31-32) |
| Ferritina (ng/ml) - Mediana (RIC) | 37,9 (18-95) | 34,4 (18-93) | 54,8 (20-101) |
| Maf® - Mediana (RIC) | 9,5 (8-11) | 9,3 (8-10) | 10,3 (9-11) |
IMC: índice de masa corporal. VCM: volumen corpuscular medio; HCM: hemoglobina corpuscular media; CHCM: concentración de hemoglobina corpuscular media; Maf®: factor de anemia microcítica. Los parámetros con distribución normal se muestran como media (desviación estándar - DE). Los parámetros que no se distribuyen normalmente se muestran como mediana (RIC - Rango intercuartil).
Luego de la categorización según el nivel de ferritina (≤ 30 ng/mL), no se encontró asociación con sexo (p = 0,302). La media del IMC (desviación estándar) fue mayor entre varones comparado con mujeres (p = 0,048). Los índices eritrocitarios medidos por el hemograma fueron menores en los que presentaban deficiencia de hierro en comparación con las personas con reservas de hierro normal (p < 0,001) (Tabla 2). Se observó una relación estadísticamente significativa entre deficiencia de hierro y el Maf® (p < 0,001) (Figura 1A). En la figura 1B podemos observar una correlación positiva fuerte y significativa (rho = 0,73; p < 0,001) entre el Maf® y ferritina.
Tabla 2 Relación de deficiencia de hierro y los parámetros hematológicos en postulantes a donar sangre.
| Característica | Estado del hierro | ||
|---|---|---|---|
| Ferritina ≤ 30 ng/ml | Ferritina >30 ng/ml | Valor de p | |
| Edad (años) - Media (DE) | 33,6 (9,7) | 35 (10,8) | 0,385 |
| Sexo (%) | 0,302 | ||
| Femenino | 61 (45,5) | 73 (54,5) | |
| Masculino | 8 (32) | 17 (68) | |
| IMC (Kg/m2) - Media (DE) | 26,3 (3,5) | 27,4 (3,3) | 0,048 |
| Hemoglobina (g/dL) - Mediana (RIC) | 10,5(9-11) | 11,8(11-12) | <0,001 |
| Hematocrito (%) - Mediana (RIC) | 33,7(29-36) | 36,9(35-38) | <0,001 |
| VCM (fL) - Mediana (RIC) | 72,9 (66-78) | 87,2(83-91) | <0,001 |
| CHM (pg) - Mediana (RIC) | 22,4(20-25) | 27,9(27-29) | <0,001 |
| CHCM (g/dL) - Mediana (RIC) | 31,1(30-32) | 31,9(31-32) | <0,001 |
| Maf® - Mediana (RIC) | 7,7(6-9) | 10,3(10-11) | <0,001 |
IMC: índice de masa corporal. VCM: volumen corpuscular medio; HCM: hemoglobina corpuscular media; CHCM: concentración de hemoglobina corpuscular media; Maf®: factor de anemia microcítica.
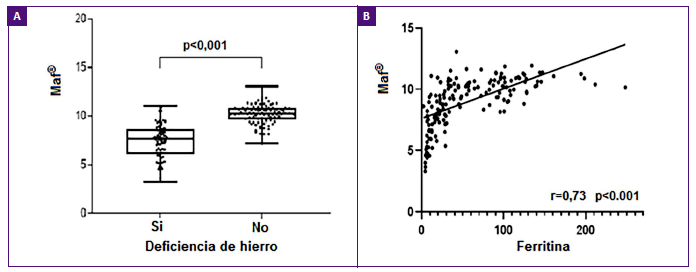
Figura 1. A. Relación entre deficiencia de hierro (ferritina ≤30 ng/ml) y Maf® en postulantes diferidos a donar sangre. B. Correlación entre ferritina y Maf® ® en postulantes diferidos a donar sangre.
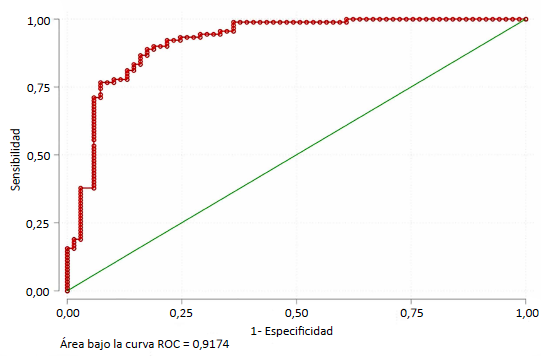
Se realizó la curva ROC para Maf® para evaluar su rendimiento diagnóstico como marcador de DH cuando el valor de ferritina es ≤ 30 ng/mL. El área bajo la curva (AUC) fue de 0,917 (p < 0,001); con un punto de corte ≥ 8,97 para diferenciar postulantes para donar sangre con niveles de ferritina ≤ 30 ng/mL. Con dicho corte la sensibilidad fue de 90% y la especificidad de 81,2% (Figura 2).
DISCUSIÓN
El presente estudio se realizó en una muestra de postulantes a donar sangre que fueron diferidos por tener valores de hemoglobina debajo de los rangos aceptados. Nuestro hallazgo principal fue que aquellos con DH (ferritina ≤ 30 ng/mL) tenían valores significativamente más bajos de Maf® en comparación con los que tenían ferritina normal. Además, el análisis ROC evidenció que el Maf® tenia buena capacidad de discriminación diagnóstica para la detección de DH, proporcionando nueva evidencia en el ámbito de la medicina transfusional en nuestro medio.
El aplazamiento de donantes debido a hemoglobina baja ocurre en el 10% de los que intentan donar sangre, entre estos, la causa más común es la anemia por deficiencia de hierro 19. La edad más frecuente entre los donantes diferidos es entre los 21 a 40 años 20. El sexo es otra condición importante en el hallazgo de DH, pues fue más frecuente en mujeres premenopáusicas, también es frecuente entre donantes repetitivos 1,5. Nuestros resultados muestran un grupo importante de mujeres que han sido diferidas por hemoglobina en rangos no aceptados, lo que denota un riesgo elevado de presentar DH. A pesar de esto no encontramos una relación significativa entre DH y el sexo; esto podría deberse al tamaño de la muestra, el perfil demográfico y la metodología de la investigación usada en este estudio. En este estudio la población estudiada principalmente fueron mujeres y fue producto de la aplicación del punto de corte de diferimiento de donantes de sangre (hemoglobina menor de 12,5 g/dL en mujeres y 13,5 g/dL en varones).
Los índices eritrocitarios obtenidos por el hemograma muestran una asociación significativa con la DH, lo cual es similar a reportes previos. Estudios muestran una relación entre los valores de hemoglobina, VCM y HCM con deficiencia de hierro 21,22. Estos hallazgos son explicados por mecanismos fisiológicos, en donde un estado de almacenamiento de hierro inadecuado se ve reflejado en niveles de ferritina disminuidos; por lo que al tener menos hierro disponible para al eritropoyesis y formación de la hemoglobina, habrá una disminución de los índices de los glóbulos rojos 23.
Estos parámetros también han sido usados en donantes de sangre, ya que un aumento de la frecuencia de donaciones se asocia a valores más bajos de VCM y HCM, sin embargo, estos parámetros, por sí solos, no podrían evidenciar un estado de DH, por lo que se necesitaría una marcador adicional que evalué estadios del metabolismo de hierro 24,25. Los resultados obtenidos podría deberse a que la muestra estudiada eran postulantes para donar sangre diferidos por tener valores de hemoglobina no aceptados para la donación, lo cual explica una mayor posibilidad de alteraciones en los niveles de hierro.
Los postulantes a donar sangre con DH tenían niveles más bajos de Maf® comparados con los que tenían valores de ferritina normales. Estudios previos realizados en población sana informaron que el Maf® podría discriminar estadios de DH, siendo eficaz y barato para su valoración 2,22. Nuestros resultados son similares a Dopsaj et al.2, quienes reportaron una asociación entre eritropoyesis deficiente de hierro y el Maf® en atletas sanos. En donantes de sangre también se ha encontrado diferencias significativas cuando se comparó con donantes con depleción de hierro y DH 17; de la misma forma, Karagülle et al.22 reportaron en mujeres una asociación de anemia por deficiencia de hierro y Maf® mostrando una correlación positiva (r = 0,781), ambos estudios son concordantes con nuestros hallazgos.
Por lo descrito, un valor disminuido de Maf® podría estar indicando una posible DH latente definida en función de la disminución de la ferritina incluso en ausencia de anemia, por lo que, ante un valor disminuido de Maf® se debería corroborar con otra prueba que valore el estado el hierro, sirviendo de alerta de esta condición clínica y así identificarla.
La literatura es escasa sobre el uso de Maf® como prueba diagnóstica para DH. Karagülle et al.22 en un mujeres turcas determinó que este parámetro podría ser usado para el diagnóstico de anemia por deficiencia de hierro con un punto de corte de 10,14 (96,5% de sensibilidad y 97,6% de especifidad). Este parámetro también se utilizó para evaluar depleción de hierro en atletas teniendo un valor diagnóstico regular con un punto de corte de 13,03 (AUC: 0,690 [CI 95% 0,607-0,765; p< 0,001]) 2. Singh et al. 17 en donantes de sangre, obtuvo un punto de corte de 10,71 (sensibilidad de 90,3% y especifidad de 71%) lo cual permitía diferenciar entre donantes con DH de los donantes normales, este estudio fue realizado en su mayoría en varones diferidos para donar sangre con valores de hemoglobina menores de 12,5 g/dl.
Los puntos de corte observados varían con respecto a nuestros resultados debido a las diferencias en la población estudiada. Sin embargo, creemos que son válidos y podrían tener un papel útil en la estratificación de riesgo para la selección de donantes de sangre, principalmente en los que presenten un déficit de hierro, ya que es habitual que no cursen con anemia, pero podrían estar en camino a desarrollarla 1.
Los analizadores hematológicos Beckman Coulter han propuesto al Maf® como una herramienta de detección temprana de deficiencia de hierro, es calculado de forma sencilla usando fórmulas matemáticas, además es poco costoso 26,27. El Maf® permite examinar modalidades anormales de los eritrocitos, ya que su cálculo tiene en cuenta el VCM, así como la hemoglobina 22. Ambos parámetros van sufriendo alteraciones cuando empieza a disminuir los niveles de ferritina y traen alteraciones en la hemoglobinización de los glóbulos rojos 1. La ferritina como marcador detecta alteraciones del metabolismo del hierro en sus diferentes estadios 6. Nuestros resultados muestran una asociación significativa con el Maf®, por lo que podría ser usado como un parámetro de ayuda en la selección del donante de sangre, siempre y cuando, estos resultados se confirmen con otros estudios prospectivos y comparativos y así determinar su utilidad.
Nuestro estudio presenta limitaciones. En primer lugar, este estudio incluyó participantes a donar solo de nuestra institución, por lo que, los resultados no son extrapolables ni representativos a la población peruana. En segundo lugar, se incluyó solo a personas con valores de hemoglobina menores de 12,5 g/dL en mujeres y menores de 13,5 g/dL en varones, y no se incluyó a toda la población que acudía a donar. En tercer lugar, podría haber una asociación inespecífica con enfermedades crónicas o en el caso de otras hemoglobinopatías que no han sido evaluadas en este estudio, en donde la ferritina no es muy sensible para el diagnóstico de deficiencia de hierro, ya que puede ser afectado por inflamación.
La fortaleza de este estudio se basó en la realización de una evaluación estandarizada de la ferritina para obtener un diagnóstico preciso de deficiencia de hierro en postulantes a donar sangre. Además, se determinó el comportamiento de un parámetro poco conocido en nuestro medio como el Maf®.
En conclusión, encontramos que la deficiencia de hierro estuvo asociado a valores menores de Maf®, además, este parámetro tuvo una adecuada discriminación para identificar donantes con ferritina ≤ 30 ng/mL, catalogados como deficientes en hierro. Si bien, es cierto no es el método definitivo para excluir donantes de sangre no calificados, se plantea la posibilidad de que pueda ser usado como cribado sin costos adicionales y de manera rápida debido a su facilidad de obtención. Para tener una mayor exactitud sería recomendable el uso de otras pruebas, como dosaje de hierro sérico, saturación de transferrina, hemoglobina reticulocitaria, entre otros.