Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista de Investigaciones Veterinarias del Perú
versión impresa ISSN 1609-9117
Rev. investig. vet. Perú vol.30 no.2 Lima abr./jun. 2019
http://dx.doi.org/10.15381/rivep.v30i2.14887
ARTÍCULOS PRIMARIOS
Metabolitos sanguíneos y parámetros zootécnicos en lechones destetados a dos edades y con adición de antimicrobianos en el alimento
Blood metabolites and zootechnical parameters in piglets weaned at two ages and with the addition of antimicrobials in the feed
Felipe Patiño F.1, Víctor Herrera F.1, Daniela López D.2, Jaime Parra S.2
1 Facultad de Medicina Veterinaria y Zootecnia, Fundación Universitaria Autónoma de las Américas sede Medellín, Colombia
2 Facultad de Ciencias Agrarias, Universidad Nacional de Colombia, sede Medellín, Colombia
3 E-mail: fpatinof@unal.edu.co
RESUMEN
Se evaluó el efecto de la adición de antimicrobianos sobre parámetros zootécnicos y metabólicos en lechones destetados. Se utilizaron 150 lechones, la mitad destetados a los 21 días y la otra mitad a los 28 días. Se tomaron muestras de sangre y control de peso los días 1, 15 y 30 posdestete y se hicieron controles diarios de temperatura rectal y presencia de diarrea. Los cerdos fueron alimentados con una dieta comercial basal y fueron distribuidos en cinco tratamientos: D1 (dieta basal); D2: adición de bacitracina de zinc; D3: adición de Bacillus subtillis; D4; adición de aceite esencial de orégano, D5: adición de ácidos orgánicos. Se utilizó un diseño completamente al azar en un arreglo de parcelas divididas (cinco dietas, tres repeticiones). Los animales que consumieron la dieta D3 (con probiótico) presentaron el mejor índice de conversión alimenticia, mayor ganancia de peso, menor índice de severidad de diarreas (ISD) y mejores parámetros metabólicos (p<0.05), especialmente con relación a los animales de D1 y D2. Los animales destetados a los 21 días presentaron menores índices zootécnicos, mayor ISD y menores valores metabólicos (p<0.05) en comparación a los animales destetados a los 28 días. Se concluye que la adición de B. subtillis y el destete a los 28 días de edad presentan los mejores resultados y puede ser una alternativa nutricional importante para reemplazar los antibióticos promotores de crecimiento en la alimentación en cerdos.
Palabras clave: antibiótico; destete; diarrea; lechón; probiótico
ABSTRACT
The effect of the addition of antimicrobials on zootechnical and metabolic parameters in weaned piglets was evaluated. A total of 150 piglets were used, half weaned at 21 days and the other half at 28 days. Blood samples and weight control were taken on days 1, 15 and 30 post-weaning and daily controls of rectal temperature and occurrence of diarrhoea were recorded. The pigs were fed with a commercial diet and five treatments were used: D1 (basal diet); D2: addition of Zinc Bacitracin; D3: addition of Bacillus subtillis; D4; addition of oregano essential oil, D5: addition of organic acids. A completely random design was used in an arrangement of divided plots (five diets, three repetitions). The animals that consumed the D3 diet (with probiotic) had the best feed conversion ratio, the greatest body weight gain, the lowest severity index of diarrhoea (SID) and the best metabolic parameters (p<0.05), especially in relation to animals in D1 and D2. The weaned animals at 21 days had lower zootechnical indexes, higher ISD and lower metabolic values (p<0.05) compared to animals weaned at 28 days. It is concluded that the addition of B. subtillis and a weaning at 28 days of age showed the best results and this can be an important nutritional alternative to replace antibiotic growth promoters in pig feeding.
Key words: antibiotic; diarrhoea; piglet; probiotic; weaning
INTRODUCCIÓN
Los lechones están expuestos a condiciones estresantes durante el destete, incluyendo cambios en la composición de la dieta, instalaciones y desafíos bacterianos (Zhou et al., 2012). Esto es especialmente crítico en los sistemas modernos de producción de cerdos donde los lechones son destetados alrededor de los 21 días de edad (Yang et al., 2016). Este periodo puede inducir una disfunción de la barrera intestinal, trastornos digestivos y una tasa de crecimiento reducida (Kim et al., 2012; Begum et al., 2016).
El intestino representa un ecosistema microbiano dinámico en el que los microorganismos del intestino (microbiota) tienen funciones metabólicas y protectoras específicas (Dhruw et al., 2015). En la primera semana después del destete se presentan drásticas disminuciones en las poblaciones microbianas benéficas intestinales (principalmente Lactobacillus spp y Streptococcus spp) e incrementos en el número de bacterias patógenas, especialmente coliformes (mayormente E. coli) (Londoño et al., 2016).
Los antibióticos han sido utilizados como aditivos en alimentos para la eliminación o reducción de bacterias patógenas y como promotores del crecimiento en la producción animal (Heo et al., 2013). Esta práctica ha demostrado eficiencia en el aumento de las tasas de crecimiento, la utilización del alimento y reducción de la mortalidad por enfermedades clínicas (Thacker, 2013). No obstante, la presencia de residuos de antibióticos en los productos de origen animal y el desarrollo de resistencia bacteriana a los antibióticos han llevado a la prohibición de los antibióticos promotores de crecimiento; estimulando el desarrollo de investigaciones para encontrar otros productos que promuevan el crecimiento (Begum et al., 2015).
En el desarrollo de alternativas a los antibióticos para mantener la salud y el rendimiento de los cerdos se incluyen los probióticos (Gutiérrez et al., 2013), prebióticos (Naqid et al., 2015), acidificantes (Suiryanrayna y Ramana, 2015), extractos de plantas (Cho y Kim, 2015) y nutracéuticos como el cobre y el zinc (Bednorz et al., 2013). Por lo anterior, el objetivo de este trabajo fue de cuantificar los metabolitos sanguíneos en lechones destetados a dos edades, alimentados con diferentes antimicrobianos en el alimento y su asociación con parámetros zootécnicos.
MATERIALES Y MÉTODOS
Consideraciones Éticas
Todos los procedimientos experimentales fueron llevados a cabo de acuerdo con las guías propuestas por «The International Guiding Principles for Biomedical Research Involving Animals» (CIOMS, 2012). Esta investigación fue avalada por el Comité de Ética en la Experimentación Animal de la Universidad Nacional de Colombia, Sede Medellín (CEMED 012 del 4 de mayo de 2016).
Localización
El trabajo de campo se realizó en la Estación Agraria San Pablo de la Universidad Nacional de Colombia, sede Medellín, localizada en el municipio de Rionegro, región oriente del departamento de Antioquia (Colombia). El predio se localiza a una altitud de 2100 msnm, en una zona de vida bosque muy húmedo montano bajo (bmh-MB), con una temperatura entre 12 y 18 °C, precipitación anual de 2280 mm y una humedad relativa de 75%.
Animales
Se utilizaron 150 lechones (hembras y machos), cruce terminal comercial. La mitad (75 animales) fue destetada a los 28 días con un peso de 7.8 ± 0.4 kg, y la otra mitad fue destetada a los 21 días con un peso de 5.6 ± 0.3 kg. Los animales fueron alojados en grupos de cinco. El alimento y el agua se ofreció a voluntad durante 30 días (etapa de precebo). Los lechones no recibieron alimento sólido ni de antibióticos durante la lactancia.
Instalaciones y Equipos
Los cerdos fueron alojados en corrales levantados del piso (1.2 x 2.3 m), con piso de malla metálica. Los corrales se encuentran en módulos (espacios) con 10 jaulas por módulo. En los primeros 15 días del experimento se colocaron lechoneras de madera en los corrales y se mantuvo una temperatura ambiental de 26 °C por medio de calentadores de gas producido por un biodigestor, controlando la temperatura con cortinas.
Dietas
Los animales fueron alimentados con una dieta comercial, libre de antibióticos, que cumplía con los requerimientos mínimos nutricionales (NRC, 2012), a la que se le adicionaron agentes antimicrobianos según los siguientes tratamientos:
-
Dieta control (DC): sin antimicrobiano.
-
Dieta 2 (D2): con antibiótico promotor de crecimiento (Bacitracina de Zinc).
-
Dieta 3 (D3): con Bacillus subtilis pb6 (PTA 6737).
-
Dieta 4 (D4): con aceite esencial de orégano (Lippia origanoides) (AEO).
-
Dieta 5 (D5): con ácido orgánico (AO). Mezcla de ácidos cítrico, fumárico, benzoico, sórbico, ascórbico, láctico y butirato de sodio.
La cantidad de Bacitracina de Zinc fue a razón de 350 ppm, de B. subtilis a razón de 50 mg/kg de alimento con una inclusión de 108 UFC; AEO a razón de 150 ppm; ácido orgánico a razón de 0.4% (relación p/p).
Variables Clínicas
La temperatura rectal se midió diariamente por las mañanas durante 15 días con un termómetro digital LD-00045 (LORD®) por 30 segundos. La presencia de diarreas se observó por 30 días. La consistencia de las heces fue determinada por dos evaluadores mediante observación directa durante la toma de temperatura. Para esto, se empleó una escala de 0 a 3 donde: 0 indica heces normales, sin presencia de diarrea; 1 describe una diarrea ligera y pastosa; 2 indica una diarrea moderada, semilíquida; y 3 indica una diarrea severa, muy líquida. La calificación diaria fue sumada para calcular el índice de severidad de la diarrea (Reis de Souza et al., 2010) a partir de la siguiente ecuación: ISD=(ΣCFd)/Pe dónde ISD = Índice de Severidad de Diarrea; CFd = calificación de la consistencia fecal diaria; Pe = periodo experimental.
Variables Productivas
Los parámetros zootécnicos fueron tomados los días 1, 15 y 30 posdestete. Se llevaron registros de la cantidad de alimento ofrecido y rechazado para calcular el consumo total y la conversión alimenticia. La ganancia diaria de peso (GDP) fue (peso final peso inicial) / (días de muestreo). El índice de conversión alimenticia (ICA) fue (consumo de alimento) / (ganancia de peso). Los animales y el alimento ofrecido-rechazado fueron pesados a las 07:00 horas por medio de una balanza digital OCS150C (Century®) y IPJE192507 (Demarkt®), respectivamente.
Muestras
Se colectaron 10 ml de sangre de la vena yugular en un tubo sin anticoagulante los días 1, 15 y 30 posdestete. Las muestras fueron centrifugadas de inmediato por medio de una centrífuga 800-1 (CDEK®) a 4000 rpm por 5 minutos, para luego ser almacenadas en frío y transportadas el mismo día al Laboratorio de Bioanálisis de la Universidad de Antioquia. Los metabolitos evaluados fueron: alanino aminotransferasa (ALT), creatinina, fosfatasa alcalina, glucosa, colesterol, triglicéridos, fósforo y calcio. La cuantificación de los analitos en suero se realizó mediante los estuches comerciales Slides VITROS® (Ortho Clinical Diagnostics, EEUU) específicos para cada analito, siguiendo las instrucciones del fabricante. Para la medición de las densidades ópticas se utilizó un analizador bioquímico VITROS® DT60II (Ortho Clinical Diagnostics, EEUU) (Londoño y Parra, 2015).
Análisis Estadístico
Se realizó un diseño de bloques al azar (tres bloques) en un arreglo de parcelas divididas. Para la conformación de los bloques se tomó en consideración los tres módulos donde se realizó el experimento. Cada tratamiento tuvo un total de tres repeticiones (cinco lechones por repetición). El análisis estadístico fue desarrollado usando el procedimiento GLM de SAS® (2007). Las diferencias entre tratamientos y periodos fueron determinadas por la media de mínimos cuadrados (LS Means) y se utilizó la prueba de Duncan para detectar significancia (p<0.05) entre las medias.
RESULTADOS
Los cerdos presentaron un buen estado de salud y condición corporal, sin signos de enfermedad que causaran su retiro o sacrificio inmediato. No se encontró interacción estadística entre las dietas, los días de evaluación y la edad de destete para las variables respuesta en el estudio, por lo que no fue necesario analizar y desglosar dichos factores de manera independiente.
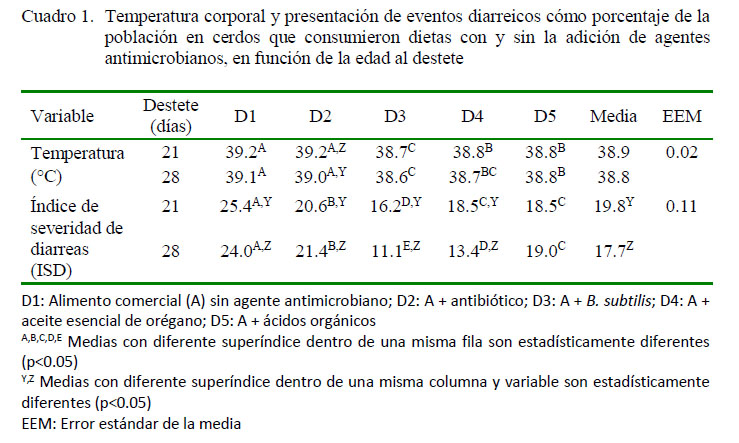
Los resultados de las variables clínicas se muestran en el Cuadro 1. No hubo diferencia significativa para la variable temperatura entre las dietas D1 y D2, pero mostraron valores más altos con respecto a las otras dietas (p<0.05), tanto en los lechones destetados a los 21 como a los 28 días; sin embargo, no se evidenció diferencia estadística para la variable temperatura por efecto de la edad de destete en general.
Para la variable índice de severidad de la diarrea (ISD) se encontró diferencia significativa entre las dietas (p<0.05). La dieta D3 presentó los valores más bajos en comparación con las otras dietas, en especial con las dietas D1 y D2, que tuvieron los valores más altos de ISD, tanto en los lechones destetados a los 21 como a los 28 días. Así mismo, los cerdos destetados a los 28 días presentaron un ISD más bajo que los cerdos destetados a los 21 días (p<0.05).
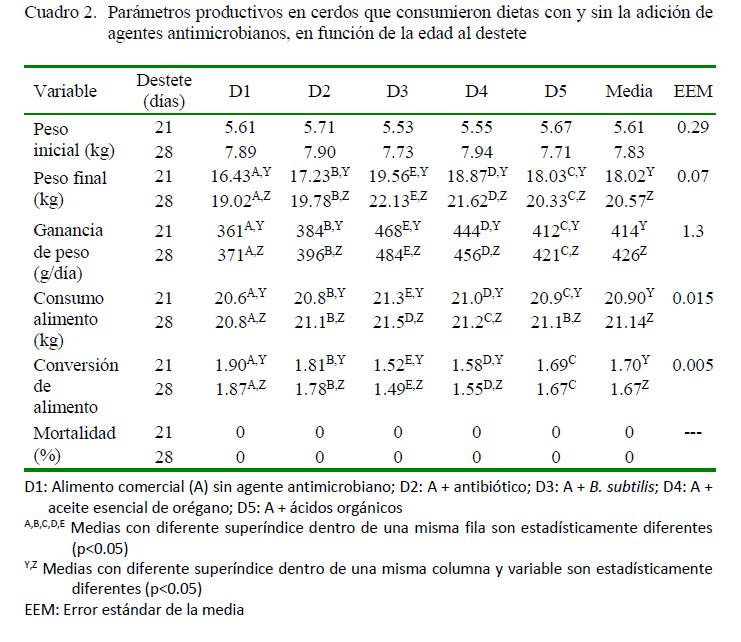
En Cuadro 2 se presentan los resultados de los parámetros zootécnicos. Para las variables conversión, ganancia de peso, consumo de alimento y peso final hubo diferencia estadística significativa (p<0.05) entre todas las dietas, siendo D3 la que presentó el mejor resultado para estas variables, y D1 los resultados más pobres, tanto para animales destetados a los 21 días como para los destetados a los 28 días. Asimismo, los animales destetados a los 28 días presentaron mejores resultados para las variables GDP, CA, peso final y consumo de alimento (p<0.05). Por otro lado, no hubo casos de muerte por enfermedad en el estudio.
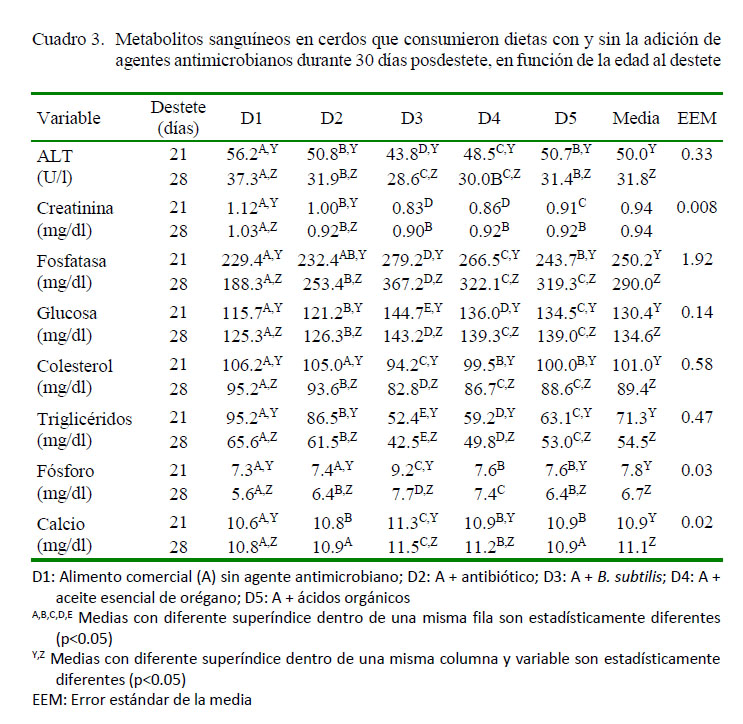
El Cuadro 3 muestra los valores de los metabolitos sanguíneos para las dietas experimentales en función de la edad del destete.
Se encontró diferencia significativa (p<0.05) entre D1 y D2 destetados a los 21 días, excepto para la fosfatasa, colesterol y fósforo, y para la variable calcio en cerdos destetados a los 28 días. En las demás dietas, D3, D4 y D5 presentaron diferencias significativas entre sí (p<0.05), donde D3 mostró niveles más altos de fosfatasa, glucosa, fósforo y calcio y niveles más bajos de ALT, creatinina, colesterol y triglicéridos. Cabe resaltar que D4 presentó niveles similares con D3 en las variables ALT en cerdos destetados a los 28 días y creatinina en cerdos destetados a los 21 días.
En el Cuadro 3 se observa, además, diferencia significativa (p<0.05) entre cerdos destetados a los 21 y 28 días de edad para todos los metabolitos, excepto para creatinina, donde no se presentó diferencia significativa en el valor global, pero hubo diferencias entre en las dietas D1 y D2.
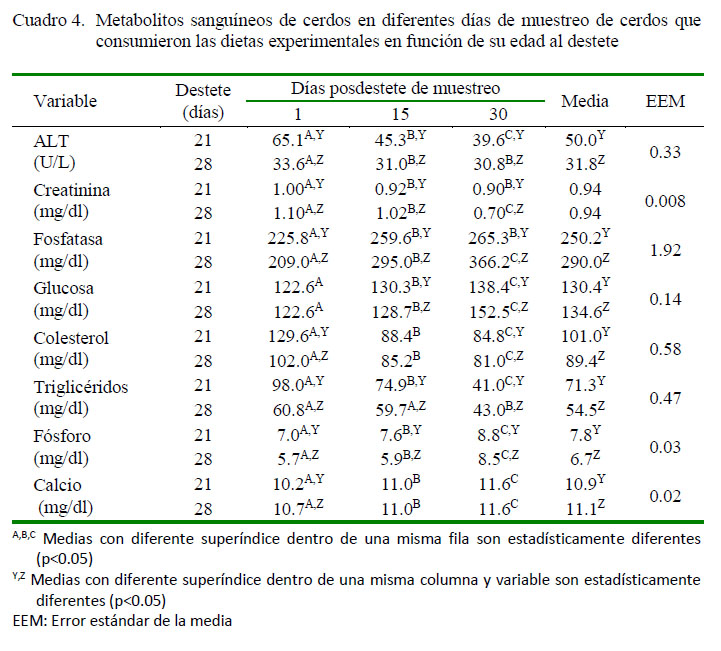
En el Cuadro 4 se evidencia diferencia significativa entre días de muestreo (p<0.05) en todos los metabolitos, donde ALT, fosfatasa, glucosa, fosforo y calcio aumentan con la edad, mientras que los demás disminuyen con el tiempo, tanto para los cerdos destetados a los 21 como a los 28 días. Así mismo, hubo diferencia significativa (p<0.05) entre las edades de destete para todos los metabolitos con excepción de la creatinina.
DISCUSIÓN
En el presente estudio se encontró que D3 presentó los mejores índices productivos para las dos edades de destete. La mayor GDP y mejor CA concuerda con Michiels et al. (2016) quiénes adicionaron B. subtilis en el alimento de lechones destetados a los 20 días de edad. La dieta D3 presentó el índice más bajo de diarreas, siendo esta la mejor dieta, y que concuerda con el trabajo de Giang et al. (2012) donde se hizo el destete a los 28 días y los cerdos fueron suplementados con una mezcla de B. subtilis y Saccharomyces boulardii, presentado una disminución significativa de las diarreas en comparación con dietas basales sin probióticos.
La dieta D4 presentó una buena respuesta productiva para la GDP y la CA, aunque inferior a la dieta D3, lo que concuerda con Li et al. (2012), quienes con la adición de un aceite esencial a 100 y 150 ppm lograron aumentos significativos de la GDP y la CA en cerdos destetados. En forma similar, la dieta D4 mostró un bajo ISD, solo superada por D3, en concordancia con el trabajo de Zeng et al. (2015), quiénes indican que la menor incidencia de diarrea se debe al aumento de lactobacilos y la reducción de E. coli en la microbiota intestinal. En el presente estudio se asoció con una mejor morfología intestinal en los diferentes segmentos, composición microbiana y cambios en las mucinas intestinales (datos no mostrados).
En la actualidad, los criadores de cerdos tienden a aplicar el destete precoz para obtener más camadas por año. Además, los criadores de cerdos utilizan un sistema de administración de lotes, que permite que el destete se produzca en momentos fijos, lo que implica que las crías son tratadas a nivel de camada y no como individuos (Vermeulen et al., 2016). En el presente estudio se evidenció que los cerdos destetados a una edad más precoz (21 días) mostraron un menor índice productivo en comparación a los cerdos destetados a los 28 días, lo cual concuerda con el trabajo de Vega et al. (2012), donde evaluaron 24 granjas comerciales con destete temprano (21-24 d), moderadas (25-27 d) y tardías (28-31 d), encontrando que las granjas con destete más temprano tenían los índices productivos más bajos. Así mismo, el ISD más alto en este estudio se presentó en cerdos destetados a los 21 días, posiblemente debido a que los animales tienen menor capacidad de adaptación al nuevo medio y alimentación y, por lo tanto, son más susceptibles a los cambios microbianos intestinales, favoreciendo el aumento de la población de bacterias patógenas como E. coli (McLamb et al., 2013).
Los niveles de glucosa sérica aumentaron en los animales que consumieron la dieta D3 y los niveles más bajos se presentaron en D1 y D2, resultados que concuerdan con Mohana y Kim (2014), que adicionaron E. faecium a la dieta, y con Londoño y Parra (2015), quienes adicionaron cepas probióticas en el alimento, probablemente debido al aumento en la digestibilidad de los nutrientes y al mejor aprovechamiento de las proteínas y carbohidratos (Cai et al., 2015).
Los niveles de triglicéridos y colesterol en cerdos alimentados con D1 y D2 fueron los más altos, mientras que en D3 fueron los más bajos. Forte et al. (2016), asimismo, adicionaron B. subtilis en el alimento de gallinas ponedoras comerciales, logrando disminuir la concentración de colesterol y triglicéridos en sangre, mostrando el potencial reductor de estos dos factores en sangre por parte de los probióticos. Estudios con diversos tipos de probióticos han demostrado una reducción de los niveles séricos de colesterol, como es el caso de Lactobacillus casei y Bifidobacterium animalis que disminuyeron los niveles de colesterol en ratas obesas de laboratorio (Bubnov et al., 2017), así como el Enterococus faecium (Londoño y Parra, 2015; Zhang et al., 2017), Lactobacillus plantarum (Bosch et al., 2014), Lactobacillus acidophilus (Song et al., 2015).
Se han encontrado que algunas cepas de probióticos producen hidrolasa de sales biliares (BSH), permitiendo que las cepas puedan metabolizar estas sales evitando su reabsorción. Esto podría conducir a la reducción del colesterol sérico, ya sea al aumentar la formación de nuevos ácidos biliares o al reducir la solubilidad y absorción del colesterol a través de la luz intestinal (Choi et al., 2015). Además, algunas bacterias tienen la capacidad de inmovilizar e incorporar colesterol dietético en sus membranas (Lye et al., 2010; Bosch et al., 2014). La reducción de colesterol y de triglicéridos puede resultar benéfico, tanto para los lechones como para el consumidor final de la carne de cerdo, ya que personas con altos niveles de colesterol LDL y niveles bajos de colesterol HDL suelen tener niveles altos de triglicéridos en sangre (Ponnampalam et al., 2011), pudiéndose disminuir la incidencia de enfermedades cardiovasculares en el hombre (McAloon et al., 2016).
La dieta D3 presentó los niveles séricos más altos de calcio y fosforo, similar a los hallazgos de Hosseini et al. (2013) en pollos de engorde. Así mismo, Londoño y Parra (2015) aumentaron los niveles séricos de estos dos elementos al adicionar E. faecium en la dieta. Los probióticos tienen la capacidad de producir la enzima fitasa, que puede liberar minerales que no son disponibles por la acción del fitato, resultando en una mayor disponibilidad de minerales como calcio y fósforo (Parvaneh et al., 2014).
El destete es una actividad productiva que genera graves problemas en la cría de cerdos comerciales durante la primera semana después del destete, que a menudo da como resultado el «síndrome de estrés posdestete (PWSD)» (Campbell et al., 2013), la disminución de la actividad de las enzimas digestivas intestinales, disminución de la respuesta inmune, y aumento de las citoquinas (Hu et al., 2013). El hígado es uno de los órganos que se ven afectados con el estrés del destete, sufriendo lesión oxidativa inducida, apoptosis y la pérdida de función, aumentando la enzima aspartato aminotransferasa (AST) y la ALT (Hu et al., 2013).
La ALT en suero es un marcador bioquímico, que no es solo un bioindicador de daño hepático, sino que también es un predictor para evaluar la salud general (Liu et al., 2014). En el presente estudio se observó una reducción de ALT con la adición de B. subtilis en el alimento, lo que indicaría un buen funcionamiento de órganos, en especial del hígado. En forma similar, Liu et al. (2014) adicionaron una cepa probiótica de Lactobacillus johnsonii en el alimento obteniendo un menor nivel de ALT en comparación a la dieta control (con antibiótico).
CONCLUSIONES
-
La inclusión de agentes antimicrobianos diferentes a los antibióticos, especialmente Bacillus subtilis en la dieta de cerdos en fase posdestete resultó en una menor incidencia de diarreas, mejores parámetros metabólicos, mayor ganancia de peso y mejor conversión alimenticia.
-
Los cerdos destetados a los 28 días presentaron los mejores resultados para las variables en estudio en comparación con aquellos destetados a los 21 días.
-
El uso de B. subtilis puede ser considerado como una buena alternativa al uso de antibióticos como promotores de crecimiento cuando son suministrados en dietas de cerdos en fases criticas del crecimiento como el destete.
Literatura citada
1. Bednorz C, Oelgeschläger K, Kinnemann B, Hartmann S, Neumann K, Pieper R, Bethe A, et al. 2013. The broader context of antibiotic resistance: zinc feed supplementation of piglets increases the proportion of multiresistant Escherichia coli in vivo. Int J Med Microbiol 303: 396-403. doi: 10.1016/j.ijmm.2013.06.004 [ Links ]
2. Begum M, Hossain MM, Kim IH. 2016. Effects of fenugreek seed extract supplementation on growth performance, nutrient digestibility, diarrhoea scores, blood profiles, faecal microflora and faecal noxious gas emission in weanling piglets. J Anim Physiol An N 100: 11211129. doi: 10.1111/jpn.12496 [ Links ]
3. Begum M, Li HL, Hossain MM, Kim, IH. 2015. Dietary bromelainC.3.4.22.32 supplementation improves performance and gut health in sows and piglets. Livestock Sci 180: 177-182. doi: 10.1016/j.livsci.2015.07.013 [ Links ]
4. Bosch M, Fuentes MC, Audivert S, Bonachera MA, Peiró S, Cuñé J. 2014. Lactobacillus plantarum CECT 7527, 7528 and 7529: probiotic candidates to reduce cholesterol levels. J Sci Food Agr 94: 803-809. doi: 10.1002/jsfa.6467 [ Links ]
5 Bubnov RV, Babenko LP, Lazarenko LM, Mokrozub VV, Demchenko OA, Nechypurenko OV, Spivak MY. 2017. Comparative study of probiotic effects of Lactobacillus and Bifidobacteria strains on cholesterol levels, liver morphology and the gut microbiota in obese mice. EPMA J 8: 357-376. doi: 10.1007/s13167-017-0117-3 [ Links ]
6. Cai L, Indrakumar S, Kiarie E, Kim IH. 2015. Effects of a multi-strain Bacillus species-based direct-fed microbial on growth performance, nutrient digestibility, blood profile, and gut health in nursery pigs fed corn-soybean mealbased diets. J Anim Sci 93: 4336-4342. doi: 10.2527/jas.2015-9056 [ Links ]
7. Campbell JM, Crenshaw JD, Polo J. 2013. The biological stress of early weaned piglets. J Anim Sci Biotechnol 4: 1-4. doi: 10.1186/2049-1891-4-19 [ Links ]
8. Cho JH, Kim IH. 2015. Effects of microencapsulated organic acids and essential oils on growth performance and intestinal flora in weanling pigs. Rev Colomb Cienc Pec 28: 229-237. doi: 10.17533/udea.rccp.v28n3a3 [ Links ]
9 Choi SB, Lew LC, Yeo SK, Parvathy NS, Liong MT. 2015. Probiotics and the BSH-related cholesterol lowering mechanism: a Jekyll and Hyde scenario. Crit Rev Biotechnol 35: 392-401. doi: 10.3109/07388551.2014.889077 [ Links ]
10. [CIOMS] Council for International Organization of Medical Sciences. 2012. International guiding principles for biomedical research involving animals. [Internet]. Available in: https://grants.nih.gov/grants/olaw/guiding_principles_2012.pdf [ Links ]
11. Dhruw K, Verma AK, Agarwal N, Singh P, Patel BHM. 2015. Effect of live Lactobacillus acidophilus NCDC 15 and CURD as probiotics on blood biochemical profile of early weaned piglets. Int J Bio-resource Stress Manag 6: 330-334. doi: 10.5958/0976-4038.-2015.00054.8 [ Links ]
12. Forte C, Moscati L, Acuti G, Mugnai C, Franciosini MP, Costarelli S, Cobellis G, et al. 2016. Effects of dietary Lactobacillus acidophilus and Bacillus subtilis on laying performance, egg quality, blood biochemistry and immune response of organic laying hens. J Anim Physiol An N 100: 977-987. doi: 10.1111/jpn.12408 [ Links ]
13. Giang HH, Viet TQ, Ogle B, Lindberg JE. 2012. Growth performance, digestibility, gut environment and health status in weaned piglets fed a diet supplemented with a complex of lactic acid bacteria alone or in combination with Bacillus subtilis and Saccharomyces boulardii. Livestock Sci 143: 132-141. doi: 10.1016/j.livsci.2011.09.003 [ Links ]
14. Gutiérrez LA, Montoya OI, Vélez JMZ. 2013. Probióticos: una alternativa de producción limpia y de remplazo a los antibióticos promotores de crecimiento en la alimentación animal. Rev. P+L 8: 135-146. [ Links ]
15. Heo JM, Opapeju FO, Pluske JR, Kim JC, Hampson DJ, Nyachoti CM. 2013. Gastrointestinal health and function in weaned pigs: a review of feeding strategies to control post-weaning diarrhoea without using in-feed antimicrobial compounds. J Anim Physiol An N 97: 207-237. doi: 10.1111/j.14390396.2012.01284 [ Links ]
16. Hosseini SA, Meimandipour A, Alami F, Mahdavi A, Mohiti-Asli M, Lotfollahian H, Cross D. 2013. Effects of ground thyme and probiotic supplements in diets on broiler performance, blood biochemistry and immunological response to sheep red blood cells. Ital J Anim Sci 12: e19. doi: 10.4081/ijas.2013.e19 [ Links ]
17. Hu CH, Xiao K, Luan ZS, Song J. 2013. Early weaning increases intestinal permeability, alters expression of cytokine and tight junction proteins, and activates mitogen-activated protein kinases in pigs. J Anim Sci 91: 1094-1101. doi: 10.2527/jas.2012-5796 [ Links ]
18. Kim JC, Hansen CF, Mullan BP, Pluske JR. 2012. Nutrition and pathology of weaner pigs: Nutritional strategies to support barrier function in the gastrointestinal tract. Anim Feed Sci Technol 173: 3-16. doi: 10.1016/j.anifeedsci.2011.12.022 [ Links ]
19. Li P, Piao X, Ru Y, Han X, Xue L, Zhang H. Ki. 2012. Effects of adding essential oil to the diet of weaned pigs on performance, nutrient utilization, immune response and intestinal health. Asian Austral J Anim 25: 1617-1626. doi: 10.5713/ajas.2012.12292
20. Liu Z, Ning H, Que S, Wang L, Qin X, Peng T. 2014. Complex association between alanine aminotransferase activity and mortality in general population: a systematic review and meta-analysis of prospective studies. Plos One 9: e91410. doi: 10.1371/journal.pone.0091410 [ Links ]
21. Londoño S, Lallès J, Parra J. 2016. Effect of probiotic strain addition on digestive organ growth and nutrient digestibility in growing pigs. Rev Fac Nac Agron 69: 7911-7918. doi: 10.15446/rfna.v69n2.59136 [ Links ]
22. Londoño S, Parra J. 2015. Efecto de la adición de cepas probióticas sobre metabolitos sanguíneos en cerdos en crecimiento. Biotecnol Sector Agropec Agroind 13: 49-56. doi: 10.18684/BSAA(13)49-56 [ Links ]
23. Lye HS, Rahmat-Ali GR, Liong MT. 2010. Mechanisms of cholesterol removal by Lactobacilli under conditions that mimic the human gastrointestinal tract. Int Dairy J 20: 169-175. doi: 10.1016/j.idairyj.2009.10.003 [ Links ]
24. McAloon CJ, Boylan LM, Hamborg T, Stallard N, Osman F, Lim PB, Hayat SA. 2016. The changing face of cardiovascular disease 2000-2012: an analysis of the World Health Organisation global health estimates data. Int J Cardiol 224: 256-264. doi: 10.1016/j.ijcard.2016.09.026 [ Links ]
25. McLamb L, Gibson AJ, Overman EL, Stahl C, Moeser AJ. 2013. Early weaning stress in pigs impairs innate mucosal immune responses to enterotoxigenic E. coli challenge and exacerbates intestinal injury and clinical disease. Plos One 8: e59838. doi: 10.1371/journal.pone.0059838 [ Links ]
26. Michiels J, Degroote J, Ovyn A, Possemiers S, De Smet S, Nakamura N. 2016. Feeding Bacillus subtilis C3102 to sows and suckling piglets and to weaned piglets improves parameters of gut health and feed: gain ratio in weaners. J Anim Sci 94(Suppl 3): 135-137. doi: 10.2527/jas2015-9763 [ Links ]
27. (Enterococcus faecium) supplementation on the growth performance, digestibility and blood profiles in weanling pigs. Vet Med-Czech 59: 527- 535. doi: 10.17221/7817-VETMED
28. Naqid IA, Owen JP, Maddison BC, Gardner DS, Foster N, Tchórzewska MA, et al. 2015. Prebiotic and probiotic agents enhance antibody-based immune responses to Salmonella typhimurium infection in pigs. Anim Feed Sci Tech 201: 57-65. doi: 10.1016/j.anifeedsci.2014.12.005 [ Links ]
29. NRC. 2012. Nutrient requirements of swine. 11th ed. Washington DC: Nattional Academic Press, [ Links ]
30. Parvaneh K, Jamaluddin R, Karimi G, Erfani R. 2014. Effect of probiotics supplementation on bone mineral content and bone mass density. Sci World J 2014: 595962. doi: 10.1155/2014/595962 [ Links ]
31. Ponnampalam EN, Lewandowski P, Nesaratnam K, Dunshea FR, Gill H. 2011. Differential effects of natural palm oil, chemicallyand enzymaticallymodified palm oil on weight gain, blood lipid metabolites and fat deposition in a pediatric pig model. Nutr J 10: 53. doi: 10.1186/1475-2891-10-53 [ Links ]
32. Reis de Souza TC, Mariscal G, Escobar K. 2010. Algunos factores fisiológicos y nutricionales que afectan la incidencia de diarreas posdestete en lechones. Vet México 41: 275-288. [ Links ]
33. Song M, Park S, Lee H, Min B, Jung S, Park S, Kim E, Oh S. 2015. Effect of Lactobacillus acidophilus NS1 on plasma cholesterol levels in diet-induced obese mice. J Anim Sci 98: 1492-1501. doi: 10.3168/jds.2014-8586 [ Links ]
34. Suiryanrayna MV, Ramana JV. 2015. A review of the effects of dietary organic acids fed to swine. J Anim Sci Biotechnol 6: 45. doi: 10.1186/s40104015-0042-z [ Links ]
35. Thacker PA. 2013. Alternatives to antibiotics as growth promoters for use- in swine production: a review. J Anim Sci Biotechnol 4: 35. doi: 10.1186/2049-1891-4-35 [ Links ]
36. Vega R, Estrella C, Valera A, Calud A, Villar E. 2012. Performance of selected Philippine commercial piggery farms weaning at different ages. Philipp J Vet Anim Sci 38: 127-133. [ Links ]
37. Vermeulen L, Van Beirendonck S, Bulens A, Van Thielen J, Driessen B. 2016. Sire line of pigs affects weaning weight, growth performance, and carcass characteristics of offspring. J Anim Sci 94: 4360-4368. doi: 10.2527/jas.2016-0591 [ Links ]
38. Yang H, Xiong X, Wang X, Tan B, Li T, Yin Y. 2016. Effects of weaning on intestinal upper villus epithelial cells of piglets. Plos One 11: 36939. doi: 10.1038/srep36939 [ Links ]
39. Zeng Z, Xu X, Zhang Q, Li P, Zhao P, Li Q, Liu J, Piao X. 2015. Effects of essential oil supplementation of a lowenergy diet on performance, intestinal morphology and microflora, immune properties and antioxidant activities in weaned pigs. J Anim Sci 86: 279-285. doi: 10.1111/asj.12277 [ Links ]
40. Zhang F, Qiu L, Xu X, Liu Z, Zhan H, Tao X, Shah NP, Wei H. 2017. Beneûcial effects of probiotic cholesterol-lowering strain of Enterococcus faecium WEFA23 from infants on dietinduced metabolic syndrome in rats. J Dairy Sci 100: 1618-1628. doi: 10.3168/ jds.2016
41. Zhou TX, Cho JH, Kim IH. 2012. Effects of supplementation of chitooligosaccharide on the growth performance, nutrient digestibility, blood characteristics and appearance of diarrhea in weanling pigs. Livestock Sci 144: 263-268. doi: 10.1016/j.livsci.2011.12.009 [ Links ]
Recibido:16 de julio de 2018
Aceptado para publicación: 24 de enero de 2019