Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Acta Médica Peruana
versión On-line ISSN 1728-5917
Acta méd. peruana v.24 n.1 Lima ene./abr. 2007
ARTÍCULOS DE REVISIÓN
Ascitis
Ascites
Rossana Román Vargas1
1. Médico Jefe del Servicio de Hepatología Hospital Nacional Edgardo Rebagliati Martins - ESSALUD.
RESUMEN
La ascitis es el acúmulo anormal de líquido en la cavidad abdominal, que en el caso del paciente cirrótico obedece a una conjugación de factores determinantes. Diversas teorías se han elaborado al respecto a lo largo de las décadas anteriores, sin embargo el concepto actual es que el principal mecanismo patofisiológico de formación de ascitis es un estado de vasodilatación periférica permanente en el cirrótico, asociado a una relativa hipoperfusión renal que a su vez determina la activación de una serie de mecanismos retenedores de sodio y agua. Es un fenómeno progresivo cuya historia natural se puede ver como un espectro de enfermedad, teniendo como evento extremo al síndrome hepato-renal, con ascitis refractaria al tratamiento diurético y la mayor frecuencia de colonización bacteriana del líquido ascítico, fenómeno conocido como peritonitis bacteriana espontánea. El siguiente artículo revisa la patofisiología, diagnóstico, complicaciones y aspectos terapéuticos de la ascitis en el paciente cirrótico.
Palabras claves: ascitis, vasodilatación periférica, renina-angiotensinaaldosterona, síndrome hepato-renal, ascitis refractaria, paracentesis, diuréticos, peritonitis bacteriana espontánea.
ABSTRACT
Ascites is the abnormal accumulation of fluid into the peritoneal cavity, which in the cirrhotic patient is due to a number of determinant factors. Many theories have been elaborated in that regard during the previous decades, however the current concept states that the chief pathophysiologic mechamism of ascites formation is a permanent state of peripheral vasodilation in the cirrhotic patient, associated with a relative renal hypoperfusion, which in turn activates a host of sodium and water retaining mechanisms. It is a progressive phenomenon and its natural history can be viewed as a spectrum of disease, having at one end of the spectrum the so called hepatorenal syndrome, with ascites refractory to diuretic treatment and a higher frequency of bacterial colonization of the ascitic fluid, so called spontaneous bacterial peritonitis. This article reviews the pathophysiology, diagnosis, complications and therapeutic aspects of ascites in the cirrhotic patient.
Key words: ascites, peripheral vasodilation, rennin-angiotensin-aldosteron, hepatorenal syndrome, refractory ascites, paracentesis, diuretics, spontaneous bacterial peritonitis.
DEFINICIÓN
Ascitis es la acumulación de líquido en la cavidad peritoneal. Representa un estado de retención corporal total de sodio y agua y su causa más frecuente es la cirrosis, independientemente de la etiología1. Ver Tabla 1.
Los pacientes con cirrosis avanzada, tienen dificultad, en mantener dentro de límites normales los fluidos extracelulares, lo que genera la acumulación de líquido en la cavidad peritoneal, esto asociado a una disfunción renal, especialmente retención de sodio y agua, y vasoconstricción renal.
TEORÍAS EN LA GÉNESIS DE LA ASCITIS Existen tres teorías:
1. Volumen circulante bajo: la hipertensión portal provoca una contracción del volumen circulante efectivo (aquella parte del volumen circulante que es efectiva en estimular los receptores de volumen)2. Se combinan para ésto: a) La hipertensión portal
b) La dilatación del lecho vascular esplácnico.
c) Hipoalbuminemia
d) La vasodilatación periférica asociada a los shunts
El riñón se comporta como si al individuo le faltara volumen, necesitando sodio y agua y por tanto, lo retiene. La reducción de volumen circulante efectivo promueve el aumento de la renina, angiotensina y aldosterona, los baroreceptores estimulados provocan aumento de noradrenalina probablemente responsable de vasocontricción renal y la vasopresina se eleva (baroreceptores de volumen).
2. Volumen circulante elevado: el primer elemento sería la retención de sodio con expansión del volumen plasmático. En realidad la retención de sodio precede a la formación de ascitis.
El aumento de la presión venosa hepática, se trasmite a los sinusoides que tienen una rica inervación y receptores de presión. La expansión del volumen plasmático sería responsable del desarrollo de ascitis.
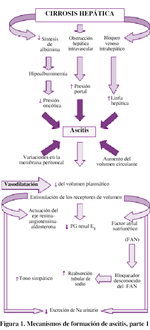
3. Vasodilatación arterial periférica: en realidad combina las previas. Ni la formación de ascitis y la retención de sodio y agua inducida por la hipovolemia, ni una primaria retención de sodio por el riñón con expansión de volumen posterior son el mecanismo primario. El cirrótico está en un estado de vasodilatación arterial con frecuente presencia de shunts arterio-venosos. Esto lleva a menor llenamiento del árbol vascular y aumento del débito cardíaco, con estimulación hormonal de renina, angiotensina aldosterona, noradrenalina y vasopresina. Esto conduce a vasoconstricción renal y retención de sodio y agua. El factor natriurético está aumentado en cirróticos con ascitis, como expresión de un intento compensador que no logra su objetivo. La característica disminución del clearence de agua libre del cirrótico, es secundaria al aumento de la hormona antidiurética. La vasodilatación esplácnica está mediada por el óxido nítrico, que es un poderoso vasodilatador presente en las células endoteliales y que actúa en forma paracrina. A medida que esto va en aumento, se llega al síndrome hepatorenal.
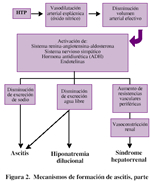
Además, el aumento de la presión sinusoidal, conduce a una mayor producción de linfa: los sinusoides no poseen membrana basal, lo cual los hace muy permeables. El flujo linfático aumenta linealmente con el aumento de la presión y la presión hidrostática elevada en el sinusoide hace que el flujo atraviese el espacio de Disse y se produzca una extravasación de linfa al peritoneo a través de la cápsula hepática, lo que ayuda a la focalización de la ascitis. Ver Figuras 1 y 2.
CUADRO CLÍNICO
Este varía de acuerdo a la severidad de la ascitis. Generalmente es la primera descompensación del paciente cirrótico. Uno de los hallazgos iniciales, es la matidez en flancos, la cual debe ser desplazable con la rotación del paciente a la derecha o a la izquierda. Cuando la ascitis es mayor, podemos encontrar el signo de la oleada positiva, y cuando ésta es masiva hallaremos un abdomen con piel lustrosa debido a una ascitis a tensión, acompañada generalmente de dificultad respiratoria, debido a la elevación de los hemidiafragmas. Después del examen del abdomen, el examen físico general puede ayudar a definir la causa de ascitis La presencia de eritema palmar, telangiectasias en los brazos o tórax, hipertrofia parotidea, ginecomastia, circulación colateral abdominal, sugieren que la ascitis es debida a enfermedad hepática3.
DIAGNÓSTICO Y ETIOLOGÍAS DIFERENCIALES
Se debe realizar:
1. Evaluación del grado de la función hepática
Hemograma, determinación de glicemia, albúmina, y tiempo de protrombina
2. Ecografía abdominal
Todo paciente cirrótico con ascitis debe ser explorado ecográficamente por varios motivos: * Descartar la presencia de un carcinoma hepatocelular. * Descartar la presencia de trombosis portal (contraindicación de trasplante hepático). * Valorar el tamaño del hígado, ya que un hígado pequeño indica una probabilidad de sobrevida muy corta. * Descartar otras patologías tales como: quistes intrabadominales, distensión gaseosa, etc.
3.- Paracentesis diagnóstica
Todo paciente con ascitis debe ser sometido a paracentesis diagnóstica, la cual puede realizarse con una aguja N° 22, en el punto medio entre la cicatriz umbilical y la sínfisis púbica, o en el cuadrante inferior izquierdo, en el punto que une los dos tercios internos con el tercio externo entre la cicatriz umbilical y la espina iliaca antero superior izquierda. Tabla 2.
Pruebas diagnósticas del líquido ascítico
1. Recuento celular: es la prueba más útil. El recuento habitual de leucocitos en un L. A. con ascitis no complicadas es de 280 cel/mm3 . Normalmente el recuento de PMN está entre el 27 y el 30% del total del recuento celular. El valor de corte normal de PMN es de 250 cel/mm3 .La causa más frecuente de recuento elevado de leucocitos es la peritonitis bacteriana espontánea, (PBE) en la que se aprecia un recuento aumento a predominio de PMN, (se revisará posteriormente en la sección complicaciones). En la tuberculosis peritoneal y en la carcinomatosis , existe un aumento a predominio de linfocitos.
2. Gradiente albúmina en suero y en líquido ascítico (GASA): Se sustrae la concentración de albúmina del líquido ascítico a la del suero, ambas muestras deben ser del mismo día. La determinación de esta gradiente divide a las causas de ascitis en dos grandes grupos: - Si es mayor de 1,1: está asociada a hipertensión portal en 90% de los casos. - Si es menor de 1,1: la ascitis es debida a otra causa diferente a hipertensión portal.
3. Cultivo: debido a que entre el 10 a 27% de los pacientes con cirrosis y ascitis tienen PBE, al momento de la admisión al hospital ( sin signos o síntomas en 2/3 de los casos), se debe realizar cultivo del líquido ascítico, en frascos de hemocultivo, con volúmenes entre 10 y 20 ml de líquido ascítico, tan pronto sea extraído el líquido ascítico, ya que esta técnica, comparada con la técnica de siembra en el laboratorio es más sensible, aumentando la positividad del cultivo de 42% a 90%.
4. Proteínas totales: es de menor ayuda diagnóstica que la determinación de GASA. Aproximadamente el 20% de los cirróticos con ascitis pueden tener proteínas totales en L.A > 2,5 g/dL, y es erroneamente catalogado como exudado. Por otro lado los pacientes con ascitis en tratamiento con diuréticos, hasta en 2/3 de los casos pueden elevar las proteínas a rango de exudado, llevando a errores diagnósticos de probable malignidad o tuberculosis.
5. Tinción de Gram: generalmente es de poca utilidad debido a que el recuento de colonias en el líquido ascítico es muy bajo (1 org/ml). Aún si se centrifugan 50 ml de L.A, la sensibilidad es del 10%.
6. Citología: es de alto valor cuando se sospecha de carcinomatosis peritoneal. Debe ser examinada el mismo día de tomada la muestra
7. Tuberculosis: la visualización de bacilos ácido alcohol resistentes (BAAR), es muy baja 0% - 2%. La prueba de adenosindeaminasa (ADA), enzima producida por el microorganismo, tiene una especificidad > al 90%, pero la sensibilidad disminuye dramáticamente ante la presencia de cirrosis.
TRATAMIENTO
El tratamiento de la ascitis en el paciente cirrótico, ha sufrido muchos cambios en las últimas décadas, conjuntamente con la evaluación de la función hepática, ya mencionada anteriormente, se debe realizar una evaluación de la función renal, mediante pruebas de creatinina, úrea, depuración de creatinina, y electrolitos en sangre, así como también un examen de sedimento y electrolitos en orina5. Valores de creatinina en sangre igual o superior a 1,5 mg/dl, orientan al diagnóstico de síndrome hepatorenal. Para poder decidir el tipo de tratamiento, debemos estimar el volumen del líquido ascítico, el cual se debe realizar de una manera semicuantitativa en grados: Grado 1: Ascitis de pequeño volumen. Grado 2: Ascitis de moderado volumen. Grado 3: Ascitis de gran volumen.
El grado de tensión de la ascitis no sólo depende del volumen sino también de la indemnidad del tono muscular de la pared abdominal. Se debe también examinar la presencia de edemas periféricos.
Bases del tratamiento:
1. Restricción de la ingesta de sodio: la pérdida de líquido y peso están directamente relacionadas al balance de sodio, sin necesidad de restricción de la ingesta de fluidos. La base del tratamiento consiste en la restricción de ingesta de sodio (2 gr/día). La restricción de sodio, mejora la sobrevida del paciente cirrótico. Sólo entre el 10 a 15% de paciente responden al tratamiento exclusivamente con dieta6,7.
2. Evitar la restricción indiscriminada de líquidos: se ha demostrado que la restricción de volumen conlleva a hipernatremia. Sólo está indicado la restricción de volumen en los casos de severa hiponatremia (Na sérico < 120 mmol/L)
3. Diuréticos: la dosis de diuréticos dependerá del grado de ascitis. Se debe iniciar con dosis en la mañana de furosemida y espironolactona, a la dosis de 40 mg de la primera y 100 mg de la segunda, la dosis irá en aumento, manteniendo siempre la misma proporción entre ambos diuréticos. No se recomienda fraccionar la dosis en dos o tres tomas al día, ya que los resultados son los mismos, y de otro lado, la administración de diuréticos por la tarde o noche, causaría disconfort en el paciente ya que provocaría micción durante la noche, provocando insomnio y malestar. El uso de furosemida endovenosa, no se recomienda, aunque el paciente se encuentre en anasarca, ya que esta droga administrada por vía endovenosa disminuye dramáticamente la filtración glomerular, debido a la hipotensión arterial que produce. Por otro lado se ha demostrado buena absorción oral de la furosemida pese al edema existente.
No existe límite de pérdida de peso diario para aquellos pacientes con ascitis y edema masivo. Una vez que se ha se ha resuelto el edema periférico se aconseja perder 0,5 Kg. por día. La dosis de ambos diuréticos puede ser aumentada simultáneamente, si la pérdida de peso y la natriuresis son inadecuadas, (manteniendo la relación 100mg : 40 mg). La dosis tope es de 400 mg de espironolactona y 160 mg de furosemida. Aquellos pacientes que no responden a estas dosis se les considera como ascitis refractaria o ascitis resistente a los diuréticos y deben ser incluidos en la lista de espera de trasplante hepático. La ascitis intratable por diuréticos es aquella que no puede ser satisfactoriamente eliminada o cuya recidiva precoz no puede ser evitada debido al desarrollo de complicaciones relacionadas con los diuréticos que impiden el uso de dosis efectivas de estos fármacos (encefalopatía hepática, insuficiencia renal inducida por diuréticos, hiponatremia, hipo o hiperkalemia).
4. Paracentesis a gran volumen: Está indicada en aquellos pacientes con ascitis grado 3 o ascitis a tensión. El volumen medio de la ascitis en estos pacientes es de alrededor de 10 L. En este grupo de pacientes el tratamiento de elección es la paracentesis a gran volumen, asociada a la infusión endovenosa de alúmina humana (8 gr por cada litro de ascitis removido). El uso de otros expansores de volumen como la poligelina o el dextrano 70, son menos eficaces que la albúmina en prevenir la disfunción circulatoria posparacentesis. Este trastorno es clínicamente asintomático y se caracteriza por un aumento marcado de la actividad de renina plasmática, y se asocia con una recidiva más rápida de la ascitis y un acortamiento de la sobrevida8. Una vez tratados los pacientes con paracentesis, deben ser tratados con dieta hiposódica y diuréticos para evitar la reacumulación de ascitis.
5. Shunt peritoneo –venoso: el shunt peritoneo- venoso o shunt de Leveen o Denver, fue popularizado en la década de los 70, como tratamiento fisiológico de la ascitis. Sin embargo se han reportado muchas complicaciones tales como oclusión del shunt, e infecciones del líquido ascítico y coagulación vascular diseminada, lo que ha hecho que no se utilice más este procedimiento.
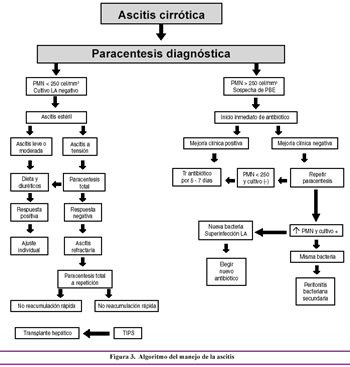
6. Shunt transyugular portosistémico intrahepático: (TIPS): el TIPS es un shunt porto cava latero lateral, colocado por un radiólogo intervencionista. La técnica fue propuesta para el tratamiento de sangrado por várices, pero estudios no controlados han propuesto que éste podría ser un tratamiento para la ascitis refractaria.; sin embargo estudios randomizados han demostrado que el TIPS empeora la sobrevida en este grupo de pacientes, empeorando las alteraciones hemodinámicas asociadas con cirrosis9,10. En la Figura 3 se aprecia el algoritmo de manejo de la ascitis.
PERITONITIS BACTERIANA ESPONTÁNEA
La peritonitis bacteriana espontánea (PBE) es la infección bacteriana del líquido ascítico en ausencia de un foco infeccioso intrabadominal.
En la mayoría de los casos, las bacterias causantes de PBE son bacilos aerobios gramnegativos procedentes de la propia flora intestinal del paciente, debido a las numerosas alteraciones que presentan los pacientes cirróticos en los mecanismos de defensa antimicrobiana, entre los que destacan el sobrecrecimiento bacteriano intestinal, alteraciones de la membrana intestinal, disminución de la actividad del sistema retículo endotelial y alteraciones en la inmunidad humoral inespecífica sérica y del líquido ascítico11. Estas alteraciones favorecen el paso de determinadas bacterias desde la propia luz intestinal del paciente al líquido ascítico, probablemente a través de los ganglios linfáticos mesentéricos, fenómeno conocido como translocación bacteriana5.
La PBE es una complicación frecuente y grave de la cirrosis. La incidencia fluctúa entre el 10 y el 30%. Aproximadamente el 50 a 60% son de adquisición extrahospitalaria. La supervivencia a esta afección es del 30%; sin embargo los pacientes que sobreviven a un episodio de PBE tienen mal pronóstico a mediano plazo, ya que su sobrevida al año es de sólo 30 a 50%5.
Diagnóstico: generalmente es de curso asintomático y ocasionalmente puede presentar sintomatología tal como: dolor abdominal, signos peritoneales, fiebre. Frecuentemente se presenta de forma inespecífica, como encefalopatía, deterioro de la función renal, sin cuadro clínico de infección abdominal. El diagnóstico de PBE se basa en un recuento de neutrófilos en líquido ascítico > 250 cel/mm3 con o sin cultivo positivo.
Variantes de la PBE
*Bacteriascitis: consiste en la positividad del cultivo del líquido ascítico con un recuento de PMN < 250 cel/mm3. Puede corresponder a tres situaciones: - Bacterascitis asintomátca: colonización espontánea transitoria del líquido ascítico, que suele autolimitarse sin tratamiento. Se recomienda repetir la paracentesis, y sólo si persiste el cultivo positivo o los PMN son > 250 cel/mm3 , debe recibir tratamiento antibiótico. - Bacteriascitis sintomática: cuando el paciente presenta clínica de PBE, se recomienda tratamiento antibiótico.
- Bacteriascitis secundaria: como colonización bacteriana secundaria a una infección extraperitoneal, que obviamente debe tratarse con antibióticos.
PBE con cultivo negativo: antes llamada ascitis neutrocítica sugiriendose que tendría mejor pronóstico que la PBE. El recuento de neutrófilos es > de 250 cel/mm3 pero el cultivo es negativo.
Peritonitis séptica: infección del líquido ascítico como consecuencia de un foco séptico abdominal, el cual requiere generalmente de tratamiento quirúrgico.
Tratamiento: ante todo paciente con diagnóstico de PBE (recuento PMN > de 250 cel/mm3 ) , se debe iniciar tratamiento antibiótico empírico, sin esperar el resultado de los cultivos. El tratamiento antibiótico ideal deberá cumplir los siguientes requisitos: actividad sobre las bacterias más frecuentemente responsables de PBE (enterobacterias y estreptococos), concentraciones adecuadas en líquido ascítico, y ausencia de efectos indeseables sobre la función hepática y renal. La cefotaxima es el antibiótico que más se ha utilizado, y se sigue considerando el fármaco de elección. La dosis recomendada es de 2 gr/12 hs. vía EV por 5 a 7 días. Otras alternativas: ceftriaxona, amoxicilina/ácido clavulánico. han demostrado seguridad y eficacia similares a cefotaxima12. Debe evitarse el uso de aminoglucósidos debido al riego de nefrotoxicidad y la precipitación de un síndrome hepatorenal.
Tratamiento oral: en casos de PBE no complicada (sin encefalopatía, shock, ileo, hemorragia digestiva), se ha observado que la administración de ofloxacina a dosis de 400 mg/12 hr puede ser tan eficaz y más económica que el tratamiento con cefotaxima, sin observarse efectos secundarios13. Sin embargo no se puede recomendar actualmente la utilización de este esquema universalmente (fuera de protocolos de estudio debidamente diseñados) para el tratamiento de PBE y el paciente con dicha condición debe ser hospitalizado para tratamiento endovenoso.
Monitorización del tratamiento: se aconseja realizar una paracentesis de control a las 48 hs de iniciado el tratamiento, debiéndose observar una reducción de al menos el 25% en el recuento inicial y la negativización del cultivo. Recientemente se ha demostrado que aquellos pacientes con PBE . con bilrrubina sérica > de 4 mg/dl o nitrógeno ureico en sangre mayor de 30 mg/dl, se beneficarían más si conjuntamente a la terapia antibiótica se usara albúmina endovenosa a la dosis de 1,5 g/K de peso en el primer día y 1 g/K en el tercer día.
Profilaxis: teniendo en cuenta el mal pronóstico de los pacientes cirróticos después de desarrollar una PBE, es conveniente prevenir esta complicación: - Pacientes con hemorragia digestiva: el 20% de los pacientes cirróticos con hemorragia digestiva ingresan con alguna infección y aproximadamente entre el 35 a 60% desarrollaran infección durante los primeros días de la hospitalización. Diversos estudios han demostrado la eficacia de profilaxis antibiótica, y en un meta-análisis se ha observado que dicha profilaxis aumenta la sobrevida. La profilaxis más aceptada es la administración de norfloxacina 400mg C/12 hr por 7 días por vía oral14. - Pacientes con antecedentes de PBE: el riesgo de recurrencia es del 35 al 70% al año de seguimiento. En este grupo de pacientes se recomienda la profilaxis con norfloxacina 400 mg/día de por vida. - Pacientes con ascitis sin PBE previa: si los niveles de proteínas en líquido ascítico son menores a 1 g/dl, se recomienda la profilaxis con norfloxacina 400 mg/día, durante la hospitalización15.
AGRADECIMIENTOS
Agradecemos a la Sociedad Peruana de Medicina Interna por la autorización de reproducción parcial del contenido del libro denominado: Tópicos Selectos en Medicina Interna: Gastroenterología.
REFERENCIAS BIBLIOGRÁFICAS
1. Moreau R, Lebrec D. Acute renal failure in patients with cirrhosis: perspectives in the age of MELD. Hepatol 2003; 37: 233-243. [ Links ]
2. Moore KP, Wong F, Ginès P, Garcia-Tsao G, Jimenez W, Planas R, Arroyo V. The management of ascites in cirrhosis: Report on the Consensus Conference of the International Ascites Club. Hepatology 2003,38:258- 266. [ Links ]
3. Arroyo V, Jiménez W. Clinical need for antidiuretic hormone antagonists in cirrhosis. Hepatology 2003; 37: 13-15. [ Links ]
4. Guevara M. Tratamiento del síndrome hepatorrenal. Gastroenterol Hepatol 2003; 26(4): 270-274 [ Links ]
5. Boyer TD. Transjugular intrahepatic portosystemic shunt: Current status. Gastroenterology 2003; 124: 1700-1710 [ Links ] 6. Arroyo V, Guevara M, Ginès P. Hepatorenal syndrome in cirrhosis: Pathogenesis and treatment. Gastroenterology 2002,122:1658-1676. [ Links ]
7. Ortega R, Ginès P, Uriz J, Cárdenas A, Calahorra B, De las Heras D, Guevara M, Bataller R, Jimenez W, arroyo V, Rodés J. Terlipressin therapy with and without albumin for patients with hepatorenal syndrome: Results of a prospective, nonrandomized study. Hepatology 2002,36:941-948. [ Links ]
8. Rössle M, Ochs A, Gülberg V, Siegerstetter V, Holl J, Deibert P, Olschewski M, Reiser M, Gerbes AL. A comparison of paracentesis and transjugular intrahepatic portosystemic shunting in patients with ascites. N Engl J Med 2000; 342: 1701-1707. [ Links ]
9. Rosa H, Silveiro A O, Perini R F, Arruda C B. Bacterial infections in cirrhotic patients and its relationship with alcohol. Am J Gastroenterol 2000; 95: 1290-1293. [ Links ]
10. Runyon BA. Management of adult patients with ascites caused by cirrhosis. Hepatology 1998, 27: 264-272. [ Links ]
11. Ascites .Seminars in Liver Disease 1997;17(3): 163 - 260 [ Links ]
12. Ginès A, Fernández-Esparrach G, Monescillo A, Planas R, Solà R, Ginès P, Terg R, Inglada L, Vaqué P, Salerno F, Vargas V, Jiménez W, Arroyo V, Rodés J. Randomized trial comparing albumin, dextran 70 and polygeline in cirrhotic patients with ascites treated by paracentesis. Gastroenterology 1996,111:1002-1010. [ Links ]
13. Arroyo V, Ginès P, Gerbes AL, Dudley FJ, Gentilini P, Laffi G, Reynolds TB, Ring-Larsen H, Schölmerich J. Definition and diagnostic criteria of refractory ascites and hepatorenal syndrome in cirrhosis. Hepatology 1996; 23: 164-176. [ Links ]
14. Runyon BA. Care of patients with ascites. N Eng J Med 1994; 330: 337-342 [ Links ]
15. Runyon B A. Patients with deficient ascitic fluid opsonic activity are predisposed to spontaneous bacterial peritonitis. Hepatology 1988; 8: 632-635. [ Links ]
CORRESPONDENCIA
Rossana Román