INTRODUCCIÓN
Las 2-oxazolinas son monómeros que polimerizan vía polimerización catiónica por apertura de anillo y producen polímeros lineales1,2. Iniciadores de esta polimerización son, por ejemplo, el tosilato y triflato de metilo, entre otros1. La característica más importante de esta polimerización es que transcurre de forma “viva” o sea sin reacciones secundarias tales como reacciones de terminación o de transferencia de cadena y por esto se pueden obtener polímeros con grados de polimerización y funcionalización prefijados3,4,5. La polimerización de las 2-oxazolinas permite elaborar arquitecturas poliméricas tales como, por ejemplo, polímeros telequélicos, macromonómeros, copolímeros en bloque, copolímeros injertados, hidrogeles, etc1,2,3,4,5,6,7.
Los polímeros telequélicos son polímeros que contienen funciones químicas en sus dos extremos de cadena. Estas funciones químicas pueden ser, por ejemplo, aminas, ácidos carboxílicos, grupos vinilo, etc.3 Estos polímeros pueden ser sintetizados, por ejemplo, vía el método de terminación donde se introduce la función química mediante la reacción del agente terminador con la cadena propagante. Los polímeros telequélicos sirven para sintetizar diversos polímeros tales como, por ejemplo, hidrogeles, lipogeles, polímeros cíclicos, etc1,3. La Administración de Alimentos y Medicamentos (FDA) de los Estados Unidos considera a la polimetiloxazolina y polietiloxazolina como polímeros biocompatibles y por esta razón existe un gran interés de los grupos de investigación en el mundo en este tipo de polímeros para aplicarlos al campo de la medicina2.
En esta investigación se presenta la síntesis y caracterización de polímetros telequélicos de polioxazolinas funcionalizados con grupos etil xantato y vinilo en el final de la cadena polímérica.
PARTE EXPERIMENTAL
Las sustancias utilizadas en esta investigacíon fueron usadas como recibidas o fueron purificadas y secadas segun métodos estandar descritos en la literatura6,7,8,9,10. Cloruro de succinilo metilico (pureza: 97%, procedencia: Aldrich), hidrocloruro de 2-cloroetilamonio (97%, Merck), trietilamina (98%, Merck), 2-etil-2-oxazolina (97% Merck), fue destilada antes de su uso, 4-vinilbencilcloruro (97%, Aldrich) destilado, piperazina (97%, Aldrich). Los análisis espectrométricos de resonancia magnética nuclear (RMN), espectrometría infrarroja (FTIR), espectrometría ultravioleta/visible (UV/Vis) y cromatografía de permeación en gel (GPC) de las sustancias usadas o generadas en esta investigación se realizaron mediante métodos estándar de la literatura.6,7,8
Cromatografo de permeación en gel (GPC), Water System, detector IR 410, UV 486, columna ultrastyrolgels 7 micrometros, porosidad 500, 103, 104 y 105 Angstrom. Espectrómetro de resonáncia magnética nuclear (RMN) Bruker Advance III 500 NMR, 500.13 MHz para 1H y 125.75 MHz para 13C, solvente cloroformo deuterado. Espectrómetro infrarrojo (FTIR) Perkin Elmer, Spectrum 100, método ATR. Espectrómetro Ultravioleta visible Thermoelectron Corporation, modelo Helios Gamma.
Purificación del iniciador 1,4-trans-Dibromobuteno (DBB)
Se agregó 4,11 g. de DBB a un vaso de 100 ml y luego se adicionó 10 mL de hexano y se calentó hasta 70°C hasta completa disolución. Se dejó de agitar, y se enfrió el líquido hasta temperatura ambiente. Se observó la formación de cristales blancos de DBB, los cuales se filtraron y se volvieron a disolver en hexano (10 mL) a 70°C, se volvió a enfriar la solución y se obtuvieron nuevamente los cristales de DBB. El DBB se secó y se guardó a baja temperatura (5°C) en un balón herméticamente cerrado y purgado con nitrógeno.
1H-RMN (CDCl3) δ: 3,95 (-CH2-Br); 5,98 (H-C=C).
Purificación del etil xantato de potasio
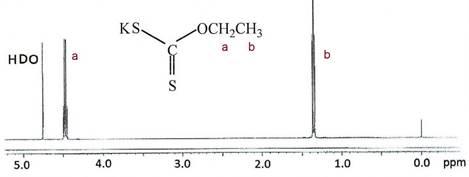
El etil xantato de potasio se purificó mediante recristalizaciones en tolueno y heptano11. Se disolvió 9,3 g. de etil xantato de potasio en 200 mL de acetona a 40°C. La solución se filtró y se concentró mediante evaporación. A la solución se le agregó lentamente 800 mL de tolueno, destilado y seco. Se observó la precipitación del etil xantato de potasio. Se eliminó el solvente sobrenadante y se secó con un flujo de nitrógeno seco. Se repitió el procedimiento utilizando hexano como medio precipitante. Finalmente, el etil xantato de potasio, se guardó en oscuridad y a baja temperatura (5°C). El porcentaje de perdida en el proceso de purificación fue del 30%. Se confirmó su estructura por resonáncia magnética nuclear (Fig. 1). 1H-RMN (D2O) δ: 1,35 (CH3), triplete); 4,45 (CH2-O, cuadruplete), 4,75 (HDO).
Determinación de la pureza del etil xantato de potasio mediante espectrometría ultravioleta/visible11.
Se pesó 0,069 g. de etil xantato de potasio purificado en un vaso de 100 mL y se disolvió con 50 mL agua destilada. Se colocó en fiola de 100 mL, y se enrazó con agua pura. Se tomó una alícuota de 8,8 mL que se llevó a una fiola de 500 mL y se enrazó con agua destilada. Finalmente, mediante espectrometría UV/vis, se midió la absorbancia máxima de esta solución acuosa de etil xantato de potasio a 226 nm y 302 nm. La relación entre la absorbancia del pico a 226 nm y el de 302 nm fue de 0,50 estando en concordancia con la literatura10. Se utilizó la absorbancia del etil xantato de potasio a 302 nm para hallar el coeficiente de extinción (ε) de este compuesto, y se obtuvo un valor de 17350, que esta en concordancia con lo reportado en la literatura para el etil xantato de potasio puro (17500)11. Entonces, de los resultados de UV y RMN se estimó que el etil xantato de potasio tiene alta pureza.
Síntesis de 2-Metoxicarboniletil-2-oxazolina (EsterOxa),6,9
En primer lugar, se sintetizó el 7-cloro-4-oxo-5-azaheptanoato de metilo mediante la reacción, en 150 mL de diclorometano, de cloruro de succinilo metílico (20 g.) y el hidrocloruro de 2-cloroetilamonio (15.4 g.) en presencia de trietilamina (30 g.) a 0°C. Se obtuvo un rendimiento de 74%. Luego, en una segunda etapa, se obtuvo la 2-metoxicarboniletil-2-oxazolina (EsterOxa) a partir de la ciclación de 19 g. 7-cloro-4-oxo-5-azaheptanoato de metilo con 7.6 g. de carbonato de sodio anhidro, y la aplicación de vacío (0,5 mmHg) durante 60 minutos5,6,8. El rendimiento fue del 60%. La EsterOxa se caracterizó por RMN: 1H-RMN (CDCl3) δ: 2,44 (-CH2CH2CO-); 2,58 (CH2-CO); 3,67 (CH3OCO); 3,71 (CH2-N=); 4,17 (CH2-O). 13C-RMN (CDCl3) δ: 22,5 (-CH2CH2CO-); 29,6 (-CH2CH2CO); 51,4 (CH3OCO); 53,8 (CH2-N=C); 66,9 (CH2-O-C); 165,9 (N=C-O); 172,3 (O-C=O).
Síntesis de 4-Vinilbencilpiperazina (4-VBP)12
La síntesis de la 4-VBP esta descrita en la literatura por Nuyken y colaboradores.12 Esta síntesis consiste en hacer reaccionar a 0°C el cloruro de vinilbencilo con un gran exceso molar (15/1) de piperazina anhidra en cloroformo anhidro. Se obtuvo un líquido amarillo rojizo con 95% de rendimiento.
1H-RMN (en CDCl3) δ: 1,51 (NH); 2,40 (NCH2-); 2,83 (CH2-NH); 3,46 (Ar-CH2); 5,2; 5,7, 6,7 (CH2-CH-); 7,3 (Har).
Síntesis de polímeros telequélicos con grupos terminales etil xantato
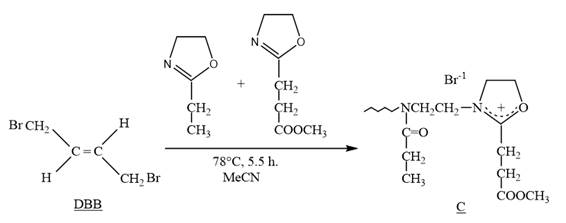
En primer lugar, se realizó la polimerización de los monómeros 2-etil-2-oxazolina (Etoxa) y 2-metoxicarboniletil-2-oxazolina (Esteroxa) (en una proporción molar de Etoxa/Esteroxa= 80/20), vía una polimerización catiónica por apertura de anillo, iniciada por el 1,4-trans-dibromobuteno (DBB) en acetonitrilo a 78°C en un tiempo de reacción de 5,5 horas y se determinó que en este tiempo de reacción se alcanzó el 100% de conversión de los monómeros. En segundo lugar, se realizaron todos los demas experimentos usando este tiempo de reacción y bajo las mismas condiciones de reacción.
Ejemplo típico: (Polímero P1): Se colocó en un reactor, bajo atmósfera de nitrógeno seco, 0,5 g. (2,33 mmoles) de DBB, 4,12 g. (41,6 mmoles ) de EtOxa, 1,62 g. (10,3 mmoles) de EsterOxa y 12,5 mL de acetonitrilo. Se polimerizó a 78°C y luego de 5,5 horas se enfrió la mezcla de reacción a temperatura ambiente y se terminó la polimerización con 3,7 g. (23,3 mmol) de etil xantato de potasio disuelto en 50 mL de acetonitrilo. Se filtró la mezcla de reacción y se evaporó el solvente a presión artmósferica. Luego, se agregó 40 mL de diclorometano (para disminuir la viscosidad de la mezcla) y se lavó, tres veces con 25 mL de una solución saturada de cloruro de sodio (para eliminar la sal remanente de etil xantato de potasio). Finalmente, a la mezcla se le agregó 4 g. de MgSO4 para secar la solución. Posteriormente, se filtró la mezcla y se evaporó el solvente obteniéndose un polímero. Se disolvió el polímero en 20 mL de cloroformo y se precipitó en 200 mL de éter dietílico. Se repitió este proceso (disolución-precipitación) tres veces y finalmente el polímero seco se guardó en un vial herméticamente cerrado a 5°C, bajo atmósfera de nitrógeno seco. Este polímero se caracterizó mediante RMN y FTIR: 1H-RMN (CDCl3) δ: 1,12 (-CH3); 1,42 (CH3-CH2-OC=S); 2,39 (-CO-CH2-CH3); 2,65 (-CH2CH2-CO-O); 3,45 (N-CH2); 3,65 (O-CH3); 3,95 (=CHCH2); 4,65 (O-CH2-CH3); 5,53 (=CH-).
13C-RMN (CDCl3) δ: 174,5 (C=O); 127,5 (C=C); 70,6 (S-COCH2); 51,7 (OCH3); 50,0 (=CH-CH2); 45,3 (NCH2CH2); 33,6 (-CH2SC); 25,9 (COCH2CH3); 13,7(-CSO-CH2CH3), 9.3 (COCH2CH3). FTIR (cm-1): 2,978 (C−H alifático), 1,734 (C=O, éster), 1,629 (N-C=O amida), 1,193 (C=S)13.
En el caso del telequélico terminado con grupos vinilo se procedió de forma similar solo que al momento de realizar la terminación se agregó 2,82 g. de 4-vinilbencilpiperazina (caso de polímeros PB) a la mezcla de reacción. Para desprotonar el final de cadena del polímero se agitó la mezcla con carbonato de potasio a 20°C durante 12 horas. Se filtró y se precipitó en éter dietílico, tres veces. Se caracterizó vía RMN:
1H-RMN (CDCl3) δ: 1,10 (-CH3); 2,30 (-CO-CH2-CH3); 2,65 (-CH2CH2-COO); 3,40 (N-CH2); 3,65 (O-CH3); 3,95 (=CHCH2); 5,3, 5,7 (CH2-CH); 5,5 (=CHCH2); 6,7 (=CH-), 7,2-7,6 (Har).
Ciclación del polímero telequélico conteniendo funciones etilxantato.
Procedimiento típico: en un frasco de vidrio, se disolvieron 2,0 g del polímero P1 y 0,7583 (10,4 mmoles) g. de n-butilamina en 500 mL de tetrahidrofurano (THF), el cual fue previamente secado con sódio metálico y destilado. En el frasco de vidrio se hizo burbujear aire con ayuda de una bombilla y una pipeta durante 24 horas. Después de este periodo se eliminó el tetrahidrofurano por evaporación hasta que se obtuvo el polímero seco. Se disolvió el polímero en cloroformo y se precipitó en éter dietílico. Se filtró y se secó el polímero obtenido. El polímero se guardó en un vial herméticamente cerrado y se le denominó P1-S-S. Este polímero se caracterizó por RMN.
1H-RMN (CDCl3) δ: 1,13 (-CH3); 2,39 (-CO-CH2-CH3); 2,6 (-CH2-CO-O); 2,85 (-CH2-S-S-CH2-); 3,45 (N-CH2-CH2-N); 3,65 (O-CH3); 3,95 (=CHCH2); 5,53 (=CH-).
RESULTADOS Y DISCUSIÓN
Los monómeros 2-etil-2-oxazolina (Etoxa) y 2-metoxicarboniletil-2-oxazolina (Esteroxa) fueron polimerizados vía una polimerización catiónica por apertura de anillo, iniciada por el 1,4-trans-dibromobuteno (DBB). En todos los experimentos siempre se uso un tiempo de reacción de 5,5 horas a 78°C porque en este tiempo de reacción, y bajo las mismas condiciones de reacción, se alcanzó el 100% de conversión de los monómeros. Se varió el porcentaje molar de EsterOxa entre 18 y 44% para que en una investigación posterior los grupos éster se pueda hidrolizar y obtener grupos ácido carboxílicos que pueden posibilitar introducir nuevas funcionalidades y propiedades a los polímeros telequélicos. El iniciador 1,4-trans-dibromo buteno (DBB) es un iniciador de doble funcionalidad y entonces se inician dos cadenas poliméricas por cada molécula de iniciador DBB.
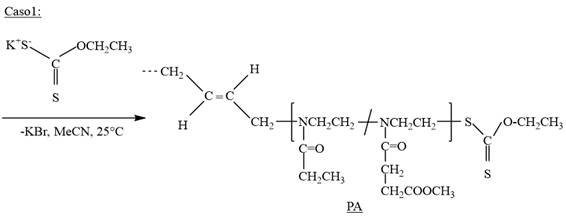
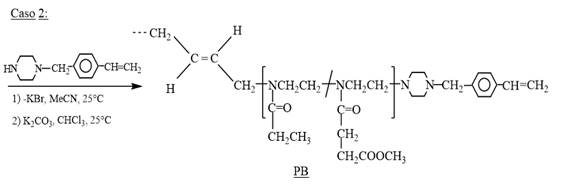
Síntesis y caracterización de los polímeros telequélicos con grupos terminales etil xantatoEsquema 1 Caso 1 Caso 2
Los telequélicos de EtOxa y de EsterOxa con grupos etil xantato fueron obtenidos mediante la terminación de la polimerización con una solución de etilxantato de potasio en acetonitrilo (Esquema 1, caso 1). Al terminar la polimerización con el etil xantato de potasio se introdujo este grupo funcional en los dos finales de cadena del polímero formándose así un polímero telequélico. En la Tabla 1 (Polímeros PA) aparecen las condiciones de la polimerización y los resultados obtenidos en la misma. La estructura de los polímeros telequélicos fue confirmada mediante los espectros 1H y 13C RMN (Ejemplo, espectros 1H RMN de PA2 y 13C RMN de PA1 en Fig 2 y 3, respectivamente). Los porcentajes molares de los monómeros Etoxa y Esteroxa en los copolímeros telequélicos se hallaron mediante el análisis cuantitativo del espectro 1H RMN (Fig. 2), comparando las señales “f“ (de Etoxa) versus “h+i“ (de Esteroxa) y esta razón fue similar a la razon molar inicial de estos monómeros (Tabla 1). El grado de polimerización de los polímeros telequélicos fue hallado comparando la suma de las señales “f“ y “h+i“ versus la señal del iniciador “a“ y fueron muy cercanos al valor de la relación molar inicial (Etoxa+Esteoxa)/Iniciador) (Tabla 1). Esto fue una evidencia de que la polimerización transcurrió en forma “viva” o sea solo ocurrieron las reacciones de iniciación y de propagación y no las reacciones secundarias tales como las reacciones de transferencia de cadena o de terminación. La funcionalización con grupos etil xantato fue determinada comparando las integrales de las señales „c“ y „a“. Sin embargo, los porcentajes de funcionalización con etil xantato no fueron mayores al 82% a pesar de que usó un gran exceso molar (de 10 a 1) de etil xantato de potasio en la reacción de terminación para forzar estadistícamente la inclusión de esta sustancia en el final de cadena. Este resultado significa que algunos extremos de las cadenas poliméricas de los polímeros telequélicos no contuvieron el grupo etil xantato. Es probable que la terminación habría ocurrido por reacción de las cadenas propagantes oxazolínicas con restos de humedad en algún componente del sistema de reacción o que, como se postula más adelante, una parte del grupo etil xantato incorporado al polímero se perdiera en el proceso de purificación por reacciones secundarias. Entonces, como resultado se obtuvo una mezcla de polímeros, algunos (porcentaje mayor) conteniendo dos grupos etil xantato en sus dos extremos (polímeros telequélicos) y un pequeño porcentaje de los polímeros con un solo grupo etil xantato en sus extremos de cadena.
trans
Tabla 1 Síntesis de los polímeros telequélicos. Condiciones de reacción y resultados.
| Polímeroa | Mi/DBBb | Mf/DBBc | Mn(RMN)d | Esteroxae | Fg |
| PA1 | 22 | 25 | 3040 | 18 | 64 |
| PA2 | 25 | 29 | 3380 | 19 | 69 |
| PA3 | 22 | 25 | 2770 | -f | 80 |
| PA4 | 24 | 24 | 3160 | 35 | 82 |
| PB1 | 21 | 22 | ........ | 22 | 69 |
| PB2 | 22 | 23 | ........ | 56 | 98 |
a)Denominación del polímero telequélico con grupos etil xantato (PA) y con grupos vinilo (PB), b) Relación molar inicial (Etoxa + Esteroxa)/Iniciador, c) Grado de polimerización = Relación molar experimental (Etoxa + Esteroxa)/Iniciador en el polímero telequélico obtenida vía análisis cuantitativo de 1H RMN d) Peso molecular obtenido a partir del grado de polimerización experimental del telequélico obtenido vía el espectro 1H RMN, e) Porcentaje molar de Esteroxa en el polímero telequélico (1H RMN), f) En el caso de PA3 solo se usó Etoxa, g) Funcionalización del polímero telequélico obtenida mediante 1H-RMN a traves de la comparación entre la señal “c”de los grupos etil xantato (o las señales “k y l” de los grupos vinilo) y las señales “a” y “b” del iniciador.
En todos los experimentos siempre se usó acetonitrilo como solvente, y una temperatura y tiempo de reacción de 78°C y 5.5 horas, respectivamente.
Los valores de peso molecular y dispersión de peso molecular fueron 2,600, y 1.35 y de 2,500 y 1.32 para PA1 y PA2, respectivamente. Estos valores fueron obtenidos mediante cromatografia de permeación en gel (GPC). Para todos los copolímeros se usó una relación molar inicial de 20% molar de EsterOxa y 80% molar de Etoxa, excepto para PA4 que se usó 40 % molar de Esteroxa y 60% molar de EtOxa. Para PB1 se usó 20 % molar de Esteroxa y 80% molar de EtOxa y para PB2 se usó 50% molar Etoxa y 50% molar Esteroxa, respectivamente.
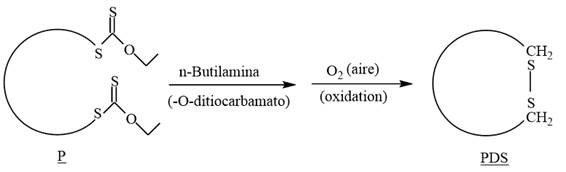
Adicionalmente, se llevó a cabo una reacción de modificación de los polímeros telequélicos PA1 y PA2. Se realizó la reacción de ciclizacion del polímero telequélico mediante la aminólisis del grupo etil xantato con un exceso de n-butilamina, obteniendose grupos tioles en los extremos de cadena y luego estos grupos se oxidaron con el oxígeno del aire, en tetrahidrofurano, para conseguir finalmente grupos disulfuro que cerraban la estructura del polímero obteniéndose así polímeros cíclicos (Esquema 2).
Cabe mencionar que la reacción anterior se llevó a cabo en forma muy diluida, según datos de la literatura14, para evitar estadistícamente la reacción de dimerización de los polímeros (reacción intermolecular) y favorecer al máximo la ciclación o reacción intramolecular del polímero.
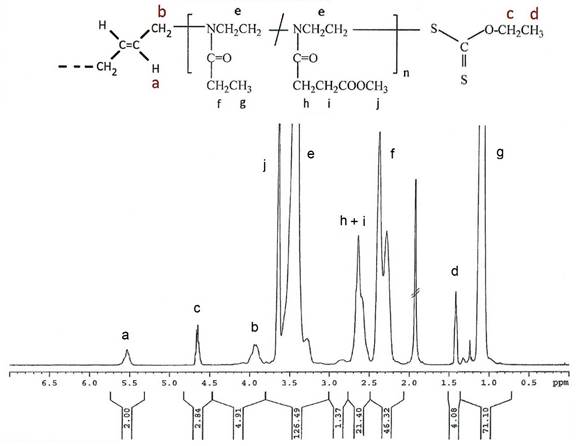
Figura 2 Espectro 1H RMN del polímero telequélico PA2 (Etoxa (81% molar) y Esteroxa (19% molar), 2n=29) terminado con grupos etil xantato. Funcionalización con etil xantato = 69%.
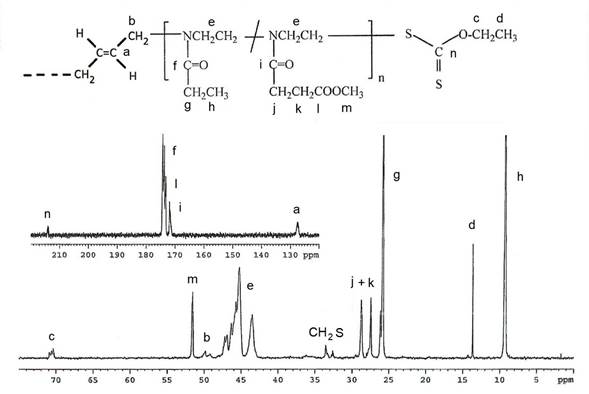
Figura 3 Espectro 13C RMN del polímero telequélico PA1, 2n=25) terminado con grupos etil xantato. Funcionalización con etil xantato = 64%.
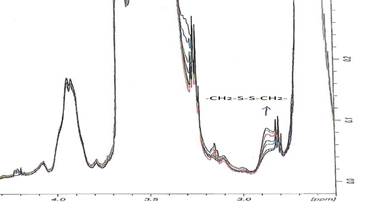
En el espectro 1H RMN de los polímeros ciclados se observó la desaparición de la señal de los grupos metilo y metileno del etil xantato de potasio en 1,4 y 4,5 ppm, respectivamente y la aparición de la señal de los grupos metilenos (-CH2-S-S-CH2) del disulfuro en 2,8 ppm (Fig. 4). La reacción de ciclización de PA2 fue estudiada mediante la técnica de RMN y se obtuvo una secuencia de espectros de 1H RMN donde se observó, conforme transcurría el tiempo, la desaparición paulatina de las señales de los grupos etil xantato y la aparición simultánea de las señales del grupo O-tiocarbamato (producto de la ciclización) y del grupo disulfuro en 2,8 ppm (Fig. 5 y 6).
Esquema 2. Reacción de ciclización de los polímeros PA1 y PA2. Donde P=PA1 o PA2
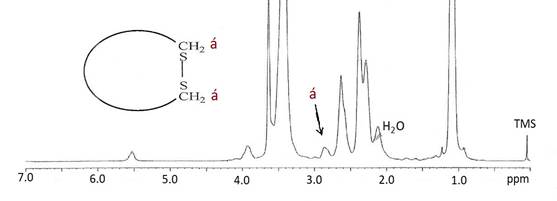
Figura 4 Espectros 1H RMN del polímero telequélico PA1, después de ser ciclado. Se observa la desaparición de las señales del grupo etil xantato en 1,4 y 4,65 ppm.
Cabe mencionar que en el espectro 1H RMN de los polímeros telequélicos tambien se observa esta señal en modo mas débil (señal en 2,8 ppm Fig. 2). Por esto, es posible que en la síntesis del polímero telequélico si se obtuviera inicialmente una mayor funcionalización de los polímeros telequélicos con grupos xantato pero que esta funcionalización disminuyera en el proceso de purificación de los polímeros debido posiblemente a una hidrólisis parcial del grupo etil xantato. Es conocido de la literatura que los compuestos que contienen atomos de azufre, tales como los xantatos, disufuros, tioles, etc, son químicamente muy inestables15,16.
El interés en la obtención de polímeros cíclicos es que este tipo de polímeros pueden utilizarse, por ejemplo, para adsorberse sobre superficies de nanopartículas metálicas, por ejemplo, nanopartículas de hierro posibilitando una alta estabilidad de las mismas14
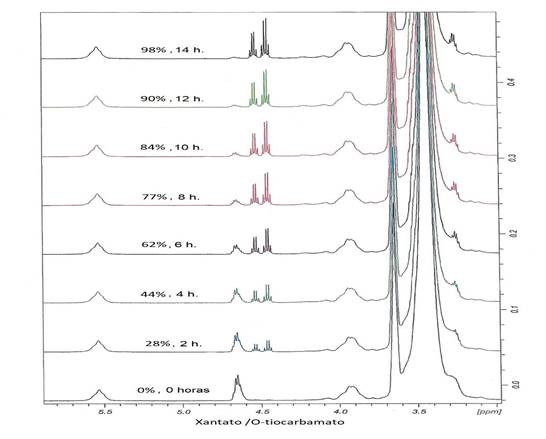
Figura 5 Secuencia de espectros 1H RMN de PA2 en el proceso de ciclización. Se obtuvo un rendimiento del 98% al cabo de 14 horas de la reacción llevada a cabo en el tubo de RMN.
Síntesis y caracterización de los copolímeros telequélicos con grupos terminales vinilo
Se sintetizaron también telequélicos de Etoxa y Esteroxa conteniendo grupos vinilo en los extremos de cadena. Esto se realizó mediante una polimerización catiónica por apertura de anillo de los mencionados monómeros, la cual fue iniciada por el dibromobuteno (DBB) en acetonitrilo y en este caso la terminación fue llevada a cabo con la 4-vinilbencilpiperazina (4-VBP) (Esquema 1, caso 2). Con este método se consiguió introducir en el final de cadena los grupos vinilo. Los polímeros telequélicos fueron denominados PB1 y PB2. Los resultados se consignan en la Tabla 1.
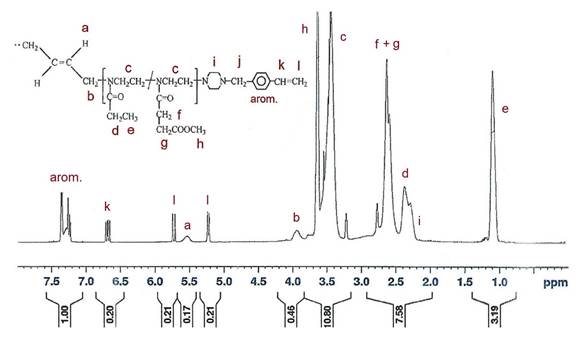
Figura 7 Espectro 1H RMN del polímero telequelico PB2 (Etoxa 44% molar y Esteroxa 56% molar, 2n=24) terminado con grupos vinilo. Funcionalización aproximada con grupos vinilo= 98%.
Se determinó, mediante los espectros RMN de estos polímeros, que PB1 y PB2 tuvieron un grado de polimerización de 22 y 23, un contenido de Esteroxa de 22 y 56% molar en concordancia con el valor teórico de 25 y 50 % molar y también que su funcionalización fue de 69 y 98%, respectivamente (Fig. 7). La funcionalización de 98% se consiguió cuando se usó en la etapa de terminación un exceso de agente terminador del 600% ya que de esta manera se forzó en términos estadísticos la reacción del terminador (4-VBP) con la cadena propagante en tanto que con una terminación equimolar solo se obtuvo 69% de funcionalización.
CONCLUSIONES
Se elaboraron nuevos polímeros telequélicos a partir de la polimerización por apertura de anillo de la 2-etil-2-oxazolina y 2-éster-2-oxazolina terminada por el etil xantato de potasio y la 4-vinilbencil-piperazina. Estos polímeros telequélicos contuvieron grupos etil xantato o vinilo en sus extremos de cadena. La funcionalización máxima obtenida con grupos etil xantato fue del 82% molar debido posiblemente a la inestabilidad de los grupos terminales etil xantato en el final de cadena. Los telequélicos con grupos xantato fueron ciclados mediante una reacción de aminólisis con n-butilamina y posterior oxidación, con oxígeno, de los tioles generados. Se formaron copolímeros cíclicos conteniendo grupos disulfuro. Por otro lado, con los polímeros telequélicos de polioxazolinas conteniendo grupos vinilo en sus finales de cadena se consiguió obtener 98% de funcionalización con estos grupos cuando se usó un gran exceso del agente terminador.