INTRODUCCIÓN
Las cáscaras de huevo de gallina han constituido durante años parte del material de descarte, tanto de la industria alimentaria como de los hogares y, usualmente, se desechan junto con los desperdicios urbanos. En ocasiones, se utilizan como material adsorbente de aguas residuales, como pigmentos en las industrias de pintura y del papel, como aditivo en la industria alimentaria, como relleno en la industria de la construcción o para extraer colágeno a partir de las membranas. Si bien estas aplicaciones contribuyen a disminuir el impacto ambiental, aún resultan insuficientes.
Según el Ministerio de Desarrollo Agrario y Riego (MIDAGRI), en el Perú se consumieron 15.2 kg de huevo per cápita en 2022, lo que equivale a 242 unidades por persona. Esto significa que cada peruano consumió un huevo diario durante el 67% del año. La producción nacional de huevo durante 2022 continuó con su tendencia al alza y alcanzó las 510 962 toneladas (Asociación Peruana de Avicultura [APA], 2023). Esto generó aproximadamente 58 249 toneladas de cáscaras de huevo que probablemente fueron desechadas al medio ambiente, ya que son ignoradas durante las preparaciones culinarias y en procesos de producción como la mayonesa, panificación, huevo deshidratado pasteurizado, yema y clara pasteurizada deshidratada, entre otros.
Debido a la importante cantidad de calcio que contienen las cáscaras de huevo, este estudio se realizó con la finalidad de obtener nuevos productos. Además, las cáscaras de huevo, como subproducto de la industrialización del huevo, podrían representar una opción para cubrir las necesidades nutricionales de la población. Al descomponer los compuestos originales de las cáscaras para formar nuevos compuestos, en este caso en forma de citrato mediante el proceso de lixiviación ácida, se podría beneficiar al organismo humano y contribuir con la disminución de residuos sólidos.
El objetivo de esta investigación fue obtener citrato de calcio de las cáscaras de huevo de gallina para ser utilizado como suplemento vitamínico y como aditivo en la producción de alimentos en la industria alimentaria. Como hipótesis general, se propone que las cáscaras de huevo de gallina, usualmente desechadas junto con los desperdicios urbanos y teniendo en cuenta la importante cantidad de carbonato de calcio en forma de calcita que contienen, pueden ser utilizadas para la extracción de calcio en forma de citrato de calcio, lo que beneficiaría la salud humana.
Las cáscaras de huevo
Las cáscaras de los huevos de aves son envolturas calcáreas y biomineralizadas, formadas por cristales de carbonato de calcio depositados en una matriz orgánica o red proteica. Representan entre el 10% y el 12.81% del peso del huevo (Nys et al., 2004; Yenice et al., 2016). El contenido de carbonato de calcio (CaCO3) oscila entre el 93.6% y el 95.0% (Fernández y Arias, 2000; Nys et al., 2004), mientras que el contenido de calcio se sitúa entre el 35.5% y el 44.3% (Park y Sohn, 2018; Rendón et al., 2003). El carbonato de magnesio tiene un contenido promedio del 0.8% y el fosfato tricálcico, un promedio del 0.73% (Fernández y Arias, 2000). Las cáscaras también contienen P, K, Na, Ni, Mn, Co, Be, V, Sr, Zn, Fe, Cu, Cr, F y Se (Park y Sohn, 2018; Schaafsma et al., 2000); asimismo, contienen niveles muy bajos de Pb, Al, Cd y Hg, que son potencialmente tóxicos (Schaafsma et al., 2000). La contaminación microbiana de las cáscaras de huevo es alta, donde destaca la presencia de aerobios, anaerobios y coliformes (Sharma et al., 2022), debido a la procedencia de los huevos, tanto de la microbiota de la cloaca y las plumas como de los sistemas de crianza en jaulas.
El calcio como mineral de gran importancia para el organismo humano
El calcio es el mineral más abundante en el organismo humano y forma parte de la reserva o depósito para la formación y mantenimiento de huesos y dientes, junto con el fosfato y el magnesio (Martínez de Victoria, 2016). Alrededor del 99% se encuentra como hidroxiapatita en el tejido óseo. El calcio cumple funciones de mineralización, crecimiento y maduración de los huesos. Puede ejercer su función reguladora de forma pasiva o activa. Cuando los niveles de calcio plasmático regulan las reacciones enzimáticas, se trata de la forma pasiva, mientras que la forma activa se ejerce mediante la concentración intracelular de Ca2+ (Martínez de Victoria, 2016). Además, el calcio participa en los procesos metabólicos y se absorbe en forma iónica (Ca2+), por lo que previamente debe liberarse de los complejos a los que está unido por acción enzimática y del potencial de hidrógeno (pH). En el estómago, los complejos de calcio son solubles debido al pH proporcionado por el ácido clorhídrico; en el medio intestinal, el aumento del pH favorece su precipitación y su absorción principalmente en el duodeno y el yeyuno proximal, cuyo pH oscila entre 3.5 y 6.7 (Farré y Frasquet, 1999).
El citrato de calcio como suplemento vitamínico
El citrato de calcio es la sal cálcica del ácido 2-hidroxi-1,2,3-propanotricarboxílico tetrahidratada. Es un polvo cristalino, blanco, inodoro, soluble en agua e insoluble en alcohol. Según el sistema de clasificación Anatomical Therapeutic Chemical (ATC) y la Defined Daily Dose (DDD) de la Organización Mundial de la Salud, el citrato de calcio se encuentra en el grupo A12 del ATC con el código A12AA09 (WHO Collaborating Centre for Drug Statistics Methodology, 2024).
El citrato de calcio ofrece ventajas como una mejor absorción y biodisponibilidad en comparación con otras sales. Puede administrarse con o sin alimentos sin que ello afecte su absorción, por lo que puede utilizarse en cualquier momento del día, y su uso es seguro en casos de litiasis renal (Zurita, 2002). Se utiliza como complemento nutricional o como fuente de calcio administrada por vía oral. Ayuda a prevenir y tratar las insuficiencias de calcio en el organismo humano, al igual que contribuye a mantener los huesos y dientes sanos. Es soluble en el ácido gástrico e insoluble en la sección del duodeno, de manera que solo una fracción de calcio está disponible para su absorción.
El calcio presente en los alimentos y suplementos es calcio elemental y se encuentra en forma de compuesto, principalmente como carbonato, citrato, lactato y fosfato, los cuales presentan distintos grados de absorción y biodisponibilidad (Zurita, 2002). Cuanto más soluble es una sal de calcio o de magnesio, más eficaz es en términos de absorción y biodisponibilidad.
La mejor manera de obtener calcio es a través de los alimentos; sin embargo, existe un porcentaje importante de la población que no consume la cantidad recomendada de calcio, además de magnesio, vitamina D (Olza et al., 2017) y fósforo (Martínez de Victoria, 2016). Esto se debe a que no los ingieren en su alimentación diaria, por lo que es necesario añadir suplementos a su dieta; la cantidad de suplementos dependerá de cuánto calcio se obtiene de los alimentos. Los suplementos de calcio se absorben mejor cuando se ingieren con los alimentos y cuando se toman en dosis pequeñas (500 mg o menos) varias veces al día.
En el mercado existen múltiples compuestos de calcio, cuyo contenido de calcio elemental oscila entre el 9% y el 40%, así como distintas vías de administración según la presentación. Los suplementos a base de carbonatos contienen un 40% de Ca, los citratos un 21%, los gluconatos un 9%, los lactatos un 13% y las harinas de hueso, valvas de ostra y dolomitas un 30 % (Zurita, 2002). Las sales o complejos de calcio y magnesio también se utilizan como suplementos nutricionales (Rodríguez et al., 2014), por lo que deben ser considerarlos dentro de la alimentación.
El calcio desempeña una función fundamental en el organismo humano, ya que, además de fortalecer los huesos, ayuda a que los músculos, el corazón y los nervios funcionen correctamente. Si no se obtiene suficiente calcio en la dieta, el organismo tomará de los huesos el calcio que necesita. Con el tiempo, este proceso debilita los huesos y aumenta el riesgo de desarrollar osteoporosis. Esta es una enfermedad que provoca que los huesos se debiliten y se vuelvan frágiles. Las personas con osteoporosis tienen un mayor riesgo de quebrarse o fracturarse los huesos. Hay evidencia científica que justifica la suplementación de calcio y vitamina D en pacientes que padecen tanto de osteoporosis como de deficiencia de esta vitamina en dosis diarias de 2000 unidades internacionales (UI) o 0.05 mg de vitamina D3 (colecalciferol). Cualquier fármaco que se utilice para el tratamiento de la osteoporosis debe prescribirse junto con un suplemento de calcio y vitamina D3 (Sosa y Gómez, 2021).
En la búsqueda de materias primas que contengan calcio con mayor biodisponibilidad, Rodríguez et al. (2014) obtuvieron sal de citrato de calcio y magnesio a partir de depósitos de dolomita, debido a que la dolomita es un mineral compuesto por carbonato doble de calcio y magnesio [CaMg(CO3)2], para ello, utilizaron soluciones de ácido cítrico como material de extracción. De manera similar, Vásquez y Glorio (2007) obtuvieron citrato de calcio y magnesio a partir de conchas de choro (Aulacomya ater [Molina]), que también están compuestas de material calcáreo, empleando soluciones de ácido clorhídrico como agente de lixiviación. En estas investigaciones se obtuvo el citrato de calcio y magnesio para posteriormente utilizarlo en la elaboración de productos como el néctar de durazno. En un esfuerzo por mejorar los procesos o proponer métodos alternativos, Rosas et al. (2018) utilizaron cáscaras de huevo molidas como fuente de calcio en la elaboración de pastas tipo fettuccine con el objeto de proveer alimentos ricos en calcio. De la misma manera, Pérez et al. (2018) emplearon micropolvos de cáscaras de huevo en la elaboración de un yogurt funcional y fortificado. En estas últimas investigaciones se añadieron los polvos de cáscaras de huevo directamente en las preparaciones de productos alimenticios.
METODOLOGÍA
Se inició con la contextualización de la información sobre las características y composición de las cáscaras de huevo de gallina, el método de lixiviación ácida y los suplementos vitamínicos a base de citrato. Luego, se realizó la experimentación según el número de tratamientos especificados en el diseño experimental, se obtuvieron resultados que fueron discutidos y, finalmente, se llegó a las conclusiones de la investigación.
Materiales
Las cáscaras de huevo de gallina se obtuvieron del material de descarte proveniente de la unidad productiva de panificación del Programa Profesional de Ingeniería Química de la Universidad Nacional de San Agustín, donde se utilizan huevos de gallina para la producción diaria. El zumo de limón se obtuvo de los frutos denominados «limón común» o «limón criollo» de la variedad sutil (Citrus aurantifolia Swingle), adquiridos en el mercado local. Los insumos químicos para las determinaciones fisicoquímicas y el contenido de minerales fueron adquiridos en laboratorios locales. La experimentación, los análisis fisicoquímicos, el análisis de minerales y el análisis microbiológico se realizaron en los laboratorios de química inorgánica y de bioprocesos industriales del Programa Profesional de Ingeniería Química de la misma universidad. La metodología aplicada en la investigación se desarrolló en dos etapas: la primera consistió en el pretratamiento de las cáscaras de huevo de gallina y la segunda en la obtención del citrato de calcio.
Pretratamiento de las cáscaras de huevo de gallina
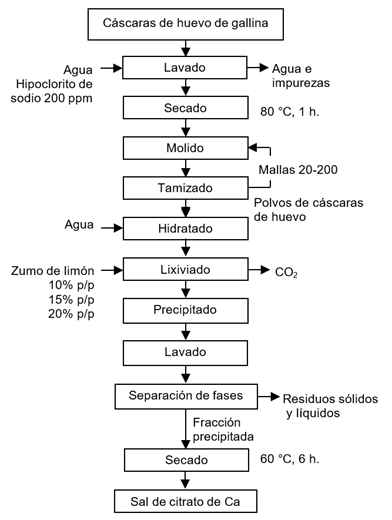
El pretratamiento consistió en el lavado de las cáscaras de huevo y la disminución del tamaño de partícula (Figura 1) para incrementar la superficie de contacto y mejorar el rendimiento en el proceso de obtención del citrato de calcio. La proporción de cáscaras de huevo sucias era alta y no se tenía evidencia de que los huevos hubieran sido sometidos a un adecuado lavado antes de su uso. Después de acopiarlas, se lavaron con agua y se eliminaron las impurezas; esta operación fue rápida ya que las impurezas se encontraban ligeramente adheridas a las cáscaras. Se desinfectaron por inmersión en una solución de 200 ppm de hipoclorito de sodio durante 20 minutos, luego fueron lavadas nuevamente para retirar residuos del hipoclorito de sodio.
Posteriormente, se introdujeron en una estufa eléctrica a una temperatura de 80 °C por un lapso de 15 minutos. Seguidamente, se sometieron a molienda. Debido a su tamaño voluminoso y estructura frágil, fue necesario usar un molino de discos para la trituración previa. Para obtener una molienda fina, se utilizó un molinillo eléctrico de granos (Nima de acero inoxidable, 300 W). Finalmente, las cáscaras molidas se tamizaron en un conjunto de tamices (W.S. Tyler Ro-Tap RX-29 Sieve Shaker), de malla US Standard ASTM E-11 y abertura en micrómetros (µm), con la finalidad de obtener las proporciones y tamaños de granulometría adecuados.
Obtención del citrato de calcio por lixiviación ácida
Este proceso consistió en la extracción del citrato de calcio con el ácido cítrico del zumo de limón, tal como se muestra en la Figura 1. Previo al proceso de extracción, se agregó agua sobre las cáscaras de huevo molidas en una proporción del 50% del peso del soluto, con la finalidad de hidratar las cáscaras de huevo molidas e incrementar la velocidad de reacción. El vaso de precipitados con las cáscaras de huevo molidas e hidratadas se colocó sobre un agitador magnético, se añadió el zumo de limón de forma lenta, fraccionada y con agitación para evitar reboses del contenido por la efervescencia producida por el desprendimiento de gas, en proporciones de cáscara de huevo molidas y zumo de limón del 10, 15 y 20% p/p, en tiempos de reacción de 2, 4 y 6 horas.
Al término del proceso de extracción, se distinguieron tres fases, las cuales se separaron físicamente mediante tamizado y filtración. La fracción precipitada se sometió a lavados con agua destilada y, posteriormente, fue secada en una estufa a una temperatura de 60 °C durante 6 horas. Finalmente, se sometió a molienda fina y tamizado en un tamiz número 140. Para la extracción del citrato de calcio, se realizaron tratamientos para evaluar la granulometría, las proporciones de soluto y el tiempo de reacción, con la finalidad de encontrar parámetros óptimos para la obtención del citrato de calcio.
Para la caracterización de las cáscaras de huevo y del citrato de calcio, se determinó su composición química. El análisis de humedad se realizó conforme a la norma técnica peruana (NTP 209.008); la materia orgánica, mediante el método Walkley-Black; el contenido de calcio, por el método espectrofotométrico; el fósforo, con el método colorimétrico; el magnesio mediante el método complexométrico; y los carbonatos, por el método gasovolumétrico. Para la determinación de metales totales se utilizó el método de espectrometría de masa con plasma acoplado inductivamente (ICP-MS).
Análisis microbiológico
El citrato de calcio extraído es un precipitado pulverulento y el solvente usado es materia orgánica, ambos muy propensos a contaminarse. Para determinar su inocuidad, se realizó un recuento total de hongos y levaduras mediante una siembra por incorporación sobre agar oxitetraciclina gentamicina, y un recuento de bacterias y aerobios mesófilos empleando el medio agar plate count en una siembra por incorporación de placas estériles (International Commission on Microbiological Specifications for Foods [ICMSF], 2011).
Análisis sensorial
Para garantizar el grado de aceptación del citrato de calcio como suplemento vitamínico, se realizó una evaluación organoléptica diferenciada, utilizando un diseño experimental de bloques al azar para diez muestras de citrato de calcio en polvo. Se empleó la prueba de aceptabilidad con el método de escala hedónica y se trabajó con un panel de diez personas adultas no entrenadas y consumidoras habituales de suplementos de calcio. Estas personas indicaron su nivel de agrado mediante puntajes del uno al cinco, diferenciándose de la siguiente manera: (1) «me disgusta mucho», (2) «me disgusta moderadamente», (3) «no me gusta ni me disgusta», (4) «me gusta moderadamente» y (5) «me gusta mucho». Esta evaluación se aplicó para los atributos de olor, color, sabor y textura con el fin de determinar el producto con mejores atributos.
RESULTADOS
Composición química de la cáscara de huevo
Los resultados obtenidos del análisis de la composición química de la muestra de cáscaras de huevo se presentan en la Tabla 1.
Tabla 1 Composición química de las cáscaras de huevo de gallina.
| Componente | Contenido (%) |
|---|---|
| Carbonato de calcio - CaCO3 | 88.93 |
| Carbonato de magnesio - MgCO3 | 0.85 |
| Fosfato cálcico - Ca3(PO4)2 | 1.81 |
| Materia orgánica | 5.81 |
| Humedad | 2.60 |
Fuente: Elaboración propia.
Granulometría de los polvos de las cáscaras de huevo
Las cáscaras de huevo fueron sometidas a molienda fina y se obtuvo polvos de cáscaras a diferente granulometría, desde la malla 20 hasta la malla 200 US STD, expresada en materia retenida, tal como se muestra en la Tabla 2.
Tabla 2 Granulometría de los polvos de cáscaras de huevo de gallina.
| Malla | Masa retenida | ||
|---|---|---|---|
| US STD | Abertura (µm) | (g) | (%) |
| 20 | 850 | 17.91 | 1.79 |
| 30 | 595 | 277.78 | 27.78 |
| 40 | 425 | 327.64 | 32.76 |
| 60 | 250 | 134.47 | 13.45 |
| 100 | 150 | 46.95 | 4.70 |
| 140 | 106 | 36.73 | 3.67 |
| 200 | 75 | 113.01 | 11.30 |
| Fondo del tamizado | 45.51 | 4.55 | |
| Total | 1000.00 | 100.00 | |
Fuente: Elaboración propia.
Rendimiento de la obtención del citrato de calcio
El rendimiento o cantidad de citrato de calcio obtenido se evaluó considerando tres aspectos: granulometría, proporción de soluto cáscaras de huevo molidas y tiempo de reacción. Cabe destacar que el contenido promedio de ácido cítrico en el limón fue del 5%. En la experimentación, se utilizaron diferentes proporciones en porcentaje peso a peso (% p/p) con el fin de maximizar el rendimiento.
Para determinar el rendimiento en función de la granulometría, se realizaron siete tratamientos (M) para la extracción del citrato de calcio de las cáscaras de huevo molidas con tamaños de mallas 20, 30, 40, 60, 100, 140 y 200, como se muestra en la Tabla 3. La proporción inicial de cáscaras de huevo molidas y zumo de limón fue del 20% p/p y el tiempo de reacción química fue de 4 h.
Tabla 3 Proporciones de soluto después de ocurrida la reacción química.
| Tratamiento | Malla US STD | Proporción final del soluto (% p/p) | Diferencia (%) |
|---|---|---|---|
| M 1 | 20 | 23.88 | 3.88 |
| M 2 | 30 | 23.86 | 3.86 |
| M 3 | 40 | 23.78 | 3.78 |
| M 4 | 60 | 23.76 | 3.76 |
| M 5 | 100 | 23.68 | 3.68 |
| M 6 | 140 | 23.46 | 3.46 |
| M 7 | 200 | 23.44 | 3.44 |
Fuente: Elaboración propia.
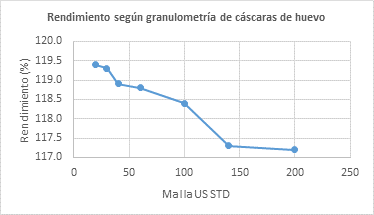
El comportamiento del rendimiento del proceso de lixiviación a diferentes mallas se muestra en la Figura 2.
Para determinar el rendimiento en función de las proporciones de soluto, se realizaron ocho tratamientos (S) con diferentes proporciones de cáscaras de huevo molidas en zumo de limón, como se muestra en la Tabla 4, con un tamaño de malla 30 y 4 h de tratamiento.
Tabla 4 Comparación de las proporciones de soluto inicial y final.
| Tratamiento | Proporción de soluto (% p/p) | Cantidad (g) | |||
|---|---|---|---|---|---|
| Inicial | Final | Producto | Residuo sólido | Membrana | |
| S1 | 5 | 8.56 | 5.24 | 1.90 | 1.42 |
| S2 | 10 | 14.78 | 8.14 | 5.22 | 1.42 |
| S3 | 15 | 19.22 | 6.34 | 11.02 | 1.86 |
| S4 | 20 | 24.32 | 5.54 | 17.42 | 1.36 |
| S5 | 25 | 28.38 | 4.50 | 22.52 | 1.36 |
| S6 | 30 | 34.74 | 5.44 | 28.26 | 1.04 |
| S7 | 35 | 38.50 | 4.14 | 33.28 | 1.08 |
| S8 | 40 | 42.94 | 3.58 | 38.30 | 1.06 |
Fuente: Elaboración propia.
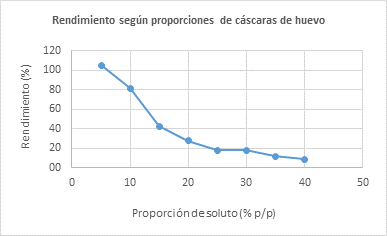
Los mejores resultados se obtuvieron en las soluciones con las menores proporciones de soluto, es decir 5%, 10% y 15% p/p. En la Figura 3, se observa un punto de inflexión a partir del 20% de cáscaras de huevo molidas, donde el rendimiento comienza a disminuir.
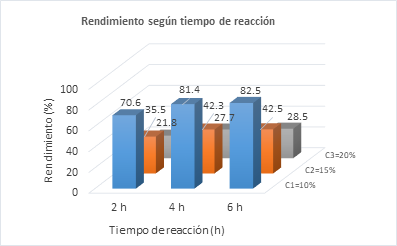
Finalmente, el rendimiento en función del tiempo de reacción y proporciones de soluto se evaluó en nueve tratamientos (T). Se trabajó con proporciones de cáscaras de huevo molidas de 10%, 15% y 20% p/p y tiempos de reacción de 2, 4 y 6 horas, como se muestra en la Figura 4.
Contenido de calcio en el producto final
Una vez obtenido el citrato de calcio, se procedió a evaluar el contenido de calcio de los diferentes tratamientos utilizando el espectrofotómetro de fluorescencia. Los resultados mostraron variaciones en la concentración de calcio en todos los casos, las cuales se detallan en la Tabla 5, correspondientes a proporciones de soluto de 10%, 15% y 20%, y a tiempos de reacción de 2, 4 y 6 horas.
Tabla 5 Rendimiento según proporciones de cáscaras de huevo molidas.
| Tratamiento | Proporción de soluto (% p/p) | Tiempo de reacción (h) | Contenido de calcio (%) |
|---|---|---|---|
| T1 | 10 | 2 | 20.65 |
| T2 | 10 | 4 | 20.80 |
| T3 | 10 | 6 | 20.83 |
| T4 | 15 | 2 | 20.02 |
| T5 | 15 | 4 | 20.36 |
| T6 | 15 | 6 | 20.38 |
| T7 | 20 | 2 | 19.42 |
| T8 | 20 | 4 | 19.68 |
| T9 | 20 | 6 | 19.72 |
Fuente: Elaboración propia.
Los contenidos promedio de calcio para las proporciones de 10%, 15% y 20% p/p fueron de 20.76%, 20.25% y 19.61%, respectivamente (Figura 5). En comparación, el contenido de calcio en los suplementos comerciales en complejos de citrato es del 21%.
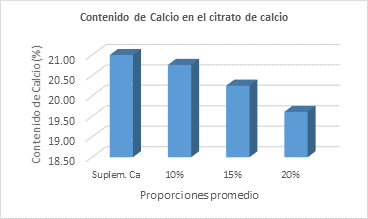
Fuente: Elaboración propia.
Figura 5 Contenido de calcio en proporciones promedio de cáscaras de huevo y suplementos de calcio.
Contenido de minerales en las cáscaras de huevo, producto final y residuos
El contenido de metales que se muestra en la Tabla 6 corresponde a las cáscaras de huevo de gallina usados en la experimentación, al producto obtenido en base seca del tratamiento T3 y a los residuos, tanto sólidos como líquidos. Este contenido se determinó mediante el análisis de metales por ICP-MS.
Tabla 6 Contenido mineral de las cáscaras de huevo, producto final y residuos en partes por millón (ppm).
| Mineral | Cáscaras de huevo | Producto final (T3) | Residuos | ||
|---|---|---|---|---|---|
| Experimental | Bibliografía* | Líquido | Sólido | ||
| Calcio (Ca) | 355 700.0 | 443 450.00 | 208 300.0 | 21 700.0 | 24 670.0 |
| Magnesio (Mg) | 4 500.0 | 3 468.20 | 1 036.0 | 14 700.0 | 3 542.0 |
| Sodio (Na) | 2 700.0 | 467.76 | 2 173.0 | 8 726.0 | 1 830.0 |
| Potasio (K) | 3 700.0 | 403.93 | 3 803.0 | 125 700.0 | 6 732.0 |
| Fósforo (P) | 1 000.0 | 1 093.40 | 353.8 | 7 667.0 | 753.5 |
| Hierro (Fe) | 51.7 | - | 32.4 | 51.9 | 45.9 |
| Estroncio (Sr) | 26.0 | - | 34.7 | 6.4 | 22.9 |
| Boro (B) | 20.8 | - | 13.8 | 41.5 | 19.6 |
| Bario (Ba) | 43.7 | - | 9.9 | 16.5 | 37.7 |
| Manganeso (Mn) | 7.5 | 0.06 | 7.2 | - | 7.7 |
| Aluminio (Al) | 21.1 | - | 8.4 | 23.0 | 17.1 |
| Estaño (Sn) | 62.4 | - | 5.1 | 103.0 | 5.4 |
| Cobre (Cu) | 4.8 | - | 3.2 | 12.8 | 3.9 |
| Zinc (Zn) | 8.2 | - | 3.2 | 46.1 | 10.0 |
| Cromo (Cr) | 1.7 | - | 1.0 | 5.8 | 1.5 |
| Selenio (Se) | 1.6 | - | 1.2 | 31.6 | 0.8 |
| Níquel (Ni) | 0.9 | 0.15 | 1.0 | 2.3 | 0.9 |
| Silicio (Si) | 2.2 | - | 0.1 | 95.3 | 2.7 |
| Vanadio (V) | 1.1 | 0.38 | 1.4 | - | 0.9 |
| Litio (Li) | 1.0 | - | 0.2 | 3.2 | 0.7 |
| Cobalto (Co) | 0.4 | 0.19 | 0.4 | 0.8 | 0.4 |
| Plata (Ag) | - | - | 0.6 | 5.7 | - |
| Bismuto (Bi) | 0.4 | - | - | 0.7 | - |
| Molibdeno (Mo) | 0.4 | - | - | - | 0.4 |
| Plomo (Pb) | 1.2 | - | - | 7.5 | 0.6 |
| Berilio (Be) | - | 0.03 | - | - | - |
Nota: (-) Por debajo de los límites de detección. (*) The Influence of Hen Aging on Eggshell Ultrastructure and Shell Mineral Components (Park y Sohn, 2018).
Fuente: Elaboración propia.
Análisis microbiológico del citrato de calcio obtenido
Mediante el análisis microbiológico del producto final (citrato de calcio), se evaluaron parámetros microbiológicos constituidos por el recuento de mohos (hongos), levaduras, aerobios en placa (mesófilos) y la presencia de salmonela. En todos los casos, se obtuvieron valores del recuento microbiano en unidades formadoras de colonias (UFC) inferiores a los límites de detección especificados en la norma, es decir, <10 UFC/g, excepto en el caso de la salmonela, cuya ausencia fue total.
Análisis sensorial del citrato de calcio obtenido
Luego de haber obtenido los puntajes numéricos de cada atributo de los panelistas, se aplicó el análisis de varianza (ANOVA). Para observar el grado de aceptación de los panelistas, se determinaron la media y la desviación estándar. Los mejores resultados se obtuvieron en los atributos de textura, seguidos del sabor, color y olor, tal como se muestra en la Tabla 7. Para verificar la diferencia entre los tratamientos, se determinó el estadístico F, que arrojó un valor de F (0.414) para todos los atributos, menor que el valor crítico de F (3.354).
Tabla 7 Resultados del análisis de varianza de cada atributo evaluado.
| Atributo | Suma de cuadrados | Grados de libertad | Promedio de los cuadrados | F | Probabilidad | Valor crítico de F |
|---|---|---|---|---|---|---|
| Olor | 0.267 | 2 | 0.133 | 0.414 | 0.665 | 3.354 |
| Color | 0.245 | 2 | 0.133 | 0.414 | 0.665 | 3.354 |
| Sabor | 0.222 | 2 | 0.133 | 0.414 | 0.665 | 3.354 |
| Textura | 0.224 | 2 | 0.133 | 0.414 | 0.665 | 3.354 |
Fuente: Elaboración propia.
Análisis estadístico
Se realizó el análisis de varianza ANOVA (Tabla 8) para evaluar la hipótesis alterna planteada (H1) y determinar si existe una diferencia estadísticamente significativa entre las mediciones de nueve tratamientos (desde T1 hasta T9), cada uno con dos repeticiones. Se obtuvo una media de 48.017 y una desviación estándar de 23.278, con un nivel de significancia del 0.05 de probabilidad. Los valores de F calculados (41.711) fueron superiores a los valores críticos de F (4.256).
Tabla 8 Resultado del análisis de varianza del rendimiento en los nueve tratamientos.
| Origen de las variaciones | Suma de cuadrados | Grados de libertad | Promedio de los cuadrados | F | Probabilidad | Valor crítico de F |
|---|---|---|---|---|---|---|
| Muestra | 284.29 | 2 | 142.145 | 41.711 | 1.34E-09 | 4.256 |
| Columnas | 8896.46 | 2 | 4448.232 | 13040.418 | 2.63E-16 | 4.256 |
| Interacción | 27.56 | 4 | 6.889 | 20.196 | 1.61E-04 | 3.633 |
| Dentro del grupo | 3.07 | 9 | 0.341 | |||
| Total | 9211.38 | 17 |
Fuente: Elaboración propia.
Asimismo, se utilizó el programa SPSS versión 27 para realizar la prueba de Tukey con la finalidad de comparar los tratamientos y los grupos. Se obtuvieron las medias para los grupos en los subconjuntos homogéneos, como se muestra en la Tabla 9, con un término de error correspondiente a la media cuadrática (Error) de 0.356, un tamaño de muestra de media armónica de 6 y un nivel de significancia (α) de 0.05
DISCUSIÓN
Composición química de las cáscaras de huevo
De acuerdo con los resultados obtenidos del análisis de la composición química de las cáscaras de huevo, se obtuvo carbonato de calcio en una proporción del 88.93%, es decir, se trata del componente de mayor concentración. Este resultado permitió reafirmar que la cáscara de huevo de gallina es un material que contiene cantidades importantes de calcio. No obstante, este resultado difiere del obtenido por Nys et al. (2004), quienes reportaron una composición del 95%, y por Neunzehn et al. (2015), cuyo reporte fue de 93.6%. Estas diferencias, que se expresan en una proporción del 6.07% y 4.67%, respectivamente, pueden atribuirse a la mezcla de cáscaras de huevo de gallina utilizadas en este estudio, las cuales poseen distintas características en cuanto a la pigmentación, el grosor y los sistemas de crianza de las gallinas, ya que se trabajó con material de descarte.
El carbonato de magnesio se encontró en una proporción de 0.85% y el fosfato tricálcico en una proporción de 1.81%. El contenido de carbonato de magnesio mostró un valor superior respecto al encontrado por Fernández y Arias (2000) y Pérez et al. (2018), mientras que el fosfato tricálcico mostró un valor ligeramente superior. El contenido de materia orgánica fue de 5.81% y el de humedad fue de 2.6%. Ambos valores son ligeramente superiores, probablemente debido a la mezcla de cáscaras de huevo de gallina utilizada.
Granulometría de los polvos de las cáscaras de huevo
El tamaño de grano fue determinante para realizar la extracción del citrato de calcio por la estructura que posee. Algunas partes de las cáscaras son muy fuertes y concisas, mientras que otras son más débiles; la estructura varía o se degrada con la edad de la gallina (Park y Sohn, 2018). Se obtuvo mayor cantidad de masa retenida en la malla 40, con un 32.76%, y en la malla 30, con un 27.78%. La diferencia en el tamaño de los polvos obtenidos por Pérez et al. (2018) puede atribuirse al tiempo de molienda aplicado, a los equipos utilizados y, sobre todo, a los fines investigativos, más que al tipo de estructura de las cáscaras de huevo de gallina.
Rendimiento de la obtención del citrato de calcio
Debido a la finura de los polvos de las cáscaras de huevo, sobre todo de las mallas 100, 140 y 200, el producto se confunde con los residuos sólidos no reaccionantes, lo que dificultó su separación. Por ello, el rendimiento se evaluó en función de la proporción de sólidos formados tras la reacción química y se obtuvieron proporciones de soluto finales superiores al 20% p/p en todos los casos.
Existe una ligera diferencia en la formación del soluto al final de la reacción. Las mallas 20 y 30 registraron los mayores rendimientos, mientras que las mallas 100, 140 y 200 tuvieron menores rendimientos (Figura 2). Esto podría deberse a la escasa superficie de reacción por tratarse de un material muy pulverulento, lo que impide la libre migración de los átomos y provoca que la solución se sature demasiado. Esto quiere decir que el tamaño de partícula es fundamental, por lo que debe tenerse en cuenta el tamaño óptimo para evitar las sobresaturaciones y permitir el libre desarrollo de la reacción química.
Según las proporciones de soluto, los mejores resultados se obtuvieron en las soluciones con concentraciones más bajas, es decir, al 5%, 10% y 15% p/p, mientras que al 20% p/p se observaron cambios mínimos. La desventaja de usar proporciones menores es que conlleva a un mayor gasto en zumo de limón, lo que evidencia la baja rentabilidad de la obtención de citrato en proporciones muy bajas. Por ello, las proporciones al 10%, 15% y 20% p/p se consideran óptimas. Se observa también una cantidad significativa de membrana, atribuible al uso íntegro de las cáscaras de huevo, es decir, sin previa separación de las membranas. Estas constituyen el componente orgánico que representa entre el 3% y el 3.5% del peso de las cáscaras del huevo.
Según el tiempo de reacción y proporciones de soluto, los mejores resultados del producto obtenido (citrato de calcio) correspondieron a los tratamientos T2 y T3, con rendimientos del 81.4% y 82.5% en 4 y 6 horas de reacción, respectivamente. Pasado ese tiempo, la producción aumentó ligeramente, por lo que se considera como tiempo óptimo las 6 horas de reacción química en el tratamiento T3. Si la reacción se prolonga más tiempo, existe el riesgo de contaminación por tratarse con materia orgánica.
Contenido de calcio en el producto final
A partir de un contenido inicial de calcio del 35.57% en las cáscaras de huevo, los resultados obtenidos muestran rendimientos de 58.05%, 58.48% y 58.56% en los tratamientos T1, T2 y T3; 56.28%, 57.24% y 57.30% en los tratamientos T4, T5 y T6; y 54.60%, 55.33% y 55.44% en los tratamientos T7, T8 y T9. Los mejores resultados se observaron en el tratamiento T3; sin embargo, es importante resaltar que la variación en T2 fue mínima y su tiempo de reacción también fue menor. Ambos pueden considerarse los mejores tratamientos, ya que evitan el riesgo de contaminación de la sustancia por tiempos de reacción prolongados. En consecuencia, el tiempo óptimo de reacción se establece entre 4 y 6 horas.
Los contenidos promedio de calcio obtenidos en las proporciones de 10%, 15% y 20% p/p fueron de 20.76%, 20.25% y 19.61%, respectivamente. Se observa una ligera diferencia entre los tratamientos estudiados (Figura 5), con el mayor contenido de calcio registrado en la proporción del 10% p/p. Al comparar estos resultados con los suplementos de citrato de calcio comerciales, cuyo contenido de calcio es del 21%, se encontró que no existe mucha diferencia, pues los valores obtenidos son muy similares, sobre todo en los que tratamientos que corresponden al 10% p/p. Los valores obtenidos fueron de 20.65% en T1, 20.80% en T2 y 20.83% en T3, con diferencias de 1.66%, 0.95% y 0.81%, respectivamente, en relación con los suplementos comerciales. Esto indica que una muestra de 5 g de citrato de calcio, correspondiente a la dosis diaria para un adulto, contiene 1032.5 mg de Ca en T1, 1040.0 mg en T2 1041.5 mg y en T3. Todos estos valores se encuentran dentro de los límites recomendables de 700, 1000 o 1200 mg por día, según las etapas de vida (Instituto Nacional de Artritis y Enfermedades Musculoesqueléticas y de la Piel [NIAMS, por sus siglas en inglés], 2023).
Al comparar el contenido de calcio (20.83%) y el de magnesio (1.036%) del citrato de calcio obtenido con los hallazgos de Vásquez y Glorio (2007), no existe mucha diferencia. En su estudio, los autores reportaron un contenido de calcio elemental del 20.5% y un contenido de magnesio del 0.0927% en el citrato de calcio y magnesio derivado de cáscaras de choro (Aulacomya ater Molina). Sin embargo, al compararlos con los resultados presentados por Rodríguez et al. (2014), se evidencia una gran diferencia, ya que estos encontraron un contenido de 10.47% de calcio y 4.67% de magnesio en forma de citrato de calcio y magnesio. Esta diferencia se debe a la materia prima utilizada: mientras que las cáscaras de huevo contienen calcita con un 88.93% de carbonato de calcio y un 0.85% de carbonato de magnesio, la dolomita posee carbonato doble de calcio y magnesio [CaMg(CO3)2], con un 30.41% de óxido de calcio (CaO) y un 21.86% de óxido de magnesio (MgO), además de otros compuestos que influyen en el contenido final de calcio.
Además, al comparar el contenido de calcio (20.83%) del citrato de calcio obtenido y el resultado obtenido por Rosas et al. (2018), quienes reportaron un contenido de calcio promedio del 9.06% en la pasta tipo fettuccine enriquecida con cascarón de huevo, se observó una diferencia aproximada del 50%. Por su parte, Pérez et al. (2018) reportaron un contenido de calcio del 0.232% (232 mg/100g) en el yogurt funcional fortificado, un valor significativamente inferior respecto al obtenido en la presente investigación. Las diferencias en el contenido de calcio podrían deberse a la adición directa de las cáscaras de huevo en polvo sin tratamiento previo, como es el caso de la obtención del citrato de calcio, lo que constituye la base de los suplementos en forma de citratos.
Contenido de minerales de las cáscaras de huevo, producto final y residuos
Además del Ca y Mg, se encontraron los metales Na, K y P en cantidades ligeramente inferiores a los contenidos de las cáscaras de huevo, pero muy próximas a los obtenidos por Vásquez y Glorio (2007). Cabe resaltar que el contenido de Ca2+ disminuye con la edad de la gallina, mientras que el Na+ y K+ tienden a aumentar (Park y Sohn, 2018). Asimismo, se detectaron en menor proporción los metales Fe, Sr, B, Ba, Mn, Al, Sn, Cu y Zn, con valores inferiores a los obtenidos por Rodríguez et al. (2014), quienes reportaron contenidos de SiO2, Al2O3 y Fe2O3. Se detectó la presencia de Cr, Se, Ni, Si, V, Li, Co y Ag en cantidades muy reducidas, similares a las halladas en las cáscaras de huevo según Park y Sohn (2018). No se hallaron rastros de As, Be, Cd, Hg, Ti ni Tl en el producto final, tampoco en las cáscaras de huevo, ni en los residuos, a diferencia de Rodríguez et al. (2014), quienes sí reportaron presencia de Cd, Pb, Hg y As. Finalmente, se confirmó la presencia de Bi, Mo y Pb en las cáscaras de huevo, en concordancia con los hallazgos de Milbradt et al. (2015), quienes no detectaron Cd ni Pb en muestras de cáscaras huevo, al igual que Dos Santos et al. (2010), quienes tampoco identificaron Cd, Pb o Hg en sus análisis.
Las cáscaras de huevo presentan ventajas sobre otras fuentes de calcio debido a la ausencia de elementos perjudiciales para la salud. Este material de desecho tiene el potencial de ser aprovechado en diversas aplicaciones importantes para la industria y para la humanidad. En los residuos sólidos y líquidos, se observó una reducción en la concentración de todos los elementos respecto a su contenido inicial en las cáscaras de huevo; no obstante, lo valores obtenidos varían de acuerdo al material y proporciones utilizadas. En términos generales, el contenido de magnesio, sodio, potasio y fósforo es mínimo, por lo que un ligero incremento en la dosis de ingesta no superaría los límites permisibles. Además, el contenido de níquel, molibdeno, aluminio, boro, arsénico y cadmio está muy por debajo de esos límites permisibles.
Análisis microbiológico del citrato de calcio obtenido
El análisis microbiológico de todas las muestras reveló que los valores del recuento microbiano se mantuvieron por debajo de los límites de detección (<10 UFC/g), además de la ausencia total de salmonella. Esto indica que el citrato de calcio obtenido es apto para el consumo humano y su uso en la industria alimentaria.
Análisis sensorial del citrato de calcio obtenido
El análisis sensorial para determinar el grado de aceptación de los panelistas, basado en atributos como textura, sabor, color y olor, demuestra que no hubo diferencias estadísticamente significativas en el tratamiento T3, con un nivel de confiabilidad del 95%. Dado que este tratamiento presentó los mejores rendimientos, se observa que el producto obtenido es agradable al paladar.
Análisis estadístico
De acuerdo al análisis ANOVA, los valores de p fueron inferiores a 0.05 y los valores del estadístico F calculado (41.711) fueron superiores a los valores críticos de F (4.256), por lo que se acepta la hipótesis alterna (H1) y se evidencia una diferencia estadísticamente significativa en el rendimiento de la obtención del producto final. Asimismo, utilizando la prueba de Tukey, se obtuvo las medias para los grupos en los subconjuntos homogéneos (Tabla 9), con un término de error que es la media cuadrática (error) de 0.356, un tamaño de la muestra de la media armónica de 6 y un nivel de significación (α) de 0.05. La mayor diferencia se obtuvo en los tratamientos T3 y T7; se observó que el tratamiento T3 fue el más eficiente, con un rendimiento del 82.5%. Este valor fue aceptado como el mejor rendimiento para una concentración del 10% de cáscara de huevo en zumo de limón y un tiempo de reacción de 6 horas. Dicho tratamiento tuvo un contenido de calcio del 20.83% en el producto final, lo que representó un rendimiento del 58.56% respecto al contenido de calcio de las cáscaras de huevo.
CONCLUSIONES
Las cáscaras de huevo de gallina contienen un 88.93% de carbonato de calcio, lo que las reafirma como una sustancia natural y una fuente importante de este mineral. El 11.07% restante corresponde a carbonato de magnesio, fosfato de calcio, materia orgánica y humedad. Al someter las cáscaras de huevo a un proceso de lixiviación con ácido cítrico proveniente del zumo de limón, se obtuvo citrato de calcio con un rendimiento del 82.5% en el tratamiento T3 y un contenido de calcio del 20.83% en el producto final. Este valor corresponde a un rendimiento del 58.56% respecto a su contenido inicial, utilizando una concentración del 10% p/p de cáscaras de huevo y zumo de limón, es decir, el tratamiento T3 es el más adecuado para obtener citrato de calcio. Por lo tanto, se concluye que una menor proporción de cáscaras de huevo en zumo de limón, favorece una mayor extracción de calcio en forma de citrato, mientras que una mayor concentración de cáscaras de huevo permite obtener una mayor cantidad de calcio extraído en esta forma.
Asimismo, se concluye que existe una interacción significativa entre el contenido de las cáscaras de huevo y la concentración del ácido cítrico presente en el zumo de limón, lo que influye significativamente en la eficiencia de las distintas concentraciones evaluadas.
Se concluye también que tanto la materia prima como los métodos de extracción influyen en el contenido de calcio del producto final, ya sea en el citrato de calcio o en el producto alimenticio elaborado. Los residuos sólidos y líquidos resultantes del proceso aún contienen minerales que pueden aprovecharse en la producción de alimentos balanceados, fertilizantes y otros productos. Además, este proceso contribuye a reducir los índices de contaminación provenientes de la industria alimentaria y de los hogares, dándoles un nuevo uso.
Finalmente, debido a las limitaciones socioeconómicas, no se contó con equipos e instrumentos de medición de última generación. No obstante, la implementación de estos recursos y el establecimiento de convenios con especialistas del sector sería beneficioso.











 texto en
texto en