INTRODUCCIÓN
La eventración gigante con pérdida de dominio es una patología que afecta la calidad de vida de los pacientes, tiene altos índices de morbimortalidad y recidiva. Los defectos crónicos de la pared van creciendo y alterando de forma progresiva la fisiología de la pared abdominal, haciendo difícil que el contenido del saco sea devuelto a la cavidad abdominal. En términos operacionales una hernia con pérdida de dominio se cataloga como aquella que tiene un defecto de 10cm o cuyo volumen representa por lo menos el 25% del volumen de la cavidad abdominal 1. La reparación de estos defectos puede conllevar a varios problemas fisiopatológicos graves, como el síndrome compartimental abdominal con compromiso respiratorio agudo secundario al aumento súbito de la presión intraabdominal. El manejo de estas hernias continúa siendo un reto para el cirujano sin embargo una correcta planificación prequirúrgica mejorará las condiciones para la cirugía. 2,7,8
Dentro de los efectos sistémicos que producen este tipo de hernias tenemos al compromiso ventilatorio por disociación entre la presión intratorácica e intraabdominal, condición que altera la forma normal del diafragma. Disfunción para la evacuación por alteración de la musculatura de la pared abdominal que pierde su capacidad de incrementar la presión intraabdominal, además por un efecto obstructivo cuando las asas se encuentran incluidas en el saco herniario. Dificultad para la micción por daño del músculo detrusor de la vejiga. 3
En cuanto a los efectos locales: Los músculos del complejo lateral sufren retracción y acortamiento permanente, generando su disfunción secundaria a pérdida de la capacidad para elevar la presión intraabdominal. El mesenterio y las asas intestinales por la constante irritación mecánica sufren inflamación crónica, siendo más severa en las hernias incisionales, por la fibrosis de sus bordes. El resultado de la inflamación crónica es la formación de bridas y adherencias. En cambio, la piel y el tejido subcutáneo tienden a atrofiarse por la compresión y distensión severa, ocasionando úlceras tróficas. 3
En 1940, Goñi Moreno publicó por primera vez la realización del neumoperitoneo progresivo preoperatorio para el tratamiento de las grandes hernias 5. Desde entonces, su técnica se ha ido modificando y mejorando poco a poco y es empleada en todo el mundo con buenos resultados 4.
La mayoría de los estudios describen el uso de neumoperitoneo progresivo para la reparación de las eventraciones gigantes, sin embargo, esta técnica también puede usarse para resolver las hernias inguinales y umbilicales gigantes, con buenos resultados 9.
Otra alternativa es el uso de la toxina botulínica tipo A, que produce parálisis flácida de la musculatura de la pared abdominal permitiendo su acondicionamiento previo a la realización de una plastia. Disminuye la retracción lateral de la musculatura oblicua sobre la línea media garantizando el cierre del defecto herniario sin debilitar su conformación anatómica, favoreciendo la evolución postoperatoria 11.
Durante el acto quirúrgico, la separación de componentes es una técnica que se introdujo para la reconstrucción de la pared abdominal en caso de hernias grandes y complejas. Tiene como objetivo facilitar el cierre del defecto herniario sin producir tensión. Puede ser una separación anterior cuando se realiza un corte en la aponeurosis del músculo oblicuo mayor y se accede al plano entre éste y el músculo oblicuo menor; o posterior con liberación del músculo transverso y acceso al espacio entre éste y la fascia transversalis. Además, existen las técnicas endoscópicas que cumplen con los mismos principios pero que tienen las ventajas de ser mínimamente invasivas 12. Es aconsejable utilizar material protésico en todos los casos y evitar el cierre con tensión 3.
REPORTE DEL CASO
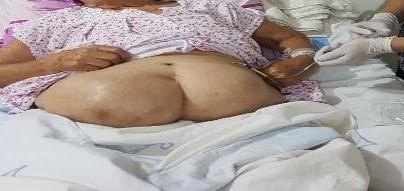
Mujer de 85 años, quien fue intervenida en dos oportunidades, hace aproximadamente 30 años de histerectomía por prolapso uterino y de laparotomía exploratoria por peritonitis; encontrándose 1 gasa quirúrgica en esta última, posteriormente presenta masa en cicatriz operatoria que fue aumentando de tamaño, asociándose a dolor tipo cólico, llenura precoz, sensación de abultamiento en pared abdominal, con implicancias negativas en su calidad de vida.
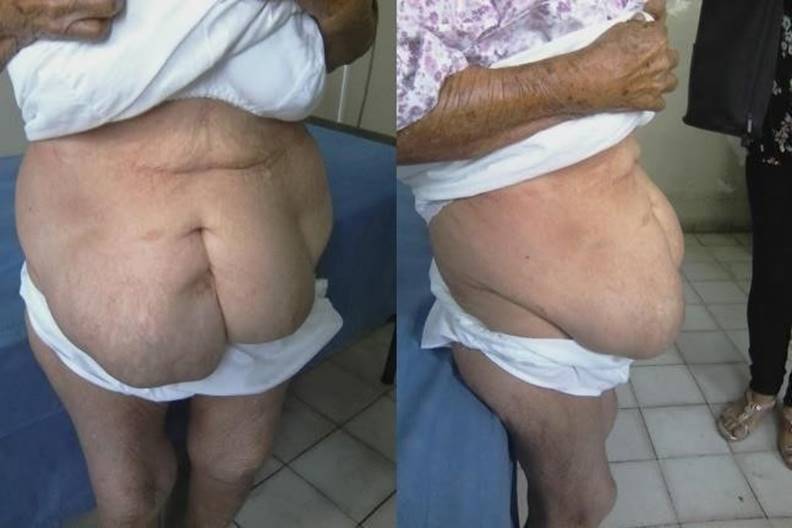
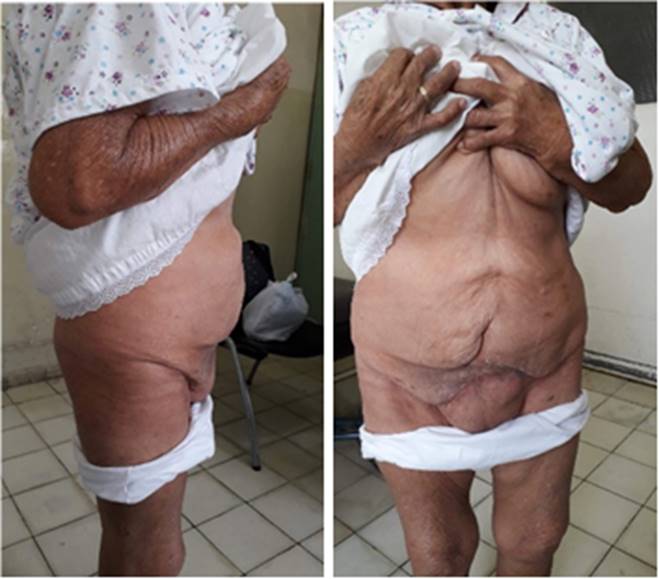
A la exploración física se observa dos masas laterales a la cicatriz mediana infraumbilical (Figura 1), de 30x20 cm y 20x15cm en el lado derecho e izquierdo respectivamente. Contenido blando, con mínima reducción, sin cambios de coloración en piel sumado a la presencia de ruidos hidroaéreos en sacos herniarios. Se palpa en el lado derecho un defecto herniario de 7 cm y en el izquierdo de 5 cm asociado a dolor leve a la movilización del contenido, sin resistencia muscular.
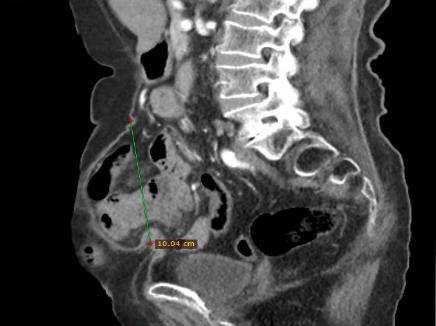
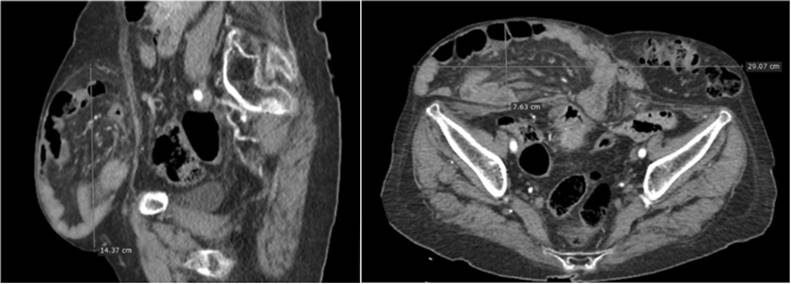
Los exámenes de laboratorio prequirúrgicos fueron normales. La tomografía de abdomen mostró defecto en la pared abdominal anterior de 10.04 cm (Figura 2), con protrusión de asas de intestino delgado, grueso y epiplón dentro de un saco herniario cuyo diámetro mayor fue de 29.07cm (Figura 3) además de escaso contenido de asas de intestino delgado dentro de cavidad abdominal. Por las características clínicas y tomográficas de la paciente se cataloga como una hernia con pérdida de dominio; por lo que, se decide realizar una intervención terapéutica asociada a neumoperitoneo progresivo preoperatorio.
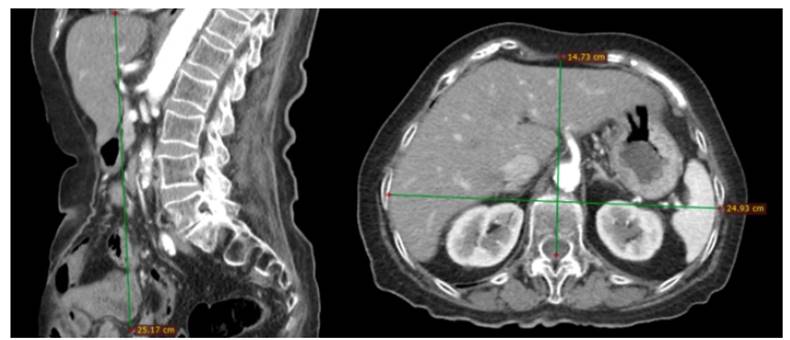
Se procede a calcular el porcentaje de volumen herniario de la paciente en estudio, en relación al volumen abdominal, para lo cual debemos considerar al saco herniario y a la cavidad abdominal como elipsoides, tomando en cuenta sus tres dimensiones (Figura 3 y Figura 4) que para este fin las denominaremos con las letras a, b y c, aplicando la siguiente fórmula, según Tanaka et. al. 6:
Tabla 1 Porcentaje de volumen herniario.
| Volumen | Cálculo | Resultado |
|---|---|---|
| Hernia | 0.52 x 14.37 x 29.07 x 7.63 | 1657.41 |
| Cavidad | 0.52 x 25.17 x 14.73 x 24.93 | 4806.31 |
Porcentaje de volumen herniario = (1657.41/4806.31) x 100 = 34.5%
Como se puede visualizar en el cuadro, obtenemos un volumen de hernia de 1657.41cm3 y de cavidad abdominal en 4806.31cm3, por lo que porcentaje de volumen herniario resulta en 34.5%. Tanaka et al 6 proponen que un índice mayor a 25% en esta medición es un predictor de necesidad de neumoperitoneo.
Se colocó un catéter venoso central en el hipocondrio izquierdo, previa aplicación de 1 gr endovenoso de cefazolina, a nivel de la línea medio clavicular, a dos centímetros del reborde costal, dirigido por ultrasonido bajo anestesia local. Es dada de alta con paracetamol 500mg condicional al dolor. Se cita a la paciente cada tres días por dos meses aplicándose inicialmente 500 cc de aire hasta llegar de manera progresiva a 1500cc/vez (Figura 5), durante las sesiones la paciente presentó episodios de disnea remitente a oxigenoterapia de apoyo. Estas sesiones se realizaron en el tópico de emergencia bajo monitoreo constante de sus funciones vitales y oximetría.
Un mes después de iniciada la aplicación del neumoperitoneo se programa una TEM abdominal para observar los cambios que se obtuvo con la técnica. Encontrándose los siguientes resultados (Figura 6, Figura 7).
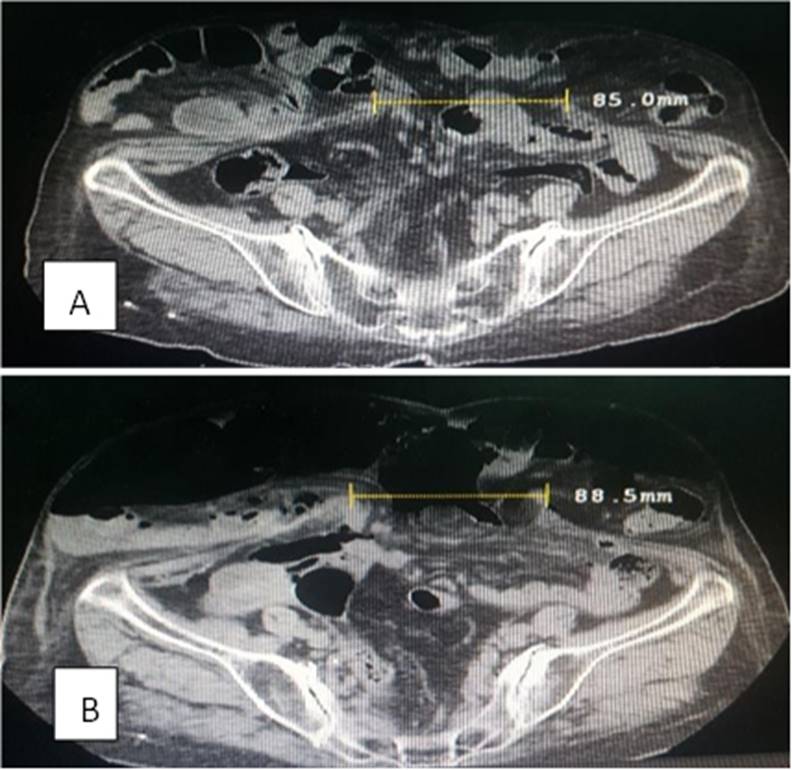
Figura 6 TEM abdominal. A. Corte transversal en TEM abdominal que muestra el diámetro máximo (85.0mm) del defecto herniario en reposo antes de aplicar neumoperitoneo. B. Corte transversal en TEM abdominal que muestra el diámetro máximo (88.5mm) del defecto herniario en reposo después de 1 mes de aplicar neumoperitoneo, se aprecia a simple vista el retorno de los intestinos a la cavidad abdominal y una disminución del volumen visceral.
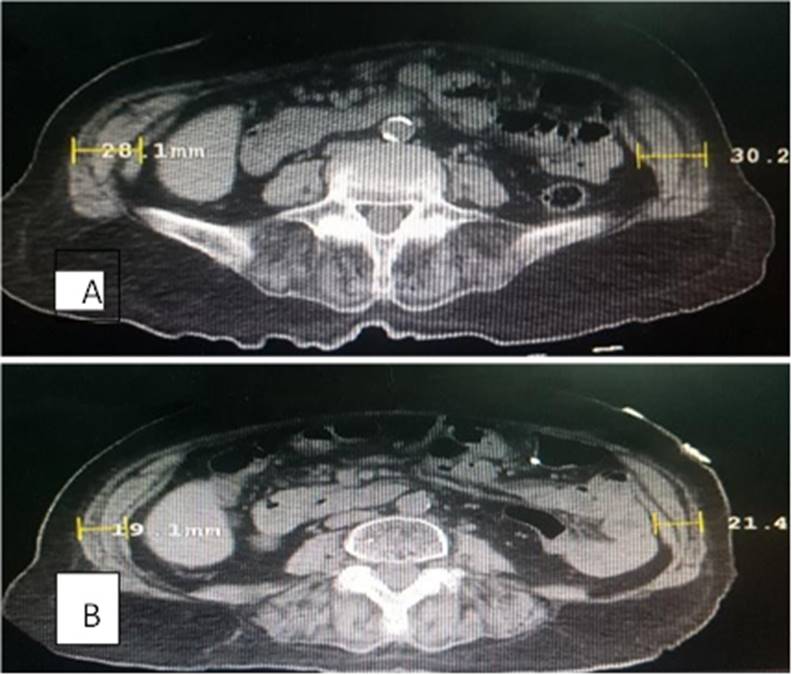
Figura 7 TEM abdominal. A. Espesor de la pared muscular bilateral en reposo antes de aplicar neumoperitoneo, el lado derecho de 28.1mm y el lado izquierdo de 30.2mm. B. Un mes después se observa una disminución bilateral del espesor de la pared, el lado derecho de 19.1mm y el lado izquierdo de 21.4 mm además de una aproximación de esta musculatura a la línea media.
Asimismo, durante el período de aplicación de neumoperitoneo, se realizó rehabilitación respiratoria con inspirómetro de incentivo.
Fue sometida a 17 sesiones de neumoperitoneo, recibiendo un total aproximado de 22 litros de aire ambiental.
Posteriormente, se programó una intervención quirúrgica que consistió en una plastia, con malla de polipropileno en espacio pre aponeurótico. Para evitar el cierre con tensión y sus complicaciones como la insuficiencia respiratoria o la hipertensión intraabdominal, se consideraron alternativas como separación de componentes anterior o técnica de Ramírez.
Paciente fue hospitalizada 5 días antes de intervención, durante su estancia recibió sus últimas 3 sesiones de neumoperitoneo.
En la intervención quirúrgica (8 semanas de iniciado el neumoperitoneo) se realiza una incisión mediana infraumbilical para individualización de sacos herniarios hasta su base. En la apertura de los mismos, se logra evidenciar que están contenidos principalmente de aire, se procede a incorporar vísceras a la cavidad abdominal sin mayores inconvenientes, previa lisis de sus adherencias a la pared del saco. Posteriormente se unifican los defectos herniarios. Debido a tensión en el cierre de estos defectos, se realiza la separación de componente anterior (Figura 8A), con cierre posterior de aponeurosis, en el plano creado entre músculo oblicuo externo e interno y además se coloca la malla (Figura 8B), con drenaje tubular en espacio subcutáneo. El procedimiento no tuvo complicaciones.
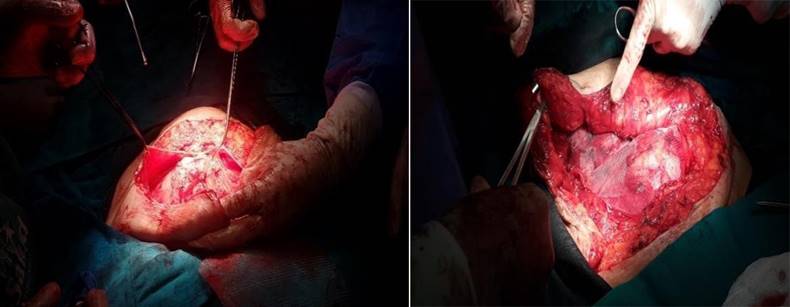
Figura 8 Intervención quirúrgica. A. Separación de componentes técnica de Ramírez. B. Colocación de malla de polipropileno
La paciente permaneció por cuatro días hospitalizada, refiriendo leve dolor en cicatriz operatoria, tolerando dieta y sin alteraciones en funciones biológicas. Se registró producción por dren tubular entre 25-56 cc hemáticos, al alta se retira dren con producción 14cc de contenido seroso. La paciente fue citada a sus controles, refiriendo mejora progresiva que se reflejaba en la ausencia de tumoración (Figura 9), escaso dolor y mayor tolerancia a los alimentos.
En el seguimiento, que a la fecha completa los 2 años 6 meses; refiere sentirse tranquila, salvo por los dolores abdominales tipo retortijones de leve intensidad y esporádicos.
DISCUSIÓN
Las hernias gigantes con pérdida de dominio siguen el mismo patrón de tratamiento que el resto, en cuanto al uso de mallas y al concepto “libre tensión”. Sin duda, una de las patologías de más difícil manejo para el cirujano general. Este ejemplo de éxito se da por la conjunción de la colaboración pacientefamilia, capacitación permanente de equipo quirúrgico, y obviamente, por la aplicación de neumoperitoneo ambulatorio preoperatorio 2 meses antes de intervención quirúrgica. Este tiempo es prolongado en comparación con el de otras series que oscila entre 7 y 20 días 10, pero obedece a que optamos por iniciar con cantidades pequeñas (500 cc/día) e ir aumentando de forma progresiva para evitar complicaciones respiratorias en la paciente por su avanzada edad, además que dichas sesiones se llevaban a cabo cada 3 días porque vivía en una ciudad lejana. El volumen total de neumoperitoneo que se colocó fue de 22 litros, lo cual está dentro del rango presentado por otras series que van desde los 10 a 25 litros 10. Algunos optan por hospitalizar a sus pacientes para la aplicación del neumoperitoneo como en la serie de 5 pacientes de Rappoport et al 1. No consideramos necesaria la medición sistemática de la presión intrabdominal (PIA). Se constató, gracias a esta técnica, que el contenido del saco herniario fue desplazándose hacia la cavidad abdominal, disminuyó el volumen visceral y los músculos de la pared abdominal se fueron adelgazando y estirando, lo cual es compatible con estudios similares como el de López et al 4. No hubo complicaciones por la aplicación del neumoperitoneo salvo leve distrés respiratorio que se presentó el primer día de insuflación y que remitió al detener la misma. Todo ello permitió, junto con la separación anterior de componentes, el regreso de las vísceras a la cavidad abdominal y el cierre sin tensión del defecto herniario, lo cual fue vital para evitar las complicaciones postoperatorias antes mencionadas, generando un gran impacto en no sólo la estética de la pared abdominal sino además en la calidad de vida de la paciente quien ahora vive sin los retortijones a los que estaba acostumbrada, puede comer sin problemas y reinsertarse a la sociedad sin temor de ser observada o rechazada.