INTRODUCCIÓN
Eucalyptus es un árbol australiano de la familia Myrtaceae, es uno de los géneros más importantes que incluye 140 géneros y unas 3,800 especies y subespecies, distribuidas en las regiones tropicales y subtropicales. Es cultivado ampliamente en Brasil, África, Sudeste de Asia y Sur de Europa (CHAH, 2016). El aceite esencial de eucalipto (AEE) al igual que otras plantas aromáticas tienen uso funcional (Mohammadhosseini et al., 2017) y debido a ello, se ha permitido que sean componentes de muchos medicamentos patentados en forma de jarabes, pastillas, gotas nasales (Bruneton, 1995) para la congestión nasal, resfriado, enfermedad bronquial y otros problemas respiratorios (van Wyk & Wink, 2017).
Se ha demostrado que el AEE en su forma de vapor resulta tóxico para bacterias, hongos, patógenos (del suelo y postcosecha) e insectos; lo que podría resultar en su uso potencial como fumigante para laboratorios, hospitales, almacenes de granos alimenticios, etc. (Dhakad et al., 2017). Su actividad antimicrobiana se atribuye a la presencia de sus componentes 1,8-cineol, β-cimeno, D-limoneno, α-pineno, α-terpineol, entre otros (Mossa et al., 2017; González-Guiñez et al., 2016; Natividad, 2019; Kringel et al., 2017).
Existen varios métodos para la extracción de aceites esenciales, los más utilizados son la extracción por arrastre de vapor y la hidrodestilación por Clevenger; sin embargo, existen otras tecnologías emergentes como la extracción asistida por microondas, extracción con microondas libre de solventes (EMLS) y con la asistencia de ultrasonido (EMAU), que han demostrado ventajas sobre la destilación tradicional, siendo más rápido, efectivo y con un menor impacto ambiental, evitando el uso de solventes (Filly et al., 2014; Nora & Borges, 2017). Sin embargo, en las comparaciones de cantidad y tipo de compuestos químicos en aceites esenciales obtenidos por microondas, se ha demostrado la aparición de mayor número de compuestos oxigenados que son más odoríferos a diferencia de otros monoterpénicos (Filly et al., 2014); que puede tener importancia sobre el efecto antioxidante y antimicrobiano (Memarzadeh et al., 2015; Zhu et al., 2020).
Por estas razones, se evaluó la influencia de la potencia y humedad de las hojas en la extracción por microondas, y el efecto del ultrasonido como pretratamiento en el rendimiento y la composición química del aceite esencial de Eucalyptus globulus.
MATERIALES Y MÉTODOS
Material vegetal. Las hojas de eucalipto (Eucalyptus globulus) procedieron de Huarochirí (Lima, Perú); éstas fueron cosechadas entre agosto y octubre de 2018, presentando una humedad promedio de 69%.
Acondicionamiento del material vegetal para la extracción. Las hojas se cortaron en un procesador de alimentos (Robot Coupe, CL50, Francia), luego se sumergieron en agua destilada a diferentes proporciones de hoja: agua (1:0,8; 1:10; 1:12,5) por 1 hora para alcanzar humedades de 70, 80 y 90%; (método 931.04 de la AOAC, 2016), y finalmente se escurrieron y empacaron en bolsas de polietileno para su almacenamiento a -18°C hasta su extracción.
Extracción por microondas libre de solventes (EMLS). La muestra descongelada (300 g) fue colocada en un recipiente de vidrio de 1L en un microondas (NEOS, Milestone, Italia) controlado por un microprocesador con sistema de control automático de temperatura por infrarrojo. La extracción se realizó a dos niveles de potencia: 300 y 600 watts, durante 30 minutos con temperatura de condensación de 4ºC, para cada una de las 3 condiciones de humedad (70, 80 y 90%); haciendo un total de 6 tratamientos. El AEE fue recolectado en un frasco ámbar y almacenado a -18°C hasta su caracterización química. Se seleccionó la potencia y porcentaje de humedad que evidenció el mayor rendimiento del AEE.
Extracción por microondas asistida con ultrasonido (EMAU). Para el estudio del efecto de la asistencia del ultrasonido como pretratamiento a la extracción con microondas, las hojas de eucalipto descongeladas, con la humedad seleccionada, puestas en una bolsa de polietileno que se selló herméticamente, se sometieron al pretratamiento con ultrasonido en un baño ultrasónico (Branson Ultrasonics, CPX-952-338R, USA). Este tratamiento se realizó a 180 watts, 40kHz y por 15 minutos, utilizando agua como medio de transmisión en una proporción de 2:1 (hojas: agua). Finalmente, se realizó la extracción por microondas a la potencia elegida.
Rendimiento de aceite esencial. El rendimiento se calculó mediante la siguiente fórmula:
%Rendimiento = (Peso de aceite esencial) / (Peso de hojas) x 100
Identificación de compuestos del AEE por Cromatografía de Gases acoplada a espectrometría de masas (CG-EM). Se llevó a cabo en un cromatógrafo de gases (Agilent Technologies, 7890, USA) acoplado a un espectrómetro de masas (Agilent Technologies, 5975C, USA), y un sistema de datos HP Chem Station, se manipuló una columna capilar J&W DB-5ms (60 m x 250 μm x 0,25μm). La rampa de temperatura empezó en 50°C y subió 5°C/min hasta 180°C; 2,5°C/min hasta 200°C por 2 minutos y finalmente a 25°C/min hasta 300°C, por 1 min. La temperatura de la cámara de ionización fue de 250°C. El gas utilizado fue helio (99,995 %) a una velocidad de flujo de 1ml/min. Los espectros de masas y corrientes iónicas fueron a 4,75 scan s-1, en el rango de m/z 35-500. Se necesitaron 20 μl de aceite esencial de eucalipto que fue diluido en 1 ml de diclorometano (QP). Para la caracterización cromatográfica de los analitos se realizó el cotejo de los tiempos de retención y los patrones de fragmentación de los espectros de masas experimentales con los hallados en la librería (database\NIST versión 2).
Análisis estadístico. Para determinar el efecto de la humedad (70, 80 y 90%) y la potencia (300 y 600 watts) en la EMLS, se analizó el rendimiento AEE (%) mediante un experimento factorial, teniendo como factores humedad (3 niveles: 70,80 y 90%) con la potencia (300 y 600 watts). Cada combinación tuvo 3 repeticiones. Se analizó el cumplimiento de los supuestos: errores con distribución normal y la homogeneidad de varianzas. Se usaron pruebas de comparación LSD de Fisher para analizar las interacciones entre los dos factores. Posteriormente, para comparar los dos métodos de extracción del aceite esencial (EMLS y EMAU) a la mejor potencia de extracción se aplicó un diseño completamente al azar (DCA). Se utilizó el programa InfoStat versión 2020.
RESULTADOS Y DISCUSIÓN
Efecto de la humedad y de la potencia en la extracción del aceite esencial por microondas libre de solventes (EMLS)
En la Tabla 1 se presentan los rendimientos a diferentes condiciones de humedad de las hojas de Eucalyptus globulus y potencias de extracción en la EMLS. Como se puede observar, se encontraron diferencias significativas entre los tratamientos evaluados, siendo el tratamiento con mayor contenido de humedad de las hojas de eucalipto (90%) y mayor potencia de extracción (600 watts), el que presentó un mayor rendimiento de aceite esencial (0,55%).
Tabla 1 Rendimiento de AEE a diferentes condiciones de humedad de las hojas de Eucalyptus globulus y potencias de extracción por microondas libre de solventes
| Humedad (%) | Rendimiento (%) | |
|---|---|---|
| Potencia de EMLS | ||
| 300 watts | 600 watts | |
| 70 | 0,02±0,006a | 0,36±0,021d |
| 80 | 0,07±0,012b | 0,45±0,025e |
| 90 | 0,15±0,013c | 0,55±0,031f |
Los resultados se expresan como el promedio ± la desviación estándar de tres repeticiones. Letras distintas (a, b, c, d y f) en la misma columna indican diferencias significativas entre ellas de menor a mayor en orden alfabético, según la prueba de comparación LSD (p ≤ 0,05).
Con respecto, al efecto de la potencia sobre el rendimiento del AEE, Gupta et al. (2013) indican que el uso de microondas genera un aumento en la temperatura de la muestra causando una degradación de las células de la planta y consecuentemente un corto tiempo de extracción. La mayor potencia de microondas hace que las moléculas en el material vegetal giren rápidamente y produzcan energía térmica detectada por el aumento de temperatura cuando se expone a la radiación de microondas (Cusma et al., 2018). A la misma conclusión llegaron Moradi et al. (2018) y Khalili et al. (2018), quienes indicaron que un incremento del 50% de la potencia aumentó la concentración de compuestos oxigenados y disminuyó los hidrocarburos monoterpenos en aceites esenciales de romero, tomillo y toronjil, respectivamente.
Asimismo, los resultados demuestran que la humedad del material vegetal en la extracción es un factor importante en el rendimiento de los aceites esenciales (Wilson et al., 2016). En la EMLS es importante un porcentaje alto de humedad para mejorar el rendimiento, este proceso coevapora el aceite esencial con el agua in situ del material vegetal (Cravotto & Carnaroglio, 2017), debido a que el calentamiento interno del agua in situ con una alta constante dieléctrica dentro del material vegetal destruye las células vegetales, y el calentamiento es rápido en este proceso (Drinić et al., 2020), lo que conduce a la ruptura de las glándulas y los receptáculos oleíferos; por lo tanto, es importante que las hojas sean humedecidas previo a la extracción (Chun-Hui et al., 2012; Khalili et al., 2018; Kusuma et al., 2018), pudiendo alcanzar humedades altas como lo reportado por Lucchesi et al. (2004) (85% para tomillo, 90% para albahaca y 95% para menta) para aumentar el rendimiento en comparación con otros procesos de extracción como el de arrastre por vapor.
Efecto del pretratamiento con ultrasonido en la extracción del aceite esencial por microondas libre de solventes (EMAU)
En la Figura 1, se puede observar los rendimientos de las extracciones sin y con la asistencia del ultrasonido. El pretratamiento con ultrasonido en la extracción con microondas sin solvente a una potencia de 600 watts tuvo un efecto significativo sobre el rendimiento, siendo este de 0,80 ± 0,02%, a diferencia de la extracción libre de solvente sin pretratamiento con ultrasonido (0,55 ± 0,005%).
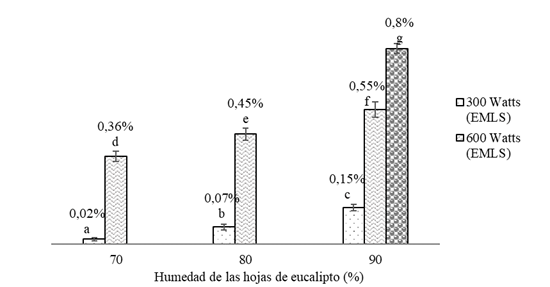
Figura 1 Rendimiento (%) del aceite esencial de hojas de Eucalyptus globulus sin y con la asistencia del ultrasonido
Resultados similares se obtuvieron para la extracción de aceite esencial de pimienta blanca en donde se comparó solo la extracción por microondas frente a la extracción de microondas asistida por ultrasonido (Wang et al., 2018). Al respecto, Bahmani et al. (2018) y El Asbahani et al. (2015) refieren que una ventaja del ultrasonido es la intensificación de la transferencia de masa y la ruptura celular en la hoja, logrando una extracción selectiva acelerando la liberación del aceite esencial de la planta, cuando se usa en combinación con otras técnicas; este efecto es significativo cuando el material vegetal posee estructuras secretoras distribuidas en las superficies de las hojas.
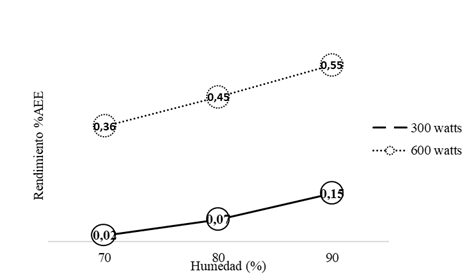
Figura 2 Rendimiento (%) del aceite esencial de hojas de Eucalyptus globulus a dos potencias de extracción
El análisis estadístico realizado (Figura 2) evidencia que a 600 watts se obtuvo una mayor media con humedad de 90%, y la interacción entre la humedad y la potencia resultó significativa (p-value 0,0442), similar comportamiento reportó Bahmani et al. (2018). Concluyendo que, a mayor potencia, mayor rendimiento de aceite esencial.
Características químicas del aceite esencial de eucalipto obtenido por EMLS y EMAU
Los componentes químicos del aceite esencial de hojas de Eucalyptus globulus con tratamientos EMLS y EMAU, se muestran en la Tabla 2. Los componentes principales en ambos tratamientos fueron eucaliptol o 1,8 cineol, α- pineno, aromadendreno, D-limoneno, varidifloreno y gurjuneno. En el análisis cromatográfico, correspondientes al 99,9% del área total, se identificó una mayor cantidad de analitos en la EMAU siendo 46 analitos en comparación a los 41 en EMLS, de los cuales 29 compuestos son comunes en ambos tratamientos de extracción y 17 son analitos adicionales en la EMAU.
Tabla 2 Componentes químicos del aceite esencial de hojas de Eucalyptus globulus con tratamientos EMLS y EMAU.
| N° | COMPONENTES | MOLÉCULA | ÁREA (%) | |
|---|---|---|---|---|
| EMLS | EMAU | |||
| 1 | α- Pineno | C10H16 | 11,10 | 11,19 |
| 2 | D-Limoneno | C20H16 | 5,36 | 5,08 |
| 3 | Eucaliptol | C10H18O | 42,43 | 37,15 |
| 4 | α-Terpineol | C10H18O | 2,23 | 0,88 |
| 5 | α-terpineol acetato | C12H20O2 | 3,34 | 6,78 |
| 6 | α-Gurjuneno | C15H25 | 3,88 | 4,03 |
| 7 | Aromadendreno | C15H24 | 10,26 | 10,14 |
| 8 | L-Alloaromadendreno | C15H25O | 3,17 | 3,21 |
| 9 | Varidifloreno | C15H24 | 4,03 | 3,26 |
| 10 | Globulol | C15H26O | 3,27 | 4,52 |
| 11 | Viridiflorol | C15H26O | 1,18 | 1,88 |
| 12 | Epiglobulol | C15H26O | -- | 1,06 |
| 13 | β-Pineno | C10H16 | 0,57 | 0,56 |
| 14 | β-Mirceno | C10H12 | 0,63 | 0,47 |
| 15 | α-Felandreno | C10H16 | 0,13 | 0,09 |
| 16 | p-Cimeno | C9H13 | 0,15 | 0,48 |
| 17 | ɤ-Terpineno | C9H15 | 0,62 | 0,20 |
| 18 | L-4-Terpineol | C10H18O | 0,37 | 0,31 |
| 19 | Acetato de geraniol | C12H20O2 | 0,42 | 0,76 |
| 20 | Isoledeno | C12H24 | 0,48 | 0,56 |
| 21 | α-Copaeno | C16H23 | 0,17 | -- |
| 22 | α-Cubebeno | C15H24 | -- | 0,13 |
| 23 | Cadineno | C15H24 | 0,18 | -- |
| 24 | β-Gurjuneno | C15H25 | 0,66 | 0,75 |
| 25 | β-Cariofileno | C15H24 | 0,14 | -- |
| 26 | 1,1,1,3 α- trimetil-7-metilenedecahidro-1H-CiclopropaENT#091;aENT#093;naftaleno | C10 | 0,21 | -- |
| 27 | 2-isopropil-5-metil-9-metillen-biciclo ENT#091;4.4.0ENT#093; dec-1-eno | C10 | -- | 0,16 |
| 28 | α-Panasinseno | C15H24 | 0,15 | -- |
| 29 | Sativeno | C15H24 | -- | 0,35 |
| 30 | Eremofileno | C15H24 | 0,63 | -- |
| 31 | α-Cariofileno | C15H24 | 0,12 | -- |
| 32 | ɤ-Gurjuneno | C15H24 | 0,33 | 0,38 |
| 33 | C15H24 | C15H24 | -- | 0,64 |
| 34 | Feniletil isovalerato | C13H18O2 | 0,43 | -- |
| 35 | Elixeno | C15H24 | 0,58 | -- |
| 36 | ɤ-Muuroleno | C15H24 | -- | 0,47 |
| 37 | α-amorfeno | C15H24 | -- | 0,23 |
| 38 | Cadineno | C15H24 | 0,18 | -- |
| 39 | ɤ-Cadineno | C15H24 | 0,33 | 0,34 |
| 40 | δ-Cadineno | C15H22 | 0,18 | 0,30 |
| 41 | Dehidroaromadendreno | C15H26O | 0,60 | 1,03 |
| 42 | Epiglobulol | C15H24 | 0,60 | 0,17 |
| 43 | α-Fameseno | C15H24 | -- | 0,17 |
| 44 | C15H24O | 0,38 | 0,27 | |
| 45 | C15H26O | C15H26O | 0,34 | 0,21 |
| 46 | β-Eudesmol | C15H26O | 0,20 | 0,56 |
| 47 | 3,3,7,11-tetrametil-triciclo ENT#091;6.3.0.0(2,4)ENT#093;Undec-8-eno | C15H24O | -- | 0,15 |
| 48 | Spatulenol | C15H26O | -- | 0,26 |
| 49 | Ledol | C15H26O | 0,29 | 0,50 |
| 50 | Bis (2-etilhexil) éster del ácido Hexanedioico | C15H26O | 0,03 | -- |
| 51 | ɤ-Cadinol | C15H26O | -- | 0,06 |
| 52 | α -Cadinol | C10H18O | -- | 0,03 |
| 53 | Guaniol | C10H18O | -- | 0,20 |
| 54 | Decahidro-1,1,3 α. trimetil-7-metilen-ENT#091;1αS-(1α,3α,7β,7α)ENT#093;-1H- ciclopropa(a)naftaleno | C26H20O10 | -- | 0,02 |
| 55 | 4-metilen-1-metil-2(2-metil-1-propen-1yl)-1-vinil-cicloheptano | C15H26 | -- | 0,18 |
| 56 | α-terpinoleno | C10H16 | -- | 0,06 |
| Total | 100 | 100 | ||
EMLS: Extracción por microondas libre de solventes; EMAU: Extracción por microondas libre de solventes asistida con ultrasonido.
Los componentes principales del AEE extraído por EMLS y EMAU son los monoterpenos oxigenados (eucaliptol 42,43%; 37,15%), hidrocarburos monoterpenos (α-pineno 11,1%; 11,2%) e hidrocarburos sesquiterpenos (aromadendreno 10,26%; 10,14%), al igual que el obtenido por González et al. (2016) y Natividad (2019). En base a los componentes mayoritarios, se identificó al quimiotipo eucaliptol/α-pineno, al igual que en otras variedades de eucalipto reportados por Elaissi et al. (2011). Dentro de los terpenos encontrados para ambas extracciones, se encuentran los hidrocarburos monoterpenos (HM) como el D-limoneno, en un porcentaje de 5,36-5,08%, similar al resultado que obtuvo Morsy (2015). La cantidad de limoneno era aproximadamente la mitad del α-pineno, diferente a lo reportado por Zrira et al. (2004) y en menor cantidad otros HM como α-felandreno, α-Terpinoleno e Isoledeno; al respecto se detectaron cantidades similares de p-cimeno, seguidas de menores cantidades de γ-terpineno para semejantes especies de Eucalyptus parvula. En Eucalyptus cinerea, se detectaron cantidades similares de α-pineno y limoneno, seguidas de menores cantidades de p-cimeno, β-mirceno y β-pineno (Zrira et al., 2004 y Coppen, 2002). También se identificaron con la EMAU, los hidrocarburos sesquiterpénicos, donde se detectaron porcentajes muy bajos (≤0,1%) de β-cariofileno, cadineno, α-panasinseno, dehidroaromadendreno, α-farmeseno, β-eudesmol, spatulenol, α-cadinol, ɤ-cadinol y cantidades ligeramente mayores (≤0,6%) de β-gurjuneno, ɤ-gurjuneno, eremofileno, epiglobulol, L-4-terpineol, isoledeno, que difieren a lo mencionado por Zrira et al. (2004).
En el AEE se obtuvo menos componentes por EMLS, esto puede deberse a que los compuestos orgánicos con bajo momento dipolar contenidos en el AEE tienen una baja interacción con microondas, en consecuencia, se extraen con mayor dificultad (Farhat et al., 2017) o incluso pueden estar sujetos a cambios en su configuración incluyendo terpenos menores Ieri et al. (2019). Por otro lado, el método de extracción por microondas produjo menos compuestos con baja polaridad, no siendo suficiente para aislar a los monoterpenos y sesquiterpenos oxigenados (Petigny et al., 2014); que podría estar relacionado a la degradación térmica de los compuestos lábiles durante la aplicación de calor del microondas por tiempos prolongados (Filly et al., 2014; Morsy, 2015 y Tran et al., 2020).
Por el contrario, con la EMAU existe un mayor número de compuestos o analitos (17) debido a que hay una mayor liberación del material soluble en el medio circundante, ya que las burbujas de cavitación producidas por el ultrasonido rompen los tricomas que se encuentran en la superficie de la hoja (Petigny et al., 2013; Wang et al., 2018 y Hu et al., 2019). Al respecto, Morsy (2015) y Seidi et al. (2016) indican que la ventaja del pretratamiento ultrasónico aumenta la extracción de compuestos monoterpenos oxigenados, lo que permite una extracción efectiva en un tiempo considerablemente más corto con una mejor calidad, cuando existe un nivel bajo de degradación térmica (Kowalski et al., 2015) haciendo este producto muy valioso para aplicarlo en cosméticos, medicinas y alimentos como un conservante natural.
Por otro lado, se evidencia que el componente eucaliptol disminuyó de 42,43 (EMLS) a 37,15 (EMAU). En general, en la EMAU se observa la reducción de monoterpenos, monoterpenos oxigenados, diterpenos y sesquiterpenos. Al respecto, Petigny et al. (2014) refiere que el ultrasonido podría tener efecto en algunos terpenos, los cuales estarían sujetos a cambios de configuración en la posición de los dobles enlaces, causando reducción de los mismos. También, Wang et al. (2018) indica que el ultrasonido podría aumentar las degradaciones de los productos naturales que incluyen compuestos no volátiles como volátiles. Además, las modificaciones en la composición están relacionados con la facilidad de liberación de los aceites esenciales de las glándulas secretoras a transformaciones de compuestos químicos inestables durante el ultrasonido (Nora & Borges, 2017) y mejorando también el rendimiento de los componentes químicos (Ullah et al., 2019).
De los compuestos valorizados por sus propiedades en el AEE se tiene al eucaliptol, aromandendreno y α-terpineol. La abundancia de 1,8-cineol o eucaliptol mostró una variabilidad entre 42 a 37%, el porcentaje es inferior a lo reportado por Ieri et al. (2019), considerando que esta variabilidad podría deberse a factores climáticos, geográficos y temporada de cosecha del eucalipto; no obstante, varios autores como Garneau et al. (2013); Godinho et al. (2014) y Hernández et al. (2018), refieren que el compuesto mayoritario en la familia de Myrtaceae, de Eucalyptus globulus es el eucaliptol. La importancia del eucaliptol es que tiene actividad biológica como antibacteriano, antifúngico, analgésico y otras propiedades antiinflamatorias (Ramezani et al., 2002; Sartorelli et al., 2007; Dehghani-Samani et al., 2015; Dhakad et al., 2017, Sharafati et al., 2018; Ieri et al., 2019). El aromadendreno se encontró en una proporción 10-10,5%; el cual es mayor a lo reportado por Kheder et al. (2020) con 3,97% para Eucalyptus camaldulensis e inferior a lo reportado por Mulyaningsih et al. (2010), quienes encontraron 31,17% en Eucalyptus globulus, y se ha comprobado que el aromadendreno contribuye de manera relevante a la actividad antimicrobiana. El α-terpineol (2-6%) es uno de los componentes del AEE, estos pueden tener una aplicación terapéutica potencial para el tratamiento de enfermedades periodentales (Harkat-Madouri et al., 2015). Otros analitos encontrados en menores proporciones son el viridiflorol, globulol, y el p-cimeno (1,2-2%, 3-4%, 0,15-0,5%), siendo semejantes con lo reportado por Elaissi et al. (2011), indicando que la sinergia de los compuestos serían los responsables de la actividad antibacteriana.
CONCLUSIÓN
El mayor contenido de humedad (90%) de las hojas de eucalipto y mayor potencia (600 watts) incrementó el rendimiento del aceite esencial de eucalipto en la extracción con microondas libre de solvente (EMLS). El pretratamiento con ultrasonido (EMAU) influyó significativamente en el rendimiento del AEE, extrayéndose 17 compuestos adicionales. El quimiotipo mayoritario encontrado fue el eucaliptol/α-pineno. Finalmente, la utilización del ultrasonido como pretratamiento es un método innovador que puede ser utilizado a mayor escala y según los fines industriales, sustituyendo a los métodos convencionales.












 uBio
uBio 


