Estimadas Editoras:
El dolor es un síntoma comúnmente informado entre las personas mayores en centros de larga estancia. La incidencia de dolor varía según la población evaluada y el tipo de medida utilizada (observación versus datos subjetivos). Para aquellas personas mayores en centros de larga estancia, los informes verbales de dolor tienden a ser altos, oscilando entre aproximadamente el 30% y el 80%.1,2) En general, la incidencia de dolor es mayor entre quienes pueden informar verbalmente sobre el dolor, para aquellos con demencia moderada a severa la información verbal puede no ser fiable. La sensación de dolor incluye cuatro dimensiones1,3: 1) la dimensión sensorial-discriminativa que aborda la ubicación, la calidad y la intensidad de dolor; 2) la dimensión afectivo-motivacional que se refiere a sentimientos de desagrado, angustia y amenaza; 3) la dimensión cognitivo-evaluativa que incluye las actitudes y creencias de las personas sobre el dolor; y 4) la dimensión social que aborda cómo las personas interactúan con sus compañeros, familiares e individuos en la sociedad. La dimensión sensorial-discriminativa de dolor, que depende de la vía nociceptiva lateral, se conserva en personas con demencia incluso cuando progresan hacia una demencia severa. Las dimensiones afectivo-motivacional y cognitivo-evaluativa están deterioradas entre las personas con demencia severa 4. En un estudio, el dolor nociceptivo se encontró como el tipo más prominente (70 %) en una población de centros de larga estancia, seguido de una combinación de dolor nociceptivo y neuropático (25 %) 5,
Estudios reportaron que, las personas con enfermedad de Alzheimer aunque podrían sentir el dolor, podrían verse menos afectadas emocionalmente por él. Sin embargo, varios estudios experimentales demostraron que es poco probable que este sea el caso, tanto los estudios de reflejo como los estudios de resonancia magnética funcional después del estímulo del dolor muestran que la reacción al dolor de los pacientes con enfermedad de Alzheimer es aún más pronunciada. La demencia vascular se ha asociado con prevalencia de dolor ligeramente superiores, probablemente debido a la posibilidad de que las lesiones de la sustancia blanca del cerebro sean la causa de dolor central. Un estudio sobre el dolor sugirió que las personas con demencia vascular tienen una intensidad de dolor similar a las personas cognitivamente intactas, pero parecen sufrir más. En la demencia frontotemporal los pacientes pueden tener un aumento en el umbral y posiblemente también en la tolerancia al dolor 5.
La evaluación competente de dolor (Tabla 1) 6, es un requisito necesario para un buen manejo del mismo e, idealmente, considera varias dimensiones, a saber, la intensidad, la ubicación, el afecto, la cognición, el comportamiento y los acompañamientos sociales. Los responsables del manejo de dolor deben estar adecuadamente informados al menos sobre la presencia e intensidad del dolor 6. El autoinforme a menudo se considera el "estándar de oro" en la evaluación de dolor. Actualmente se dispone de una amplia gama de escalas de autoinforme para evaluar el dolor, la mayoría de las cuales se han desarrollado y probado en personas mayores con demencia 7. A pesar de estudios que respaldan la confiabilidad y validez del autoinforme para personas con demencia, los profesionales de la salud y los expertos reconocen que el autoinforme por sí solo no es suficiente para estos pacientes que necesariamente están sujetos a estrategias de observación para la evaluación de dolor.(8 Refiriéndose al Mini Examen del Estado Mental, se sugirió una puntuación límite de 18 para dividir a los individuos en aquellos que aún pueden y aquellos que ya no pueden autoinformar el dolor 4.
Tabla 1 Recomendaciones para la evaluación de dolor en pacientes con demencia
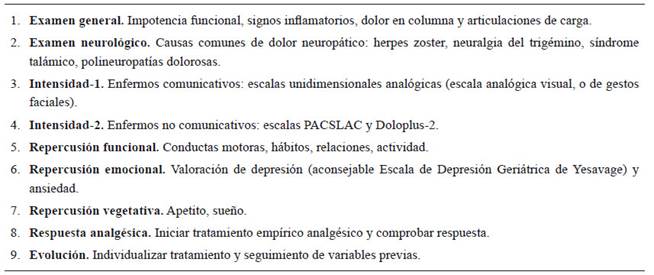
Nota: Tomado de “El neurólogo frente al dolor en la demencia”, de L Álvaro, 2015, Neurología, 30, p.9 (https://doi.org/10.1016/j.nrl.2012.02.001). CC-BY(6)
Comportamientos tales como quejas verbales, vocalizaciones negativas, suspiros, gemidos, agitación, llanto, muecas, parpadeo rápido, movimiento, inquietud, roce, fuerza, rigidez, habla verbal inapropiada y agresión pueden considerarse signos de dolor, pero en pacientes con deterioro cognitivo, estos signos pueden tomarse como síntomas conductuales y psicológicos de la demencia 9. Esto tiene implicaciones negativas, ya que los síntomas referidos pueden tratarse de forma inadecuada con antipsicóticos versus medicamentos para el dolor, y estos pacientes generalmente no reciben intervenciones conductuales para controlar el dolor 10.
Finalmente, el dolor en la demencia es muy frecuente y el cual normalmente se señala mediante la comunicación verbal, que se deteriora cada vez más en las personas con demencia. Por lo tanto, las personas con demencia sufren innecesariamente de un dolor manejable pero no reconocido. La evaluación de dolor en personas con demencia es un esfuerzo desafiante, con avances científicos que se desarrollan rápidamente. Las herramientas y protocolos de evaluación de dolor (principalmente escalas de observación) se han incorporado a las guías de evaluación de dolor en personas mayores. Para evaluar el dolor de manera efectiva, la colaboración interdisciplinaria (enfermeras, médicos y psicólogos) es esencial. El manejo de dolor en esta población vulnerable se realiza preferentemente en un entorno interdisciplinario.















