Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Medica Herediana
Print version ISSN 1018-130XOn-line version ISSN 1729-214X
Rev Med Hered vol.8 no.1 Lima Jan. 1997
Dos esquemas terapéuticos en el manejo de crisis asmática en niños.
Two therapeutics plans for management asthmatic crisis in children.
Velasco José*, Huaman Raúl*, Vargas Ronald*, Diaz Alberto*, Chiarella Pascual**, Whu Rafael***.
*Médico Cirujano, Universidad Peruana Cayetano Heredia.
**Neumólogo Pediatra, Universidad Peruana Cayetano Heredia.
***Servicio de Emergencia Pediátrica. Instituto de Salud del Niño. Universidad Peruana Cayetano Heredia.
RESUMEN
Objetivo: Comparar los efectos terapéuticos y colaterales de dos esquemas de tratamiento en la crisis asmática: la asociación de fenoterol 100 ug en microdosificador inhalatorio (MDI) con aerocámara más dexametasona endovenosa vs salbutamol 100 ug en MDI con aerocámara más hidrocortisona endovenosa. Materiales y métodos: En un estudio prospectivo, randomizado, multicéntrico y abierto, se incluyó 60 niños con crisis asmática leve-moderada (30 para cada grupo). Ambos grupos fueron comparables al ingreso. Resultados: En la evolución no hubo diferencia significativa en la frecuencia respiratoria, puntaje clínico, pico respiratorio forzado (PEF) y tremor (p>0.05), hallándose mayor taquicardia en los primeros 30 y 60 minutos en el grupo que recibió Fenoterol - Dexametasona. No se encontró diferencia significativa en la proporción de altas al final del estudio. Conclusiones: Se concluye que la asociación Fenoterol - Dexametasona y Salbutamol - Hidrocortisona son igualmente efectivas en el manejo de la crisis asmática leve - moderada en niños (Ref Med Hered 1997; 8: 5-10).
PALABRAS CLAVE: Fenoterol, salbutamol, dexametasona, hidrocortisona, asma, niños.
SUMMARY
Objective: To compare the clinical and side effects of two therapeutics schedules in the treatment of asthmatic crisis: The association of fenoterol 100 ug Metered Dose Inhaler (MDI) with spacer device plus dexamethasone IV and salbutamol 10 ug MDI with spacer device plus hydrocortisone IV. Material and Methods: In a ramdomized, prospective, longitudinal, open and multicentric trial we included 60 children with mild-moderate asthmatic crisis (30 for each group). Both groups were comparables at initial evaluation. Results: There were no significative difference in respiratory rate, clinical score, peak expiratory flow rate (PEF), and tremor (p>0.05). We found more heart rate at first 30 and 60 minutes in Fenoterol - Dexamethasone group (p£ 0.05). There were no significative differences in the amount of discharges from hospital at the end of the study (4 hours). Conclusions: We conclude that the association Fenoterol-dexamethasone and Salbutamol-Hydrocortisone are equally effective in the management of mild to moderate asthmatic crisis in children. (Rev Med Hered 1997; 8: 5-10).
KEY WORDS: Fenoterol, salbutamol, dexamethasone, hydrocortisone, asthma, children.
INTRODUCCION
El asma es una enfermedad pulmonar crónica con exacerbaciones agudas en varios grados de severidad, caracterizada por tres aspectos: obstrucción, inflamación e hiperreactividad de la vida aérea, que se pueden resolver espontáneamente o con tratamiento farmacológico (1).
El tratamiento de la crisis asmática aguda debe estar dirigido a controlar tanto la inflamación como el broncoespasmo (2,3,4). El medio más eficaz para tratar el broncoespasmo es el uso de beta 2-adrenérgicos: salbutamol (5) y fenoterol (6), por vía inhalatoria (7) en microdosificador inhalatorio con aerocámara o nebulización (8).
Los coricosteroides son los agentes antiinflamatorios más potentes para el tratamiento del asma (7,9). Su uso en las crisis ha mostrado ser poco beneficioso por si solos (10), pero asociados a los beta 2-adrenérgicos han demostrado tener igual o más beneficio que asociación de éstas con las metilxantinas (11).
La literatura internacional nos muestra en su mayoría, estudios en los que se usa salbutamol e hidrocortisona. Sin embargo en nuestros servicios de emergencia es común el uso de fenoterol (por su presentación en gotas para nebulización) y dexametasona (por su bajo costo).
El objetivo del presente trabajo es comparar la eficacia de la asociación salbutamol (100 ug) es microdosificador inhalatoria (MDI) con dexametasona endovenosa (dosis equipotentes), para el manejo de la crisis asmática leve - moderada en la población pediátrica.
MATERIALES Y METODOS
El diseño del estudio fue prospectivo, longitudinal, abierto, randomizado y multicéntrico. Los pacientes fueron tomados del servicio de Emergencia Pediátrica del Hospital Nacional Cayetano Heredia y del Instituto de Salud de Niño entre los meses de Enero y Junio de 1994. Los pacientes ingresaron al estudio en forma aleatoria de acuerdo a un número random, se llenó una ficha de datos clínicos y la autorización por escrito de los padres o tutores para la inclusión en el trabajo.
Se evaluó la frecuencia respiratoria, puntaje clínico (12), el pico espiratorio forzado (PEF) mediante un flujómetro mini wright peak flow meter (13) (el mejor de 3 intentos (14)) (15,16), la frecuencia cardiaca (17) y el tremor (7).
Protocolo terapéutico:
En el Grupo 1 se utilizó fenoterol de 100 ug/ dosis en micro-disificador inhalador (MDI) con aerocámara dos inhaladores (con separación de un minuto) a los 0, 10, 20, 30, 40, 50, 65, 80, 95, 110, 140, 170, 200 y 230 minutos(± 3 minutos) desde el ingreso, con una dosis de dexametasona endovenosa (0.3 mg/Kg de peso, máximo: 10 mg/dosis) a los 0 minutos.
En el Grupo 2 se utilizó salbutamol de 100 ug/dosis en MDI con aerocámara, con un esquema similar en MDI con aerocámara, con un esquema similar al grupo 1, y una hidrocortisona EV (7 mg/Kg de peso, máximo: 250 mg/dosis) a los 0 minutos.
La aerocámara de fabricación "casera" fue hecha a partir de un frasco plástico de suero salino de 1000 cc. De 18x8 cm, donde por un lado estaba la cara del paciente y por el otro el MDI, al accionar el MDI el paciente inhaló en forma lenta y profunda (15), ocho veces (18) y antes de la segunda inhalación se les dejó respirar aire libre por 1 minuto, para evitar el riesgo de intoxicación por el propelene (19). Los pacientes no recibieron fisioterapia respiratoria (vibro-percusión), por considerarse controversial (20) y se un método difícil de estandarizar para su análisis.
Criterios de Inclusión:
- Niños entre 5 y 13.9 años de ambos sexos, con crisis asmática leve-moderada (ya sea reagudizada o una exacerbación aguda) de menos de 72 horas de evolución, con puntaje clínico según Index Pulmonar (12) entre 4 y 9.
- Consentimiento por escrito de los padres (o tutor), para que el niño ingreso al estudio.
- Colaboración del paciente con el examen físico, flujometria y el tratamiento.
Criterios de Exclusión:
- Enfermedad del Aparato Respiratorio (aguda o crónica) diferente a la crisis asmática.
- Paciente febril (Temperatura oral ³ a 38.5ºC).
- Uso en las 6 horas previas de algún Beta - 2 adrenérgico (oral o inhalado) a dosis y técnica adecuada si usó MDI.
- Uso de un corticoide sistémico o inhalado al menos 12 horas antes del ingreso.
- Falta de consentimiento de los padres.
La duración máxima del trabajo fue hasta de 4 horas (21), realizándose la evaluación cada 30 minutos: 0, 30, 60, 90, 120, 150, 180, 210 y 240.Sin embargo el paciente pudo salir del estudio cuando se presentó alguna de las siguientes situaciones:
- Criterio de Alta: hubo mejoría clínica (puntaje clínico < 3).
- Criterio de Empeoramiento clínico: Si se presentaban con alguna complicación de la crisis asmática aguda, incremento del puntaje clínico > 2 o un PEF que disminuía más de 20% de su valor inicial.
En los casos en que al culminar las 4 horas de manejo no presentó el criterio de alta o durante el manejo presentó criterios de empeoramiento clínico fue manejado por el personal médico del servicio de emergencia.
Las dosis utilizadas para los beta 2 - agostas, fue de 1200 ug para la primera hora, 800 ug para la segunda hora y 400 ug para la tercera y cuarta hora, si la dosis efectiva es ± 15%, llegaría 180 ug para la primera hora, 120 ug para la segunda hora y 60 ug para las siguientes dos horas, haciendo un total de 360 ug, si es que el paciente se queda las 4 horas del protocolo.
Las dosis usadas para dexametasona fue 0.3 mg/Kg e hidrocortisona 7 mg/Kg; dosis mínimas en las que no hay diferencia en su efecto siendo comparables.
Análisis estadístico
El tamaño de la muestra se calculó empleando la siguiente ecuación:
n = p2 S2 / d2
donde:
n = tamaño de la muestra,
p = valor de la t student,
S2 = varianza de la frecuencia respiratoria,
d = precisión medida (estimador - media de la población).
El tamaño muestra para cada grupo fue de 30 pacientes. Para el análisis estadístico se utilizó la diferencia de las medias para las variables cuantitativas absolutas (frecuencias respiratorias, puntaje clínico y frecuencia cardiaca) y la variación de las medias para las variables cuantitativas de las medias para las variables cuantitativas porcentuales (PEF%). Para la base de datos se utilizó la hoja de cálculo Lotus versión 2.301 y para el análisis estadístico el programa SPSS PC+4.0. Para el análisis se empleó el ANDEVA, t student y Manan - Whitney para variables continuas y Chi cuadrado con corrección de Yates y el Prueba exacta de Fisher para las cualitativas, con el nivel de significacia de p<0.05.
RESULTADOS
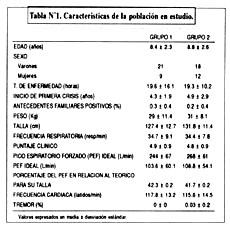
En la evaluación inicial entre ambos grupos, no se demostraron diferencias significativas (tabla Nº1). Las curvas de variación gráfica la evolución en el tiempo de la frecuencia respiratoria, puntaje clínico y PEF. No se encontró diferencia significativa entre ambos grupos en cuanto a estos parámetros en ningún momento de la evaluación.
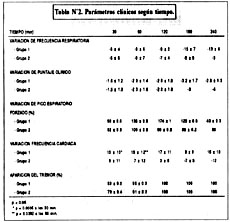
Al observar la variación de la frecuencia cardiaca vemos un rápido aumento en ambos grupos siendo este significativo (p£ 0.05) para el grupo 1 a los 30 minutos. Luego de este momento no se encontró diferencia hasta el final del estudio (Tabla Nº2).
En cuanto a la aparición del tremor, no se encontró diferencia significativa entre ambos grupos, siendo 100% hacia las 2 horas de la evaluación.
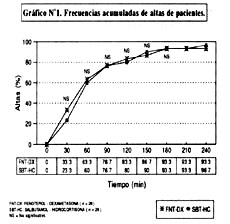
Al analizar las altas acumuladas notamos un aumento semejante de ambas curvas a lo largo del tiempo sin encontrar diferencia significativa en algún momento del estudio (Gráfico Nº1).
Al cabo de las 4 horas que duró la evaluación observamos que tanto el grupo 1 y 2 brindas altas a mas del 90% de pacientes (93.3% y 96.7% respectivamente).
De los 60 pacientes que ingresaron al estudio 67(95%) fueron dados de alta, 2(3.3%) mejoraron respecto al ingreso pero no fueron dados de alta y 1(1.67%) presentó enfisema subcutáneo requiriendo hospitalización.
DISCUSION
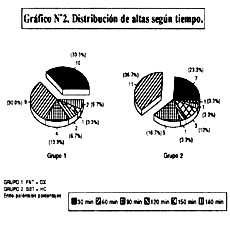
El manejo actual de la terapia broncodilatadora en la crisis asmática aguda consiste en el uso de beta 2-adrenérgicos por vía inhalatoria (7,8); el salbutamol (5,22) en MDI de 100 ug y el fenoterol en MDI de 200 ug, aunque recientemente en MDI de 100 ug (23). Trece veces más potente pero menos selectivo (24), el efecto máximo del fenoterol se alcanza a los 30 minutos (25), mientras que el salbutamol dentro de los primeros 15 minutos (23,26). Ambos tienen igual efecto broncodilatador, pero al fenoterol se le atribuyen más efectos colaterales cardiovasculares e hipocalemia que el salbutamol (17) (al emplear mayor dosis mayor por disparo (200 ug/puff) según lo reportado por Newnham et al (Grafico N°2), que no halló diferencias en los efectos cronotrópicos e inotrópicos sobre los receptores B1/B2 en pacientes normales (23), y Rázuri que no encontró diferencias en la aparición de los efectos colaterales en pacientes asmáticos leve-moderados (27,28).
La importancia de la asociación de los corticosteroides con los beta 2-adrenérgicos (9,29), es que tienen la ventaja de reducir la necesidad de la hospitalización (30,31), conducen a la resolución de la crisis (21,32), mejoran la respuesta a los beta 2 agonistas (1), evitan la taquifilaxia en pacientes que llegan a emergencia con tratamiento regular y crónico (33), incrementan con rapidez la función pulmonar (32) y recuperación de los niveles de pO2, pocas fallas terapéuticas y recurrencias (34) y la asociación de éstas tienen un efecto aditivo antes que sinérgico en las vías aéreas (29).
El factor económico es importante, se ha utilizado metilprednisolona e hidrocortisona con buenos resultados, pero son más costosos a diferencia de la dexametasona, la cual en estudios en pacientes (32) e in-vitro ha demostrado tener igual o mayores ventajas (32,35) que las antes mencionadas, lo cual hace interesante tratar de demostrar su utilidad como terapia inicial.
Los resultados permiten sugerir que no existe diferencia en cuanto a la rapidez y efectividad en proporcionar altas (93.3% vs. 96.7%) entre ambos grupos en un período de observación de 4 horas, tiempo adecuado para evaluar el efecto del corticoide según algunos autores (4,21).
Respecto a los efectos colaterales se encuentra que en la frecuencia cardiaca existe diferencia significativa hasta los 60 minutos en el grupo 1, luego no hay diferencia significativa hasta los 180 minutos, señalando que la taquicardia provocada no comprometió la mejoría clínica de los pacientes.
El tremor distal se observa en el 100% de pacientes entre los 90 y 120 minutos de iniciada la terapia.
Según Muhti et al. (36) se encontró diferencia significativa en la frecuencia cardiaca desde los 5 minutos hasta las 3 horas, concluyendo igual que Tandon et al. (37) y Wong et al. (24) que luego de la inhalación de fenoterol la frecuencia cardiaca tiende a incrementarse, mientras que disminuye con el salbutamol, pero en estos estudios se utilizó mayores dosis de fenoterol, a diferencia e Newnhan et al.(23) y Crane et al.(17), que a dosis equivalente no encontraron diferencias.
En este trabajo se proporcionó un 95% de altas (57 de 60 pacientes) dentro de un período de observación de 4 horas, a diferencia de Rázuri (27) que dio un 74% de altas (37 de 50 pacientes) en 2 horas sin asociarlos a corticoides, en pacientes con crisis asmática leve-moderada.
Se concluye que la asociación de fenoterol-dexametasona y salbutamol -hidrocortisona es igualmente efectiva en el manejo de crisis leve moderada en niños.
REFERENCIAS BIBLIOGRAFICAS
1.National Asthma Education Program. Guidelines for the Diagnosis and Managment of Asthma. Bethsda, MD: National Heart, Lung and Blood Institute, 1991. US Dept of Healt and Human Services publication NIH 91-3042A. J Allergy Clin Immunol 1991; 88: 425-38. [ Links ]
2.Reed CE. Aerosol Steroids as Primary treatment of Mild Asthma. N Engl J Med 1991; 325(6): 425-6. [ Links ]
3.Spelucin J, Alamo C, Koc D, Peña G, Sánchez E. Hidrocortisona en el manejo de la crisis asmática infantil. Pediátrica 1992; 1(3): 25-31. [ Links ]
4.Tai A, Levy N, Bearman JE. Methylprednisolone Therapy for Acute Asthma in infants and Toddlers: A Controlled Clinical Trial. Pediatrics 1990; 86(3): 350-6. [ Links ]
5.Katz RW, Kelly HW, Crowley MR, Grad R, McWilliams BC, Murphy SJ. Safety of Continuos Nebulized Albuterol for Bronchospasm in Infants and Children. Pediatrics 1993; 92(5): 666-9. [ Links ]
6.Chairman JO. Asthma: A follow up statement from an International Pediatric Asthma Consensus Group. Arch Dis Child 1992; 67: 240-8. [ Links ]
7.Barnes PJ. A new approach to the treatment of asthma. NEJM 1989; 321(22): 1517-27. [ Links ]
8.Mc Fadden ER. Therapy of acute asthma. J Allergy Clin Inmunol 1989; 84(2): 158-8. [ Links ]
9.Rubin BK, Marcushamer S, Priel I, App EM. Manejo de la crisis asmática en el niño. Revisión Pediatric Pulmonol 1990; 8: 45-47. [ Links ]
10.Fanta CH, Rossing TH, McFadden ER. Glucocorticoids in acute asthma. A critical controlled trial. Am J Med 1983; 74(5): 845-51. [ Links ]
11.Di Giulio GA, Kercsmar CM, Krug SE, et al. Hospital treatment of asthma: Lack of benefit from Theophylline given in adittion to nebulized Albuterol and Intravenously administered Corticosteroid. J Pediatr 1993; 122: 464-9. [ Links ]
12.Bierman CW, Pierson WE. The pharmacologic managment of status asthmaticus in children. Pediatrics 1974; 154: 245-7. [ Links ]
13.Perks WH, Tams IP, Thompson DA, Prowse K. An Evaluation of the Mini-Wright Peak Flow Meter. Thorax 1979; 34: 79-81. [ Links ]
14.Mueller GA, Eigen H. Pruebas de función pulmonar en niños asmáticos. Clínicas Pediátricas Norteamericanas 1992; 4: 1335-51. [ Links ]
15.Farga V. Aplicación clínica del estudio funcional respiratorio. Rev Med Chile 1983; 111: 861-8. [ Links ]
16.Kelly CA, Gibson GJ. Relation between FEVI and peak expiratory flow in patients with chronic air flow obstruction. Thorax 1988; 43: 335-6. [ Links ]
17.Crane J, Burgess C, Beasley R. Cardiovascular and hipokalemic effects of inhaled salbutamol, fenoterol and isoprenalina. Thorax 1989; 44: 136-40. [ Links ]
18.Lee H, Evans HE. Aerosol bag for administration of broncodilators to young asthmatic children. Pediatrics 1984; 73(2): 230-2. [ Links ]
19.Benton G, Thomas RC, Nickerson BG, McQuitty JC. Okikawa the Pediatric Emergency Departament. AJDC 1989; 143(6): 678-81. [ Links ]
20.Kirillof LH, Owens GR, Rogers RM, Mazzocco MC. Does chest physical therapy work?. Chest 1985; 88(3): 436-44. [ Links ]
21.Littenberg B, Gluck EH. A controlled trial of Methylprednisolone in the emergency treatment of acute asthma. NEJM 1986; 314(3): 150-2. [ Links ]
22.Frew AJ, Holgate S. Clinical pharmacology of asthma. Implications for treatment. Drugs 1993; 46(5): 847-62. [ Links ]
23.Newnham DM, Wheeldon NM, Lipworth BJ, Mc Devitt DG. Single dosing comparison of the relative cardiac b 1/b 2 activity if inhaled fenoterol and salbutamol in normal subjects. Thorax 1993; 48: 656-58. [ Links ]
24.Wong CS, Pavord ID, Williams J, Britton JR. Tattersfield of fenoterol, salbutamol and terbutaline in asthma. Lancet 1990; 336: 1396-9. [ Links ]
25.Reilly PA, Yahav J, Mindorff C, Kazim F, Levison H. Dose response characteristics of nebulized fenoterol in asthmatic children. J Pediatr 1983; 121(1): 121-6. [ Links ]
26.Walker SR, Evans ME, Richards AJ, Paterson JW. The clinical pharmacology of oral and inhaled salbutamol. Clin Pharmacol Ther 1972; 13(6): 861-7. [ Links ]
27.Rázuri A. Comparación de Fenoterol inhalador versus Salbutamol inhalador en Crisis asmática en Niños. Tesis Bachiller en Medicina. Lima, Peru. Universidad Peruana Cayetano Heredia. 1994. [ Links ]
28.Chiarella P, Rázuri A, García A, Ugarte C, Whu R, Zegarra O. Crisis asmática en niños: comparación de dos terapias inhalatorias. Acta Médica Peruana 1993; 17 (1): 26-35. [ Links ]
29.Tattersfield AE, Barnes PJ. b 2 - Agonist and corticosteroids: New developments and controversies. Report of a meeting in November 1991. Am Rev Respir Dis 1992; 146: 1637-41. [ Links ]
30.Kattan M, Gurwitz D, Levinson H. Corticosteroids in status asthmaticus J Pediatr 1980; 96(3): 596-9. [ Links ]
31.Kuo E, Kesten S. A retrospective comparative study of in hospital management of acute severe asthma: 1984-1989. Chest 1993; 103(6): 1655-61. [ Links ]
32.Pierson WE, Bierman CW, Kelley VC. A Double - Blind trial of corticosteroids therapy in status asthmaticus. Pediatrics 1974; 54(3): 282-8. [ Links ]
33.Holgate ST, Baldwin CJ, Tattersfield AE. b -Adrenergic agonist resistance in normal human airways. Lancet 1977; 1: 375-7. [ Links ]
34.Lehtonen L. Steroids in acute severe asthma. Lancet 1992; 340: 1384-6. [ Links ]
35.Lamas AM, Leon OG, Scheleimer RP. Glucocorticoids inhibit eosinophil responses to granulocyte - Macrophage colony stimulating factor. J Immunol 1991; 147(1): 254-9. [ Links ]
36.Huhti E, Poukkula A. Clinical comparison of fenoterol and albuterol administered by inhalation. Chest 1978; 73(3): 348-51. [ Links ]
37.Tandon MK. Cardiopulmonary effects of fenoterol and salbutamol aerosols. Chest 1980; 77(3): 429-31. [ Links ]